第四节 元素(23张PPT)
图片预览







文档简介
第四节 元素
鲁教版·九年级化学上册
新课导入
人们很早就意识到,所有物质都是由几种亘古不变的基本成分 ——“元素”组成的。
水
火
土
气
元素——究竟是什么?
新课探究
元素与元素符号
组成物质世界的元素究竟是什么?
所有的物质都是由原子、分子、离子等基本粒子构成的,这些基本粒子才是组成物质的元素。
观点 1
分子在化学变化中可以再分,是容易变的;而原子是不变的,并且分子是由原子构成的,离子是由原子得失电子后形成的,所以原子才是组成世界万物的元素。
观点 2
原子核中质子数相同的原子在化学变化中表现出来的性质几乎完全相同。
把具有相同质子数的原子归为一类,每一类原子称为一种元素。
质子数为 1 的一类原子
氢元素
质子数为 6 的一类原子
碳元素
质子数为 8 的一类原子
氧元素
水 H2O
由氢和氧两种元素组成
二氧化碳 CO2
由碳和氧两种元素组成
有些物质,如氢气、氧气、碳等,只由一种元素组成,属于单质。
有些物质,如水、二氧化碳、氯化钠等,由两种或两种以上元素组成,属于化合物。
物质
混合物
纯净物
单质
化合物
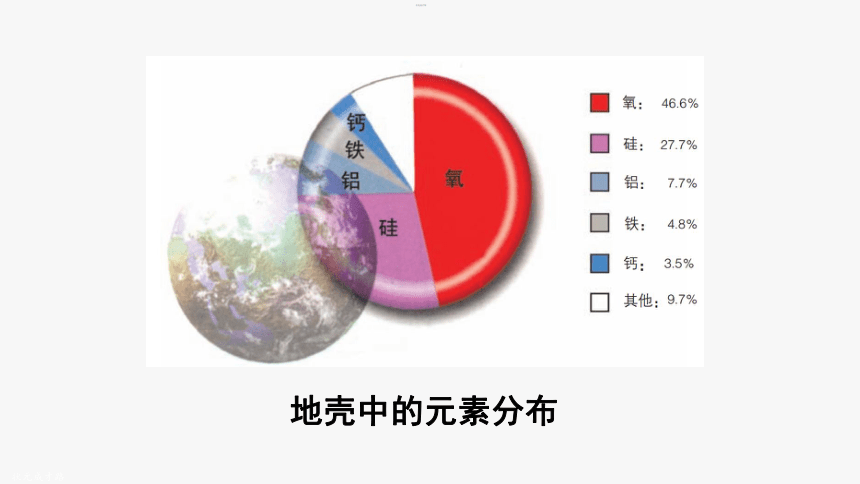
地壳中的元素分布
为方便区分和交流,国际上规定每种元素都采用统一的符号来表示,这种符号叫做元素符号。
H
O
氢元素
氧元素
元素符号能表示一种元素,还能表示这种元素的一个原子。
Cl
表示氯元素
表示一个氯原子
【总结】
①元素只讲种类,不讲个数;原子既讲种类又讲个数。
②原子用于描述物质的微观结构;元素用于描述物质的宏观组成。
+19
2 8 8 1
+20
2 8 8 2
氢(H)
氦(He)
锂(Li)
铍(Be)
硼(B)
碳(C)
氮(N)
氧(O)
氟(F)
氖(Ne)
钠(Na)
镁(Mg)
铝(Al)
硅(Si)
磷(P)
硫(S)
氯(Cl)
氩(Ar)
钾(K)
钙(Ca)
一些常见元素的名称、符号和原子结构示意图
化学元素汉语名称的由来
氢(H)、氧(O)、钠(Na)等化学元素的汉语名称,是我国近代化学先驱徐寿创造的。
徐寿(1818 – 1884)
1869年,徐寿在翻译《化学鉴原》时发现大部分元素在汉语中没有对应的名称。于是,他把化学元素进行了分类:
(1)对于金、银、铜、铁、锡、铅、硫等国人早已定名的元素,继续沿用旧名。
(2)对于一些有特定性质的元素,则采用意译的方式,如轻气、养气、淡气等(后来分别演变为氢、氧、氮,但仍保持原字的读音)。
(3)对于其他元素,将元素的英文名称的首音节或次音节译为发音类似的汉字,再加以汉字部首大致区分元素的类别。
例如:凡是金属元素(汞除外)均使用 “钅”部首;而非金属元素则分别加“气” “氵”或“石”部首,以表示其单质在通常状况下的存在状态是气态、液态或固态,如硒、碘、钙、铍、锂、钠、镍等元素名称都是根据这一原则创造的。
元素周期表简介
1869 年,俄国化学家门捷列夫在前人研究的基础上,把当时已经发现的 63 种元素按照相对原子质量由小到大的顺序排列起来,并分成几行,使性质相似的元素排在同一列中,从而得到第一张元素周期表。
原子序数
(核电荷数)
元素符号
元素名称
相对原子质量
原子序数=核电荷数=核内质子数=核外电子数
如今的元素周期表是把目前已发现并被正式命名的 112 种元素按照原子核内质子数由小到大的顺序排列而成的,共有 7 个横行、18个纵行,每一个横行叫做一个周期,每一个纵行叫做一个族。
元素周期表是学习和研究化学、探索未知世界最有力的工具之一。它为发现新的元素和化合物、预测新元素的结构和性质提供了线索,为我们深入学习和掌握物质性质及其变化规律提供理论指导。
随堂演练
1.(1)写出下面符号表示的含义。
①Cl , ;
②2Fe ;nS 。
(2)上述符号中既表示宏观意义,又表示微观意义的是 ,只表示微观含义的是 。
(3)请写出一种既能表示一种元素,又能表示该元素的一个原子,还能表示这种单质的元素符号 。
氯元素
一个氯原子
2个铁原子
n个硫原子
Cl
2Fe、nS
Hg(或Na等)
2. 元素周期表是学习和研究化学的重要工具,试根据图示回答相应问题:
(1)图甲是铯元素在元素周期表中的信息,则铯元素属于 (填“金属”或“非金属”)元素,该元素原子的核外电子数为 。
金属
55
(2)图乙为元素周期表的一部分,X、Y、Z 代表三种不同元素,以下 判断正确。
A. 原子序数 Z>Y
B. 核外电子数:X = Y
C. Y 和 Z 处于同一周期
AC
课后作业
1.完成课本的练习;
2.完成练习册本课时的习题.
鲁教版·九年级化学上册
新课导入
人们很早就意识到,所有物质都是由几种亘古不变的基本成分 ——“元素”组成的。
水
火
土
气
元素——究竟是什么?
新课探究
元素与元素符号
组成物质世界的元素究竟是什么?
所有的物质都是由原子、分子、离子等基本粒子构成的,这些基本粒子才是组成物质的元素。
观点 1
分子在化学变化中可以再分,是容易变的;而原子是不变的,并且分子是由原子构成的,离子是由原子得失电子后形成的,所以原子才是组成世界万物的元素。
观点 2
原子核中质子数相同的原子在化学变化中表现出来的性质几乎完全相同。
把具有相同质子数的原子归为一类,每一类原子称为一种元素。
质子数为 1 的一类原子
氢元素
质子数为 6 的一类原子
碳元素
质子数为 8 的一类原子
氧元素
水 H2O
由氢和氧两种元素组成
二氧化碳 CO2
由碳和氧两种元素组成
有些物质,如氢气、氧气、碳等,只由一种元素组成,属于单质。
有些物质,如水、二氧化碳、氯化钠等,由两种或两种以上元素组成,属于化合物。
物质
混合物
纯净物
单质
化合物
地壳中的元素分布
为方便区分和交流,国际上规定每种元素都采用统一的符号来表示,这种符号叫做元素符号。
H
O
氢元素
氧元素
元素符号能表示一种元素,还能表示这种元素的一个原子。
Cl
表示氯元素
表示一个氯原子
【总结】
①元素只讲种类,不讲个数;原子既讲种类又讲个数。
②原子用于描述物质的微观结构;元素用于描述物质的宏观组成。
+19
2 8 8 1
+20
2 8 8 2
氢(H)
氦(He)
锂(Li)
铍(Be)
硼(B)
碳(C)
氮(N)
氧(O)
氟(F)
氖(Ne)
钠(Na)
镁(Mg)
铝(Al)
硅(Si)
磷(P)
硫(S)
氯(Cl)
氩(Ar)
钾(K)
钙(Ca)
一些常见元素的名称、符号和原子结构示意图
化学元素汉语名称的由来
氢(H)、氧(O)、钠(Na)等化学元素的汉语名称,是我国近代化学先驱徐寿创造的。
徐寿(1818 – 1884)
1869年,徐寿在翻译《化学鉴原》时发现大部分元素在汉语中没有对应的名称。于是,他把化学元素进行了分类:
(1)对于金、银、铜、铁、锡、铅、硫等国人早已定名的元素,继续沿用旧名。
(2)对于一些有特定性质的元素,则采用意译的方式,如轻气、养气、淡气等(后来分别演变为氢、氧、氮,但仍保持原字的读音)。
(3)对于其他元素,将元素的英文名称的首音节或次音节译为发音类似的汉字,再加以汉字部首大致区分元素的类别。
例如:凡是金属元素(汞除外)均使用 “钅”部首;而非金属元素则分别加“气” “氵”或“石”部首,以表示其单质在通常状况下的存在状态是气态、液态或固态,如硒、碘、钙、铍、锂、钠、镍等元素名称都是根据这一原则创造的。
元素周期表简介
1869 年,俄国化学家门捷列夫在前人研究的基础上,把当时已经发现的 63 种元素按照相对原子质量由小到大的顺序排列起来,并分成几行,使性质相似的元素排在同一列中,从而得到第一张元素周期表。
原子序数
(核电荷数)
元素符号
元素名称
相对原子质量
原子序数=核电荷数=核内质子数=核外电子数
如今的元素周期表是把目前已发现并被正式命名的 112 种元素按照原子核内质子数由小到大的顺序排列而成的,共有 7 个横行、18个纵行,每一个横行叫做一个周期,每一个纵行叫做一个族。
元素周期表是学习和研究化学、探索未知世界最有力的工具之一。它为发现新的元素和化合物、预测新元素的结构和性质提供了线索,为我们深入学习和掌握物质性质及其变化规律提供理论指导。
随堂演练
1.(1)写出下面符号表示的含义。
①Cl , ;
②2Fe ;nS 。
(2)上述符号中既表示宏观意义,又表示微观意义的是 ,只表示微观含义的是 。
(3)请写出一种既能表示一种元素,又能表示该元素的一个原子,还能表示这种单质的元素符号 。
氯元素
一个氯原子
2个铁原子
n个硫原子
Cl
2Fe、nS
Hg(或Na等)
2. 元素周期表是学习和研究化学的重要工具,试根据图示回答相应问题:
(1)图甲是铯元素在元素周期表中的信息,则铯元素属于 (填“金属”或“非金属”)元素,该元素原子的核外电子数为 。
金属
55
(2)图乙为元素周期表的一部分,X、Y、Z 代表三种不同元素,以下 判断正确。
A. 原子序数 Z>Y
B. 核外电子数:X = Y
C. Y 和 Z 处于同一周期
AC
课后作业
1.完成课本的练习;
2.完成练习册本课时的习题.
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
