人教版九年级下册化学《 10.2 酸和碱的中和反应》课件(37张PPT)
文档属性
| 名称 | 人教版九年级下册化学《 10.2 酸和碱的中和反应》课件(37张PPT) |
|
|
| 格式 | ppt | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-09-10 00:00:00 | ||
图片预览







文档简介
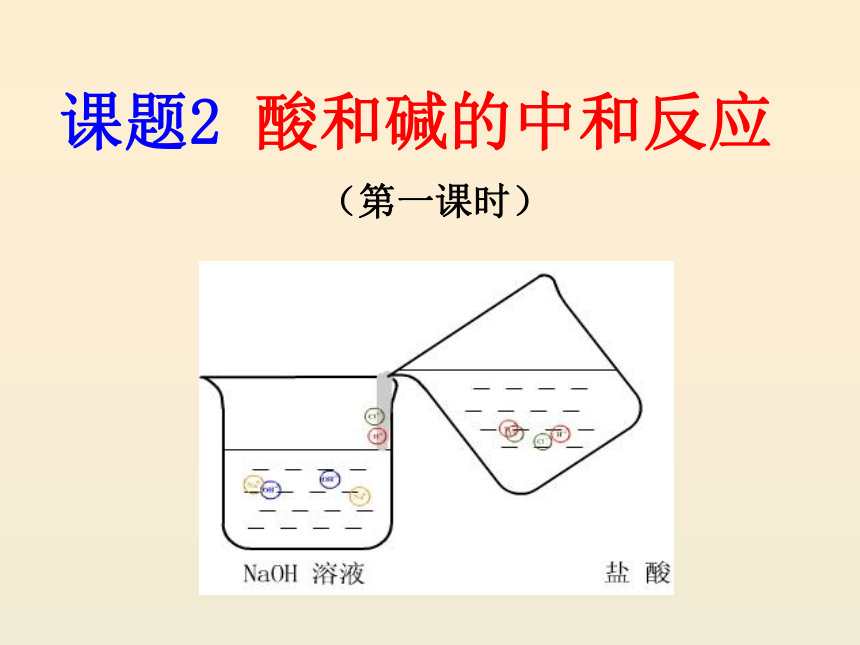
(共37张PPT)
课题2 酸和碱的中和反应
(第一课时)
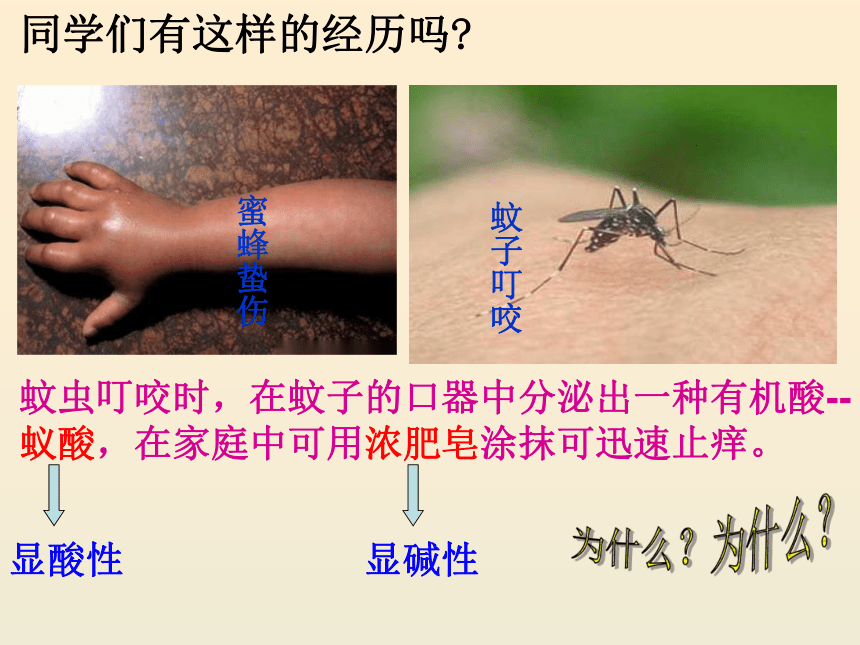
同学们有这样的经历吗
蜜蜂蛰伤
蚊子叮咬
蚊虫叮咬时,在蚊子的口器中分泌出一种有机酸--蚁酸,在家庭中可用浓肥皂涂抹可迅速止痒。
显碱性
显酸性
学习目标
1、知道酸和碱之间发生的中和反应
2、了解中和反应的实质
3、了解中和反应在实际中的应用
自学指导一
请大家阅读课本P60与P61第一段的有关中和反应,2分钟后回答:
1、认真观察实验10-8,能够正确描述现象,
并进行分析相关问题
2、熟记中和反应的定义
3、知道中和反应的实质是什么?
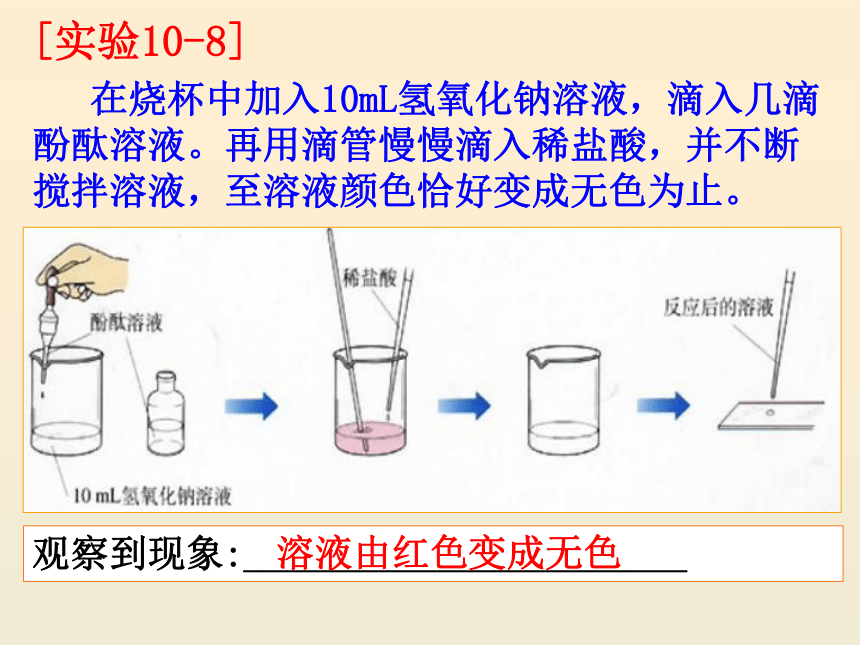
[实验10-8]
在烧杯中加入10mL氢氧化钠溶液,滴入几滴酚酞溶液。再用滴管慢慢滴入稀盐酸,并不断搅拌溶液,至溶液颜色恰好变成无色为止。
观察到现象:_______________________
溶液由红色变成无色
答:防止稀盐酸滴加过量。
答:显色作用。
2. 为什么在操作中必须逐滴滴入稀盐酸?
1. 酚酞在实验中起什么作用?
注意: 滴加盐酸至红色恰好变成无色时即止。
否则盐酸过量。
讨论:
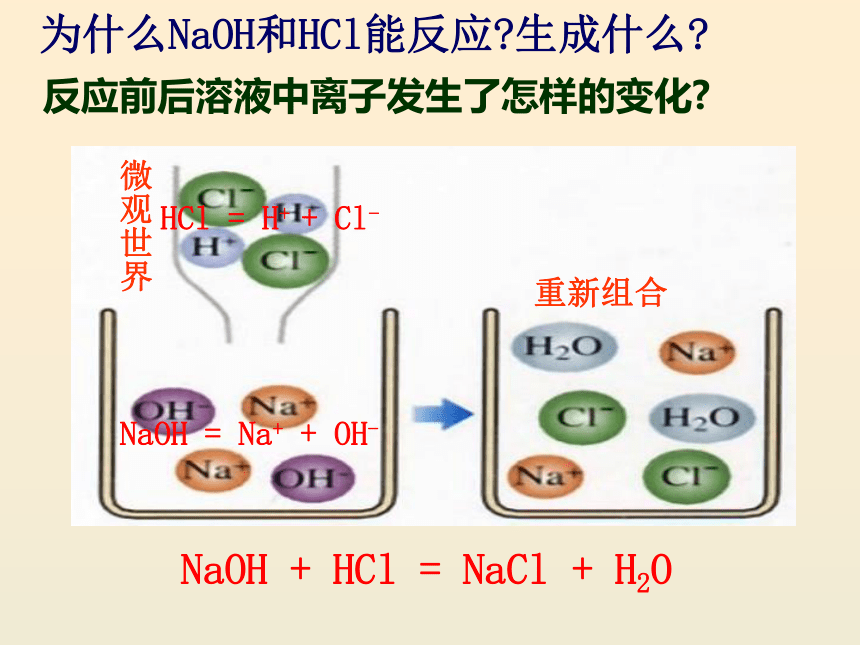
为什么NaOH和HCl能反应 生成什么
反应前后溶液中离子发生了怎样的变化
重新组合
微观世界
NaOH = Na+ + OH-
HCl = H+ + Cl-
NaOH + HCl = NaCl + H2O
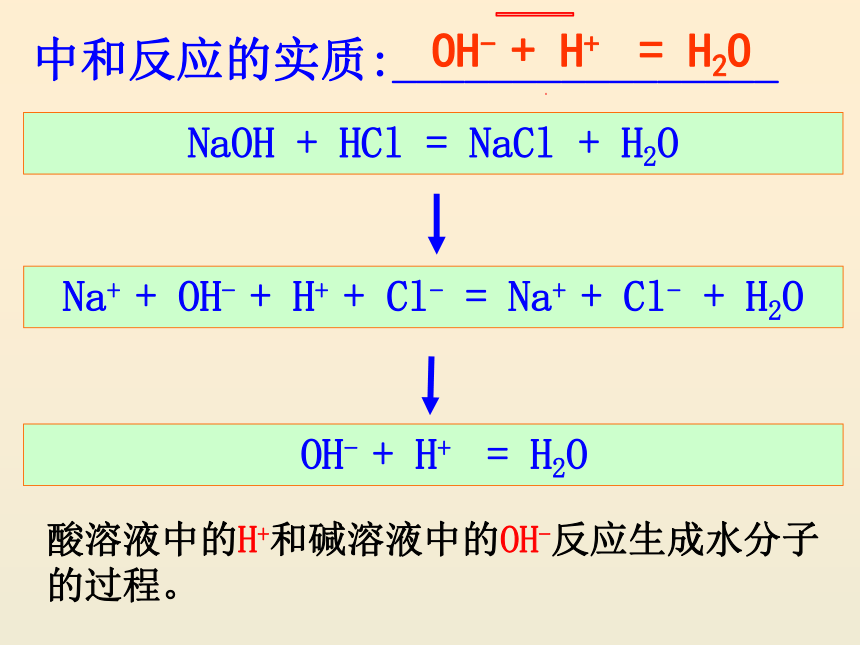
中和反应的实质:________________
酸溶液中的H+和碱溶液中的OH-反应生成水分子的过程。
NaOH + HCl = NaCl + H2O
Na+ + OH- + H+ + Cl- = Na+ + Cl- + H2O
OH- + H+ = H2O
OH- + H+ = H2O
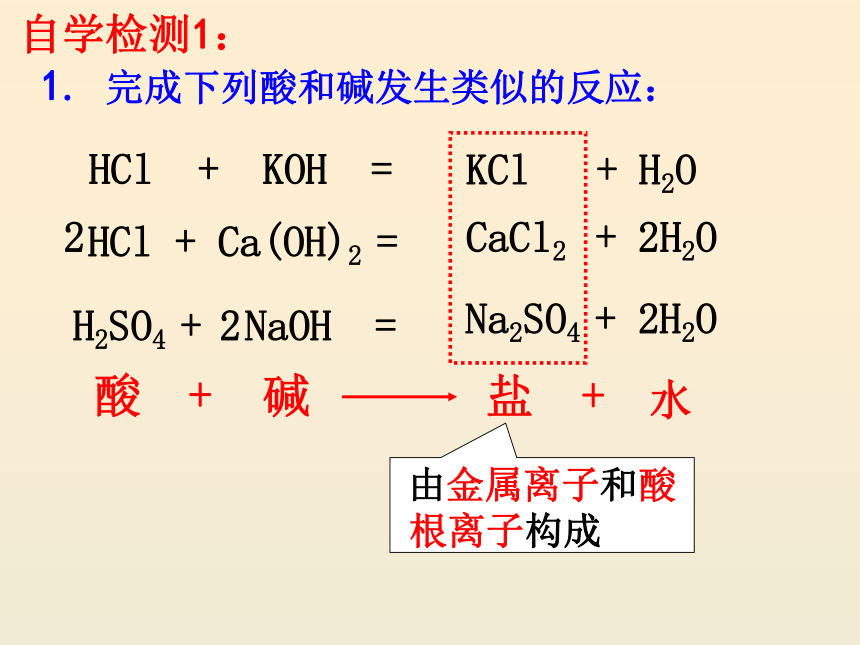
HCl + KOH =
HCl + Ca(OH)2 =
KCl + H2O
CaCl2 + 2H2O
2
2
盐
酸
碱
水
+
+
由金属离子和酸
根离子构成
H2SO4 + NaOH =
Na2SO4 + 2H2O
自学检测1:
1. 完成下列酸和碱发生类似的反应:
什么叫盐?什么叫中和反应?
酸 + 碱 → 盐 + 水
1.盐:
______________________________________
2.中和反应:
________________________________
如:KNO3、 NaCl、 KMnO4、 KClO3、 CuSO4、
NH4NO3、 NH4HCO3、 Cu2(OH)2CO3
由金属离子和酸根离子构成的化合物。
酸和碱作用生成盐和水的反应。
自学检测:
2.下列反应是不是中和反应?说明理由
① Fe2O3 + 6HCl = 2FeCl3 + 3H2O
② CO2 + Ca(OH)2 = CaCO3↓+ H2O
③ Ca(OH)2 + H2SO4 = CaSO4 + 2H2O
不是;反应物不是酸和碱
不是;反应物不是酸和碱
是;反应物是酸和碱且生成了盐和水
启示:有盐和水生成的反应不一定是中和反应
3.下列各组物质通常借助指示剂才能证明发生
反应的是( )
A、氢氧化铜和稀盐酸 B、石灰石和稀盐酸
C、氢氧化钙与二氧化碳反应
D、烧碱和稀硫酸
D
4.下列反应中属于中和反应的是( )
A、Zn + 2HCl = ZnCl2 + H2↑
B、CuO + 2HCl = CuCl2 + H2O
C、Ba(OH)2+ H2SO4 = BaSO4↓+ 2H2O
D、AgNO3 + HCl = AgCl↓+ HNO3
5.下列物质属于盐的是( )
A、HCl B、CuO C、BaSO4 D、Al(OH)3
C
C
自学检测:
自学指导二
请大家阅读课本P61有关“中和反应在实际中的应用”这部分的内容,2分钟后:
1、记住中和反应在实际中的具体应用
2、完成当堂练习
二、中和反应在实际中的应用
1、改变土壤的酸碱性
植物需要在一定酸碱性的土壤中生长,但近年来由于不合理使用化肥,或酸雨的形成,破坏土壤的酸碱性,不利于植物的生长,应怎样去改变酸性土壤?
用熟石灰中和:____________________________
①能用生石灰代替熟石灰吗?为什么?
可以; CaO + H2O ==Ca(OH)2
②能否用NaOH代替熟石灰?为什么?
不能;
NaOH具有强烈的腐蚀性,影响农作物的生长,同时造价相对熟石灰较高,来源不够广泛。
Ca(OH)2+ 2HCl = CaCl2 + 2H2O
2、处理工厂的废水
某硫酸厂排出的废水中含有硫酸等杂质,严重危害当地的生态环境,你会怎样处理这些废水呢?
用熟石灰进行中和:________________________
Ca(OH)2+H2SO4=CaSO4+2H2O
3、用于医药
(1)胃酸的主要成分是盐酸。
胃药的主要成分氢氧化铝。
氢氧化铝能中和酸:_________________________
Al(OH)3+3HCl=AlCl3+3H2O
(2)被蚊虫叮咬后,涂一些含有碱性的物质的药水。
氨水、肥皂水等
如:________________________
讨论:举出生活中利用中和反应的实例
成份:氢氧化铝等
1.斯达舒治疗胃酸过多症:
2、在以前家里做面食的时候要放碱面.因为发酵好的馒头是酸性的;要用碱面中和一下,才不会有酸酸的味道
3、松花蛋加工的主要原料:食盐、纯碱、生石灰、水等。吃皮蛋时有涩味,可加点食醋中和其碱性,变得美味爽口
BC
1.一些国家正在试用碳酸水浇灌某些植物,其作
用是( )A.改良酸性土壤 B.改良碱性土壤
C.促进植物的光合作用 D.在植物上方形成温室
2.某同学不小心被黄蜂蛰了(黄蜂毒液呈碱性),为了减轻疼痛可以涂抹( )
A.浓硫酸 B食醋 C.食盐水 D.肥皂水
3.下列关于物质的用途的叙述不正确的是( )
A.盐酸可用来除铁锈
B.稀硫酸在实验室里常用作干燥剂
C.氢氧化钠可用作制肥皂和造纸工业
D.生石灰可用来改良酸性土壤
B
B
自学检测2:
名称 氢氧化钠 硫酸 氧化铁
化学式 CuSO4
类别
1.下列物质属于盐的是( )
A CuO B Cu(OH)2 C CuSO4 D HCl
2.填写下表(类别按酸、碱、盐、氧化物填写)
堂堂清
3.完成下列化学方程式:
① Cu(OH)2 + H2SO4 = _____ + _____
② KOH + _____ = K2SO4 + _____
③用稀盐酸除水垢(主要成分是碳酸钙和氢氧化镁)
课题2 酸和碱的中和反应
(第二课时)
学习目标
1、了解酸碱度的含义、PH的变化范围与酸碱
度的关系
2、学会用pH试纸检验溶液的酸碱度
3、了解溶液酸碱度在实际中的意义
学习重点
会用pH试纸检验溶液的酸碱度
自学指导 一
1
快速阅读课本P61- 62有关“溶液酸碱度的表示法”内容,5分钟后记住下列内容:
1、利用酸碱指示剂只能试验溶液 _______,却
不能精确地检验溶液的________________(即
溶液酸碱度)。
2、溶液酸碱度的表示方法是_____。
3、pH的范围是:________。
4、测定pH最简便的方法是使用 ________。
测定时,在白瓷板或玻璃片上放一小片pH试纸,用_________将待测液滴到该试纸上,把试纸 显示的颜色与_____________对照,即可得出
待测液的_____。
酸碱性
酸碱性强弱程度
pH
0~14
pH试纸
pH
玻璃棒
标准比色卡
中性溶液pH = 7
碱性溶液pH﹥7: pH越大,碱性越强。
酸性溶液pH﹤7: pH越小,酸性越强。
溶液的酸碱性与pH的关系:
活动与探究:用PH试纸测定一些溶液的pH
(1)测定几种稀溶液的pH:
pH pH pH
稀硫酸 稀盐酸 氢氧化钠溶液
pH的测定方法:
pH试纸(精确度:1)
pH计(精确度:0.01)
当堂练习:
1.某溶液的pH=3,则该溶液( )
A.呈酸性 B.呈碱性 C.呈中性 D.无法判定
2.已知苹果汁的近似pH为2.9~3.3,在苹果汁中滴入紫色石蕊试液,显示的颜色( )
A.无色 B.红色 C.蓝色 D.紫色
3.下列各PH表示溶液酸性最强的是( )
A.pH=14 B.pH=7 C.pH=1 D.pH=0
A
B
D
自学指导二
请大家阅读课本P63-P64有关的内容,3分钟后:
1、了解身边常见物质及人体体液和排泄物
的pH:
2、了解溶液的酸碱度有哪些重要意义?
3、了解洗发剂和护发剂的酸碱性
实验10-10:测定生活中的一些物质的PH,说明
它们的酸碱性:
PH 酸碱性 PH 酸碱性
橘汁 3 汽水 6
糖水 7 自来水 7
牛奶 7 唾液 7
番茄汁 6 草木灰水 11
肥皂水 10 洗洁精 12
1.身边常见物质的pH
2.人体内的一些液体和排泄物的正常pH范围
血浆 7.35~7.45
唾液 6.6 ~ 7.1
胃液 0.9 ~ 1.5
乳汁 6.6 ~ 7.6
胆汁 7.1 ~ 7.3
胰液 7.5 ~ 8.0
尿液 4.7 ~ 8.4
粪便 4.6 ~ 8.4
3.了解溶液的酸碱度的重要意义
1、化工生产中许多反应必须在一定的pH 溶液里才能进行。
2、农业生产中,农作物一般适宜在___________的土壤里生长。
3、测定雨水的pH,可以了解空气的污染情况。
4、测定人体液的pH,可以了解人体的健康状况。
pH为7或接近7
正常雨水的pH______;为什么不是等于7?原因是:空气的CO2与雨水反应。反应方程式为 ___________________.酸雨的pH_______,形成酸雨的主要气体是___________.
≈5.6
CO2+H2O=H2CO3
<5.6
SO2 、NO2
探究:洗发剂和护发剂的酸碱度(P64)
一.测一测洗发剂或护发剂的PH:
二.讨论:
1.一般情况下,我们使用的洗发用品是酸性还是碱
性的?
2.洗发时,为什么用过洗发剂后再用护发剂对头发
有保护作用?
3.从清洁效果和护发的角度考虑,你应该怎样使用
洗发用品?
一般情况下,洗发剂是弱碱性的;护发剂是弱酸性的。
洗发剂显碱性,容易侵蚀头发。用过洗发剂后再用显
酸性的护发剂中和头发上的洗发剂,对头发有保护作用。
先用弱碱性的洗发剂清洁头发,再用弱酸性的护发剂
调节头发和毛皮的酸碱平衡,从而保护头发。
当堂训练2:
C
1.一些食物的近似pH如下:番茄4.0-4.4,苹果是
2.9-3.3,牛奶是6.3-6.6,蛋清是7.6-8.0,下
列不正确的是( )
A.胃酸过多的人应少食苹果
B.番茄汁属酸性食品
C.牛奶和鸡蛋清均属碱性食品
D.苹果汁酸性比牛奶强
2.二氧化碳饱和溶液的pH=5.6,酸性比其强的
雨水称为酸雨。一场雨后从甲地测得雨水的
pH=4,乙地测得雨水的pH=6.6,则( )
A.甲地酸雨 B.乙地酸雨
C.均是酸雨 D.都不是酸雨
A
3.有一瓶无色溶液的PH是4.5,取少量注入试
管中,再滴入几滴酚酞试液,溶液呈____色,
如果要使试管中溶液的PH升为10,可以采取
__________________的方法。
无
滴加PH>10碱溶液
4.有一瓶无色溶液的PH是9.5,取少量注入试
管中,再滴入几滴酚酞试液,溶液呈____色,
如果要使试管中溶液的PH降为5,可以采取
__________________的方法。
红
滴加PH<5酸溶液
5.将一定量PH=3和PH=8的两种溶液混合后,溶
液的PH可能是( )
A PH=2 B PH=6 C PH=8 D PH=11
B
6.向氢氧化钠溶液中滴加稀盐酸至过量。下列各图中能表示溶液的pH与所加稀盐酸体积的关系的是( )
A
7.向盐酸中滴加蒸馏水至过量。下列各图中能表示溶液的pH与所加蒸馏水体积的关系的是( )
D
7.在用稀盐酸和氢氧化钠溶液进行中和反应实验时,反
应过程中溶液的酸碱度变化如图13所示。
(1)该反应的化学方程为:_____________________。
(2)该实验操作是将___________滴加到另一种溶液中
(3)当加入溶液的质量为a g时,所得溶液中的溶质为
(写化学式)_____________。
(4)当加入溶液的质量为b g时,
向所得溶液中滴加酚酞溶液,
溶液呈_____色。
NaOH+HCl=NaCl+H2O
氢氧化钠溶液
HCl、NaCl
红
堂堂清
1、用pH试纸测定白醋的酸碱度时,如先将试纸
用蒸馏水润湿,再把白醋滴到试纸上,则测得
的结果与白醋实际的pH比较( )
A.偏低 B.偏高 C.相等 D.无法比较
2、两种溶液混合后pH=7,这两种溶液的pH可能
是( )
A.pH=0和pH=7 B.pH=5和pH=6
C.pH=8和pH=10 D.pH=4和pH=13
3、下列物质分别溶于水,pH大于7的是( )
A.SO3 B.CO2 C.HCl D.CaO
4.小明同学为测定某稀盐酸的质量分数,向
7.3克的该稀盐酸中逐渐滴加20%的氢氧化钠
溶液,反应后溶液的PH值与加入的氢氧化钠
溶液的质量关系如图:
求:稀盐酸的质量分数为多少?
PH
7
0
20g
m
课题2 酸和碱的中和反应
(第一课时)
同学们有这样的经历吗
蜜蜂蛰伤
蚊子叮咬
蚊虫叮咬时,在蚊子的口器中分泌出一种有机酸--蚁酸,在家庭中可用浓肥皂涂抹可迅速止痒。
显碱性
显酸性
学习目标
1、知道酸和碱之间发生的中和反应
2、了解中和反应的实质
3、了解中和反应在实际中的应用
自学指导一
请大家阅读课本P60与P61第一段的有关中和反应,2分钟后回答:
1、认真观察实验10-8,能够正确描述现象,
并进行分析相关问题
2、熟记中和反应的定义
3、知道中和反应的实质是什么?
[实验10-8]
在烧杯中加入10mL氢氧化钠溶液,滴入几滴酚酞溶液。再用滴管慢慢滴入稀盐酸,并不断搅拌溶液,至溶液颜色恰好变成无色为止。
观察到现象:_______________________
溶液由红色变成无色
答:防止稀盐酸滴加过量。
答:显色作用。
2. 为什么在操作中必须逐滴滴入稀盐酸?
1. 酚酞在实验中起什么作用?
注意: 滴加盐酸至红色恰好变成无色时即止。
否则盐酸过量。
讨论:
为什么NaOH和HCl能反应 生成什么
反应前后溶液中离子发生了怎样的变化
重新组合
微观世界
NaOH = Na+ + OH-
HCl = H+ + Cl-
NaOH + HCl = NaCl + H2O
中和反应的实质:________________
酸溶液中的H+和碱溶液中的OH-反应生成水分子的过程。
NaOH + HCl = NaCl + H2O
Na+ + OH- + H+ + Cl- = Na+ + Cl- + H2O
OH- + H+ = H2O
OH- + H+ = H2O
HCl + KOH =
HCl + Ca(OH)2 =
KCl + H2O
CaCl2 + 2H2O
2
2
盐
酸
碱
水
+
+
由金属离子和酸
根离子构成
H2SO4 + NaOH =
Na2SO4 + 2H2O
自学检测1:
1. 完成下列酸和碱发生类似的反应:
什么叫盐?什么叫中和反应?
酸 + 碱 → 盐 + 水
1.盐:
______________________________________
2.中和反应:
________________________________
如:KNO3、 NaCl、 KMnO4、 KClO3、 CuSO4、
NH4NO3、 NH4HCO3、 Cu2(OH)2CO3
由金属离子和酸根离子构成的化合物。
酸和碱作用生成盐和水的反应。
自学检测:
2.下列反应是不是中和反应?说明理由
① Fe2O3 + 6HCl = 2FeCl3 + 3H2O
② CO2 + Ca(OH)2 = CaCO3↓+ H2O
③ Ca(OH)2 + H2SO4 = CaSO4 + 2H2O
不是;反应物不是酸和碱
不是;反应物不是酸和碱
是;反应物是酸和碱且生成了盐和水
启示:有盐和水生成的反应不一定是中和反应
3.下列各组物质通常借助指示剂才能证明发生
反应的是( )
A、氢氧化铜和稀盐酸 B、石灰石和稀盐酸
C、氢氧化钙与二氧化碳反应
D、烧碱和稀硫酸
D
4.下列反应中属于中和反应的是( )
A、Zn + 2HCl = ZnCl2 + H2↑
B、CuO + 2HCl = CuCl2 + H2O
C、Ba(OH)2+ H2SO4 = BaSO4↓+ 2H2O
D、AgNO3 + HCl = AgCl↓+ HNO3
5.下列物质属于盐的是( )
A、HCl B、CuO C、BaSO4 D、Al(OH)3
C
C
自学检测:
自学指导二
请大家阅读课本P61有关“中和反应在实际中的应用”这部分的内容,2分钟后:
1、记住中和反应在实际中的具体应用
2、完成当堂练习
二、中和反应在实际中的应用
1、改变土壤的酸碱性
植物需要在一定酸碱性的土壤中生长,但近年来由于不合理使用化肥,或酸雨的形成,破坏土壤的酸碱性,不利于植物的生长,应怎样去改变酸性土壤?
用熟石灰中和:____________________________
①能用生石灰代替熟石灰吗?为什么?
可以; CaO + H2O ==Ca(OH)2
②能否用NaOH代替熟石灰?为什么?
不能;
NaOH具有强烈的腐蚀性,影响农作物的生长,同时造价相对熟石灰较高,来源不够广泛。
Ca(OH)2+ 2HCl = CaCl2 + 2H2O
2、处理工厂的废水
某硫酸厂排出的废水中含有硫酸等杂质,严重危害当地的生态环境,你会怎样处理这些废水呢?
用熟石灰进行中和:________________________
Ca(OH)2+H2SO4=CaSO4+2H2O
3、用于医药
(1)胃酸的主要成分是盐酸。
胃药的主要成分氢氧化铝。
氢氧化铝能中和酸:_________________________
Al(OH)3+3HCl=AlCl3+3H2O
(2)被蚊虫叮咬后,涂一些含有碱性的物质的药水。
氨水、肥皂水等
如:________________________
讨论:举出生活中利用中和反应的实例
成份:氢氧化铝等
1.斯达舒治疗胃酸过多症:
2、在以前家里做面食的时候要放碱面.因为发酵好的馒头是酸性的;要用碱面中和一下,才不会有酸酸的味道
3、松花蛋加工的主要原料:食盐、纯碱、生石灰、水等。吃皮蛋时有涩味,可加点食醋中和其碱性,变得美味爽口
BC
1.一些国家正在试用碳酸水浇灌某些植物,其作
用是( )A.改良酸性土壤 B.改良碱性土壤
C.促进植物的光合作用 D.在植物上方形成温室
2.某同学不小心被黄蜂蛰了(黄蜂毒液呈碱性),为了减轻疼痛可以涂抹( )
A.浓硫酸 B食醋 C.食盐水 D.肥皂水
3.下列关于物质的用途的叙述不正确的是( )
A.盐酸可用来除铁锈
B.稀硫酸在实验室里常用作干燥剂
C.氢氧化钠可用作制肥皂和造纸工业
D.生石灰可用来改良酸性土壤
B
B
自学检测2:
名称 氢氧化钠 硫酸 氧化铁
化学式 CuSO4
类别
1.下列物质属于盐的是( )
A CuO B Cu(OH)2 C CuSO4 D HCl
2.填写下表(类别按酸、碱、盐、氧化物填写)
堂堂清
3.完成下列化学方程式:
① Cu(OH)2 + H2SO4 = _____ + _____
② KOH + _____ = K2SO4 + _____
③用稀盐酸除水垢(主要成分是碳酸钙和氢氧化镁)
课题2 酸和碱的中和反应
(第二课时)
学习目标
1、了解酸碱度的含义、PH的变化范围与酸碱
度的关系
2、学会用pH试纸检验溶液的酸碱度
3、了解溶液酸碱度在实际中的意义
学习重点
会用pH试纸检验溶液的酸碱度
自学指导 一
1
快速阅读课本P61- 62有关“溶液酸碱度的表示法”内容,5分钟后记住下列内容:
1、利用酸碱指示剂只能试验溶液 _______,却
不能精确地检验溶液的________________(即
溶液酸碱度)。
2、溶液酸碱度的表示方法是_____。
3、pH的范围是:________。
4、测定pH最简便的方法是使用 ________。
测定时,在白瓷板或玻璃片上放一小片pH试纸,用_________将待测液滴到该试纸上,把试纸 显示的颜色与_____________对照,即可得出
待测液的_____。
酸碱性
酸碱性强弱程度
pH
0~14
pH试纸
pH
玻璃棒
标准比色卡
中性溶液pH = 7
碱性溶液pH﹥7: pH越大,碱性越强。
酸性溶液pH﹤7: pH越小,酸性越强。
溶液的酸碱性与pH的关系:
活动与探究:用PH试纸测定一些溶液的pH
(1)测定几种稀溶液的pH:
pH pH pH
稀硫酸 稀盐酸 氢氧化钠溶液
pH的测定方法:
pH试纸(精确度:1)
pH计(精确度:0.01)
当堂练习:
1.某溶液的pH=3,则该溶液( )
A.呈酸性 B.呈碱性 C.呈中性 D.无法判定
2.已知苹果汁的近似pH为2.9~3.3,在苹果汁中滴入紫色石蕊试液,显示的颜色( )
A.无色 B.红色 C.蓝色 D.紫色
3.下列各PH表示溶液酸性最强的是( )
A.pH=14 B.pH=7 C.pH=1 D.pH=0
A
B
D
自学指导二
请大家阅读课本P63-P64有关的内容,3分钟后:
1、了解身边常见物质及人体体液和排泄物
的pH:
2、了解溶液的酸碱度有哪些重要意义?
3、了解洗发剂和护发剂的酸碱性
实验10-10:测定生活中的一些物质的PH,说明
它们的酸碱性:
PH 酸碱性 PH 酸碱性
橘汁 3 汽水 6
糖水 7 自来水 7
牛奶 7 唾液 7
番茄汁 6 草木灰水 11
肥皂水 10 洗洁精 12
1.身边常见物质的pH
2.人体内的一些液体和排泄物的正常pH范围
血浆 7.35~7.45
唾液 6.6 ~ 7.1
胃液 0.9 ~ 1.5
乳汁 6.6 ~ 7.6
胆汁 7.1 ~ 7.3
胰液 7.5 ~ 8.0
尿液 4.7 ~ 8.4
粪便 4.6 ~ 8.4
3.了解溶液的酸碱度的重要意义
1、化工生产中许多反应必须在一定的pH 溶液里才能进行。
2、农业生产中,农作物一般适宜在___________的土壤里生长。
3、测定雨水的pH,可以了解空气的污染情况。
4、测定人体液的pH,可以了解人体的健康状况。
pH为7或接近7
正常雨水的pH______;为什么不是等于7?原因是:空气的CO2与雨水反应。反应方程式为 ___________________.酸雨的pH_______,形成酸雨的主要气体是___________.
≈5.6
CO2+H2O=H2CO3
<5.6
SO2 、NO2
探究:洗发剂和护发剂的酸碱度(P64)
一.测一测洗发剂或护发剂的PH:
二.讨论:
1.一般情况下,我们使用的洗发用品是酸性还是碱
性的?
2.洗发时,为什么用过洗发剂后再用护发剂对头发
有保护作用?
3.从清洁效果和护发的角度考虑,你应该怎样使用
洗发用品?
一般情况下,洗发剂是弱碱性的;护发剂是弱酸性的。
洗发剂显碱性,容易侵蚀头发。用过洗发剂后再用显
酸性的护发剂中和头发上的洗发剂,对头发有保护作用。
先用弱碱性的洗发剂清洁头发,再用弱酸性的护发剂
调节头发和毛皮的酸碱平衡,从而保护头发。
当堂训练2:
C
1.一些食物的近似pH如下:番茄4.0-4.4,苹果是
2.9-3.3,牛奶是6.3-6.6,蛋清是7.6-8.0,下
列不正确的是( )
A.胃酸过多的人应少食苹果
B.番茄汁属酸性食品
C.牛奶和鸡蛋清均属碱性食品
D.苹果汁酸性比牛奶强
2.二氧化碳饱和溶液的pH=5.6,酸性比其强的
雨水称为酸雨。一场雨后从甲地测得雨水的
pH=4,乙地测得雨水的pH=6.6,则( )
A.甲地酸雨 B.乙地酸雨
C.均是酸雨 D.都不是酸雨
A
3.有一瓶无色溶液的PH是4.5,取少量注入试
管中,再滴入几滴酚酞试液,溶液呈____色,
如果要使试管中溶液的PH升为10,可以采取
__________________的方法。
无
滴加PH>10碱溶液
4.有一瓶无色溶液的PH是9.5,取少量注入试
管中,再滴入几滴酚酞试液,溶液呈____色,
如果要使试管中溶液的PH降为5,可以采取
__________________的方法。
红
滴加PH<5酸溶液
5.将一定量PH=3和PH=8的两种溶液混合后,溶
液的PH可能是( )
A PH=2 B PH=6 C PH=8 D PH=11
B
6.向氢氧化钠溶液中滴加稀盐酸至过量。下列各图中能表示溶液的pH与所加稀盐酸体积的关系的是( )
A
7.向盐酸中滴加蒸馏水至过量。下列各图中能表示溶液的pH与所加蒸馏水体积的关系的是( )
D
7.在用稀盐酸和氢氧化钠溶液进行中和反应实验时,反
应过程中溶液的酸碱度变化如图13所示。
(1)该反应的化学方程为:_____________________。
(2)该实验操作是将___________滴加到另一种溶液中
(3)当加入溶液的质量为a g时,所得溶液中的溶质为
(写化学式)_____________。
(4)当加入溶液的质量为b g时,
向所得溶液中滴加酚酞溶液,
溶液呈_____色。
NaOH+HCl=NaCl+H2O
氢氧化钠溶液
HCl、NaCl
红
堂堂清
1、用pH试纸测定白醋的酸碱度时,如先将试纸
用蒸馏水润湿,再把白醋滴到试纸上,则测得
的结果与白醋实际的pH比较( )
A.偏低 B.偏高 C.相等 D.无法比较
2、两种溶液混合后pH=7,这两种溶液的pH可能
是( )
A.pH=0和pH=7 B.pH=5和pH=6
C.pH=8和pH=10 D.pH=4和pH=13
3、下列物质分别溶于水,pH大于7的是( )
A.SO3 B.CO2 C.HCl D.CaO
4.小明同学为测定某稀盐酸的质量分数,向
7.3克的该稀盐酸中逐渐滴加20%的氢氧化钠
溶液,反应后溶液的PH值与加入的氢氧化钠
溶液的质量关系如图:
求:稀盐酸的质量分数为多少?
PH
7
0
20g
m
同课章节目录
