醇醛的一轮复习-甘油醛的性质和应用
文档属性
| 名称 | 醇醛的一轮复习-甘油醛的性质和应用 |

|
|
| 格式 | zip | ||
| 文件大小 | 432.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-09-10 00:00:00 | ||
图片预览




文档简介
(共12张PPT)
白黎芦醇
教学目标:
1、掌握醇、醛的化学性质
2、理解有机官能团的相互转化
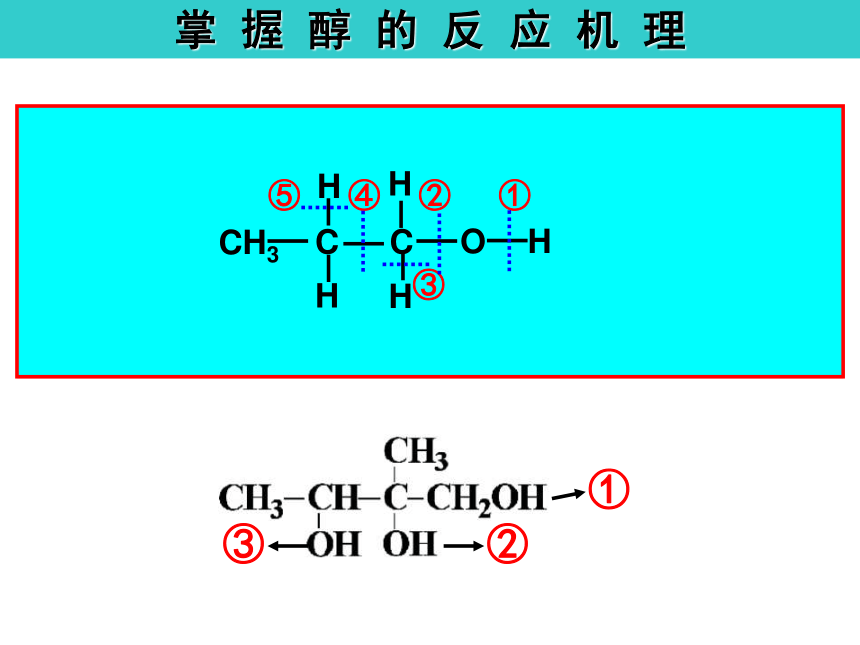
掌
握
醇
的
反
应
机
理
⑤
④
②
①
③
H
CH3
H
H
H
C
C
O
H
①
②
③
CH3-CH2-
CH2OH
C
H
2
C
O
H
CH3
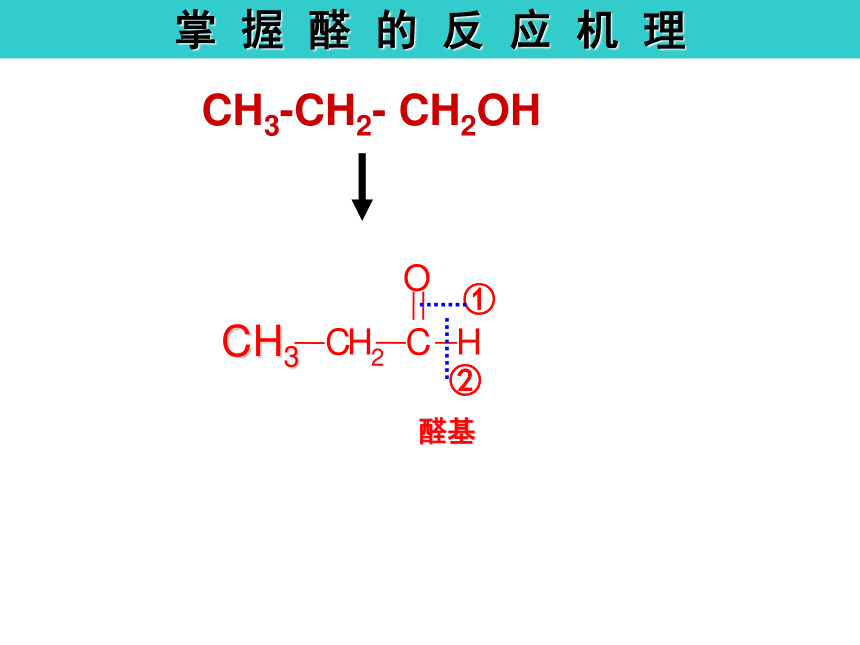
醛基
①
②
掌
握
醛
的
反
应
机
理
CH2OH-CHOH-
CHO
甘油醛
最简单的醛糖
思考:甘油醛具有那些化学性质?
丙糖
认
识
甘
油
醛
CH2OHCHOH
CHO
+
2Na
→
CH2ONaCHONa
CHO
+
H2↑
怎样证明参加反应的是羟基H而不是烃基H?
【例1】0.1
mol
某有机物完全燃烧后生成0.3molCO2,同质量的该有机物与足量的金属钠反应生成0.1molH2,该有机物可能是(
)
A.丙三醇
B.1,2-丙二醇
C.甘油醛
D.乙二醇
B
C
测定乙醇与钠反应产生氢气体积的装置
BC
甘油醛的性质探究
探究1:CH2OH-CHOH-
CHO能否使溴水
褪色?引起褪色的可能是什么官能团?如何加以证明?
探究2:CH2OH-CHOH-
CHO能否使酸性高锰酸钾褪色?引起褪色的可能是什么官能团?如何加以证明?
CH2OH-CHOH-
CHO与溴水发生氧化反应还是加成反应?如何证明?
甘油醛的性质探究
甘
油
醛
的
应
用
如何用:
CH2OH-CHOH-
CHO
CH2OH-CHOH-
COOH
?
如何用:
CH2OH-CHOH-
CHO
CH3-CHOH-
COOH
?
马氏规则:不对称烯烃与卤化氢发生加成反应,氢原子通常会加到含氢较多的不饱和碳原子上。
取一洁净试管,加入2ml2%的AgNO3溶液,再逐滴滴入2%的稀氨水,至生成的沉淀恰好溶解。
AgNO3+NH3.H2O
AgOH↓+NH4NO3
AgOH+NH3.H2O
[Ag(NH3)2]OH+2H2O
如何配制银氨溶液?
【例2】某实验小组用下列装置进行乙醇的催化氧化实验。
(1)实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学方程式:
、
。
在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该反应是
反应(填放热或吸热)。
2Cu
+
O2
2CuO
CH3CH2OH
+
CuO
CH3CHO
+
Cu
+
H2O
放热
(2)甲和乙两个水浴作用不相同。甲的作用是:
;
乙的作用是:
。
加热乙醇,使其挥发与空气中的氧气充分混合
冷却,使生成的乙醛冷凝成为液体
【探究】某实验小组用下列装置进行乙醇的催化氧化实验。
(3)反应进行一段时间后,试管a中能收集到不同的物质,它们是
。集气瓶中收集到的气体的主要成分是
。
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有
。
乙醛、乙醇、水
氮气(少量氧气等)
乙酸
【探究】某实验小组用下列装置进行乙醇的催化氧化实验。
装置甲
装置乙
【探究】某实验小组用下列装置进行乙醇的催化氧化实验。
(5)实验评价:两套装置都可以实现醇到醛的氧化,你认为哪套装置更有意义?
白黎芦醇
教学目标:
1、掌握醇、醛的化学性质
2、理解有机官能团的相互转化
掌
握
醇
的
反
应
机
理
⑤
④
②
①
③
H
CH3
H
H
H
C
C
O
H
①
②
③
CH3-CH2-
CH2OH
C
H
2
C
O
H
CH3
醛基
①
②
掌
握
醛
的
反
应
机
理
CH2OH-CHOH-
CHO
甘油醛
最简单的醛糖
思考:甘油醛具有那些化学性质?
丙糖
认
识
甘
油
醛
CH2OHCHOH
CHO
+
2Na
→
CH2ONaCHONa
CHO
+
H2↑
怎样证明参加反应的是羟基H而不是烃基H?
【例1】0.1
mol
某有机物完全燃烧后生成0.3molCO2,同质量的该有机物与足量的金属钠反应生成0.1molH2,该有机物可能是(
)
A.丙三醇
B.1,2-丙二醇
C.甘油醛
D.乙二醇
B
C
测定乙醇与钠反应产生氢气体积的装置
BC
甘油醛的性质探究
探究1:CH2OH-CHOH-
CHO能否使溴水
褪色?引起褪色的可能是什么官能团?如何加以证明?
探究2:CH2OH-CHOH-
CHO能否使酸性高锰酸钾褪色?引起褪色的可能是什么官能团?如何加以证明?
CH2OH-CHOH-
CHO与溴水发生氧化反应还是加成反应?如何证明?
甘油醛的性质探究
甘
油
醛
的
应
用
如何用:
CH2OH-CHOH-
CHO
CH2OH-CHOH-
COOH
?
如何用:
CH2OH-CHOH-
CHO
CH3-CHOH-
COOH
?
马氏规则:不对称烯烃与卤化氢发生加成反应,氢原子通常会加到含氢较多的不饱和碳原子上。
取一洁净试管,加入2ml2%的AgNO3溶液,再逐滴滴入2%的稀氨水,至生成的沉淀恰好溶解。
AgNO3+NH3.H2O
AgOH↓+NH4NO3
AgOH+NH3.H2O
[Ag(NH3)2]OH+2H2O
如何配制银氨溶液?
【例2】某实验小组用下列装置进行乙醇的催化氧化实验。
(1)实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学方程式:
、
。
在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该反应是
反应(填放热或吸热)。
2Cu
+
O2
2CuO
CH3CH2OH
+
CuO
CH3CHO
+
Cu
+
H2O
放热
(2)甲和乙两个水浴作用不相同。甲的作用是:
;
乙的作用是:
。
加热乙醇,使其挥发与空气中的氧气充分混合
冷却,使生成的乙醛冷凝成为液体
【探究】某实验小组用下列装置进行乙醇的催化氧化实验。
(3)反应进行一段时间后,试管a中能收集到不同的物质,它们是
。集气瓶中收集到的气体的主要成分是
。
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有
。
乙醛、乙醇、水
氮气(少量氧气等)
乙酸
【探究】某实验小组用下列装置进行乙醇的催化氧化实验。
装置甲
装置乙
【探究】某实验小组用下列装置进行乙醇的催化氧化实验。
(5)实验评价:两套装置都可以实现醇到醛的氧化,你认为哪套装置更有意义?
