人教版高中选修5化学3.2【醛】课件(39张PPT)
文档属性
| 名称 | 人教版高中选修5化学3.2【醛】课件(39张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-09-11 00:00:00 | ||
图片预览





文档简介
(共39张PPT)
第三章
烃的含氧衍生物
第二节
醛
第二节
醛
一、乙醛
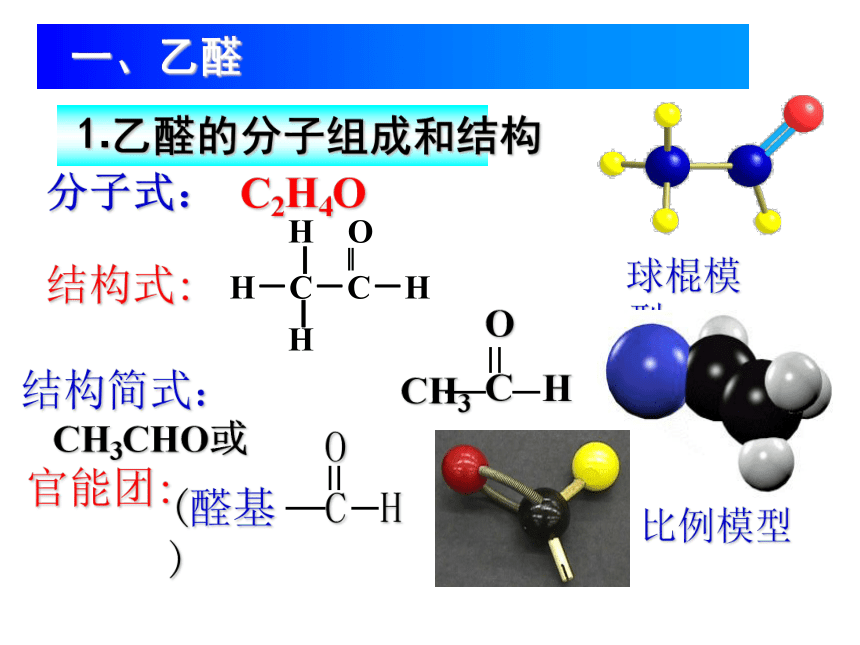
⒈乙醛的分子组成和结构
⒉乙醛的物理性质
⒋乙醛的用途
⒊乙醛的化学性质:
1、醛类的结构特点和通式
2、醛的化学通性
3、同分异构体
4、常见的醛;①甲醛;②乙二醛
二、醛类
⒌乙醛的工业制法
⑴
加成反应
⑵
氧化反应
一、乙醛
结构式:
分子式:
C2H4O
结构简式:CH3CHO或
CH3
C
O
H
(醛基)
C
O
H
官能团:
比例模型
球棍模型
⒈乙醛的分子组成和结构
H
O
▏
‖
H-C-C-H
▏
H
乙醛是无色、有刺激性气味的液体,密度比水小,沸点是
20.8℃,易挥发,易燃烧,能和水、乙醇、乙醚、氯仿等互溶
思考:乙醛、苯、CCl4均为无色液体,如何用最简便的方法鉴别?
一、乙醛
⒉乙醛的物理性质
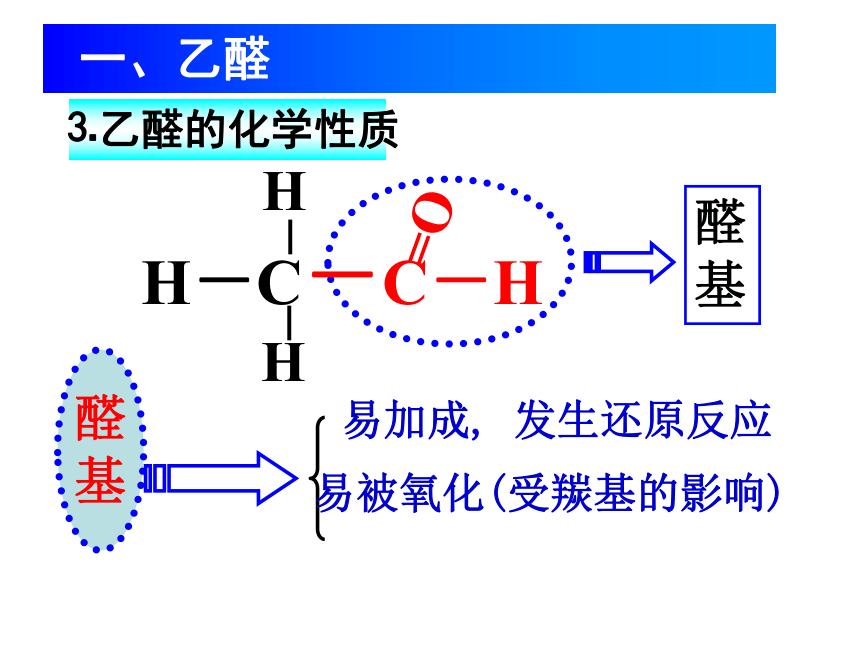
醛基
易加成,
发生还原反应
H-C-C-H
-
H
H
-
O=
醛
基
易被氧化(受羰基的影响)
一、乙醛
⒊乙醛的化学性质
一、乙醛
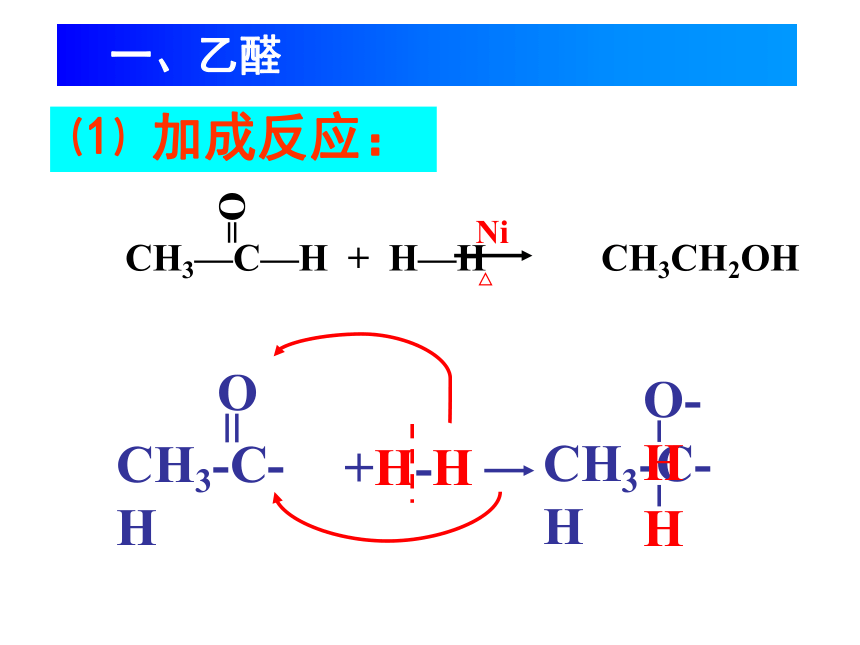
⑴
加成反应:
O=
CH3—C—H
+
H—H
CH3CH2OH
Ni
△
CH3-C-H
O
+H-H
CH3-C-H
O-H
H
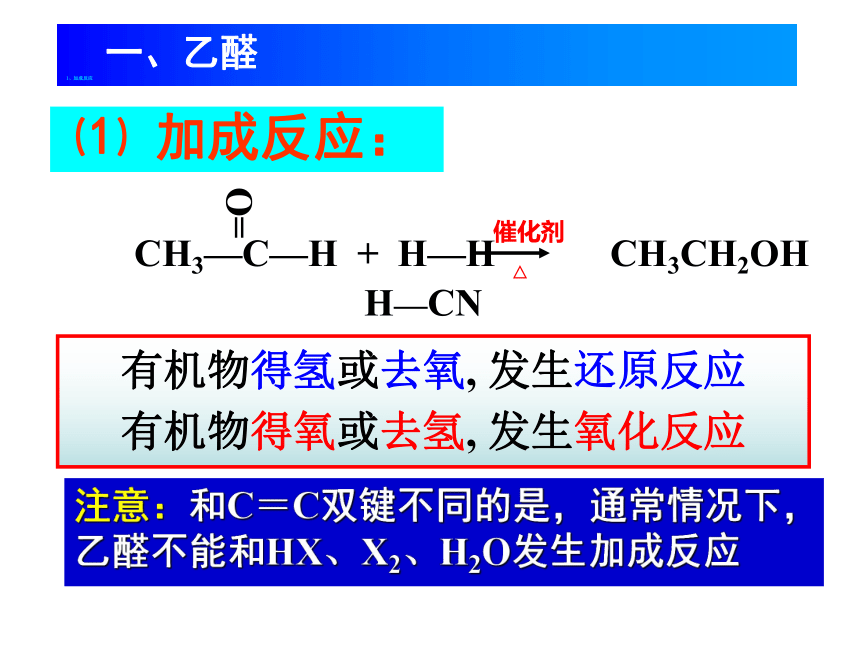
⑴
加成反应:
O=
CH3—C—H
+
H—H
CH3CH2OH
催化剂
△
有机物得氢或去氧,
发生还原反应
有机物得氧或去氢,
发生氧化反应
H—CN
注意:和C=C双键不同的是,通常情况下,乙醛不能和HX、X2、H2O发生加成反应
一、乙醛
1、加成反应
⑵
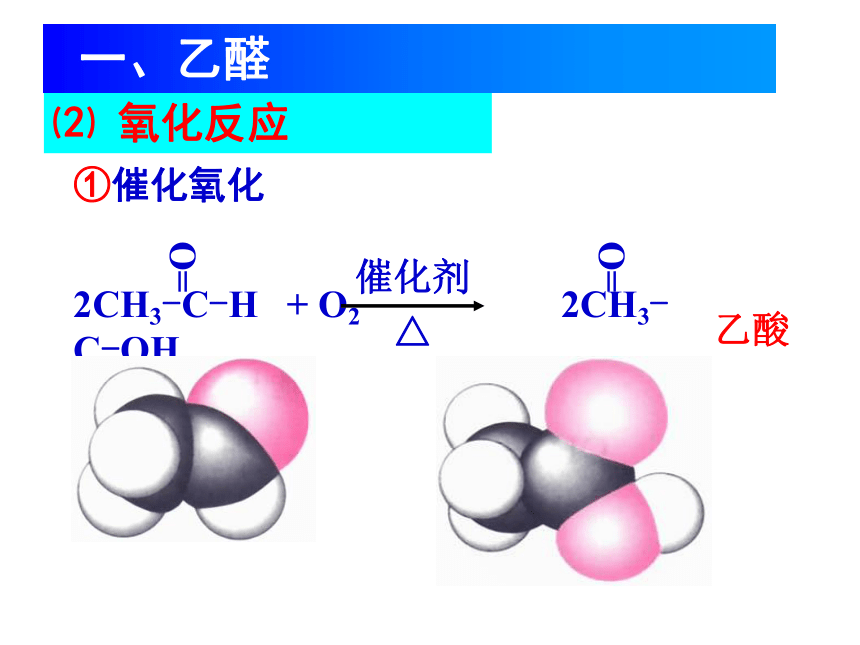
氧化反应
①催化氧化
2CH3-C-H
+
O2
2CH3-C-OH
催化剂
△
O=
O=
乙酸
一、乙醛
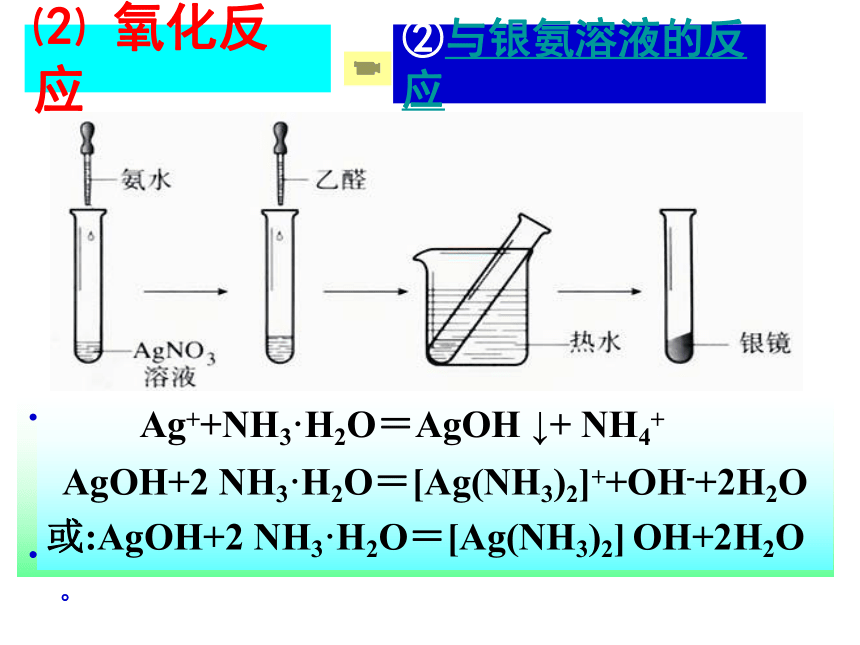
②与银氨溶液的反应
在洁净的试管里加入1
mL2%的AgNO3溶液,然后一边摇动试管,一边逐滴滴入2%的稀氨水,至最初产生的沉淀恰好溶解为止(这时得到的溶液叫做银氨溶液)。再滴入3滴乙醛,振荡后把试管放在热水中温热。
????不久可以看到,试管内壁上附着一层光亮如镜的金属银。
Ag++NH3·H2O=AgOH
↓+
NH4+
AgOH+2
NH3·H2O=[Ag(NH3)2]++OH-+2H2O
或:AgOH+2
NH3·H2O=[Ag(NH3)2]
OH+2H2O
⑵
氧化反应
②
银镜反应---与银氨溶液的反应
CH3CHO
+
2
+
2OH-
[
]
Ag(NH3)2
+
水浴
△
CH3COO-
+
NH4+
+
2Ag↓
+
3NH3
+
H2O
说明:
(
1
)乙醛被氧化
(
2
)此反应可以用于醛基的检验和测定
水浴
CH3CHO+2[Ag(NH3)2]OH
CH3COONH4+
2Ag
↓
+3NH3+H2O
⑵
氧化反应
1.试管内壁应洁净
2.必须用水浴加热,不能用酒精灯加热。
3.加热时不能振荡试管和摇动试管。
4.配制银氨溶液时,氨水不能过多或过少[只能加到AgOH
(Ag2O)棕色沉淀刚好消失]
5.实验后,银镜用HNO3浸泡,再用水洗
做银镜反应的注意几个事项
⑵
氧化反应
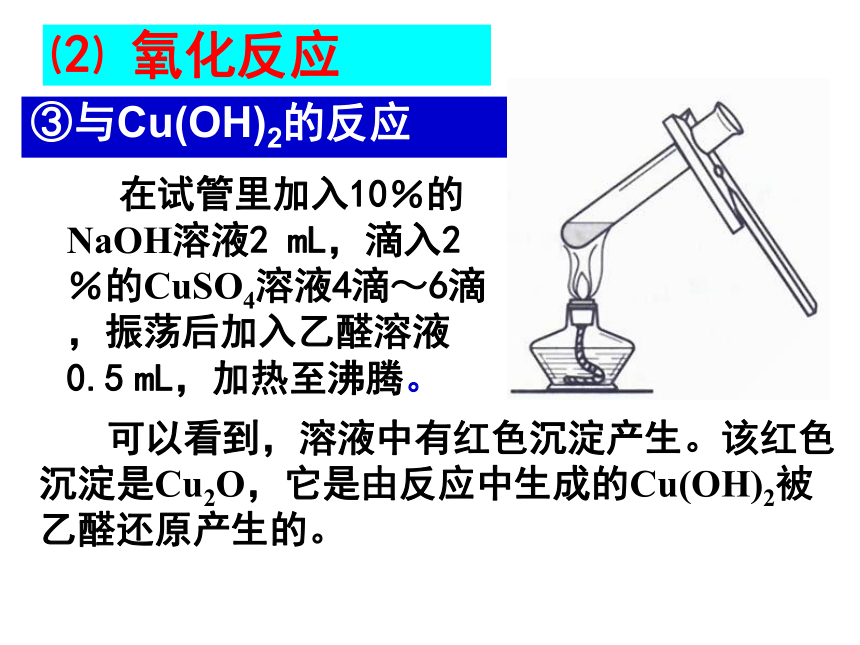
③与Cu(OH)2的反应
在试管里加入10%的NaOH溶液2
mL,滴入2%的CuSO4溶液4滴~6滴,振荡后加入乙醛溶液0.5?mL,加热至沸腾。
可以看到,溶液中有红色沉淀产生。该红色沉淀是Cu2O,它是由反应中生成的Cu(OH)2被乙醛还原产生的。
⑵
氧化反应
③乙醛与Cu(OH)2的反应
Cu2++2OH-
=
Cu(OH)2(新制蓝色絮状)
NaOH
△
2Cu(OH)2+CH3CHO
CH3COOH+Cu2O+2H2O
该实验可用于检验醛基的存在.
1.Cu(OH)2应现配现用;
2.成功条件:碱性环境(碱过量)、加热.
乙醛能被溴水和酸性高锰酸钾溶液氧化吗?
问题
注意
醛基的检验方法:
思考:用葡萄糖代替乙醛做与新制的氢氧化铜反应的实验也现了砖红色沉淀,该实验结果可说明什么?
(1)与新制的银氨溶液反应有光亮的银镜生成
(2)与新制的Cu(OH)2共热煮沸有砖红色沉淀生成
一、乙醛
小
结
氧化
还原
氧化
—C—H
O=
,是既有氧化性,又有还原性,
其氧化还原关系为:
醇
醛
羧酸
O=
—C—H
⑴
氧化(得氧)
,断C—H键:
Cu
△
2CH3CHO
+
O2
2CH3COOH
⑵
醛还原(加氢)
,断C=O键:
O=
R—C—H
+
H2
R—CH2—OH
Ni
△
O=
—C—H
乙酸
2CH3CHO
+
O2
2CH3COOH
催化剂
乙醛是有机合成工业中的重要原料,主要用来生产乙酸、丁醇、乙酸乙酯等。如:
⒋乙醛的用途
一、乙醛
一、乙醛
PdCl2-CuCl2
100℃-110℃
(3)乙烯氧化法:
2CH2=CH2+O2
2CH3CHO
(1)乙醇氧化法:
2CH3CH2OH+O2
Cu
2CH3CHO+2H2O
△
(2)乙炔水化法:
+H2O
催化剂
CH3CHO
⒌乙醛的工业制法:
H
C
C
O
H
H
H
C
O
H
H
H
C
C
O
H
H
H
C
H
H
甲醛
乙醛
丙醛
……
C
O
H
R
醛
二、醛类
⑴分子里由烃基跟醛基相连而构成的化合物
R—CHO
⑵饱和一元醛的通式:CnH2nO
(
n≥1)
1、醛类的结构特点和通式
CnH2n+1—CHO
二、醛类
(1)可以与氢发发生加成(还原)反应
2、醛的化学通性
(2)可以发生氧化反应
醛
银镜反应
被新制的氢氧化铜悬浊液氧化
被氧气氧化
使高锰酸钾酸性溶液褪色
——生成醇
二、醛类
(2)醛的氧化反应——氧化为羧酸
RCHO
+
2[Ag(NH3)2]+
+
2OH
RCOO
+
NH4+
+
2Ag
+
3NH3
+
H2O
RCHO
+
2Cu(OH)2
RCOOH
+
Cu2O
+
2H2O
△
(1)醛的加成反应——还原成醇
RCHO
H2
催化剂
△
RCH2OH
二、醛类
-CHO、Ag、Cu2O的物质的量的关系
-CHO-----
2
Ag
1
2
1
R-CHO
R-COOH
【O】
-CHO----Cu2O
1
醛在氧化反应中有关计量关系
二、醛类
●相同碳原子数的醛、酮、互为
同分异构体.通式:CnH2nO
例:
(1)写出C3H6O的链状可能结构简式.
(2)写出C5H10O表示醛的同分异构体.
提示:醛可看成是醛基取代了烃中的氢原子,书写同分异构体时应把醛写在端点
4种
4种
二、醛类
3、同分异构体
C5H10O→C4H9CHO
醛可看成醛基取代了烃中的氢原子,书写同分异构体时应把醛写成
:
R-CHO
再判断烃基-R有几种同分异构体
-C4H9有四种同分异构体
想一想:如何写出C5H10O表示醛的同分异构体
乙醛
是无色、有刺激性气味的液体,比水轻,沸点低,仅20.8℃。易挥发,易燃烧,跟水、乙醇、乙醚、氯仿等互溶。
甲醛
俗名蚁醛,是一种无色、有强烈刺激性气味的气体,易溶于水,质量分数为35%~40%的水溶液叫做福尔马林。具有防腐和杀菌能力。
其它的醛
CHO
CHO
乙二醛
CH2
CH
CHO
丙烯醛
CHO
苯甲醛
4、常见的醛
二、醛类
结构:
性质
:
与乙醛相似
不同点:
①、常温下甲醛为无色有刺激性气味的气体。
②、甲醛中有2个活泼氢可被氧化。
C
O
H
H
C
O
H
H
O
O
H2CO3
1mol甲醛最多可以还原得到多少molAg?
4、甲醛
甲醛的化学性质
从结构:
H—C—H
分析
O=
(注意:相当于含有两个醛基的特殊结构)
H—C—H
+
4
2NH4+
+
CO3
2-
+
6NH3
+
4Ag↓+
2H2O
[
]
Ag(NH3)2
+
+
4OH-
△
O=
氧化反应:
—
OH
O=
H—C—H
—
OH
CH2
[
]n
n
+
n
+
nH2O
HCl
100℃·
酚醛树脂
缩聚反应:
单体间除缩合生成一种高分子化合物外,
还生成一种小分子(如H2O、NH3等)化合物.
加聚反应只生成一种高分子化合物.
缩聚反应:
还原反应:
O=
H—C—H
+
H—H
CH3OH
Ni
△
小节
第二节
醛
一、乙醛
⒈乙醛的分子组成和结构
⒉乙醛的物理性质
⒋乙醛的用途
⒊乙醛的化学性质
1、醛类的结构特点和通式
2、醛的化学通性
3、同分异构体
4、常见的醛;①甲醛;②乙二醛
二、醛类
⒌乙醛的工业制法:
⑴
加成反应
⑵
氧化反应
醛和酮共同之处是都含羰基(-C-)
C
H
O
R
C
R’
O
R
醛
酮
饱和一元酮的组成通式也是CnH2nO,最简单的酮是R和R’都是甲基的丙酮。醛酮可构成类别异构体
丙酮没有还原性,不跟银氨溶液起银镜反应。在催化剂存在的条件下,可以跟H2起加成反应还原成醇。
丙酮无色液体,有气味,易挥发,易燃烧。可跟水、乙酸、乙醚任意比互溶。是重要的有机溶剂。
O
OH
CH3
C
CH3
+
H2
CH3
CH
CH3
催化剂
酮(和醛)
O
已知烯烃经O3氧化后,在锌存在下水解可得醛和酮。
R1-C=CH-R3
R2
O3
H2O、Zn
R1-C=O
R2
+
R3CHO
现有分子式为C7H14的某烯烃,它与氢气加成反应生成
2,3-二甲基戊烷,它经臭氧氧化后在锌存在下水解生成乙醛和一种酮
(
R-C-R’)由此推断该有机物的结构简式为
O
1、烯烃氧化生成醛和酮
CH3-CH=O
+CH2-CHO
CH3-CH-CH-CHO
OH
H
H
CH3CH=CH-CHO
△
-H2O
已知两个醛分子在一定条件下可以自身加成。反应过程如下:
R-CH2-CH=O
+R-CH-CHO
R-CH2-CH-C-CHO
OH
H
H
R
RCH2CH=C-CHO
R
△
H2O
试以乙醛为原料制取正丁醇(CH3CH2CH2CH2OH)
H2
催化剂
CH3CH2CH2CH2OH
2、醛的自身加成反应
⑴、某学生用1mol/LCuSO4溶液2mL和0.5mol/LNaOH溶液4mL混合后加入40%的甲醛溶液0.5mL,加热到沸腾未见红色沉淀生成。主要原因是(
)
A.甲醛的量太少
B.
CuSO4的量太少
C.NaOH的量太少
D.加热时间太短
√
C
⑵、有机物甲能发生银镜反应,甲催化加氢还原成有机物乙,
1mol乙跟足量的金属钠反应放出标准状况下的氢气22.4L,据此推断乙一定不是(
)
A.HOCH2CH2OH
B.HOCH2-CH-CH3
C.CH3-CH-CH-CH3
D.CH3CH2OH
OH
OH
OH
⑶、醛类因被氧化为羧酸,而易使酸性高锰酸钾溶液或溴水褪色。向乙醛中滴入酸性KMnO4溶液,可观察到的现象是
现已知柠檬醛的结构式为:
CH3-C=CHCH2CH2-C=CH-C-H
CH3
CH3
O
若要检验其中的碳碳双键,其实验方法是
√
√
溶液由紫色变无色
CD
先加新制的Cu(OH)2使醛基氧化。然后再用酸性KMnO4溶液(或溴水)检验碳碳双键,碳碳双键能使酸性KMnO4溶液(或溴水)褪色
⑷、下列物质中不能发生银镜反应的是(
)
A.乙醛
B.苯酚
C.酒精
D.葡萄糖
B
C
⑸、下列混合溶液可以用分液漏斗分离的一组是(
)
A.乙醛和水
B.乙醛和乙醇
C.甲醛和水
D.苯和水
D
⑹、3g某醛和足量的银氨溶液反应,结果析出43.2gAg
则该醛是(
)
A.甲醛
B.乙醛
C.丙醛
D.丁醛
A
2HCHO
+
NaOH(浓)
→
HCOONa
+
CH3OH
属康尼查罗反应,下列说法正确的是
A
此反应是氧化还原反应
B
甲醛只被氧化成甲酸
C
甲醛只被还原成甲醇
D
甲醛既被氧化成甲醇又被还原为甲酸
(A)
在日常生活中我们都会有这样的疑问,
为什么有的人喝酒“千杯万杯都不醉”,而有的人喝一点酒后就面红耳赤,情绪激动甚至酩酊大醉?酒量的大小到底与什么有关呢?
人的酒量大小,与酒精在人体内的代谢产物和过程有很大关系。乙醇进入人体内,首先在乙醇脱氢酶的作用下氧化为乙醛,然后又在乙醛脱氢酶的作用下将乙醛氧化为乙酸,并进一步转化为CO2和H2O。如果人体内这两种脱氢酶的含量都很大的话,酒精的代谢速度就很快。但如果人体内这两种脱氢酶的
含量不够大,
例如缺少乙醛脱氢酶,
饮酒后就会引起体内乙醛积累,导
致血管扩张而脸红。
原来如此啊!
第三章
烃的含氧衍生物
第二节
醛
第二节
醛
一、乙醛
⒈乙醛的分子组成和结构
⒉乙醛的物理性质
⒋乙醛的用途
⒊乙醛的化学性质:
1、醛类的结构特点和通式
2、醛的化学通性
3、同分异构体
4、常见的醛;①甲醛;②乙二醛
二、醛类
⒌乙醛的工业制法
⑴
加成反应
⑵
氧化反应
一、乙醛
结构式:
分子式:
C2H4O
结构简式:CH3CHO或
CH3
C
O
H
(醛基)
C
O
H
官能团:
比例模型
球棍模型
⒈乙醛的分子组成和结构
H
O
▏
‖
H-C-C-H
▏
H
乙醛是无色、有刺激性气味的液体,密度比水小,沸点是
20.8℃,易挥发,易燃烧,能和水、乙醇、乙醚、氯仿等互溶
思考:乙醛、苯、CCl4均为无色液体,如何用最简便的方法鉴别?
一、乙醛
⒉乙醛的物理性质
醛基
易加成,
发生还原反应
H-C-C-H
-
H
H
-
O=
醛
基
易被氧化(受羰基的影响)
一、乙醛
⒊乙醛的化学性质
一、乙醛
⑴
加成反应:
O=
CH3—C—H
+
H—H
CH3CH2OH
Ni
△
CH3-C-H
O
+H-H
CH3-C-H
O-H
H
⑴
加成反应:
O=
CH3—C—H
+
H—H
CH3CH2OH
催化剂
△
有机物得氢或去氧,
发生还原反应
有机物得氧或去氢,
发生氧化反应
H—CN
注意:和C=C双键不同的是,通常情况下,乙醛不能和HX、X2、H2O发生加成反应
一、乙醛
1、加成反应
⑵
氧化反应
①催化氧化
2CH3-C-H
+
O2
2CH3-C-OH
催化剂
△
O=
O=
乙酸
一、乙醛
②与银氨溶液的反应
在洁净的试管里加入1
mL2%的AgNO3溶液,然后一边摇动试管,一边逐滴滴入2%的稀氨水,至最初产生的沉淀恰好溶解为止(这时得到的溶液叫做银氨溶液)。再滴入3滴乙醛,振荡后把试管放在热水中温热。
????不久可以看到,试管内壁上附着一层光亮如镜的金属银。
Ag++NH3·H2O=AgOH
↓+
NH4+
AgOH+2
NH3·H2O=[Ag(NH3)2]++OH-+2H2O
或:AgOH+2
NH3·H2O=[Ag(NH3)2]
OH+2H2O
⑵
氧化反应
②
银镜反应---与银氨溶液的反应
CH3CHO
+
2
+
2OH-
[
]
Ag(NH3)2
+
水浴
△
CH3COO-
+
NH4+
+
2Ag↓
+
3NH3
+
H2O
说明:
(
1
)乙醛被氧化
(
2
)此反应可以用于醛基的检验和测定
水浴
CH3CHO+2[Ag(NH3)2]OH
CH3COONH4+
2Ag
↓
+3NH3+H2O
⑵
氧化反应
1.试管内壁应洁净
2.必须用水浴加热,不能用酒精灯加热。
3.加热时不能振荡试管和摇动试管。
4.配制银氨溶液时,氨水不能过多或过少[只能加到AgOH
(Ag2O)棕色沉淀刚好消失]
5.实验后,银镜用HNO3浸泡,再用水洗
做银镜反应的注意几个事项
⑵
氧化反应
③与Cu(OH)2的反应
在试管里加入10%的NaOH溶液2
mL,滴入2%的CuSO4溶液4滴~6滴,振荡后加入乙醛溶液0.5?mL,加热至沸腾。
可以看到,溶液中有红色沉淀产生。该红色沉淀是Cu2O,它是由反应中生成的Cu(OH)2被乙醛还原产生的。
⑵
氧化反应
③乙醛与Cu(OH)2的反应
Cu2++2OH-
=
Cu(OH)2(新制蓝色絮状)
NaOH
△
2Cu(OH)2+CH3CHO
CH3COOH+Cu2O+2H2O
该实验可用于检验醛基的存在.
1.Cu(OH)2应现配现用;
2.成功条件:碱性环境(碱过量)、加热.
乙醛能被溴水和酸性高锰酸钾溶液氧化吗?
问题
注意
醛基的检验方法:
思考:用葡萄糖代替乙醛做与新制的氢氧化铜反应的实验也现了砖红色沉淀,该实验结果可说明什么?
(1)与新制的银氨溶液反应有光亮的银镜生成
(2)与新制的Cu(OH)2共热煮沸有砖红色沉淀生成
一、乙醛
小
结
氧化
还原
氧化
—C—H
O=
,是既有氧化性,又有还原性,
其氧化还原关系为:
醇
醛
羧酸
O=
—C—H
⑴
氧化(得氧)
,断C—H键:
Cu
△
2CH3CHO
+
O2
2CH3COOH
⑵
醛还原(加氢)
,断C=O键:
O=
R—C—H
+
H2
R—CH2—OH
Ni
△
O=
—C—H
乙酸
2CH3CHO
+
O2
2CH3COOH
催化剂
乙醛是有机合成工业中的重要原料,主要用来生产乙酸、丁醇、乙酸乙酯等。如:
⒋乙醛的用途
一、乙醛
一、乙醛
PdCl2-CuCl2
100℃-110℃
(3)乙烯氧化法:
2CH2=CH2+O2
2CH3CHO
(1)乙醇氧化法:
2CH3CH2OH+O2
Cu
2CH3CHO+2H2O
△
(2)乙炔水化法:
+H2O
催化剂
CH3CHO
⒌乙醛的工业制法:
H
C
C
O
H
H
H
C
O
H
H
H
C
C
O
H
H
H
C
H
H
甲醛
乙醛
丙醛
……
C
O
H
R
醛
二、醛类
⑴分子里由烃基跟醛基相连而构成的化合物
R—CHO
⑵饱和一元醛的通式:CnH2nO
(
n≥1)
1、醛类的结构特点和通式
CnH2n+1—CHO
二、醛类
(1)可以与氢发发生加成(还原)反应
2、醛的化学通性
(2)可以发生氧化反应
醛
银镜反应
被新制的氢氧化铜悬浊液氧化
被氧气氧化
使高锰酸钾酸性溶液褪色
——生成醇
二、醛类
(2)醛的氧化反应——氧化为羧酸
RCHO
+
2[Ag(NH3)2]+
+
2OH
RCOO
+
NH4+
+
2Ag
+
3NH3
+
H2O
RCHO
+
2Cu(OH)2
RCOOH
+
Cu2O
+
2H2O
△
(1)醛的加成反应——还原成醇
RCHO
H2
催化剂
△
RCH2OH
二、醛类
-CHO、Ag、Cu2O的物质的量的关系
-CHO-----
2
Ag
1
2
1
R-CHO
R-COOH
【O】
-CHO----Cu2O
1
醛在氧化反应中有关计量关系
二、醛类
●相同碳原子数的醛、酮、互为
同分异构体.通式:CnH2nO
例:
(1)写出C3H6O的链状可能结构简式.
(2)写出C5H10O表示醛的同分异构体.
提示:醛可看成是醛基取代了烃中的氢原子,书写同分异构体时应把醛写在端点
4种
4种
二、醛类
3、同分异构体
C5H10O→C4H9CHO
醛可看成醛基取代了烃中的氢原子,书写同分异构体时应把醛写成
:
R-CHO
再判断烃基-R有几种同分异构体
-C4H9有四种同分异构体
想一想:如何写出C5H10O表示醛的同分异构体
乙醛
是无色、有刺激性气味的液体,比水轻,沸点低,仅20.8℃。易挥发,易燃烧,跟水、乙醇、乙醚、氯仿等互溶。
甲醛
俗名蚁醛,是一种无色、有强烈刺激性气味的气体,易溶于水,质量分数为35%~40%的水溶液叫做福尔马林。具有防腐和杀菌能力。
其它的醛
CHO
CHO
乙二醛
CH2
CH
CHO
丙烯醛
CHO
苯甲醛
4、常见的醛
二、醛类
结构:
性质
:
与乙醛相似
不同点:
①、常温下甲醛为无色有刺激性气味的气体。
②、甲醛中有2个活泼氢可被氧化。
C
O
H
H
C
O
H
H
O
O
H2CO3
1mol甲醛最多可以还原得到多少molAg?
4、甲醛
甲醛的化学性质
从结构:
H—C—H
分析
O=
(注意:相当于含有两个醛基的特殊结构)
H—C—H
+
4
2NH4+
+
CO3
2-
+
6NH3
+
4Ag↓+
2H2O
[
]
Ag(NH3)2
+
+
4OH-
△
O=
氧化反应:
—
OH
O=
H—C—H
—
OH
CH2
[
]n
n
+
n
+
nH2O
HCl
100℃·
酚醛树脂
缩聚反应:
单体间除缩合生成一种高分子化合物外,
还生成一种小分子(如H2O、NH3等)化合物.
加聚反应只生成一种高分子化合物.
缩聚反应:
还原反应:
O=
H—C—H
+
H—H
CH3OH
Ni
△
小节
第二节
醛
一、乙醛
⒈乙醛的分子组成和结构
⒉乙醛的物理性质
⒋乙醛的用途
⒊乙醛的化学性质
1、醛类的结构特点和通式
2、醛的化学通性
3、同分异构体
4、常见的醛;①甲醛;②乙二醛
二、醛类
⒌乙醛的工业制法:
⑴
加成反应
⑵
氧化反应
醛和酮共同之处是都含羰基(-C-)
C
H
O
R
C
R’
O
R
醛
酮
饱和一元酮的组成通式也是CnH2nO,最简单的酮是R和R’都是甲基的丙酮。醛酮可构成类别异构体
丙酮没有还原性,不跟银氨溶液起银镜反应。在催化剂存在的条件下,可以跟H2起加成反应还原成醇。
丙酮无色液体,有气味,易挥发,易燃烧。可跟水、乙酸、乙醚任意比互溶。是重要的有机溶剂。
O
OH
CH3
C
CH3
+
H2
CH3
CH
CH3
催化剂
酮(和醛)
O
已知烯烃经O3氧化后,在锌存在下水解可得醛和酮。
R1-C=CH-R3
R2
O3
H2O、Zn
R1-C=O
R2
+
R3CHO
现有分子式为C7H14的某烯烃,它与氢气加成反应生成
2,3-二甲基戊烷,它经臭氧氧化后在锌存在下水解生成乙醛和一种酮
(
R-C-R’)由此推断该有机物的结构简式为
O
1、烯烃氧化生成醛和酮
CH3-CH=O
+CH2-CHO
CH3-CH-CH-CHO
OH
H
H
CH3CH=CH-CHO
△
-H2O
已知两个醛分子在一定条件下可以自身加成。反应过程如下:
R-CH2-CH=O
+R-CH-CHO
R-CH2-CH-C-CHO
OH
H
H
R
RCH2CH=C-CHO
R
△
H2O
试以乙醛为原料制取正丁醇(CH3CH2CH2CH2OH)
H2
催化剂
CH3CH2CH2CH2OH
2、醛的自身加成反应
⑴、某学生用1mol/LCuSO4溶液2mL和0.5mol/LNaOH溶液4mL混合后加入40%的甲醛溶液0.5mL,加热到沸腾未见红色沉淀生成。主要原因是(
)
A.甲醛的量太少
B.
CuSO4的量太少
C.NaOH的量太少
D.加热时间太短
√
C
⑵、有机物甲能发生银镜反应,甲催化加氢还原成有机物乙,
1mol乙跟足量的金属钠反应放出标准状况下的氢气22.4L,据此推断乙一定不是(
)
A.HOCH2CH2OH
B.HOCH2-CH-CH3
C.CH3-CH-CH-CH3
D.CH3CH2OH
OH
OH
OH
⑶、醛类因被氧化为羧酸,而易使酸性高锰酸钾溶液或溴水褪色。向乙醛中滴入酸性KMnO4溶液,可观察到的现象是
现已知柠檬醛的结构式为:
CH3-C=CHCH2CH2-C=CH-C-H
CH3
CH3
O
若要检验其中的碳碳双键,其实验方法是
√
√
溶液由紫色变无色
CD
先加新制的Cu(OH)2使醛基氧化。然后再用酸性KMnO4溶液(或溴水)检验碳碳双键,碳碳双键能使酸性KMnO4溶液(或溴水)褪色
⑷、下列物质中不能发生银镜反应的是(
)
A.乙醛
B.苯酚
C.酒精
D.葡萄糖
B
C
⑸、下列混合溶液可以用分液漏斗分离的一组是(
)
A.乙醛和水
B.乙醛和乙醇
C.甲醛和水
D.苯和水
D
⑹、3g某醛和足量的银氨溶液反应,结果析出43.2gAg
则该醛是(
)
A.甲醛
B.乙醛
C.丙醛
D.丁醛
A
2HCHO
+
NaOH(浓)
→
HCOONa
+
CH3OH
属康尼查罗反应,下列说法正确的是
A
此反应是氧化还原反应
B
甲醛只被氧化成甲酸
C
甲醛只被还原成甲醇
D
甲醛既被氧化成甲醇又被还原为甲酸
(A)
在日常生活中我们都会有这样的疑问,
为什么有的人喝酒“千杯万杯都不醉”,而有的人喝一点酒后就面红耳赤,情绪激动甚至酩酊大醉?酒量的大小到底与什么有关呢?
人的酒量大小,与酒精在人体内的代谢产物和过程有很大关系。乙醇进入人体内,首先在乙醇脱氢酶的作用下氧化为乙醛,然后又在乙醛脱氢酶的作用下将乙醛氧化为乙酸,并进一步转化为CO2和H2O。如果人体内这两种脱氢酶的含量都很大的话,酒精的代谢速度就很快。但如果人体内这两种脱氢酶的
含量不够大,
例如缺少乙醛脱氢酶,
饮酒后就会引起体内乙醛积累,导
致血管扩张而脸红。
原来如此啊!
