第二章第一节物质的分类 同步练习(含答案)
文档属性
| 名称 | 第二章第一节物质的分类 同步练习(含答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-09-14 00:00:00 | ||
图片预览



文档简介
中小学教育资源及组卷应用平台
第二章第一节物质的分类同步练习(含答案)
第I卷(选择题)
一、单选题
1.按照物质的树状分类和交叉分类,HNO3应属于( )
①酸 ②氢化物 ③氧化物 ④含氧酸 ⑤难挥发性酸 ⑥强氧化性酸 ⑦一元酸 ⑧化合物
A.①②③④⑤⑥⑦⑧
B.①④⑥⑦⑧
C.①⑧
D.①④⑤⑥⑦
2.下列关于物质分类的叙述中,不正确的是
A.H2SO4属于酸
B.KOH属于碱
C.NO属于氧化物
D.石灰水属于纯净物
3.下列分散系属于悬浊液的是()
A.硅酸溶胶
B.蔗糖溶液
C.泥浆水
D.氢氧化铁胶体
4.我国科学家在世界上第一次为一种名为“钴酞菁”的分子(直径为)恢复了磁性。“钴酞菁”分子结构和性质与人体内的血红素及植物体内的叶绿素非常相似。下列关于“钻酞菁”分子的说法中正确的是()
A.在水中形成的分散系能产生丁达尔效应
B.“钴酞菁”分子既能透过滤纸,也能透过半透膜
C.分子直径比钠离子小
D.在水中所形成的分散系属于悬浊液
5.下列分散系中,分散质微粒直径最大的是()
A.新制氢氧化铜悬浊液
B.淀粉溶液
C.溴的四氯化碳溶液
D.雾
6.对下列物质分类全部正确的是
①纯碱②食盐水③石灰水④烧碱⑤液态氧⑥KClO3
A.碱——①④
B.纯净物——③④⑤
C.盐——①⑥
D.混合物——②⑤
7.新型冠状病毒可通过气溶胶传播,气溶胶属于胶体的一种。下列关于胶体的叙述,正确的是()
A.依据丁达尔效应可将分散系分为溶液、胶体与浊液
B.胶体的本质特征是具有丁达尔效应
C.雾是气溶胶,在阳光下可观察到丁达尔效应
D.溶液中溶质粒子的运动有规律,胶体中分散质粒子的运动无规律,即做布朗运动
8.下列各组物质中,前一种是化合物,后一种是混合物的是()
A.铝土矿,洁净的雨水
B.红磷,空气
C.氢氧化钾,含铜80%的氧化铜
D.蒸馏水,粗盐
9.生物学家借助新的显微技术,成功观察到小于200纳米的微粒。下列分散系中,分散质粒径最小的是
A.雾
B.蛋白质溶液
C.石灰乳
D.KNO3溶液
10.古诗词是我国重要的文化遗产,下列诗句中加点字部分示涉及化学反应的是
A.月波成露露成霜,借与南枝作淡妆
B.春蚕到死丝方尽,蜡炬成灰泪始干
C.宝剑锋从磨砺出,梅花香自苦寒来
D.莫道雪融便无迹,雪融成水水成冰
11.下列关于酸、碱、盐的说法正确的是(
)
A.电离时生成的阳离子中有氢离子的化合物是酸
B.电离时生成的阴离子中有氢氧根离子的化合物是碱
C.电离时只生成金属阳离子和酸根离子的化合物才是盐
D.NH4Cl的电离方程式是NH4Cl=NH4++Cl-,所以NH4Cl是盐
12.下列属于碱的是(
)
A.NaHCO3
B.Na2CO3
C.Ca(OH)2
D.Cu2(OH)2CO3
13.下列关于分散系的说法不正确的是
A.分散系的稳定性:溶液>胶体>浊液
B.分散质粒子的大小:溶液>胶体>浊液
C.分散质粒子的直径为几纳米或几十纳米的分散系是胶体
D.可以用过滤的方法将悬浊液中的分散质从分散剂中分离出来
14.下列物质分类正确的是()
选项
碱
酸
盐
氧化物
A
生石灰
盐酸
纯碱
二氧化硫
B
烧碱
硫酸
氯化钠
氯酸钾
C
苛性钠
醋酸
碳酸钙
磷酸
D
苛性钾
碳酸
苏打
三氧化硫
A.A
B.B
C.C
D.D
15.当光束通过下列分散系时,能观察到丁达尔效应的是
A.KCl溶液
B.Fe(OH)3胶体
C.KOH溶液
D.Na2SO4溶液
16.新冠病毒由蛋白质外壳和单链核酸组成,直径大约在60~140nm,怕酒精,不耐高温。下列说法正确的是
A.病毒由碳、氢、氧三种元素组成
B.新冠病毒扩散到空气中不可能形成胶体
C.医用酒精能用于消毒是因为它有强氧化性
D.高温可使蛋白质发生变性
17.下列实验装置或操作与粒子直径的大小无直接关系的是()
A.过滤B.渗析
C.萃取D.丁达尔效应
18.下列分类或归类正确的是()
①液氯、氨水、干冰、碘化银均为纯净物?
②CaCl2、NaOH、HCl、IBr均为化合物??
③明矾、水银、烧碱、硫酸均为电解质④火碱、纯碱、碳酸钙都是电解质?
⑤碘酒、淀粉、云雾、纳米材料均为胶体
A.①③④
B.②③
C.②④
D.②③④⑤
19.下列逻辑关系图中正确的是
A.
B.
C.
D.
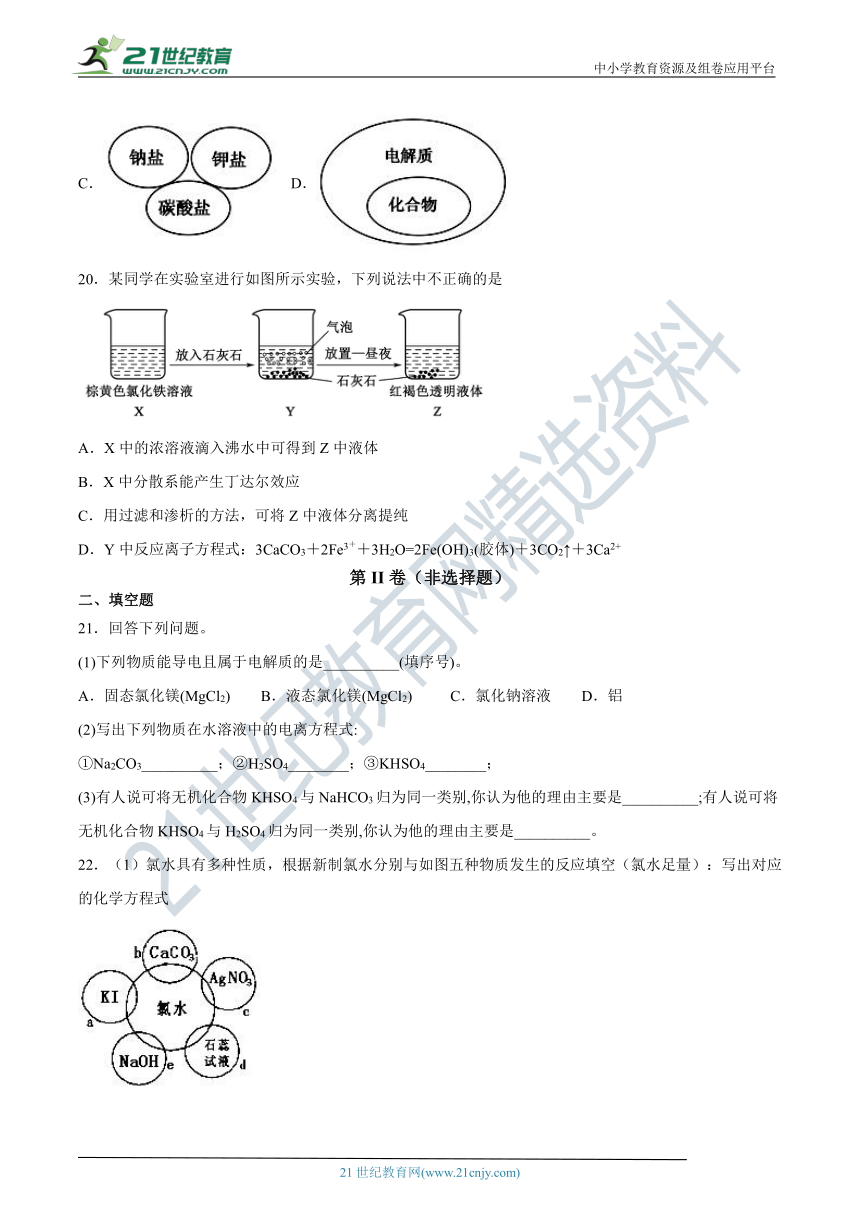
20.某同学在实验室进行如图所示实验,下列说法中不正确的是
A.X中的浓溶液滴入沸水中可得到Z中液体
B.X中分散系能产生丁达尔效应
C.用过滤和渗析的方法,可将Z中液体分离提纯
D.Y中反应离子方程式:3CaCO3+2Fe3++3H2O=2Fe(OH)3(胶体)+3CO2↑+3Ca2+
第II卷(非选择题)
二、填空题
21.回答下列问题。
(1)下列物质能导电且属于电解质的是__________(填序号)。
A.固态氯化镁(MgCl2)
B.液态氯化镁(MgCl2)
C.氯化钠溶液
D.铝
(2)写出下列物质在水溶液中的电离方程式:
①Na2CO3__________;②H2SO4________;③KHSO4________;
(3)有人说可将无机化合物KHSO4与NaHCO3归为同一类别,你认为他的理由主要是__________;有人说可将无机化合物KHSO4与H2SO4归为同一类别,你认为他的理由主要是__________。
22.(1)氯水具有多种性质,根据新制氯水分别与如图五种物质发生的反应填空(氯水足量):写出对应的化学方程式
①b__________;②c_________;③e____________;
(2)d实验时产生的现象是_____________;
(3)写出工业上用氯气通入石灰乳中制漂白粉的化学反应方程式为___________。
(4)实验室还可用高锰酸钾快速地制取氯气,反应的化学方程式如下:
填写字母2KMnO4+16HCl(浓)=5Cl2↑+2MnCl2+2KCl+8H2O
①请用双线桥标出该反应的电子转移方向和数目_____________。
②若消耗0.2mol氧化剂,则被氧化的还原剂的质量是___________。
23.现有以下十种物质:①H2SO4、②氨水、③Al、④金刚石、⑤Fe(OH)3胶体、⑥石墨、⑦空气、⑧BaSO4、⑨稀盐酸、⑩CaCO3
(1)对上述物质进行分类,将符合条件的物质的编号填入相应的位置:
符合条件
对应物质
混合物
电解质,但熔融状态下不导电
电解质,但难溶于水
单质,本身能导电
(2)从上述物质中选择合适的物质,发生下列反应,写出有关反应的离子方程式。
置换反应:____________;复分解反应:______________。
(3)鉴别物质⑤和⑨最简单的方法是:___________。
三、综合题
24.Ⅰ某课外活动小组进行Fe(OH)3胶体的制备实验并检验其性质.
(1)现有甲、乙、丙三名同学进行Fe(OH)3胶体的制备。
①甲同学的操作是:取一小烧杯,加入25mL蒸馏水加热至沸腾,向沸水中逐滴加入1~2mL
FeCl3饱和溶液,继续煮沸至混合液呈红褐色,停止加热。
②乙向饱和FeCl3溶液直接加入过量的NaOH溶液。
③丙向沸水中滴加饱和FeCl3溶液,为了使反应进行充分,煮沸10分钟。
你认为哪位同学的制备方法正确:_______,发生的化学方程式是______________。
(2)Fe(OH)3胶体稳定存在的主要原因是_____。
A.胶粒小,不受重力作用
B.胶粒带同种电荷
C.胶体具有丁达尔效应
D.胶粒能透过滤纸
(3)Fe(OH)3胶体区别于FeCl3溶液最本质的特征是________________________。
A.Fe(OH)3胶体粒子的直径在1~100nm之间
B.Fe(OH)3胶体具有丁达尔效应
C.Fe(OH)3胶体是均一的分散系
D.Fe(OH)3胶体的分散质能透过滤纸
Ⅱ根据如图所示实验装置,回答下列问题:
(1)写出下列仪器的名称:②_________,⑦__________。
(2)上述仪器中实验之前需检查装置是否会漏水的有_________________(填仪器名称)。
(3)利用装置甲制备蒸馏水时,冷凝水应从___________(填“f”或“g”)口进入。
(4)利用装置乙用CCl4从碘水中萃取碘,振荡静置后看到的现象是:________________。
(5)利用装置丁进行实验时,玻璃棒的作用是:________________________。
25.已知下列十种物质:①H2O,②Cu,③NO,④Fe2O3,⑤稀硫酸,⑥氢氧化钡,⑦饱和FeCl3溶液,⑧氨水,⑨稀硝酸,⑩硫酸铝。根据上述提供的物质,回答下列问题:
(1)属于纯净物的是__________(填序号),属于电解质的是__________(填序号)。
(2)上述物质间发生的某反应的离子方程式为H++OH?===H2O,则该反应的化学方程式为___________________________________________________。
(3)实验室制备少量Fe(OH)3胶体所用的物质有__________(填序号),反应的离子方程式为________________________________________________________。
(4)实验室配制245
mL
0.5
mol/L的硫酸铝溶液,从配制好的溶液中取出100
mL,其中含有的的数目为_______(设NA为阿伏加德罗常数的值)。
参考答案
1.B
2.D
3.C
4.A
5.A
6.C
7.C
8.D
9.D
10.B
11.D
12.C
13.B
14.D
15.B
16.D
17.C
18.C
19.B
20.B
21.BNa2CO32Na++CO32-H2SO42H++SO42-KHSO4K++H++SO42-KHSO4与NaHCO3都是由金属阳离子和酸式酸根离子构成的无机化合物,都属于酸式盐KHSO4与H2SO4都能在水溶液中电离出H+,水溶液都显酸性
22.(1)①2HCl+CaCO3=CaCl2+H2O+CO2↑
②HCl+AgNO3=AgCl↓+HNO3
③Cl2+2NaOH=NaCl+NaClO+H2O
(2)石蕊试液先变红后褪色;
(3)2Ca(OH)2+2Cl2=CaCl2+Ca(ClO)2+2H2O
(4)①②36.5g
23.(1)②⑤⑦⑨;①;⑧⑩;③⑥
(2)2A1+6H+=2Al3++3H2↑;CaCO3+2H+=Ca2++H2O+CO2↑(或其他合理答案)
(3)观察颜色(或丁达尔现象)(每空2分)
24.甲FeCl3+
3H2OFe(OH)3(胶体)+
3HClBA冷凝管蒸发皿分液漏斗、容量瓶g上层液体无色,下层液体紫红色受热均匀,防止液体飞溅
25.①②③④⑥⑩①④⑥⑩2
HNO3+
Ba(OH)2=
Ba(NO3)2+2H2O①⑦Fe
3++3
H2O
Fe(OH)3胶体+3
H+0.15NA
21世纪教育网
www.21cnjy.com
精品试卷·第
2
页
(共
2
页)
HYPERLINK
"http://21世纪教育网(www.21cnjy.com)
"
21世纪教育网(www.21cnjy.com)
第二章第一节物质的分类同步练习(含答案)
第I卷(选择题)
一、单选题
1.按照物质的树状分类和交叉分类,HNO3应属于( )
①酸 ②氢化物 ③氧化物 ④含氧酸 ⑤难挥发性酸 ⑥强氧化性酸 ⑦一元酸 ⑧化合物
A.①②③④⑤⑥⑦⑧
B.①④⑥⑦⑧
C.①⑧
D.①④⑤⑥⑦
2.下列关于物质分类的叙述中,不正确的是
A.H2SO4属于酸
B.KOH属于碱
C.NO属于氧化物
D.石灰水属于纯净物
3.下列分散系属于悬浊液的是()
A.硅酸溶胶
B.蔗糖溶液
C.泥浆水
D.氢氧化铁胶体
4.我国科学家在世界上第一次为一种名为“钴酞菁”的分子(直径为)恢复了磁性。“钴酞菁”分子结构和性质与人体内的血红素及植物体内的叶绿素非常相似。下列关于“钻酞菁”分子的说法中正确的是()
A.在水中形成的分散系能产生丁达尔效应
B.“钴酞菁”分子既能透过滤纸,也能透过半透膜
C.分子直径比钠离子小
D.在水中所形成的分散系属于悬浊液
5.下列分散系中,分散质微粒直径最大的是()
A.新制氢氧化铜悬浊液
B.淀粉溶液
C.溴的四氯化碳溶液
D.雾
6.对下列物质分类全部正确的是
①纯碱②食盐水③石灰水④烧碱⑤液态氧⑥KClO3
A.碱——①④
B.纯净物——③④⑤
C.盐——①⑥
D.混合物——②⑤
7.新型冠状病毒可通过气溶胶传播,气溶胶属于胶体的一种。下列关于胶体的叙述,正确的是()
A.依据丁达尔效应可将分散系分为溶液、胶体与浊液
B.胶体的本质特征是具有丁达尔效应
C.雾是气溶胶,在阳光下可观察到丁达尔效应
D.溶液中溶质粒子的运动有规律,胶体中分散质粒子的运动无规律,即做布朗运动
8.下列各组物质中,前一种是化合物,后一种是混合物的是()
A.铝土矿,洁净的雨水
B.红磷,空气
C.氢氧化钾,含铜80%的氧化铜
D.蒸馏水,粗盐
9.生物学家借助新的显微技术,成功观察到小于200纳米的微粒。下列分散系中,分散质粒径最小的是
A.雾
B.蛋白质溶液
C.石灰乳
D.KNO3溶液
10.古诗词是我国重要的文化遗产,下列诗句中加点字部分示涉及化学反应的是
A.月波成露露成霜,借与南枝作淡妆
B.春蚕到死丝方尽,蜡炬成灰泪始干
C.宝剑锋从磨砺出,梅花香自苦寒来
D.莫道雪融便无迹,雪融成水水成冰
11.下列关于酸、碱、盐的说法正确的是(
)
A.电离时生成的阳离子中有氢离子的化合物是酸
B.电离时生成的阴离子中有氢氧根离子的化合物是碱
C.电离时只生成金属阳离子和酸根离子的化合物才是盐
D.NH4Cl的电离方程式是NH4Cl=NH4++Cl-,所以NH4Cl是盐
12.下列属于碱的是(
)
A.NaHCO3
B.Na2CO3
C.Ca(OH)2
D.Cu2(OH)2CO3
13.下列关于分散系的说法不正确的是
A.分散系的稳定性:溶液>胶体>浊液
B.分散质粒子的大小:溶液>胶体>浊液
C.分散质粒子的直径为几纳米或几十纳米的分散系是胶体
D.可以用过滤的方法将悬浊液中的分散质从分散剂中分离出来
14.下列物质分类正确的是()
选项
碱
酸
盐
氧化物
A
生石灰
盐酸
纯碱
二氧化硫
B
烧碱
硫酸
氯化钠
氯酸钾
C
苛性钠
醋酸
碳酸钙
磷酸
D
苛性钾
碳酸
苏打
三氧化硫
A.A
B.B
C.C
D.D
15.当光束通过下列分散系时,能观察到丁达尔效应的是
A.KCl溶液
B.Fe(OH)3胶体
C.KOH溶液
D.Na2SO4溶液
16.新冠病毒由蛋白质外壳和单链核酸组成,直径大约在60~140nm,怕酒精,不耐高温。下列说法正确的是
A.病毒由碳、氢、氧三种元素组成
B.新冠病毒扩散到空气中不可能形成胶体
C.医用酒精能用于消毒是因为它有强氧化性
D.高温可使蛋白质发生变性
17.下列实验装置或操作与粒子直径的大小无直接关系的是()
A.过滤B.渗析
C.萃取D.丁达尔效应
18.下列分类或归类正确的是()
①液氯、氨水、干冰、碘化银均为纯净物?
②CaCl2、NaOH、HCl、IBr均为化合物??
③明矾、水银、烧碱、硫酸均为电解质④火碱、纯碱、碳酸钙都是电解质?
⑤碘酒、淀粉、云雾、纳米材料均为胶体
A.①③④
B.②③
C.②④
D.②③④⑤
19.下列逻辑关系图中正确的是
A.
B.
C.
D.
20.某同学在实验室进行如图所示实验,下列说法中不正确的是
A.X中的浓溶液滴入沸水中可得到Z中液体
B.X中分散系能产生丁达尔效应
C.用过滤和渗析的方法,可将Z中液体分离提纯
D.Y中反应离子方程式:3CaCO3+2Fe3++3H2O=2Fe(OH)3(胶体)+3CO2↑+3Ca2+
第II卷(非选择题)
二、填空题
21.回答下列问题。
(1)下列物质能导电且属于电解质的是__________(填序号)。
A.固态氯化镁(MgCl2)
B.液态氯化镁(MgCl2)
C.氯化钠溶液
D.铝
(2)写出下列物质在水溶液中的电离方程式:
①Na2CO3__________;②H2SO4________;③KHSO4________;
(3)有人说可将无机化合物KHSO4与NaHCO3归为同一类别,你认为他的理由主要是__________;有人说可将无机化合物KHSO4与H2SO4归为同一类别,你认为他的理由主要是__________。
22.(1)氯水具有多种性质,根据新制氯水分别与如图五种物质发生的反应填空(氯水足量):写出对应的化学方程式
①b__________;②c_________;③e____________;
(2)d实验时产生的现象是_____________;
(3)写出工业上用氯气通入石灰乳中制漂白粉的化学反应方程式为___________。
(4)实验室还可用高锰酸钾快速地制取氯气,反应的化学方程式如下:
填写字母2KMnO4+16HCl(浓)=5Cl2↑+2MnCl2+2KCl+8H2O
①请用双线桥标出该反应的电子转移方向和数目_____________。
②若消耗0.2mol氧化剂,则被氧化的还原剂的质量是___________。
23.现有以下十种物质:①H2SO4、②氨水、③Al、④金刚石、⑤Fe(OH)3胶体、⑥石墨、⑦空气、⑧BaSO4、⑨稀盐酸、⑩CaCO3
(1)对上述物质进行分类,将符合条件的物质的编号填入相应的位置:
符合条件
对应物质
混合物
电解质,但熔融状态下不导电
电解质,但难溶于水
单质,本身能导电
(2)从上述物质中选择合适的物质,发生下列反应,写出有关反应的离子方程式。
置换反应:____________;复分解反应:______________。
(3)鉴别物质⑤和⑨最简单的方法是:___________。
三、综合题
24.Ⅰ某课外活动小组进行Fe(OH)3胶体的制备实验并检验其性质.
(1)现有甲、乙、丙三名同学进行Fe(OH)3胶体的制备。
①甲同学的操作是:取一小烧杯,加入25mL蒸馏水加热至沸腾,向沸水中逐滴加入1~2mL
FeCl3饱和溶液,继续煮沸至混合液呈红褐色,停止加热。
②乙向饱和FeCl3溶液直接加入过量的NaOH溶液。
③丙向沸水中滴加饱和FeCl3溶液,为了使反应进行充分,煮沸10分钟。
你认为哪位同学的制备方法正确:_______,发生的化学方程式是______________。
(2)Fe(OH)3胶体稳定存在的主要原因是_____。
A.胶粒小,不受重力作用
B.胶粒带同种电荷
C.胶体具有丁达尔效应
D.胶粒能透过滤纸
(3)Fe(OH)3胶体区别于FeCl3溶液最本质的特征是________________________。
A.Fe(OH)3胶体粒子的直径在1~100nm之间
B.Fe(OH)3胶体具有丁达尔效应
C.Fe(OH)3胶体是均一的分散系
D.Fe(OH)3胶体的分散质能透过滤纸
Ⅱ根据如图所示实验装置,回答下列问题:
(1)写出下列仪器的名称:②_________,⑦__________。
(2)上述仪器中实验之前需检查装置是否会漏水的有_________________(填仪器名称)。
(3)利用装置甲制备蒸馏水时,冷凝水应从___________(填“f”或“g”)口进入。
(4)利用装置乙用CCl4从碘水中萃取碘,振荡静置后看到的现象是:________________。
(5)利用装置丁进行实验时,玻璃棒的作用是:________________________。
25.已知下列十种物质:①H2O,②Cu,③NO,④Fe2O3,⑤稀硫酸,⑥氢氧化钡,⑦饱和FeCl3溶液,⑧氨水,⑨稀硝酸,⑩硫酸铝。根据上述提供的物质,回答下列问题:
(1)属于纯净物的是__________(填序号),属于电解质的是__________(填序号)。
(2)上述物质间发生的某反应的离子方程式为H++OH?===H2O,则该反应的化学方程式为___________________________________________________。
(3)实验室制备少量Fe(OH)3胶体所用的物质有__________(填序号),反应的离子方程式为________________________________________________________。
(4)实验室配制245
mL
0.5
mol/L的硫酸铝溶液,从配制好的溶液中取出100
mL,其中含有的的数目为_______(设NA为阿伏加德罗常数的值)。
参考答案
1.B
2.D
3.C
4.A
5.A
6.C
7.C
8.D
9.D
10.B
11.D
12.C
13.B
14.D
15.B
16.D
17.C
18.C
19.B
20.B
21.BNa2CO32Na++CO32-H2SO42H++SO42-KHSO4K++H++SO42-KHSO4与NaHCO3都是由金属阳离子和酸式酸根离子构成的无机化合物,都属于酸式盐KHSO4与H2SO4都能在水溶液中电离出H+,水溶液都显酸性
22.(1)①2HCl+CaCO3=CaCl2+H2O+CO2↑
②HCl+AgNO3=AgCl↓+HNO3
③Cl2+2NaOH=NaCl+NaClO+H2O
(2)石蕊试液先变红后褪色;
(3)2Ca(OH)2+2Cl2=CaCl2+Ca(ClO)2+2H2O
(4)①②36.5g
23.(1)②⑤⑦⑨;①;⑧⑩;③⑥
(2)2A1+6H+=2Al3++3H2↑;CaCO3+2H+=Ca2++H2O+CO2↑(或其他合理答案)
(3)观察颜色(或丁达尔现象)(每空2分)
24.甲FeCl3+
3H2OFe(OH)3(胶体)+
3HClBA冷凝管蒸发皿分液漏斗、容量瓶g上层液体无色,下层液体紫红色受热均匀,防止液体飞溅
25.①②③④⑥⑩①④⑥⑩2
HNO3+
Ba(OH)2=
Ba(NO3)2+2H2O①⑦Fe
3++3
H2O
Fe(OH)3胶体+3
H+0.15NA
21世纪教育网
www.21cnjy.com
精品试卷·第
2
页
(共
2
页)
HYPERLINK
"http://21世纪教育网(www.21cnjy.com)
"
21世纪教育网(www.21cnjy.com)
