氯气的生产原理课件
图片预览






文档简介
(共35张PPT)
从海水中获得的化学物质
专题 2
第一单元
氯、溴、碘及其化合物
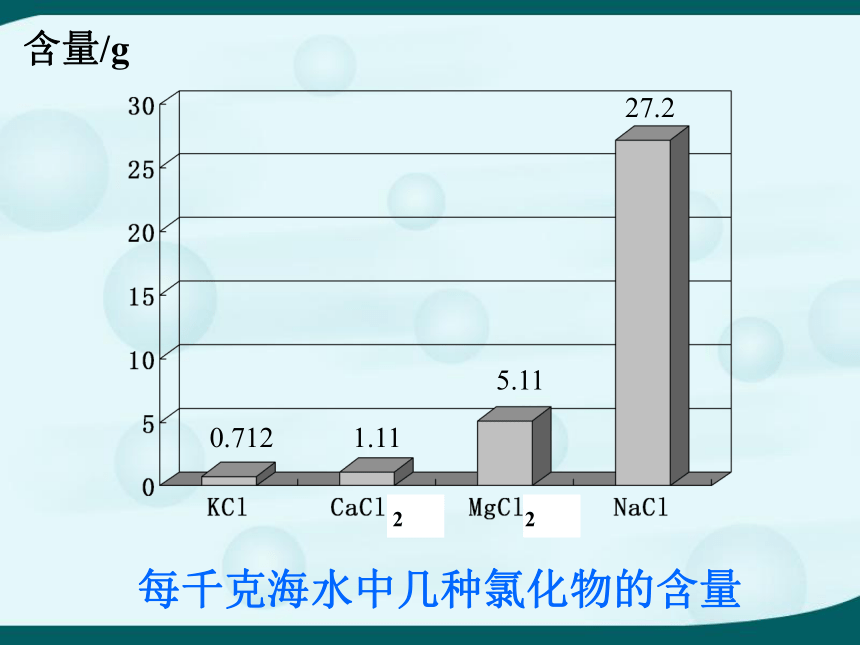
每千克海水中几种氯化物的含量
含量/g
0.712
1.11
5.11
27.2
2
2
2
查阅有关资料了解人们是如何从海水中获得氯化钠和使用氯化钠的。
人们是如何从海水中获得氯化钠的?
海水晒盐过程
海水
蒸发池
粗盐
母液
纯净的NaCl
过滤
提纯
蒸发,结晶
海水
精盐
提纯
粗盐
含泥沙、Ca2+、Mg2+、SO42-等
NaCl晶体
蒸发结晶
氯气的生产原理
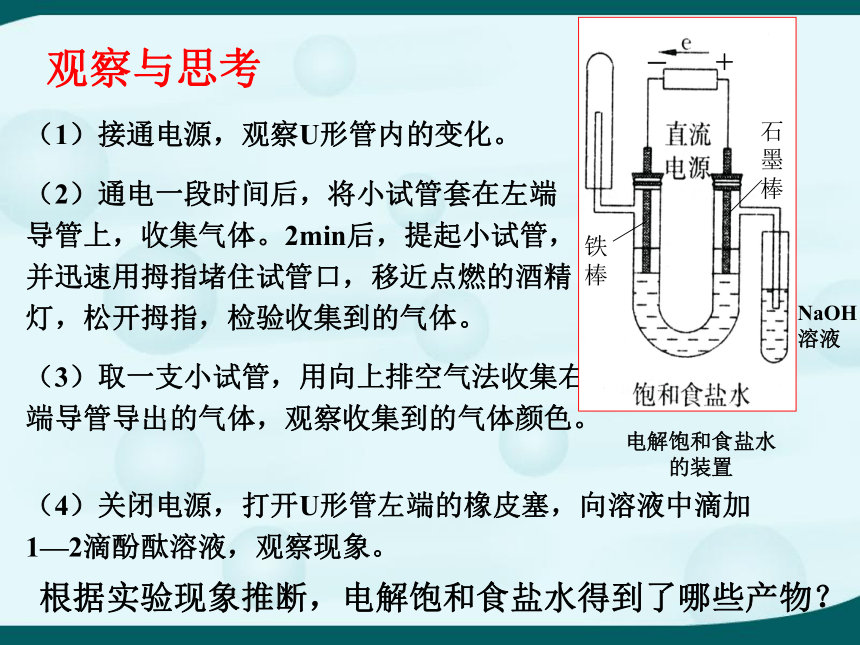
(1)接通电源,观察U形管内的变化。
(2)通电一段时间后,将小试管套在左端导管上,收集气体。2min后,提起小试管,并迅速用拇指堵住试管口,移近点燃的酒精灯,松开拇指,检验收集到的气体。
(4)关闭电源,打开U形管左端的橡皮塞,向溶液中滴加1—2滴酚酞溶液,观察现象。
(3)取一支小试管,用向上排空气法收集右端导管导出的气体,观察收集到的气体颜色。
观察与思考
NaOH溶液
电解饱和食盐水的装置
+
-
铁棒
石墨棒
根据实验现象推断,电解饱和食盐水得到了哪些产物?
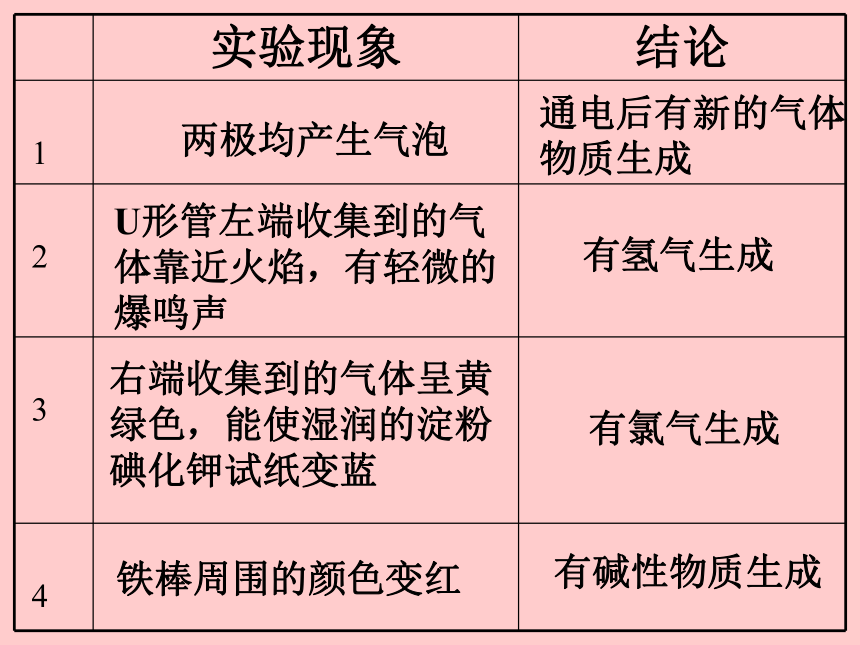
实验现象 结论
1
2
3
4
两极均产生气泡
通电后有新的气体物质生成
U形管左端收集到的气体靠近火焰,有轻微的爆鸣声
有氢气生成
右端收集到的气体呈黄绿色,能使湿润的淀粉碘化钾试纸变蓝
有氯气生成
铁棒周围的颜色变红
有碱性物质生成
2NaCl+2H2O 2NaOH+H2↑+Cl2↑
通电
电解饱和食盐水的化学方程式:
工业上电解食盐水制得氯气,还得到氢气和氢氧化钠,它们都是重要的化工原料。以电解食盐水为基础制取氯气等产品的工业称为“氯碱工业”。
-1
+1
0
0
舍勒 【瑞典】 1742一1786
18世纪,人们致力于采矿事业, 瑞典化学家舍勒 也把精力放在了软锰矿(主要成分是MnO2)的研究上。
1774年的一天当他把软锰矿粉末和浓盐酸混合加热时,惊奇的看到一种黄绿色的气体冒出。这种呛人的气体不但能使染料褪色,还有许多奇特的性质。
直到1807年,英国化学家戴维对这种气体进行了细致的研究,并于1810年11月在英国皇家学会上正式定名确认上述黄绿色气体是由一种新元素组成,英文定名为“Chlorine”,希腊文的意思是“绿色的”。
1、反应原料:
浓盐酸(液体) 与二氧化锰(固体)
2、实验原理:
MnO2 + 4HCl(浓) = MnCl2 + Cl2 ↑ + 2H2O
(二)氯气的实验室制法
3、发生装置:
固体+液体 气体
实验室制取氯气与制取氧气、氢气的装置相同吗?
根据氯气的实验室制备原理选择合适的仪器并描述装置搭建
可根据反应物状态和反应条件选择气体发生装置
发生装置
交流与讨论1
固+液→气
H2 CO2
固 + 液 → 气
固+固→气
O2
下面有四种常见的气体收集装置,请根据下列提示的Cl2的性质选择合适的装置( )
信息
1、Cl2 有毒,且密度比空气大
2、Cl2能溶于水,难溶于饱和食盐水
A
B
可根据气体的密度和溶解度选择气体收集装置
B C
收集装置
饱和食盐水
C
交流与讨论2
气体从长导管进入
讨论如何用该装置来收集CO2和 H2
CO2:气体从长导管进入
H2:气体从短导管进入
实验室制得的多余氯气可以直接排到空气中去吗?如果不可以,应如何处理?请选择合适的装置( )
可根据气体的性质选择尾气吸收装置
D1 D2
信息
1、Cl2有毒。
2、Cl2能与NaOH溶液反应,生成能溶于水的物质
3、Cl2不能燃烧
尾气处理装置
交流与讨论3
发生装置
收集装置
尾气吸收装置
这样收集到的氯气纯净吗?
请你评价、大胆质疑并且提出合理的实验解决方案。
Cl2
HCl气体
水蒸气
可根据杂质的性质选择气体净化装置.
( C2 )
( C4 C5)
信息
1、Cl2能溶于水,难溶于饱和食盐水,
HCl易溶于饱和食盐水
2、Cl2能与NaOH反应,生成能溶于水的物质
若想制得纯净、干燥的氯气,请根据提示信息选择合适的装置。
净化装置
交流与讨论4
无水CaCl2
C5
发生装置
收集装置
尾气吸收装置
净化装置
除去HCl
除去水蒸气
实验室制备氯气的改进装置图
启示:根据反应反应物的状态、反应条件、生成气体的性质等因素综合考虑而决定
实验室制气装置的选取需要考虑哪些因素?
5、收集装置:向上排空气法
或排饱和食盐水法
7、尾气处理:NaOH溶液
6、氯气的检验:湿润的淀粉碘化钾
试纸(变蓝)
4、净化装置:
饱和食盐水
浓硫酸
使用浓盐酸与足量的MnO2共热制Cl2,实际产生的Cl2总比理论值低,其主要原因是什么?
随着反应的进行,浓盐酸的物质的量浓度逐渐变小,稀盐酸与MnO2不反应,另外加热过程中,一部分浓盐酸挥发掉,也会使盐酸变稀。
1.海水中所含的化学资源中最多的是( )
A.钾和硫 B.钙和溴 C.钠和氯 D.铀和金
C
2、实验室用KMnO4制氧气,为除去粘附在试管壁上的MnO2,可用试剂是 ( )
A.汽油 B.水
C.稀盐酸 D.浓盐酸
D
3、实验室制氯气时有如下操作,操作顺序正确的是 ( ) ①连接好装置,检查气密性 ②缓缓加热,加快反应,使气体均匀逸出 ③在烧瓶中加入二氧化锰粉末 ④往分液漏斗中加入浓盐酸,再缓缓滴入烧瓶中 ⑤用向上排空气法收集氯气,尾气导入吸收剂中
A.①②③④⑤ B.④③①②⑤
C.①③④②⑤ D.①④③②⑤
C
4、工业上利用电解饱和食盐水的方法制取 、 和 。在电源正极上方收集到的气体能使湿润的 变蓝色,证明是 ;在电源负极上方收集到的气体是 ,在电极附近的水溶液中滴几滴酚酞溶液,则溶液 ,证明有 生成。若电解一段时间后,电源正极上方收集到的气体在标准状况下为4.48L,则在电源负极上方将收集到 g 气体,在溶液中产生 g 。停止通电后,待溶液混合均匀,溶液的pH会 。
Cl2
H2
NaOH
淀粉碘化钾试纸
Cl2
H2
变红
NaOH
0.4g
H2
16g
NaOH
升高
5、某学生设计如下实验装置用于制备纯净的氯气。
(1)装置中有六处错误,请指出。
① ,
② ,
③ ,
④ ,
⑤ ,
⑥ 。
烧瓶下面缺石棉网
铁圈下面缺酒精灯
原料使用了稀盐酸
不应使用长颈漏斗
盛浓硫酸的洗气瓶和盛饱和食盐水的洗气瓶位置颠倒了
洗气瓶D的气体入口导管应深插在液面下,而出口导管应靠近瓶塞
从海水中获得的化学物质
专题 2
第一单元
氯、溴、碘及其化合物
每千克海水中几种氯化物的含量
含量/g
0.712
1.11
5.11
27.2
2
2
2
查阅有关资料了解人们是如何从海水中获得氯化钠和使用氯化钠的。
人们是如何从海水中获得氯化钠的?
海水晒盐过程
海水
蒸发池
粗盐
母液
纯净的NaCl
过滤
提纯
蒸发,结晶
海水
精盐
提纯
粗盐
含泥沙、Ca2+、Mg2+、SO42-等
NaCl晶体
蒸发结晶
氯气的生产原理
(1)接通电源,观察U形管内的变化。
(2)通电一段时间后,将小试管套在左端导管上,收集气体。2min后,提起小试管,并迅速用拇指堵住试管口,移近点燃的酒精灯,松开拇指,检验收集到的气体。
(4)关闭电源,打开U形管左端的橡皮塞,向溶液中滴加1—2滴酚酞溶液,观察现象。
(3)取一支小试管,用向上排空气法收集右端导管导出的气体,观察收集到的气体颜色。
观察与思考
NaOH溶液
电解饱和食盐水的装置
+
-
铁棒
石墨棒
根据实验现象推断,电解饱和食盐水得到了哪些产物?
实验现象 结论
1
2
3
4
两极均产生气泡
通电后有新的气体物质生成
U形管左端收集到的气体靠近火焰,有轻微的爆鸣声
有氢气生成
右端收集到的气体呈黄绿色,能使湿润的淀粉碘化钾试纸变蓝
有氯气生成
铁棒周围的颜色变红
有碱性物质生成
2NaCl+2H2O 2NaOH+H2↑+Cl2↑
通电
电解饱和食盐水的化学方程式:
工业上电解食盐水制得氯气,还得到氢气和氢氧化钠,它们都是重要的化工原料。以电解食盐水为基础制取氯气等产品的工业称为“氯碱工业”。
-1
+1
0
0
舍勒 【瑞典】 1742一1786
18世纪,人们致力于采矿事业, 瑞典化学家舍勒 也把精力放在了软锰矿(主要成分是MnO2)的研究上。
1774年的一天当他把软锰矿粉末和浓盐酸混合加热时,惊奇的看到一种黄绿色的气体冒出。这种呛人的气体不但能使染料褪色,还有许多奇特的性质。
直到1807年,英国化学家戴维对这种气体进行了细致的研究,并于1810年11月在英国皇家学会上正式定名确认上述黄绿色气体是由一种新元素组成,英文定名为“Chlorine”,希腊文的意思是“绿色的”。
1、反应原料:
浓盐酸(液体) 与二氧化锰(固体)
2、实验原理:
MnO2 + 4HCl(浓) = MnCl2 + Cl2 ↑ + 2H2O
(二)氯气的实验室制法
3、发生装置:
固体+液体 气体
实验室制取氯气与制取氧气、氢气的装置相同吗?
根据氯气的实验室制备原理选择合适的仪器并描述装置搭建
可根据反应物状态和反应条件选择气体发生装置
发生装置
交流与讨论1
固+液→气
H2 CO2
固 + 液 → 气
固+固→气
O2
下面有四种常见的气体收集装置,请根据下列提示的Cl2的性质选择合适的装置( )
信息
1、Cl2 有毒,且密度比空气大
2、Cl2能溶于水,难溶于饱和食盐水
A
B
可根据气体的密度和溶解度选择气体收集装置
B C
收集装置
饱和食盐水
C
交流与讨论2
气体从长导管进入
讨论如何用该装置来收集CO2和 H2
CO2:气体从长导管进入
H2:气体从短导管进入
实验室制得的多余氯气可以直接排到空气中去吗?如果不可以,应如何处理?请选择合适的装置( )
可根据气体的性质选择尾气吸收装置
D1 D2
信息
1、Cl2有毒。
2、Cl2能与NaOH溶液反应,生成能溶于水的物质
3、Cl2不能燃烧
尾气处理装置
交流与讨论3
发生装置
收集装置
尾气吸收装置
这样收集到的氯气纯净吗?
请你评价、大胆质疑并且提出合理的实验解决方案。
Cl2
HCl气体
水蒸气
可根据杂质的性质选择气体净化装置.
( C2 )
( C4 C5)
信息
1、Cl2能溶于水,难溶于饱和食盐水,
HCl易溶于饱和食盐水
2、Cl2能与NaOH反应,生成能溶于水的物质
若想制得纯净、干燥的氯气,请根据提示信息选择合适的装置。
净化装置
交流与讨论4
无水CaCl2
C5
发生装置
收集装置
尾气吸收装置
净化装置
除去HCl
除去水蒸气
实验室制备氯气的改进装置图
启示:根据反应反应物的状态、反应条件、生成气体的性质等因素综合考虑而决定
实验室制气装置的选取需要考虑哪些因素?
5、收集装置:向上排空气法
或排饱和食盐水法
7、尾气处理:NaOH溶液
6、氯气的检验:湿润的淀粉碘化钾
试纸(变蓝)
4、净化装置:
饱和食盐水
浓硫酸
使用浓盐酸与足量的MnO2共热制Cl2,实际产生的Cl2总比理论值低,其主要原因是什么?
随着反应的进行,浓盐酸的物质的量浓度逐渐变小,稀盐酸与MnO2不反应,另外加热过程中,一部分浓盐酸挥发掉,也会使盐酸变稀。
1.海水中所含的化学资源中最多的是( )
A.钾和硫 B.钙和溴 C.钠和氯 D.铀和金
C
2、实验室用KMnO4制氧气,为除去粘附在试管壁上的MnO2,可用试剂是 ( )
A.汽油 B.水
C.稀盐酸 D.浓盐酸
D
3、实验室制氯气时有如下操作,操作顺序正确的是 ( ) ①连接好装置,检查气密性 ②缓缓加热,加快反应,使气体均匀逸出 ③在烧瓶中加入二氧化锰粉末 ④往分液漏斗中加入浓盐酸,再缓缓滴入烧瓶中 ⑤用向上排空气法收集氯气,尾气导入吸收剂中
A.①②③④⑤ B.④③①②⑤
C.①③④②⑤ D.①④③②⑤
C
4、工业上利用电解饱和食盐水的方法制取 、 和 。在电源正极上方收集到的气体能使湿润的 变蓝色,证明是 ;在电源负极上方收集到的气体是 ,在电极附近的水溶液中滴几滴酚酞溶液,则溶液 ,证明有 生成。若电解一段时间后,电源正极上方收集到的气体在标准状况下为4.48L,则在电源负极上方将收集到 g 气体,在溶液中产生 g 。停止通电后,待溶液混合均匀,溶液的pH会 。
Cl2
H2
NaOH
淀粉碘化钾试纸
Cl2
H2
变红
NaOH
0.4g
H2
16g
NaOH
升高
5、某学生设计如下实验装置用于制备纯净的氯气。
(1)装置中有六处错误,请指出。
① ,
② ,
③ ,
④ ,
⑤ ,
⑥ 。
烧瓶下面缺石棉网
铁圈下面缺酒精灯
原料使用了稀盐酸
不应使用长颈漏斗
盛浓硫酸的洗气瓶和盛饱和食盐水的洗气瓶位置颠倒了
洗气瓶D的气体入口导管应深插在液面下,而出口导管应靠近瓶塞
