氯气的性质
图片预览







文档简介
(共26张PPT)
1915年4月22日,在第一次世界大战的比利时战场上,德军正与英法联军对峙。忽然,从处于上风口的德军阵地上升起一股股黄绿色的云团,一直飘向处于下风口的英法阵地。毫无准备的英法士兵猝不及防,眼看着黄绿色的气体涌来,两万余名士兵先是咳嗽继而喘息,大多数士兵因中毒导致死亡。经统计,最终活下来的士兵大部分都是在黄绿色云团飘来时跑到了较高的山丘上才幸免于难,还有一些人是用湿手绢捂住了嘴才保住了性命,而这种使上万人丧命的气体就是氯气,而这场战争也作为战争史上第一次化学战记入了史册。
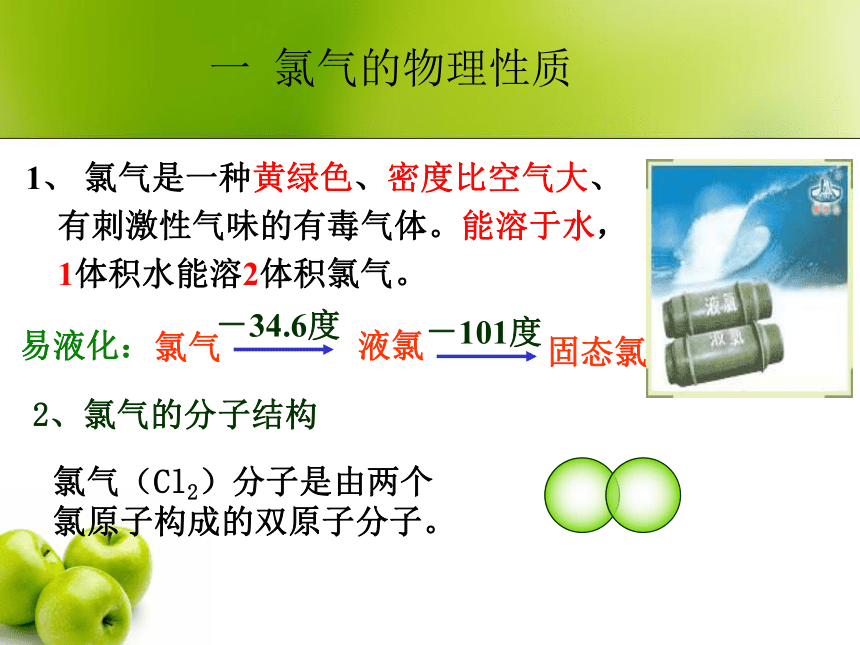
一 氯气的物理性质
2、氯气的分子结构
氯气(Cl2)分子是由两个氯原子构成的双原子分子。
1、 氯气是一种黄绿色、密度比空气大、有刺激性气味的有毒气体。能溶于水,1体积水能溶2体积氯气。
西安造纸厂氯气泄露造成59人中毒
氯气
液氯
-34.6度
固态氯
-101度
易液化:
二 氯气的化学性质
氯原子的原子结构示意图
+17
2
8
7
Cl
由于氯原子最外层电子为7个,所以它极易从外界获得1个电子达到最外层8电子稳定结构,所以氯气的化学性质极为活泼,可以与许多物质发生反应。具体表现在:
氯气可以和水反应
氯气可以和绝大多数的金属反应
氯气可以和许多非金属反应
氯气可以和碱反应
(1)氯气与金属反应
a 氯气与铁反应
点燃
2Fe+3Cl2 2FeCl3
红热的铁丝在氯气里燃烧起来,集气瓶里充满棕褐色的烟,即氯化铁晶体颗粒
化学方程式:
FeCl3溶于水显:
黄色
(K、Ca、Na、Mg、Al、Zn、Fe、Cu…)
b 氯气与铜反应
红热的铜丝在氯气里燃烧起来,集气瓶里充满棕黄色的烟,即氯化铜晶体颗粒。
点燃
Cu+Cl2 CuCl2
化学方程式:
氯化铜溶解在水里,成为蓝绿色的氯化铜溶液,溶液浓度不同时,颜色会略有不同。
小结:加热或点燃时可与大多数金属(除Au、Pt)化合,氯气显强氧化性,把变价金属(如铁、铜等)氧化成高价态。
(2) 氯气与非金属反应
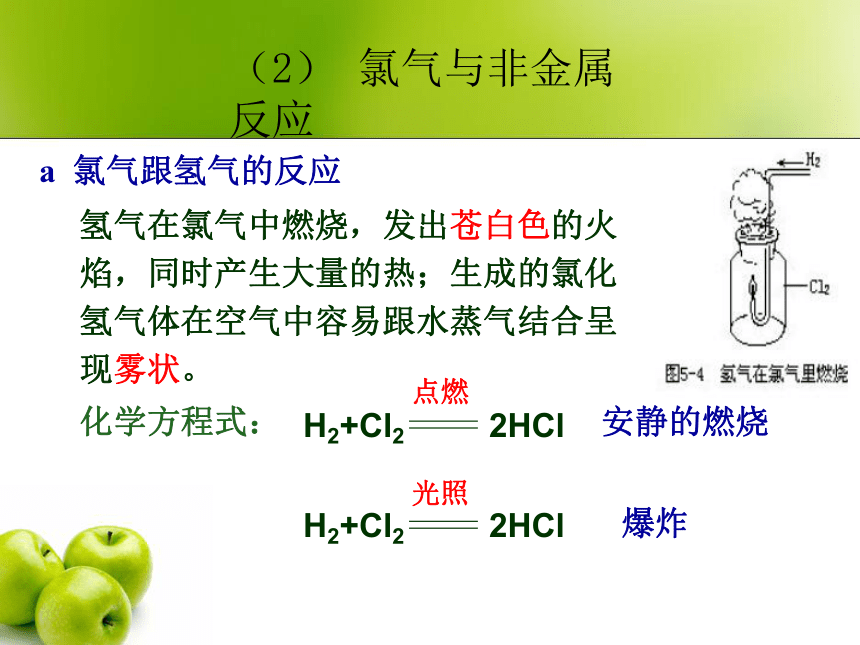
a 氯气跟氢气的反应
氢气在氯气中燃烧,发出苍白色的火焰,同时产生大量的热;生成的氯化氢气体在空气中容易跟水蒸气结合呈现雾状。
化学方程式:
点燃
H2+Cl2 2HCl
光照
H2+Cl2 2HCl
安静的燃烧
爆炸
点燃后的红磷在氯气里继续燃烧,生成三氯化磷和五氯化磷的混合物,出现白色烟雾。
b 氯气跟磷的反应
化学方程式
点燃
2P+3Cl2 2PCl3(无色液体)
点燃
2P+5Cl2 2PCl5(白色固体)
氯气量较少
氯气量较多
(3) 氯气跟水的反应
a 新制氯水成分探究
实验2
实验3
结 论
氯水既有酸性又有漂白性,盐酸显酸性,没有漂白性(HClO)
实验1
实验现象:
次氯酸有漂白性(HClO)
氯水中含有氯气,可以将I2置换出来
氯水中含有Cl-
实验4
氯水成分
次氯酸(HClO)
氯气(Cl2)
盐酸(HCl)
水(H2O)
Cl-
H+
ClO-
离子:
分子:
H2O
Cl2
HClO
氯水中的微粒有哪些?
思考:
少量OH-
b 氯气与水的反应
Cl2+H2O
可逆反应:
在相等条件下该反应既可以向正反应方向进行,又可以向逆反应方向进行。
C 次氯酸光照分解
2HClO O2 + 2HCl
光照
HCl+HClO
3. 不稳定,易分解:
现象:氯水逐渐变无色,烧瓶顶部有无色气体。
结论:氯水久置会发生变质。
保存:棕色瓶中,阴凉、避光处保存。
1. 有强氧化性、漂白性:
2. 有弱酸性 酸性:H2CO3 > HClO
HClO的性质小结:
可用于自来水杀菌、消毒,做漂白剂。
2HClO 2HCl+O2↑
光
液氯与氯水的区别?
新制氯水与久置氯水的区别?
液氯 氯水
分类
成分
性质
纯净物
混合物
分子:
离子:
Cl2、HClO、H2O
H+,Cl-,ClO-
分子:H2O
离子:H+,Cl-
新制
有氧化性,无酸性和漂白性
有酸性,强氧化性,能漂白,消毒,光照时HClO分解
久置
只有Cl2分子
实验室中使用的氯水只能现配现用
保存:棕色试剂瓶中,避光阴凉处
只有酸性
避光、密封
阴凉处保存
有效成分:NaClO
有效成分:Ca(ClO)2
(4)与碱的反应
根据氯气与水的反应原理,推测氯气与NaOH能否发生反应?若反应,其产物是什么
2NaOH+Cl2= NaClO+NaCl+H2O
2Ca(OH)2+2Cl2= Ca(ClO)2+CaCl2+2H2O
漂白粉、漂粉精
漂白液
Ca(ClO)2+CO2+H2O = CaCO3↓+2HClO
练 习
1 若一瓶氯水在阳光下放置很久,那么此时氯水的成分是什么?与新制氯水有何区别?
由于氯气与水反应生成次氯酸,而次氯酸见光易分解,Cl2 HClO HCl 这个过程不断进行,使氯水中的氯气,以及次氯酸最终全转化为HCl,所以在阳光下久置后的氯水的主要成分应是HCl。
2 用滴管将新制的氯水慢慢滴入石蕊试液,请推测将看到的实验现象。
由于氯水中含有氢离子,所以石蕊试液会先变红,然后由于次氯酸的漂白作用,又会使石蕊试液褪色。
1 氯气是黄绿色气体;密度比空气大;能溶于水,1体积水能溶2体积氯气;氯气有毒。
2 氯气的化学性质极为活泼,氯气可以和绝大多 数的金属反应,也可以和许多非金属反应
3 新制氯水成分
HClO 、HCl、 H2O
4 久制氯水成分
稀盐酸
1.下列物质属于纯净物 ( )
A. 液氯 B. 氯水 C. 石灰水 D. 盐酸
A
2. 将氯气通入紫色石蕊试液中,出现的现象是( )
A. 溶液变为红色 B. 溶液变为蓝色
C. 溶液先变红后褪色 D. 溶液不变色
C
3. 下列物质具有漂白作用的是 ( )
A.干燥的氯气 B. KCl溶液 C. 次氯酸 D. 过氧化钠
CD
课堂练习
4、下列对Cl2的性质叙述不正确的是( )
A.黄绿色 B.不溶于水
C.有毒 D.不支持燃烧
BD
5、下列化合物中,不能由氯气和相应的金属直接反应来制取的是( )
A. FeCl3 B. CaCl2 C. FeCl2 D. KCl
C
6、 氯气、液氯、盐酸、氯水中均含有 ( )
A. 氯分子 B. 氯原子 C. 氯离子 D. 氯元素
D
7、 用自来水养金鱼时,应先把自来水晒几天,目的是_____________________,有关反应的化学方程式为:_________________________ 。
除去氯气和次氯酸
Cl2+ H2O = HCl +HClO, 2HClO = 2HCl +O2↑
氯水中含有多种成分,向氯水中加入以下各种物质匀会出现明显现象和反应。请指出起作用的微粒。
(1)加入石灰石颗粒有气泡放出
(2)加入品红溶液,褪色
(3)加入氯化钠晶体,晶体逐渐消失
(4)加入硝酸银溶液产生白色沉淀
(5)加入石蕊试液先变红,后褪色
氯气泄漏现场一片苍凉
氯气泄漏现场一片苍凉
消防官兵赶赴现场救治中毒人员
氯气的危害:氯气对眼、呼吸道粘膜有刺激作用,可引起急性中毒和肺损伤;氯气可损害人全身器官和系统。
大气中氯气的浓度不得超过0.1mg/m3,生产车间不超过1mg/m3 居民区不超过0.03mg/m3。
如果中毒,保持安静,注意保温,吸入少量乙醇和乙醚蒸汽或氨气。
1915年4月22日,在第一次世界大战的比利时战场上,德军正与英法联军对峙。忽然,从处于上风口的德军阵地上升起一股股黄绿色的云团,一直飘向处于下风口的英法阵地。毫无准备的英法士兵猝不及防,眼看着黄绿色的气体涌来,两万余名士兵先是咳嗽继而喘息,大多数士兵因中毒导致死亡。经统计,最终活下来的士兵大部分都是在黄绿色云团飘来时跑到了较高的山丘上才幸免于难,还有一些人是用湿手绢捂住了嘴才保住了性命,而这种使上万人丧命的气体就是氯气,而这场战争也作为战争史上第一次化学战记入了史册。
一 氯气的物理性质
2、氯气的分子结构
氯气(Cl2)分子是由两个氯原子构成的双原子分子。
1、 氯气是一种黄绿色、密度比空气大、有刺激性气味的有毒气体。能溶于水,1体积水能溶2体积氯气。
西安造纸厂氯气泄露造成59人中毒
氯气
液氯
-34.6度
固态氯
-101度
易液化:
二 氯气的化学性质
氯原子的原子结构示意图
+17
2
8
7
Cl
由于氯原子最外层电子为7个,所以它极易从外界获得1个电子达到最外层8电子稳定结构,所以氯气的化学性质极为活泼,可以与许多物质发生反应。具体表现在:
氯气可以和水反应
氯气可以和绝大多数的金属反应
氯气可以和许多非金属反应
氯气可以和碱反应
(1)氯气与金属反应
a 氯气与铁反应
点燃
2Fe+3Cl2 2FeCl3
红热的铁丝在氯气里燃烧起来,集气瓶里充满棕褐色的烟,即氯化铁晶体颗粒
化学方程式:
FeCl3溶于水显:
黄色
(K、Ca、Na、Mg、Al、Zn、Fe、Cu…)
b 氯气与铜反应
红热的铜丝在氯气里燃烧起来,集气瓶里充满棕黄色的烟,即氯化铜晶体颗粒。
点燃
Cu+Cl2 CuCl2
化学方程式:
氯化铜溶解在水里,成为蓝绿色的氯化铜溶液,溶液浓度不同时,颜色会略有不同。
小结:加热或点燃时可与大多数金属(除Au、Pt)化合,氯气显强氧化性,把变价金属(如铁、铜等)氧化成高价态。
(2) 氯气与非金属反应
a 氯气跟氢气的反应
氢气在氯气中燃烧,发出苍白色的火焰,同时产生大量的热;生成的氯化氢气体在空气中容易跟水蒸气结合呈现雾状。
化学方程式:
点燃
H2+Cl2 2HCl
光照
H2+Cl2 2HCl
安静的燃烧
爆炸
点燃后的红磷在氯气里继续燃烧,生成三氯化磷和五氯化磷的混合物,出现白色烟雾。
b 氯气跟磷的反应
化学方程式
点燃
2P+3Cl2 2PCl3(无色液体)
点燃
2P+5Cl2 2PCl5(白色固体)
氯气量较少
氯气量较多
(3) 氯气跟水的反应
a 新制氯水成分探究
实验2
实验3
结 论
氯水既有酸性又有漂白性,盐酸显酸性,没有漂白性(HClO)
实验1
实验现象:
次氯酸有漂白性(HClO)
氯水中含有氯气,可以将I2置换出来
氯水中含有Cl-
实验4
氯水成分
次氯酸(HClO)
氯气(Cl2)
盐酸(HCl)
水(H2O)
Cl-
H+
ClO-
离子:
分子:
H2O
Cl2
HClO
氯水中的微粒有哪些?
思考:
少量OH-
b 氯气与水的反应
Cl2+H2O
可逆反应:
在相等条件下该反应既可以向正反应方向进行,又可以向逆反应方向进行。
C 次氯酸光照分解
2HClO O2 + 2HCl
光照
HCl+HClO
3. 不稳定,易分解:
现象:氯水逐渐变无色,烧瓶顶部有无色气体。
结论:氯水久置会发生变质。
保存:棕色瓶中,阴凉、避光处保存。
1. 有强氧化性、漂白性:
2. 有弱酸性 酸性:H2CO3 > HClO
HClO的性质小结:
可用于自来水杀菌、消毒,做漂白剂。
2HClO 2HCl+O2↑
光
液氯与氯水的区别?
新制氯水与久置氯水的区别?
液氯 氯水
分类
成分
性质
纯净物
混合物
分子:
离子:
Cl2、HClO、H2O
H+,Cl-,ClO-
分子:H2O
离子:H+,Cl-
新制
有氧化性,无酸性和漂白性
有酸性,强氧化性,能漂白,消毒,光照时HClO分解
久置
只有Cl2分子
实验室中使用的氯水只能现配现用
保存:棕色试剂瓶中,避光阴凉处
只有酸性
避光、密封
阴凉处保存
有效成分:NaClO
有效成分:Ca(ClO)2
(4)与碱的反应
根据氯气与水的反应原理,推测氯气与NaOH能否发生反应?若反应,其产物是什么
2NaOH+Cl2= NaClO+NaCl+H2O
2Ca(OH)2+2Cl2= Ca(ClO)2+CaCl2+2H2O
漂白粉、漂粉精
漂白液
Ca(ClO)2+CO2+H2O = CaCO3↓+2HClO
练 习
1 若一瓶氯水在阳光下放置很久,那么此时氯水的成分是什么?与新制氯水有何区别?
由于氯气与水反应生成次氯酸,而次氯酸见光易分解,Cl2 HClO HCl 这个过程不断进行,使氯水中的氯气,以及次氯酸最终全转化为HCl,所以在阳光下久置后的氯水的主要成分应是HCl。
2 用滴管将新制的氯水慢慢滴入石蕊试液,请推测将看到的实验现象。
由于氯水中含有氢离子,所以石蕊试液会先变红,然后由于次氯酸的漂白作用,又会使石蕊试液褪色。
1 氯气是黄绿色气体;密度比空气大;能溶于水,1体积水能溶2体积氯气;氯气有毒。
2 氯气的化学性质极为活泼,氯气可以和绝大多 数的金属反应,也可以和许多非金属反应
3 新制氯水成分
HClO 、HCl、 H2O
4 久制氯水成分
稀盐酸
1.下列物质属于纯净物 ( )
A. 液氯 B. 氯水 C. 石灰水 D. 盐酸
A
2. 将氯气通入紫色石蕊试液中,出现的现象是( )
A. 溶液变为红色 B. 溶液变为蓝色
C. 溶液先变红后褪色 D. 溶液不变色
C
3. 下列物质具有漂白作用的是 ( )
A.干燥的氯气 B. KCl溶液 C. 次氯酸 D. 过氧化钠
CD
课堂练习
4、下列对Cl2的性质叙述不正确的是( )
A.黄绿色 B.不溶于水
C.有毒 D.不支持燃烧
BD
5、下列化合物中,不能由氯气和相应的金属直接反应来制取的是( )
A. FeCl3 B. CaCl2 C. FeCl2 D. KCl
C
6、 氯气、液氯、盐酸、氯水中均含有 ( )
A. 氯分子 B. 氯原子 C. 氯离子 D. 氯元素
D
7、 用自来水养金鱼时,应先把自来水晒几天,目的是_____________________,有关反应的化学方程式为:_________________________ 。
除去氯气和次氯酸
Cl2+ H2O = HCl +HClO, 2HClO = 2HCl +O2↑
氯水中含有多种成分,向氯水中加入以下各种物质匀会出现明显现象和反应。请指出起作用的微粒。
(1)加入石灰石颗粒有气泡放出
(2)加入品红溶液,褪色
(3)加入氯化钠晶体,晶体逐渐消失
(4)加入硝酸银溶液产生白色沉淀
(5)加入石蕊试液先变红,后褪色
氯气泄漏现场一片苍凉
氯气泄漏现场一片苍凉
消防官兵赶赴现场救治中毒人员
氯气的危害:氯气对眼、呼吸道粘膜有刺激作用,可引起急性中毒和肺损伤;氯气可损害人全身器官和系统。
大气中氯气的浓度不得超过0.1mg/m3,生产车间不超过1mg/m3 居民区不超过0.03mg/m3。
如果中毒,保持安静,注意保温,吸入少量乙醇和乙醚蒸汽或氨气。
