人教版化学高中选修5-3.2 醛(22张PPT)
文档属性
| 名称 | 人教版化学高中选修5-3.2 醛(22张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-09-16 00:00:00 | ||
图片预览





文档简介
(共22张PPT)
第三章
烃的含氧衍生物
第二节
醛
分子里由烃基跟醛基相连而构成的化合物
醛
苯甲醛
肉桂醛
CH=CH—CHO
CHO
1.
物理性质
一、乙醛
无色液体,有强烈的刺激性气味,易挥发,易燃烧,密度比水小
沸点(℃):20.8
能跟水、乙醇、乙醚、氯仿等互溶
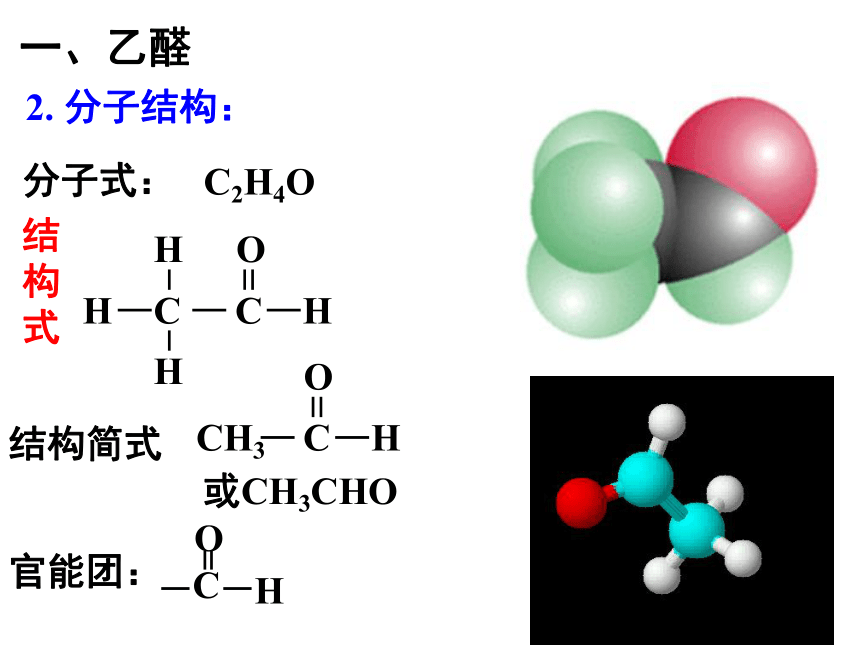
2.
分子结构:
一、乙醛
O
C
C
H
H
H
H
O
CH3
C
H
或CH3CHO
结构式
结构简式
分子式:
C2H4O
官能团:
O
C
H
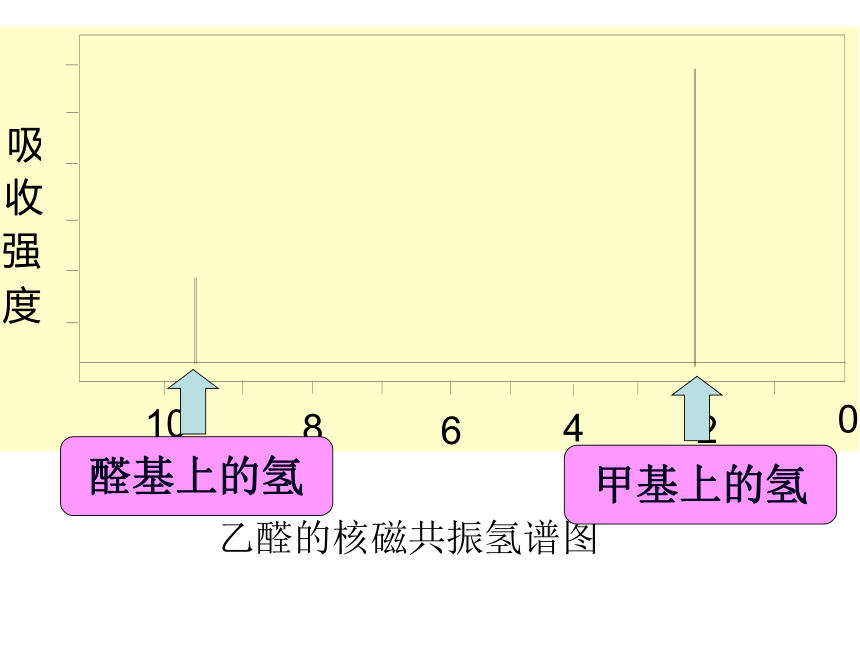
乙醛的核磁共振氢谱图
醛基上的氢
甲基上的氢
H
O
H
C
C
H
H
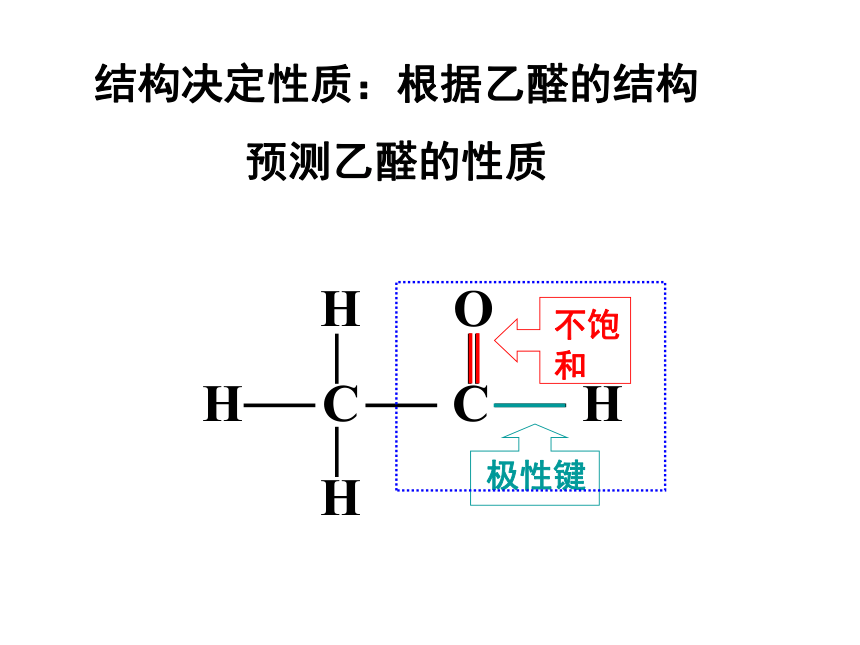
极性键
结构决定性质:根据乙醛的结构
预测乙醛的性质
不饱和
一、乙醛
3.化学性质
A.氧化反应:
P57实验3-5
①
银镜反应---与银氨溶液的反应
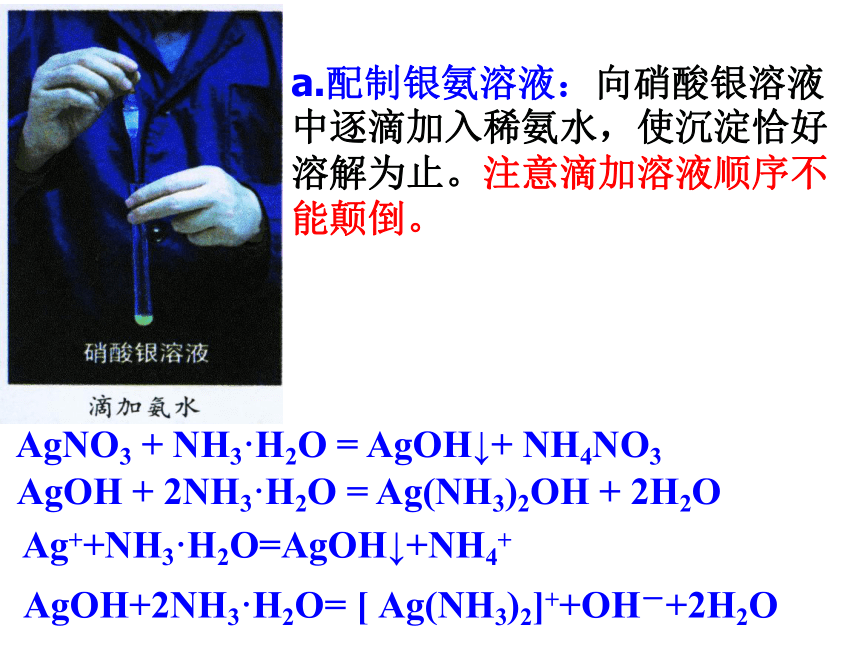
a.配制银氨溶液:向硝酸银溶液中逐滴加入稀氨水,使沉淀恰好溶解为止。注意滴加溶液顺序不能颠倒。
AgNO3
+
NH3·H2O
=
AgOH↓+
NH4NO3
AgOH
+
2NH3·H2O
=
Ag(NH3)2OH
+
2H2O
Ag++NH3·H2O=AgOH↓+NH4+
AgOH+2NH3·H2O=
[
Ag(NH3)2]++OH-+2H2O
滴入乙醛
现象:
条件:
b.
反应过程
试管内壁附着一层光亮的银镜。
水浴加热
CH3CHO
+
2Ag(NH3)2OH
△
CH3COONH4
+
2Ag↓
+
3NH3
+
H2O
CH2OH(CHOH)4CHO+2Ag(NH3)2OH
→2Ag↓+
CH2OH(CHOH)4COONH4+3NH3+H2O
你能仿照葡萄糖的银镜反应写出乙醛的银镜反应方程式吗?
1.试管内壁应洁净。
2.必须用水浴加热,不能用酒精灯加热。
3.加热时不能振荡试管和摇动试管。
4.配制银氨溶液时,氨水不能过多或过少
(只能加到最初的沉淀刚好消失)。
5.乙醛用量不可太多。
6.实验后,银镜用稀HNO3浸泡,再用水洗。
C.
做银镜反应实验的注意事项:
制备新制氢氧化铜:
在NaOH溶液中滴加少量CuSO4溶液,保证碱过量。
②
与新制氢氧化铜悬浊液反应
10%NaOH
2%CuSO4
乙醛
现象:
条件:
蓝色沉淀消失,试管中有红色沉淀。
加热至沸腾
注意:1、关注试剂加入的先后顺序及试剂的加
入量,可见,反应在碱性条件下进行。
2、
Cu(OH)2必须新制。
CH3CHO
+
2Cu(OH)2
CH3COOH
+
Cu2O↓+
2H2O
②
乙醛与新制氢氧化铜悬浊液反应
a.催化氧化的反应
2CH3CHO
+
O2
2CH3COOH
催化剂
③
与氧气反应
2CH3CHO+5O2
点燃
4CO2+4H2O
b.燃烧反应:
思考:乙醛能否使酸性高锰酸钾溶液褪色?
实验探究:乙醛能否使酸性高锰酸钾溶液褪色
结论:溶液褪色
说明乙醛可以被酸性高锰酸钾溶液氧化
B.加成反应
同时也是还原反应
还原反应:加氢或失氧
氧化反应:加氧或失氢
有机的氧化
还原反应
+
H2
CH3
—CH2—OH
△
催化剂
乙醛性质的小结:
2、还原反应(加成反应)
醛+H2
醇
1、氧化反应
a
燃烧
b
催化氧化
c
被弱氧化剂氧化
(银氨溶液、新制的Cu(OH)2)
乙酸
d
被强氧化剂氧化
(酸性高锰酸钾溶液)
1.下列配制银氨溶液的操作中,正确的是
(
)
A.在洁净的试管中加入1~2
mL
AgNO3溶液,再加入过量浓氨水,振荡,混合均匀
B.在洁净的试管中加入1~2
mL稀氨水,再逐滴加入2%
AgNO3溶液至过量
C.在洁净的试管中加入1~2
mL
AgNO3溶液,再逐滴加入浓氨水至过量
D.在洁净的试管中加2%
AgNO3溶液1~2
mL,逐滴加入2%稀氨水,边滴边振荡,至沉淀恰好溶解时为止。
D
2.洗涤做过银镜反应的试管可以选用的试剂是
(
)
A.氨水
B.NaOH溶液
C.稀硝酸
D.酒精
C
3.关于乙醛的下列反应中,乙醛被还原的是
(
)
A.乙醛的银镜反应
B.乙醛制乙醇
C.乙醛与新制氢氧化铜的反应
D.乙醛的燃烧反应
B
4.对有机物
的化学性质
叙错误的是(
)
A.能发生银镜反应
B.能使酸性高锰酸钾溶液褪色
C.1mol该有机物只能与1molH2发生加成反应
D.该有机物既能被氧化又能被还原。
CH2
CHCH
CHO
CH3
C
第三章
烃的含氧衍生物
第二节
醛
分子里由烃基跟醛基相连而构成的化合物
醛
苯甲醛
肉桂醛
CH=CH—CHO
CHO
1.
物理性质
一、乙醛
无色液体,有强烈的刺激性气味,易挥发,易燃烧,密度比水小
沸点(℃):20.8
能跟水、乙醇、乙醚、氯仿等互溶
2.
分子结构:
一、乙醛
O
C
C
H
H
H
H
O
CH3
C
H
或CH3CHO
结构式
结构简式
分子式:
C2H4O
官能团:
O
C
H
乙醛的核磁共振氢谱图
醛基上的氢
甲基上的氢
H
O
H
C
C
H
H
极性键
结构决定性质:根据乙醛的结构
预测乙醛的性质
不饱和
一、乙醛
3.化学性质
A.氧化反应:
P57实验3-5
①
银镜反应---与银氨溶液的反应
a.配制银氨溶液:向硝酸银溶液中逐滴加入稀氨水,使沉淀恰好溶解为止。注意滴加溶液顺序不能颠倒。
AgNO3
+
NH3·H2O
=
AgOH↓+
NH4NO3
AgOH
+
2NH3·H2O
=
Ag(NH3)2OH
+
2H2O
Ag++NH3·H2O=AgOH↓+NH4+
AgOH+2NH3·H2O=
[
Ag(NH3)2]++OH-+2H2O
滴入乙醛
现象:
条件:
b.
反应过程
试管内壁附着一层光亮的银镜。
水浴加热
CH3CHO
+
2Ag(NH3)2OH
△
CH3COONH4
+
2Ag↓
+
3NH3
+
H2O
CH2OH(CHOH)4CHO+2Ag(NH3)2OH
→2Ag↓+
CH2OH(CHOH)4COONH4+3NH3+H2O
你能仿照葡萄糖的银镜反应写出乙醛的银镜反应方程式吗?
1.试管内壁应洁净。
2.必须用水浴加热,不能用酒精灯加热。
3.加热时不能振荡试管和摇动试管。
4.配制银氨溶液时,氨水不能过多或过少
(只能加到最初的沉淀刚好消失)。
5.乙醛用量不可太多。
6.实验后,银镜用稀HNO3浸泡,再用水洗。
C.
做银镜反应实验的注意事项:
制备新制氢氧化铜:
在NaOH溶液中滴加少量CuSO4溶液,保证碱过量。
②
与新制氢氧化铜悬浊液反应
10%NaOH
2%CuSO4
乙醛
现象:
条件:
蓝色沉淀消失,试管中有红色沉淀。
加热至沸腾
注意:1、关注试剂加入的先后顺序及试剂的加
入量,可见,反应在碱性条件下进行。
2、
Cu(OH)2必须新制。
CH3CHO
+
2Cu(OH)2
CH3COOH
+
Cu2O↓+
2H2O
②
乙醛与新制氢氧化铜悬浊液反应
a.催化氧化的反应
2CH3CHO
+
O2
2CH3COOH
催化剂
③
与氧气反应
2CH3CHO+5O2
点燃
4CO2+4H2O
b.燃烧反应:
思考:乙醛能否使酸性高锰酸钾溶液褪色?
实验探究:乙醛能否使酸性高锰酸钾溶液褪色
结论:溶液褪色
说明乙醛可以被酸性高锰酸钾溶液氧化
B.加成反应
同时也是还原反应
还原反应:加氢或失氧
氧化反应:加氧或失氢
有机的氧化
还原反应
+
H2
CH3
—CH2—OH
△
催化剂
乙醛性质的小结:
2、还原反应(加成反应)
醛+H2
醇
1、氧化反应
a
燃烧
b
催化氧化
c
被弱氧化剂氧化
(银氨溶液、新制的Cu(OH)2)
乙酸
d
被强氧化剂氧化
(酸性高锰酸钾溶液)
1.下列配制银氨溶液的操作中,正确的是
(
)
A.在洁净的试管中加入1~2
mL
AgNO3溶液,再加入过量浓氨水,振荡,混合均匀
B.在洁净的试管中加入1~2
mL稀氨水,再逐滴加入2%
AgNO3溶液至过量
C.在洁净的试管中加入1~2
mL
AgNO3溶液,再逐滴加入浓氨水至过量
D.在洁净的试管中加2%
AgNO3溶液1~2
mL,逐滴加入2%稀氨水,边滴边振荡,至沉淀恰好溶解时为止。
D
2.洗涤做过银镜反应的试管可以选用的试剂是
(
)
A.氨水
B.NaOH溶液
C.稀硝酸
D.酒精
C
3.关于乙醛的下列反应中,乙醛被还原的是
(
)
A.乙醛的银镜反应
B.乙醛制乙醇
C.乙醛与新制氢氧化铜的反应
D.乙醛的燃烧反应
B
4.对有机物
的化学性质
叙错误的是(
)
A.能发生银镜反应
B.能使酸性高锰酸钾溶液褪色
C.1mol该有机物只能与1molH2发生加成反应
D.该有机物既能被氧化又能被还原。
CH2
CHCH
CHO
CH3
C
