人教版选修5高中化学3.3:羧酸_酯(56张PPT)
文档属性
| 名称 | 人教版选修5高中化学3.3:羧酸_酯(56张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-09-16 00:00:00 | ||
图片预览









文档简介
(共56张PPT)
第三节:羧酸
酯
一、分子组成与结构
C2H4O2
CH3COOH
结构简式:
分子式:
结构式:
官能团:
羟基
羰基
(或—COOH)
O
—C—OH
羧基
C
H
H
H
H
O
C
O
二、物理性质
无色刺激性气味液体,熔点16.6℃,低于16.6℃就凝结成冰状晶体,所以无水乙酸又称冰醋酸。乙酸易溶于水和酒精。
三、乙酸的化学性质
1、乙酸的酸性
探究活动P60——设计验证实验CH3COOH酸性强弱
酸性
H2SO3
>
CH3COOH
>
H2CO3
⑵.具酸的通性:
⑴.电离方程式:CH3COOH
CH3COO-
+
H+
⑴.电离方程式:CH3COOH
CH3COO-
+
H+
⑴.电离方程式:CH3COOH
CH3COO-
+
H+
①.利用指示剂——石蕊试液;
变红
③.与某些盐反应
与Na2CO3溶液反应生成CO2气体。
②.利用金属活动性顺序表中氢前的金属可以置换H+为H2性质。
将表面用砂纸磨过镁条插入乙酸溶液。观察现象。
酸性:
H2SO3
>
CH3COOH
>
H2CO3
2CH3COOH
+
Na2CO3→2CH3COONa
+
H2O+CO2↑
Mg
+
2CH3COOH
→
(CH3COO)2Mg
+
H2↑
与Na2SO3溶液反应不生成SO2气体
⑤.与碱性氧化物反应
④.与碱反应
CH3COOH
+
NaOH
→
CH3COONa
+
H2O
2CH3COOH
+
CuO
→
(CH3COO)2Cu
+
H2O
结论:具有酸的5点通性,是一种弱酸
【思考
交流】
你能用几种方法证明乙酸是弱酸?
方法:
1:配制一定浓度的乙酸测定PH值
2:配制一定浓度的乙酸钠测PH值
3:比较盐酸、醋酸与金属反应的速率
4:
稀释一定浓度乙酸测定PH变化
……
CH3COOH
CH3COO-+H+
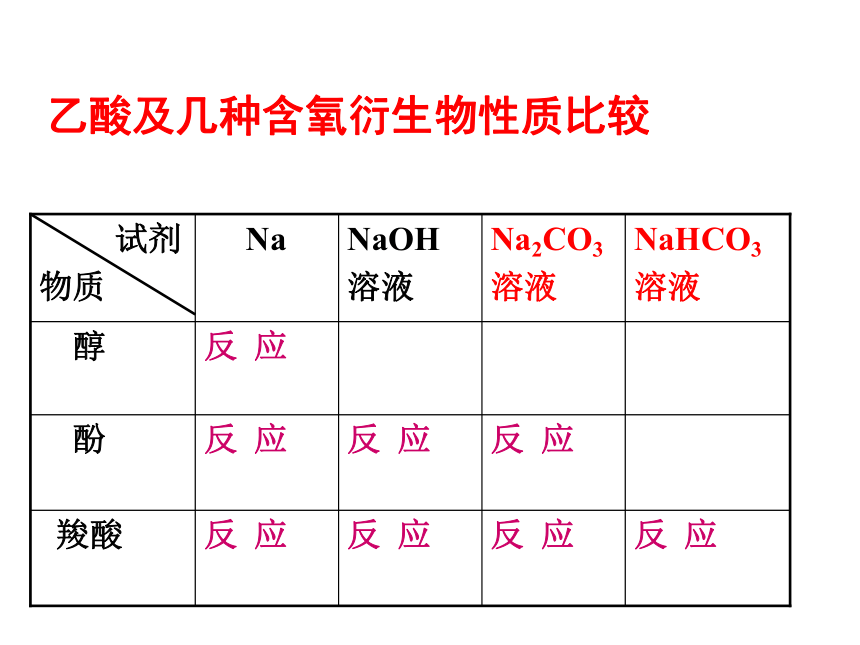
乙酸及几种含氧衍生物性质比较
反
应
反
应
反
应
反
应
羧酸
反
应
反
应
反
应
酚
反
应
醇
NaHCO3
溶液
Na2CO3
溶液
NaOH
溶液
Na
试剂
物质
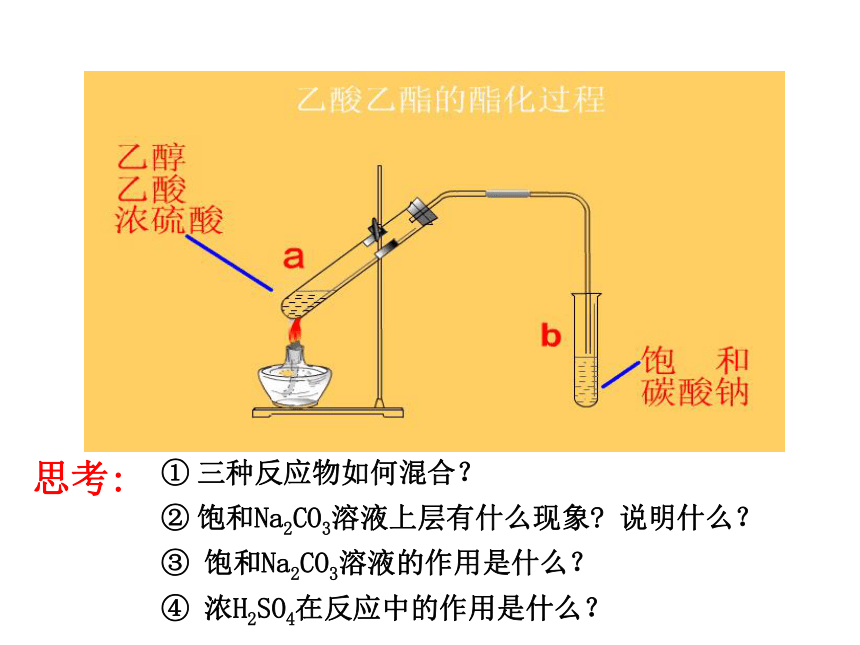
思考:
③
饱和Na2CO3溶液的作用是什么?
②
饱和Na2CO3溶液上层有什么现象?
说明什么?
①
三种反应物如何混合?
④
浓H2SO4在反应中的作用是什么?
2、酯化反应
CH3COOH
+
HOC2H5
CH3COOC2H5+H2O
定义:酸和醇起作用生成酯和水的反应叫做酯化反应。
乙酸乙酯
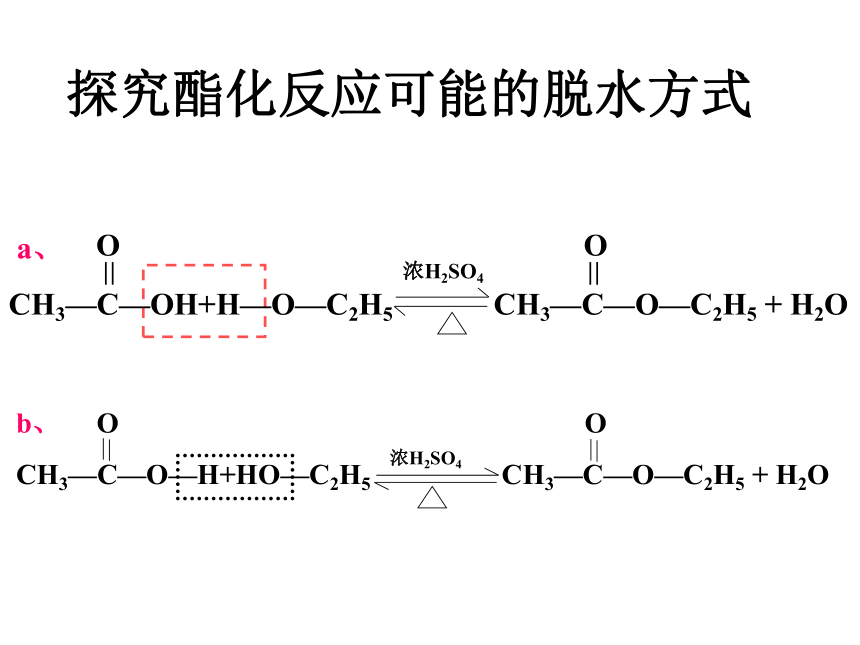
探究酯化反应可能的脱水方式
浓H2SO4
b、
O
O
CH3—C—O—H+HO—C2H5
CH3—C—O—C2H5
+
H2O
a、
CH3—C—OH+H—O—C2H5
CH3—C—O—C2H5
+
H2O
浓H2SO4
=
=
O
O
酯化反应实质:
酸脱羟基醇脱羟基上的氢原子。
CH3
C
OH
+
H
18O
C2H5
浓H2SO4
=
O
CH3
C
18O
C2H5
+
H2O
=
O
有机羧酸和无机含氧酸(如
H2SO4、HNO3等)
同位素原子示踪法
酸和醇酯化反应的类型
①一元有机羧酸与一元醇。如:
CH3COOCH3
+
H2O
CH3COOH
+
HOCH3
浓H2SO4
乙酸甲酯
②一元酸与二元醇或多元醇。如:
二乙酸乙二酯
浓H2SO4
2
③一元醇与多元羧酸分子间脱水形成酯
+2
C2H5OH
COOH
COOH
浓H2SO4
COOC2H5
COOC2H5
+2H2O
④.多元羧酸与多元醇之间的脱水反应
生成普通酯:
COOH
COOH
CH2OH
CH2OH
+
浓H2SO4
+
H2O
HOOC-COOCH2CH2OH
生成环酯:
生成高聚酯:
+
n
HOOC
COOH
n
HOCH2CH2OH
一定条件
C
C
O
CH2CH2
O
n
+
2n
H2O
O
O
浓H2SO4
+
2H2O
环乙二酸乙二酯
三种情况:生成普通酯、环状酯、髙聚酯
⑤.羟基酸自身的脱水反应
CH3CHCOOH
OH
2
浓H2SO4
CH3CHCOOCHCOOH
OH
CH3
+H2O
普通酯
CH3CHCOOH
OH
2
浓H2SO4
CH3-CH
COO
OOC
CH-CH3
+H2O
环状酯
乳酸
生成高聚酯:
一定条件
CH3
【OCHCO】n+nH2O
n
HOCHCOOH
CH3
多元羧酸与二元醇间缩聚成聚酯。如:
⑥羟基酸分子内脱水成环。如:
CH2COOH
CH2CH2OH
浓硫酸
△
O
CH2C
CH2CH2
=
O
+
H2O
+
n
HOOC
COOH
n
HOCH2CH2OH
一定条件
聚对苯二甲酸乙二酯
C
C
O
CH2CH2
O
n
+
2n
H2O
O
O
缩聚反应:
有机物分子间脱去小分子,形成高分子聚合物的反应。
1.
药品的添加顺序
2.试管倾斜加热的目的是什么?
3.浓硫酸的作用是什么?
4.得到的反应产物是否纯净?主要杂质有哪些?
5.饱和Na2CO3溶液有什么作用?
催化剂,吸水剂
不纯净;乙酸、乙醇
①
中和乙酸,消除乙酸气味对酯气味的影响,以便闻到乙酸乙酯的气味.
②
溶解乙醇。
③
冷凝酯蒸气、降低酯在水中的溶解度,以便使酯分层析出。
增大受热面积
往乙醇中滴入浓硫酸和乙酸
6.
为什么导管不插入饱和Na2CO3溶液中?有无其它防倒吸的方法?
防止受热不匀发生倒吸
酯化反应属于取代反应中的一种,
也可看作是分子间脱水反应。
思考:酯化反应属于哪一类型有机反应类型?
烷氧基取代酸中的羟基,
或者是酰基取代醇中的氢原子
四、乙酸的制法
1、乙烯氧化法:
2CH2=CH2+O2
2CH3CHO
2CH3CHO+O2
2CH3COOH
催化剂
催化剂
2、发酵法
淀粉
葡萄糖
乙醇
乙醛
乙酸
五、乙酸的用途
生产醋酸纤维、溶剂、香料、医药等
羧酸
1、羧酸:由烃基与羧基相连而构成的有机物。
2、羧酸的分类
根据烃基来分
脂肪酸:
CH3CH2COOH
CH2=CHCOOH
芳香酸:C6H5COOH
根据羧基数目分
一元酸:CH3COOH
C6H5COOH
二元酸:HOOC-COOH
多元酸
3、一元羧酸和饱和一元羧酸的通式和分子式
一元羧酸的通式:R-COOH
饱和一元羧酸通式:CnH2n+1COOH(n
≥0)
饱和一元羧酸的分子式:CnH2nO2(n≥1)
4.酸的命名:
与醛的命名方法相同
HCOOH(甲酸)、
CH3COOH(乙酸)、CH3CH2COOH(丙酸)
CH3CH2CHCOOH
2-甲基丁酸
CH3
5、几种重要的羧酸
1.甲酸(HCOOH)
结构式:
根据其结构可推断出甲酸具有些什么性质?
(1)弱酸性:
2HCOOH+Na2CO3=2HCOONa+CO2?+H2O
(2)
酯化反应
HCOOH+CH3CH2OH
HCOOCH2CH3
+
H2O
浓硫酸
△
O
OH
C
H
(3)与新制的Cu(OH)2加热反应(-CHO的性质)
2Cu(OH)2+HCOOH
+
2NaOH
Cu2O?+Na2
CO3+
4H2O
△
注:HCOOR
甲酸某酯
不但发生水解反应,还能与新制的Cu(OH)2发生反应及发生银镜反应。
O
OR
C
H
【讨论】请用一种试剂鉴别下面四种有机物?
乙醇、乙醛、乙酸、甲酸
新制Cu(OH)2悬浊液
2.乙二酸
HOOC-COOH
【物性】俗称“草酸”,无色透明晶体,通常含两个结晶水,((COOH)2?2H2O),加热至100℃时失水成无水草酸,
易溶于水和乙醇,溶于乙醚等有机溶剂。
乙二酸
+
2H2O
化学性质:草酸是最简单的饱和二元羧酸,是二元羧酸中酸性最强的,它具有一些特殊的化学性质。能使酸性高锰酸钾溶液褪色、可作漂白剂。
△
高级脂肪酸
烃基上含有较多的碳原子的羧酸叫高级脂肪酸。
硬脂酸
C18H36O2
C17H35COOH
(饱和一元酸)
软脂酸
C16H32O2
C15H31COOH
(饱和一元酸)
油酸
C18H34O2
C17H33COOH
(有一个碳碳双键是一个不饱和一元酸,)
油酸是不饱和高级脂肪酸,常温下呈液态。而硬脂酸和软脂酸在常温下呈固态。
高级脂肪酸的化学性质
(1)弱酸性,酸性比乙酸弱。
C17H35COOH+NaOH-----C17H35COONa+H2O
(2)可发生酯化反应
C17H33COOH+C2H5OH
C17H33COOC2H5+H2O
浓硫酸
△
(3)、油酸可发生加成(加H2)反应:
C17H33COOH(液态)+H2
C17H35COOH(固态)
硬脂酸不能发生上述加成反应。
催化剂
油酸可发生加成反应使溴水(X2)褪色:
C17H33COOH
+
Br2
C17H33Br2COOH
硬脂酸不能发生上述加成反应。
一、酯的概念:由羧酸与醇反应生成的一类有机物.
酯
二、酯的通式
用RCOOR,表示。
饱和一元羧酸酯的分子式:
CnH2nO2
(n≥2)
最简单的酯是甲酸甲酯:
HCOOCH3
低级酯是熔点沸点低易挥发具有芳香
气味的液体。存在于各种水果和花草中,
三.物理性质及用途:
1.物理性质:密度一般小于水,并难溶于水(乙酸乙酯微溶),易溶于乙醇和乙醚等有机溶剂。
2.酯的用途
(1)作有机溶剂;
(2)食品工业作水果香料。
振荡均匀,把三支试管同时放在70℃-80
℃的水浴中加热几分钟,观察发生的现象。
蒸馏水5.5
mL
1:5的硫酸0.5
mL蒸馏水5.0
mL
30%NaOH溶液0.5mL、蒸馏
水5.0mL
各加入6滴乙酸乙酯
1
2
3
四.酯的化学性质--酯的水解
试管3中几乎无气味
试管2中稍有气味
试管1中仍有气味
【实验现象】
试管1中乙酸乙酯没有反应
试管2和3中乙酸乙酯发生了反应。
【实验结论】
酯在酸性或碱性条件下水解,中性条件下难水解。碱性条件下酯的水解程度更大.
四.水解反应:
1.在酸中的反应方程式:
2、在碱中反应方程式:
CH3—C—OC2H5
+
NaOH
O
CH3—CONa
+
HOC2H5
O
CH3—C—O—C2H5
+
H2O
O
稀H2SO4
CH3—C—OH+H—O—C2H5
O
酯的水解反应
RCOOR,+H-OH
RCOOH
+
R,OH
水解
酯化
酯的水解和酯化互为可逆反应,酯的水解在什么条件下进行?在什么条件下水解最彻底?
酯的水解反应中,硫酸的作用是?NaOH的作用是什么?
CH3COOC2H5+H2O
CH3COOH
+
C2H5
OH
H2SO4
△
CH3COOC2H5+NaOH
CH3COONa+
C2H5OH
△
硫酸在水解反应中起催化剂的作用;
NaOH不但是催化剂,还起促进酯的水解的作用,使酯的水解完全。
O
CH3—C—O—C2H5
酯的水解
思考:水解反应的反应实质是什么?
在水解的时候断裂的是什么键?
酯的水解是酯化反应的逆反应
酯在无机酸、碱催化下,均能发生水解反应,其中在酸性条件下水解是可逆的,在碱性条件下水解是不可逆的。
酯水解的规律:
酯
+
水
无机酸
△
酸
+
醇
△
酯
+碱
有机酸盐
+
醇
五.酯的命名
根据酸和醇的名称命名为“某酸某酯”
说出下列化合物的名称:
硝酸乙酯
(3)CH3CH2O—NO2
乙酸乙酯
(2)HCOOCH2CH3
甲酸乙酯
(1)CH3COOCH2CH3
COO
CH2CH3
⑷
硝酸乙酯
苯甲酸乙酯
六.
酯的同分异构体的书写:
通CnH2nO2
结构简式:HCOOCH3
CH3COOCH
3
HCOOC2H5
名称:
甲酸甲酯
乙酸甲酯
甲酸乙酯
C4H8O2同分异构体:6种
丁酸
CH3CH2CH2COOH
CH3-CH-COOH
CH3
2-甲基丙酸
CH3CH2COOCH3
CH3COOCH2CH3
HCOOCH2CH2CH3
HCOOCH(CH3)2
丙酸甲酯
乙酸乙酯
甲酸丙酯
甲酸异丙酯
【练习】写出分子式为C8H8O2属于芳香羧酸和芳香酯的所有同分异构体
4种和6种
【练习】写出C4H8O2的属于羧酸和酯的同分异构体的结构简式
2种和4种
思考:老酒为什么格外香?
驰名中外的贵州茅台酒,做好后用坛子密封埋在地下数年后,才取出分装出售,这样酒酒香浓郁、味道纯正,独具一格,为酒中上品。它的制作方法是有科学道理的。
在一般酒中,除乙醇外,还含有有机酸、杂醇等,有机酸带酸味,杂醇气味难闻,饮用时涩口刺喉,但长期贮藏过程中有机酸能与杂醇相互酯化,形成多种酯类化合物,每种酯具有一种香气,多种酯就具有多种香气,所以老酒的香气是混合香型。浓郁而优美,由于杂醇就酯化而除去,所以口感味道也变得纯正了。
小结:几种衍生物之间的关系
1、完成下列反应的化学方程式。
(1)甲酸与甲醇与浓硫酸加热
(2)乙酸甲酯在稀硫酸中加热反应
(3)乙酸乙酯在NaOH溶液中加热反应
练习:
练习:
1.胆固醇是人体必需的生物活性物质,分子式为C27H46O
。一种胆固醇酯的液晶材料,分子式为C34H50O2
。合成这种胆固醇酯的羧酸是(
)
A.
C6H13COOH
B.
C6H5COOH
C.
C7H15COOH
D.
C3H7COOH
B
2、1mol有机物
与足量NaOH
溶
液充分反应,消耗NaOH
的物质的量为(
)
A.5mol
B.4mol
C.3mol
D.2mol
COOCH3
CH3COO
COOH
B
3、一环酯化合物,结构简式如下:
试推断:
1.该环酯化合物在酸性条件下水解的产物是什么?
写出其结构简式;
2.写出此水解产物与金属钠反应的化学方程式;
3.此水解产物是否可能与FeCl3溶液发生变色反应?
4、现有分子式为C3H6O2的四种有机物A、B、C、D,且分子内均含有甲基,把它们分别进行下列实验以鉴别之,其实验记录如下:
NaOH溶液
银氨溶液
新制Cu(OH)2
金属钠
A
中和反应
——
溶解
产生氢气
B
——
有银镜
产生红色沉淀
产生氢气
C
水解反应
有银镜
产生红色沉淀
——
D
水解反应
——
——
——
则A、B、C、D的结构简式分别为:
A:
B:
C:
D:
CH3CH2COOH
CH3CH2OHCHO
HCOOCH2CH3
CH3COOCH3
【例题】今有化合物:
(1)请写出化合物中含氧官能团的名称:
。
(2)请判别上述哪些化合物互为同分异构体:
。
(3)请分别写出鉴别甲、乙、丙化合物的方法。(指明所选试剂及主要现象即可)
鉴别甲的方法:
;
鉴别乙的方法:
;
鉴别丙的方法:
.
(4)请按酸性由强至弱排列甲、乙、丙的顺序:
。
醛基、羟基、羰基、羧基
甲、乙、丙互为同分异构体
与FeCl3溶液作用显紫色的为甲
与Na2CO3溶液作用有气泡生成的为乙
与银氨溶液共热发生银镜反应的是丙
乙>甲>丙
5.(03年高考理综试题)根据图示填空。
(1)化合物A含有的官能团是_________________。
(2)1molA与2molH2反应生成1molE,其反应方程式是______。
(3)与A具有相同官能团的A的同分异构体的结构简式是_____。
(4)B在酸性条件下与Br2反应得到D,D的结构简式是_______。
(5)F的结构简式是____。由E生成F的反应类型是__________。
油脂
高级脂肪酸的甘油酯
R1COOCH2
R2COOCH
R3COOCH2
C17H35COOCH2
C17H35COOCH2
C17H35COOCH
C15H31COOCH2
C15H31COOCH2
C15H31COOCH
C17H33COOCH2
C17H33COOCH2
C17H33COOCH
硬脂酸甘油酯(脂肪)固态
软脂酸甘油酯
油酸甘油酯(油)液态
化学性质
1、油脂的氢化
C17H33COOCH2
C17H33COOCH2
C17H33COOCH
+3H2
催化剂
C17H35COOCH2
C17H35COOCH2
C17H35COOCH
油(液态)
脂肪(固态)
2、水解反应
(1)酸性条件下水解
C17H35COOCH2
C17H35COOCH2
C17H35COOCH
+3H2O
H2SO4
△
3C17H35COOH+
CH2-OH
CH-OH
CH2-OH
在油脂酸性条件下的水解反应中,硫酸作催化剂,水解反应不完全,因其逆反应是酯化反应。
(2)油脂碱性条件下的水解
C17H35COOCH2
C17H35COOCH2
C17H35COOCH
+3NaOH
△
3C17H35COONa
CH2-OH
CH-OH
CH2-OH
+
在油脂碱性条件下的水解反应中,NaOH溶液起了催化剂和促进水解的作用,所以水解反应进行得很彻底。
油脂碱性条件下的水解反应也叫皂化反应。
工业上此反应生产肥皂。生成的高级脂肪酸钠、甘油和水形成一种胶体,不易分离,这时加入食盐,发生盐析,分成两层,上层为高级脂肪酸钠,下层为甘油和水。取上层高级脂肪酸钠加入填充剂、压滤、干燥、成型就制成了肥皂。
CH2
=CH2
CH3CH2Br
CH3CH2OH
CH3CHO
CH3COOH
CH2BrCH2Br
CH2OHCH2OH
CH=CH
练习:酸和醇的酯化反应
C2H5O—NO2
+
H2O
CH3COOCH3
+
H2O
CH3COOH
+
HOCH3
浓H2SO4
C2H5OH
+
HO—NO2
浓H2SO4
硝酸乙酯
乙酸甲酯
第三节:羧酸
酯
一、分子组成与结构
C2H4O2
CH3COOH
结构简式:
分子式:
结构式:
官能团:
羟基
羰基
(或—COOH)
O
—C—OH
羧基
C
H
H
H
H
O
C
O
二、物理性质
无色刺激性气味液体,熔点16.6℃,低于16.6℃就凝结成冰状晶体,所以无水乙酸又称冰醋酸。乙酸易溶于水和酒精。
三、乙酸的化学性质
1、乙酸的酸性
探究活动P60——设计验证实验CH3COOH酸性强弱
酸性
H2SO3
>
CH3COOH
>
H2CO3
⑵.具酸的通性:
⑴.电离方程式:CH3COOH
CH3COO-
+
H+
⑴.电离方程式:CH3COOH
CH3COO-
+
H+
⑴.电离方程式:CH3COOH
CH3COO-
+
H+
①.利用指示剂——石蕊试液;
变红
③.与某些盐反应
与Na2CO3溶液反应生成CO2气体。
②.利用金属活动性顺序表中氢前的金属可以置换H+为H2性质。
将表面用砂纸磨过镁条插入乙酸溶液。观察现象。
酸性:
H2SO3
>
CH3COOH
>
H2CO3
2CH3COOH
+
Na2CO3→2CH3COONa
+
H2O+CO2↑
Mg
+
2CH3COOH
→
(CH3COO)2Mg
+
H2↑
与Na2SO3溶液反应不生成SO2气体
⑤.与碱性氧化物反应
④.与碱反应
CH3COOH
+
NaOH
→
CH3COONa
+
H2O
2CH3COOH
+
CuO
→
(CH3COO)2Cu
+
H2O
结论:具有酸的5点通性,是一种弱酸
【思考
交流】
你能用几种方法证明乙酸是弱酸?
方法:
1:配制一定浓度的乙酸测定PH值
2:配制一定浓度的乙酸钠测PH值
3:比较盐酸、醋酸与金属反应的速率
4:
稀释一定浓度乙酸测定PH变化
……
CH3COOH
CH3COO-+H+
乙酸及几种含氧衍生物性质比较
反
应
反
应
反
应
反
应
羧酸
反
应
反
应
反
应
酚
反
应
醇
NaHCO3
溶液
Na2CO3
溶液
NaOH
溶液
Na
试剂
物质
思考:
③
饱和Na2CO3溶液的作用是什么?
②
饱和Na2CO3溶液上层有什么现象?
说明什么?
①
三种反应物如何混合?
④
浓H2SO4在反应中的作用是什么?
2、酯化反应
CH3COOH
+
HOC2H5
CH3COOC2H5+H2O
定义:酸和醇起作用生成酯和水的反应叫做酯化反应。
乙酸乙酯
探究酯化反应可能的脱水方式
浓H2SO4
b、
O
O
CH3—C—O—H+HO—C2H5
CH3—C—O—C2H5
+
H2O
a、
CH3—C—OH+H—O—C2H5
CH3—C—O—C2H5
+
H2O
浓H2SO4
=
=
O
O
酯化反应实质:
酸脱羟基醇脱羟基上的氢原子。
CH3
C
OH
+
H
18O
C2H5
浓H2SO4
=
O
CH3
C
18O
C2H5
+
H2O
=
O
有机羧酸和无机含氧酸(如
H2SO4、HNO3等)
同位素原子示踪法
酸和醇酯化反应的类型
①一元有机羧酸与一元醇。如:
CH3COOCH3
+
H2O
CH3COOH
+
HOCH3
浓H2SO4
乙酸甲酯
②一元酸与二元醇或多元醇。如:
二乙酸乙二酯
浓H2SO4
2
③一元醇与多元羧酸分子间脱水形成酯
+2
C2H5OH
COOH
COOH
浓H2SO4
COOC2H5
COOC2H5
+2H2O
④.多元羧酸与多元醇之间的脱水反应
生成普通酯:
COOH
COOH
CH2OH
CH2OH
+
浓H2SO4
+
H2O
HOOC-COOCH2CH2OH
生成环酯:
生成高聚酯:
+
n
HOOC
COOH
n
HOCH2CH2OH
一定条件
C
C
O
CH2CH2
O
n
+
2n
H2O
O
O
浓H2SO4
+
2H2O
环乙二酸乙二酯
三种情况:生成普通酯、环状酯、髙聚酯
⑤.羟基酸自身的脱水反应
CH3CHCOOH
OH
2
浓H2SO4
CH3CHCOOCHCOOH
OH
CH3
+H2O
普通酯
CH3CHCOOH
OH
2
浓H2SO4
CH3-CH
COO
OOC
CH-CH3
+H2O
环状酯
乳酸
生成高聚酯:
一定条件
CH3
【OCHCO】n+nH2O
n
HOCHCOOH
CH3
多元羧酸与二元醇间缩聚成聚酯。如:
⑥羟基酸分子内脱水成环。如:
CH2COOH
CH2CH2OH
浓硫酸
△
O
CH2C
CH2CH2
=
O
+
H2O
+
n
HOOC
COOH
n
HOCH2CH2OH
一定条件
聚对苯二甲酸乙二酯
C
C
O
CH2CH2
O
n
+
2n
H2O
O
O
缩聚反应:
有机物分子间脱去小分子,形成高分子聚合物的反应。
1.
药品的添加顺序
2.试管倾斜加热的目的是什么?
3.浓硫酸的作用是什么?
4.得到的反应产物是否纯净?主要杂质有哪些?
5.饱和Na2CO3溶液有什么作用?
催化剂,吸水剂
不纯净;乙酸、乙醇
①
中和乙酸,消除乙酸气味对酯气味的影响,以便闻到乙酸乙酯的气味.
②
溶解乙醇。
③
冷凝酯蒸气、降低酯在水中的溶解度,以便使酯分层析出。
增大受热面积
往乙醇中滴入浓硫酸和乙酸
6.
为什么导管不插入饱和Na2CO3溶液中?有无其它防倒吸的方法?
防止受热不匀发生倒吸
酯化反应属于取代反应中的一种,
也可看作是分子间脱水反应。
思考:酯化反应属于哪一类型有机反应类型?
烷氧基取代酸中的羟基,
或者是酰基取代醇中的氢原子
四、乙酸的制法
1、乙烯氧化法:
2CH2=CH2+O2
2CH3CHO
2CH3CHO+O2
2CH3COOH
催化剂
催化剂
2、发酵法
淀粉
葡萄糖
乙醇
乙醛
乙酸
五、乙酸的用途
生产醋酸纤维、溶剂、香料、医药等
羧酸
1、羧酸:由烃基与羧基相连而构成的有机物。
2、羧酸的分类
根据烃基来分
脂肪酸:
CH3CH2COOH
CH2=CHCOOH
芳香酸:C6H5COOH
根据羧基数目分
一元酸:CH3COOH
C6H5COOH
二元酸:HOOC-COOH
多元酸
3、一元羧酸和饱和一元羧酸的通式和分子式
一元羧酸的通式:R-COOH
饱和一元羧酸通式:CnH2n+1COOH(n
≥0)
饱和一元羧酸的分子式:CnH2nO2(n≥1)
4.酸的命名:
与醛的命名方法相同
HCOOH(甲酸)、
CH3COOH(乙酸)、CH3CH2COOH(丙酸)
CH3CH2CHCOOH
2-甲基丁酸
CH3
5、几种重要的羧酸
1.甲酸(HCOOH)
结构式:
根据其结构可推断出甲酸具有些什么性质?
(1)弱酸性:
2HCOOH+Na2CO3=2HCOONa+CO2?+H2O
(2)
酯化反应
HCOOH+CH3CH2OH
HCOOCH2CH3
+
H2O
浓硫酸
△
O
OH
C
H
(3)与新制的Cu(OH)2加热反应(-CHO的性质)
2Cu(OH)2+HCOOH
+
2NaOH
Cu2O?+Na2
CO3+
4H2O
△
注:HCOOR
甲酸某酯
不但发生水解反应,还能与新制的Cu(OH)2发生反应及发生银镜反应。
O
OR
C
H
【讨论】请用一种试剂鉴别下面四种有机物?
乙醇、乙醛、乙酸、甲酸
新制Cu(OH)2悬浊液
2.乙二酸
HOOC-COOH
【物性】俗称“草酸”,无色透明晶体,通常含两个结晶水,((COOH)2?2H2O),加热至100℃时失水成无水草酸,
易溶于水和乙醇,溶于乙醚等有机溶剂。
乙二酸
+
2H2O
化学性质:草酸是最简单的饱和二元羧酸,是二元羧酸中酸性最强的,它具有一些特殊的化学性质。能使酸性高锰酸钾溶液褪色、可作漂白剂。
△
高级脂肪酸
烃基上含有较多的碳原子的羧酸叫高级脂肪酸。
硬脂酸
C18H36O2
C17H35COOH
(饱和一元酸)
软脂酸
C16H32O2
C15H31COOH
(饱和一元酸)
油酸
C18H34O2
C17H33COOH
(有一个碳碳双键是一个不饱和一元酸,)
油酸是不饱和高级脂肪酸,常温下呈液态。而硬脂酸和软脂酸在常温下呈固态。
高级脂肪酸的化学性质
(1)弱酸性,酸性比乙酸弱。
C17H35COOH+NaOH-----C17H35COONa+H2O
(2)可发生酯化反应
C17H33COOH+C2H5OH
C17H33COOC2H5+H2O
浓硫酸
△
(3)、油酸可发生加成(加H2)反应:
C17H33COOH(液态)+H2
C17H35COOH(固态)
硬脂酸不能发生上述加成反应。
催化剂
油酸可发生加成反应使溴水(X2)褪色:
C17H33COOH
+
Br2
C17H33Br2COOH
硬脂酸不能发生上述加成反应。
一、酯的概念:由羧酸与醇反应生成的一类有机物.
酯
二、酯的通式
用RCOOR,表示。
饱和一元羧酸酯的分子式:
CnH2nO2
(n≥2)
最简单的酯是甲酸甲酯:
HCOOCH3
低级酯是熔点沸点低易挥发具有芳香
气味的液体。存在于各种水果和花草中,
三.物理性质及用途:
1.物理性质:密度一般小于水,并难溶于水(乙酸乙酯微溶),易溶于乙醇和乙醚等有机溶剂。
2.酯的用途
(1)作有机溶剂;
(2)食品工业作水果香料。
振荡均匀,把三支试管同时放在70℃-80
℃的水浴中加热几分钟,观察发生的现象。
蒸馏水5.5
mL
1:5的硫酸0.5
mL蒸馏水5.0
mL
30%NaOH溶液0.5mL、蒸馏
水5.0mL
各加入6滴乙酸乙酯
1
2
3
四.酯的化学性质--酯的水解
试管3中几乎无气味
试管2中稍有气味
试管1中仍有气味
【实验现象】
试管1中乙酸乙酯没有反应
试管2和3中乙酸乙酯发生了反应。
【实验结论】
酯在酸性或碱性条件下水解,中性条件下难水解。碱性条件下酯的水解程度更大.
四.水解反应:
1.在酸中的反应方程式:
2、在碱中反应方程式:
CH3—C—OC2H5
+
NaOH
O
CH3—CONa
+
HOC2H5
O
CH3—C—O—C2H5
+
H2O
O
稀H2SO4
CH3—C—OH+H—O—C2H5
O
酯的水解反应
RCOOR,+H-OH
RCOOH
+
R,OH
水解
酯化
酯的水解和酯化互为可逆反应,酯的水解在什么条件下进行?在什么条件下水解最彻底?
酯的水解反应中,硫酸的作用是?NaOH的作用是什么?
CH3COOC2H5+H2O
CH3COOH
+
C2H5
OH
H2SO4
△
CH3COOC2H5+NaOH
CH3COONa+
C2H5OH
△
硫酸在水解反应中起催化剂的作用;
NaOH不但是催化剂,还起促进酯的水解的作用,使酯的水解完全。
O
CH3—C—O—C2H5
酯的水解
思考:水解反应的反应实质是什么?
在水解的时候断裂的是什么键?
酯的水解是酯化反应的逆反应
酯在无机酸、碱催化下,均能发生水解反应,其中在酸性条件下水解是可逆的,在碱性条件下水解是不可逆的。
酯水解的规律:
酯
+
水
无机酸
△
酸
+
醇
△
酯
+碱
有机酸盐
+
醇
五.酯的命名
根据酸和醇的名称命名为“某酸某酯”
说出下列化合物的名称:
硝酸乙酯
(3)CH3CH2O—NO2
乙酸乙酯
(2)HCOOCH2CH3
甲酸乙酯
(1)CH3COOCH2CH3
COO
CH2CH3
⑷
硝酸乙酯
苯甲酸乙酯
六.
酯的同分异构体的书写:
通CnH2nO2
结构简式:HCOOCH3
CH3COOCH
3
HCOOC2H5
名称:
甲酸甲酯
乙酸甲酯
甲酸乙酯
C4H8O2同分异构体:6种
丁酸
CH3CH2CH2COOH
CH3-CH-COOH
CH3
2-甲基丙酸
CH3CH2COOCH3
CH3COOCH2CH3
HCOOCH2CH2CH3
HCOOCH(CH3)2
丙酸甲酯
乙酸乙酯
甲酸丙酯
甲酸异丙酯
【练习】写出分子式为C8H8O2属于芳香羧酸和芳香酯的所有同分异构体
4种和6种
【练习】写出C4H8O2的属于羧酸和酯的同分异构体的结构简式
2种和4种
思考:老酒为什么格外香?
驰名中外的贵州茅台酒,做好后用坛子密封埋在地下数年后,才取出分装出售,这样酒酒香浓郁、味道纯正,独具一格,为酒中上品。它的制作方法是有科学道理的。
在一般酒中,除乙醇外,还含有有机酸、杂醇等,有机酸带酸味,杂醇气味难闻,饮用时涩口刺喉,但长期贮藏过程中有机酸能与杂醇相互酯化,形成多种酯类化合物,每种酯具有一种香气,多种酯就具有多种香气,所以老酒的香气是混合香型。浓郁而优美,由于杂醇就酯化而除去,所以口感味道也变得纯正了。
小结:几种衍生物之间的关系
1、完成下列反应的化学方程式。
(1)甲酸与甲醇与浓硫酸加热
(2)乙酸甲酯在稀硫酸中加热反应
(3)乙酸乙酯在NaOH溶液中加热反应
练习:
练习:
1.胆固醇是人体必需的生物活性物质,分子式为C27H46O
。一种胆固醇酯的液晶材料,分子式为C34H50O2
。合成这种胆固醇酯的羧酸是(
)
A.
C6H13COOH
B.
C6H5COOH
C.
C7H15COOH
D.
C3H7COOH
B
2、1mol有机物
与足量NaOH
溶
液充分反应,消耗NaOH
的物质的量为(
)
A.5mol
B.4mol
C.3mol
D.2mol
COOCH3
CH3COO
COOH
B
3、一环酯化合物,结构简式如下:
试推断:
1.该环酯化合物在酸性条件下水解的产物是什么?
写出其结构简式;
2.写出此水解产物与金属钠反应的化学方程式;
3.此水解产物是否可能与FeCl3溶液发生变色反应?
4、现有分子式为C3H6O2的四种有机物A、B、C、D,且分子内均含有甲基,把它们分别进行下列实验以鉴别之,其实验记录如下:
NaOH溶液
银氨溶液
新制Cu(OH)2
金属钠
A
中和反应
——
溶解
产生氢气
B
——
有银镜
产生红色沉淀
产生氢气
C
水解反应
有银镜
产生红色沉淀
——
D
水解反应
——
——
——
则A、B、C、D的结构简式分别为:
A:
B:
C:
D:
CH3CH2COOH
CH3CH2OHCHO
HCOOCH2CH3
CH3COOCH3
【例题】今有化合物:
(1)请写出化合物中含氧官能团的名称:
。
(2)请判别上述哪些化合物互为同分异构体:
。
(3)请分别写出鉴别甲、乙、丙化合物的方法。(指明所选试剂及主要现象即可)
鉴别甲的方法:
;
鉴别乙的方法:
;
鉴别丙的方法:
.
(4)请按酸性由强至弱排列甲、乙、丙的顺序:
。
醛基、羟基、羰基、羧基
甲、乙、丙互为同分异构体
与FeCl3溶液作用显紫色的为甲
与Na2CO3溶液作用有气泡生成的为乙
与银氨溶液共热发生银镜反应的是丙
乙>甲>丙
5.(03年高考理综试题)根据图示填空。
(1)化合物A含有的官能团是_________________。
(2)1molA与2molH2反应生成1molE,其反应方程式是______。
(3)与A具有相同官能团的A的同分异构体的结构简式是_____。
(4)B在酸性条件下与Br2反应得到D,D的结构简式是_______。
(5)F的结构简式是____。由E生成F的反应类型是__________。
油脂
高级脂肪酸的甘油酯
R1COOCH2
R2COOCH
R3COOCH2
C17H35COOCH2
C17H35COOCH2
C17H35COOCH
C15H31COOCH2
C15H31COOCH2
C15H31COOCH
C17H33COOCH2
C17H33COOCH2
C17H33COOCH
硬脂酸甘油酯(脂肪)固态
软脂酸甘油酯
油酸甘油酯(油)液态
化学性质
1、油脂的氢化
C17H33COOCH2
C17H33COOCH2
C17H33COOCH
+3H2
催化剂
C17H35COOCH2
C17H35COOCH2
C17H35COOCH
油(液态)
脂肪(固态)
2、水解反应
(1)酸性条件下水解
C17H35COOCH2
C17H35COOCH2
C17H35COOCH
+3H2O
H2SO4
△
3C17H35COOH+
CH2-OH
CH-OH
CH2-OH
在油脂酸性条件下的水解反应中,硫酸作催化剂,水解反应不完全,因其逆反应是酯化反应。
(2)油脂碱性条件下的水解
C17H35COOCH2
C17H35COOCH2
C17H35COOCH
+3NaOH
△
3C17H35COONa
CH2-OH
CH-OH
CH2-OH
+
在油脂碱性条件下的水解反应中,NaOH溶液起了催化剂和促进水解的作用,所以水解反应进行得很彻底。
油脂碱性条件下的水解反应也叫皂化反应。
工业上此反应生产肥皂。生成的高级脂肪酸钠、甘油和水形成一种胶体,不易分离,这时加入食盐,发生盐析,分成两层,上层为高级脂肪酸钠,下层为甘油和水。取上层高级脂肪酸钠加入填充剂、压滤、干燥、成型就制成了肥皂。
CH2
=CH2
CH3CH2Br
CH3CH2OH
CH3CHO
CH3COOH
CH2BrCH2Br
CH2OHCH2OH
CH=CH
练习:酸和醇的酯化反应
C2H5O—NO2
+
H2O
CH3COOCH3
+
H2O
CH3COOH
+
HOCH3
浓H2SO4
C2H5OH
+
HO—NO2
浓H2SO4
硝酸乙酯
乙酸甲酯
