新人教版高中选修4化学第四节:金属的电化学腐蚀与防护ppt(44张PPT)
文档属性
| 名称 | 新人教版高中选修4化学第四节:金属的电化学腐蚀与防护ppt(44张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-09-16 00:00:00 | ||
图片预览











文档简介
(共44张PPT)
金属腐蚀的现象
锈蚀的大桥
锈蚀的闸门
锈蚀的轮船
锈蚀的楼梯
金属的腐蚀现象非常普遍:
1、钢铁生锈:
铁锈的主要成分:
金属腐蚀的不利后果有哪些?
Fe2O3·XH2O
Cu2(OH)2CO3
2、铜器表面生成铜绿:
铜绿的主要成分:
一、金属腐蚀
金属或合金与周围接触到的气体或液体
进行化学反应而腐蚀损耗的过程。
金属腐蚀
化学腐蚀
电化学腐蚀
一、金属的腐蚀
(1)定义:
(2)本质:
金属失去电子被氧化。
1、接触的介质不同,
2、发生腐蚀的化学原理不同
金属跟接触到的物质(如O2、CI2、SO2等)
直接发生化学反应而引起的腐蚀。
1、化学腐蚀
一、金属的腐蚀
(2)原理:
(1)定义:
(3)影响因素:
金属跟氧化剂直接发生氧化还原反应。
金属越活泼,越易被腐蚀;
金属所处的环境温度越高,腐蚀速率越快;
氧化剂浓度越大,腐蚀速率越快。
家用燃气灶
放在南极已差不多
90年食品罐头
一般情况下,温度的升高会加快化学反应速率。因此,温度对化学腐蚀的影响较明显。
在新疆吐鲁番和海南省两地,哪个地区铁生锈相对慢一些?为什么?
新疆吐鲁番,因为该地区相对干燥,水分稀少,而海南地区潮湿多雨,温度高,易发生电化学腐蚀。
2、电化学腐蚀
不纯的金属(或合金)跟电解质溶液接触时,会发生原电池反应,比较活泼的金属失去电子而被氧化,这种腐蚀叫做电化学腐蚀。
一、原电池:
把化学能转化为电能的装置
二、原电池原理
原电池
负极(较活泼金属)
正极(较不活泼金属或非金属导体)
三、判断原电池正、负极的方法
较活泼的金属发生氧化反应,电子从较活泼的金属(负极)通过导线流向较不活泼的金属(正极)
1、由组成原电池的两极材料判断;
2、根据电流方向或电子流动方向判断;
3、根据原电池两极发生的变化来判断;
4、电极反应现象.
复习回忆
四、构成原电池的条件:
1、自发进行的氧化还原反应
2、有两种活动性不同的金属(或一种是非金属导体如碳棒)做电极。
(一般负极与电解质发生氧化还原反应)
3、两极材料均插入电解质溶液中。
4、两极相连形成闭合回路。
科学探究
现有洁净无锈的铁钉,试管、植物油、NaCl溶液、CH3COOH溶液和煮沸后迅速冷却的蒸馏水,你也可以选用其他物品,设计实验探究铁钉锈蚀需要哪些条件,以及在什么条件下锈蚀速率快。
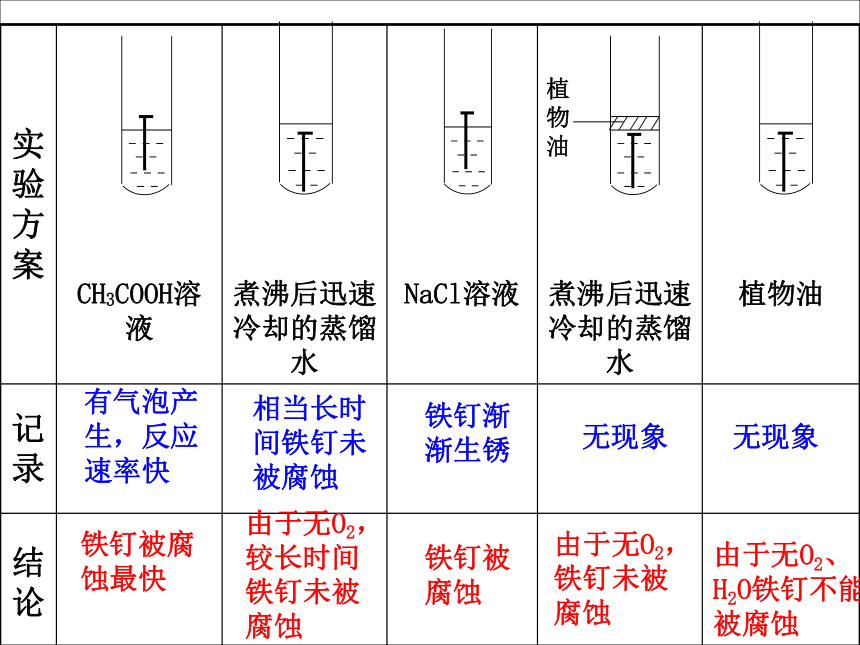
不同条件下铁钉的腐蚀
实验方案
CH3COOH溶液
煮沸后迅速冷却的蒸馏水
NaCl溶液
煮沸后迅速冷却的蒸馏水
植物油
记录
结论
有气泡产生,反应速率快
相当长时间铁钉未被腐蚀
铁钉被腐蚀最快
由于无O2,较长时间铁钉未被腐蚀
铁钉渐渐生锈
铁钉被腐蚀
无现象
由于无O2,铁钉未被腐蚀
无现象
由于无O2、H2O铁钉不能被腐蚀
植物油
总结:
铁钉遇到强酸或有O2、H2O存在的情况下,铁均可被腐蚀,遇到电解质时,一般腐蚀速率更快。
不会,因为月球上缺少水分和氧气。
请你预测一下,铁在月球上会不会生锈?为什么?
钢铁在干燥的空气里长时间不易被腐蚀,但在潮湿的空气里却很快被腐蚀,这是什么原因呢?
在潮湿的空气里,钢铁表面吸附了一层薄薄的水膜。水能电离出少量的H
+和OH
-,同时由于空气中CO2的溶解,使水里的H
+
增多:
H2O
+
CO2
H2CO3
H
+
+
HCO3
-
这样在钢铁表面形成了一层电解质溶液的薄膜,它跟钢铁里的铁和少量的碳构成无数微小的原电池。
其中铁作负极,碳作正极。
OH
-
Fe2+
Fe
C
H2
Fe2+
O2
Fe
C
e-
e-
e-
e-
e-
e-
在负极,铁失去电子而被氧化成Fe2+:
Fe
–
2e-=Fe
2+
在正极,有两种情况:
吸氧腐蚀:
2H2O
+
O2
+
4e-
=
4OH
–
析氢腐蚀:
2H
++2e
-
=
H2↑
吸氧腐蚀与析氢腐蚀(以钢铁为例)
类型
吸氧腐蚀
析氢腐蚀
条件
正极反应(C)
负极反应(Fe)
其他反应
水膜呈弱酸性或中性
O2+2H2O+4e-=4OH-
Fe-2e-=Fe2+
水膜呈酸性
2H++2e-=H2↑
Fe-2e-=Fe2+
Fe2++2OH-=Fe(OH)2↓
4Fe(OH)2
+2H2O+
O2=
4Fe(OH)3
4Fe(OH)3失去部分水转化为铁锈
化学腐蚀和电化学腐蚀都是铁等金属原子失去电子变成阳离子的过程。也就是说,金属在腐蚀过程中,发生了氧化还原反应。
金属腐蚀的本质
烧过菜的铁锅如果未及时洗净(残液中含
NaCl),第二天便出现红棕色锈斑(主要成分为Fe
2
O
3?nH2O)。请问这种腐蚀是化学腐蚀还是电化学腐蚀?为什么?
解析:属于电化学腐蚀。
因为铁锅是由生铁做成的,铁锅生锈是因为Fe-C-NaCl形成原电池。铁作负极,失去电子变成亚铁离子,从而被腐蚀。
思考与交流
讨论自行车的不同构件如链条、钢圈、支架和齿轮等分别采取了什么防锈措施?
给链条涂上机油,将钢圈表面镀上一层铬,给支架烤上一层漆,将齿轮镀上一层铬并涂上机油。
影响金属腐蚀的因素:
1、金属的本性:
金属越活泼,就越容易失去电子而被腐蚀。
2、介质:
如果金属中能导电的杂质不如该金属活泼,则容易形成原电池而使金属发生电化学腐蚀。
思考与交流
请根据生活常识以及下图总结金属防护常用的方法,并解释这些方法为什么可以达到防止金属腐蚀的目的。
健身器材刷油漆以防锈
衣架和电线的外面包上一层塑料层
某些工具的“机械转动部位”选用油脂来防锈,为什么不能用油漆
自行车的钢圈和车铃是在钢上镀上一层既耐腐蚀又耐磨的Cr
你还知道哪些防止金属腐蚀的方法?请举例说明。
用牺牲镁块的方法来防止地下钢铁管道的腐蚀,镁块必须定期更换
制成不锈钢,在金属表面镀一层比要保护的金属更活泼的金属。
用牺牲锌块的方法来保护船身,锌块必须定期更换
锌块
金属的防护方法
1、在金属表面覆盖保护层
2、改变金属的内部组织结构
3、在要保护的金属上连接一种比该金属更易失去电子的金属
刷油漆、涂机油、加塑料层……
不锈钢、马口铁、白口铁……
牺牲阳极的阴极保护法……
答案
1、钢铁发生吸氧腐蚀时,发生还原反应的电极反应式是(
)
A、
Fe
–
2e-=Fe
2+
B、
2H
+
+
2e-
=H2
↑
C、
4OH
-
-
4e-=
2H2O
+
O2
↑
D、
2H2O
+
O2
+
4e-
=
4OH
-
D
2、如图所示,各容器中盛有海水,铁在其中被腐蚀时由快到慢的顺序是(
)
A、②>①>③
B、③>②>①
C、②>③>①
Fe
Fe
Fe
Sn
Zn
A
3、下列事实不能用电化学理论解释的是
(
)
A、轮船吃水线以下的船壳上装一定数量的锌块
B、铝片不用特殊方法保护
C、纯锌与稀硫酸反应时,滴入少量的CuSO4溶液后速率加快
D、镀锌铁(在铁上镀一层锌)比镀锡耐用
B
4、有a、b、c、d四种金属。将a与b连接起来,浸入电解质溶液中,b不易腐蚀。将a、d分别投入等浓度的盐酸中,d比a反应强烈。将铜浸入b的盐溶液里,无明显变化。如果把铜浸入c的盐溶液里,有金属c析出。据此判断它们的活动性顺序由强到弱的为:
(
)
A.a
>
c
>
d
>
b
B.d
>
a
>
b
>
c
C.d
>
b
>
a
>
c
D.b
>
a
>
d
>
c
B
5、下列叙述正确的是(
)
A.锌跟稀硫酸反应制取氢气,加入少量硫酸铜溶液能加快反应速率
B.镀层破损后,白口铁(镀锌的铁)比马口铁(镀锡的铁)更易腐蚀
C.家用炒菜铁锅出现锈斑的原因是发生了化学腐蚀
D.吸氧腐蚀时正极放出氧气,析氢腐蚀时正极放出氢气
E.化学腐蚀速率超过电化学腐蚀速率,析氢腐蚀比吸氧腐蚀普遍
A
6、以下现象与电化学腐蚀无关的是(
)
A.黄铜(铜锌合金)制作的铜制品不易被腐蚀
B.生铁比纯铁容易腐蚀
C.铁质器件附有铜质配件,在接触处易生铁锈
D.银制奖牌久置后表面变暗
7、下列事实不能用电化学理论解释的是(
)
A.轮船水线下船壳上装一偶一定数量的锌块
B.铝片不用特殊方法保存
C.纯锌与稀硫酸反应时,滴入少量的硫酸铜后速率加快
D.镀锌铁比镀锡铁耐用
D
B
8、下列防腐措施中,属于电化学保护法的是(
)
A.用氧化剂使金属表面生成一层致密稳定的氧化物保护膜
B.在金属中加入一些铬或镍制成合金
C.在轮船的船壳水线以下部分装上一些锌
D.金属表面喷漆
9、下列事实不能用电化学理论解释的是(
)
A.在轮船的船壳水线以下部分装有一定量的锌块
B.镀锌的铁制品比镀锡的铁制品耐用
C.铝片不用特殊方法保护
D.粗锌跟稀硫酸反应比纯锌更快
C
C
10、埋在地下的铸铁输油管道,在下列各种情况下,腐蚀最慢的是(
)
A.在含铁元素较多的酸性土壤中
B.在潮湿疏松透气的土壤中
C.在干燥致密不透气的土壤中
D.在含碳粒较多的潮湿透气的中性土壤中
11、(2007广东)为了避免青铜器生成铜绿,以下方法正确的是(
)
A.将青铜器放在银质托盘上
B.将青铜器保存在干燥的环境中
C.将青铜器保存在潮湿的空气中
D.在青铜器的表面覆盖一层防渗的高分子膜
C
BD
12、下列金属防护的方法不正确的是(
)
A.对健身器材刷油漆以防锈
B.对某些工具的“机械转动部位”选用刷油漆方法来防锈
C.用牺牲锌块的方法来保护船身
D.自行车的钢圈上镀上一层Cr防锈
B
13、下列各组金属均有导线相连,并插入对应的液体中,其中能组成原电池的是(
)
A.
Cu
|
H2SO4(稀)
|
C
B.
Cu
|
AgNO3(aq)
|
Ag
C.
Zn
|
CCl4(稀)
|
Cu
D.
Fe
|
H2SO4(稀)
|
Fe
14、下列各组金属均有导线相连,并插入稀硫酸溶液中,其中铁被腐蚀的速度由快到慢的顺序是(
)
①Fe-Fe
②Fe-Sn
③Fe-Zn
④Cu-Fe
A.
②①③④
B.
③②④①
C.
④②③①
D.
④②①③
B
D
15、烧过菜的铁锅未及时洗去含有NaCl的残液,过一段时间算便出现红棕色的铁锈斑点,已知该锈斑为Fe(OH)3失水的产物。表示Fe(OH)3生成的电极反应式、离子方程式和化学方程式分别为:
①负极反应式:_________________________
正极反应式:_________________________
②离子方程式:_________________________
③
化学方程式:_________________________
16、电工操作中规定,不能把铜线和铝线拧在一起连接线路,这是因为:
铜线与铝线拧在一起时,铜与铝组成原电池,铝线被腐蚀而失去导电能力
金属腐蚀的现象
锈蚀的大桥
锈蚀的闸门
锈蚀的轮船
锈蚀的楼梯
金属的腐蚀现象非常普遍:
1、钢铁生锈:
铁锈的主要成分:
金属腐蚀的不利后果有哪些?
Fe2O3·XH2O
Cu2(OH)2CO3
2、铜器表面生成铜绿:
铜绿的主要成分:
一、金属腐蚀
金属或合金与周围接触到的气体或液体
进行化学反应而腐蚀损耗的过程。
金属腐蚀
化学腐蚀
电化学腐蚀
一、金属的腐蚀
(1)定义:
(2)本质:
金属失去电子被氧化。
1、接触的介质不同,
2、发生腐蚀的化学原理不同
金属跟接触到的物质(如O2、CI2、SO2等)
直接发生化学反应而引起的腐蚀。
1、化学腐蚀
一、金属的腐蚀
(2)原理:
(1)定义:
(3)影响因素:
金属跟氧化剂直接发生氧化还原反应。
金属越活泼,越易被腐蚀;
金属所处的环境温度越高,腐蚀速率越快;
氧化剂浓度越大,腐蚀速率越快。
家用燃气灶
放在南极已差不多
90年食品罐头
一般情况下,温度的升高会加快化学反应速率。因此,温度对化学腐蚀的影响较明显。
在新疆吐鲁番和海南省两地,哪个地区铁生锈相对慢一些?为什么?
新疆吐鲁番,因为该地区相对干燥,水分稀少,而海南地区潮湿多雨,温度高,易发生电化学腐蚀。
2、电化学腐蚀
不纯的金属(或合金)跟电解质溶液接触时,会发生原电池反应,比较活泼的金属失去电子而被氧化,这种腐蚀叫做电化学腐蚀。
一、原电池:
把化学能转化为电能的装置
二、原电池原理
原电池
负极(较活泼金属)
正极(较不活泼金属或非金属导体)
三、判断原电池正、负极的方法
较活泼的金属发生氧化反应,电子从较活泼的金属(负极)通过导线流向较不活泼的金属(正极)
1、由组成原电池的两极材料判断;
2、根据电流方向或电子流动方向判断;
3、根据原电池两极发生的变化来判断;
4、电极反应现象.
复习回忆
四、构成原电池的条件:
1、自发进行的氧化还原反应
2、有两种活动性不同的金属(或一种是非金属导体如碳棒)做电极。
(一般负极与电解质发生氧化还原反应)
3、两极材料均插入电解质溶液中。
4、两极相连形成闭合回路。
科学探究
现有洁净无锈的铁钉,试管、植物油、NaCl溶液、CH3COOH溶液和煮沸后迅速冷却的蒸馏水,你也可以选用其他物品,设计实验探究铁钉锈蚀需要哪些条件,以及在什么条件下锈蚀速率快。
不同条件下铁钉的腐蚀
实验方案
CH3COOH溶液
煮沸后迅速冷却的蒸馏水
NaCl溶液
煮沸后迅速冷却的蒸馏水
植物油
记录
结论
有气泡产生,反应速率快
相当长时间铁钉未被腐蚀
铁钉被腐蚀最快
由于无O2,较长时间铁钉未被腐蚀
铁钉渐渐生锈
铁钉被腐蚀
无现象
由于无O2,铁钉未被腐蚀
无现象
由于无O2、H2O铁钉不能被腐蚀
植物油
总结:
铁钉遇到强酸或有O2、H2O存在的情况下,铁均可被腐蚀,遇到电解质时,一般腐蚀速率更快。
不会,因为月球上缺少水分和氧气。
请你预测一下,铁在月球上会不会生锈?为什么?
钢铁在干燥的空气里长时间不易被腐蚀,但在潮湿的空气里却很快被腐蚀,这是什么原因呢?
在潮湿的空气里,钢铁表面吸附了一层薄薄的水膜。水能电离出少量的H
+和OH
-,同时由于空气中CO2的溶解,使水里的H
+
增多:
H2O
+
CO2
H2CO3
H
+
+
HCO3
-
这样在钢铁表面形成了一层电解质溶液的薄膜,它跟钢铁里的铁和少量的碳构成无数微小的原电池。
其中铁作负极,碳作正极。
OH
-
Fe2+
Fe
C
H2
Fe2+
O2
Fe
C
e-
e-
e-
e-
e-
e-
在负极,铁失去电子而被氧化成Fe2+:
Fe
–
2e-=Fe
2+
在正极,有两种情况:
吸氧腐蚀:
2H2O
+
O2
+
4e-
=
4OH
–
析氢腐蚀:
2H
++2e
-
=
H2↑
吸氧腐蚀与析氢腐蚀(以钢铁为例)
类型
吸氧腐蚀
析氢腐蚀
条件
正极反应(C)
负极反应(Fe)
其他反应
水膜呈弱酸性或中性
O2+2H2O+4e-=4OH-
Fe-2e-=Fe2+
水膜呈酸性
2H++2e-=H2↑
Fe-2e-=Fe2+
Fe2++2OH-=Fe(OH)2↓
4Fe(OH)2
+2H2O+
O2=
4Fe(OH)3
4Fe(OH)3失去部分水转化为铁锈
化学腐蚀和电化学腐蚀都是铁等金属原子失去电子变成阳离子的过程。也就是说,金属在腐蚀过程中,发生了氧化还原反应。
金属腐蚀的本质
烧过菜的铁锅如果未及时洗净(残液中含
NaCl),第二天便出现红棕色锈斑(主要成分为Fe
2
O
3?nH2O)。请问这种腐蚀是化学腐蚀还是电化学腐蚀?为什么?
解析:属于电化学腐蚀。
因为铁锅是由生铁做成的,铁锅生锈是因为Fe-C-NaCl形成原电池。铁作负极,失去电子变成亚铁离子,从而被腐蚀。
思考与交流
讨论自行车的不同构件如链条、钢圈、支架和齿轮等分别采取了什么防锈措施?
给链条涂上机油,将钢圈表面镀上一层铬,给支架烤上一层漆,将齿轮镀上一层铬并涂上机油。
影响金属腐蚀的因素:
1、金属的本性:
金属越活泼,就越容易失去电子而被腐蚀。
2、介质:
如果金属中能导电的杂质不如该金属活泼,则容易形成原电池而使金属发生电化学腐蚀。
思考与交流
请根据生活常识以及下图总结金属防护常用的方法,并解释这些方法为什么可以达到防止金属腐蚀的目的。
健身器材刷油漆以防锈
衣架和电线的外面包上一层塑料层
某些工具的“机械转动部位”选用油脂来防锈,为什么不能用油漆
自行车的钢圈和车铃是在钢上镀上一层既耐腐蚀又耐磨的Cr
你还知道哪些防止金属腐蚀的方法?请举例说明。
用牺牲镁块的方法来防止地下钢铁管道的腐蚀,镁块必须定期更换
制成不锈钢,在金属表面镀一层比要保护的金属更活泼的金属。
用牺牲锌块的方法来保护船身,锌块必须定期更换
锌块
金属的防护方法
1、在金属表面覆盖保护层
2、改变金属的内部组织结构
3、在要保护的金属上连接一种比该金属更易失去电子的金属
刷油漆、涂机油、加塑料层……
不锈钢、马口铁、白口铁……
牺牲阳极的阴极保护法……
答案
1、钢铁发生吸氧腐蚀时,发生还原反应的电极反应式是(
)
A、
Fe
–
2e-=Fe
2+
B、
2H
+
+
2e-
=H2
↑
C、
4OH
-
-
4e-=
2H2O
+
O2
↑
D、
2H2O
+
O2
+
4e-
=
4OH
-
D
2、如图所示,各容器中盛有海水,铁在其中被腐蚀时由快到慢的顺序是(
)
A、②>①>③
B、③>②>①
C、②>③>①
Fe
Fe
Fe
Sn
Zn
A
3、下列事实不能用电化学理论解释的是
(
)
A、轮船吃水线以下的船壳上装一定数量的锌块
B、铝片不用特殊方法保护
C、纯锌与稀硫酸反应时,滴入少量的CuSO4溶液后速率加快
D、镀锌铁(在铁上镀一层锌)比镀锡耐用
B
4、有a、b、c、d四种金属。将a与b连接起来,浸入电解质溶液中,b不易腐蚀。将a、d分别投入等浓度的盐酸中,d比a反应强烈。将铜浸入b的盐溶液里,无明显变化。如果把铜浸入c的盐溶液里,有金属c析出。据此判断它们的活动性顺序由强到弱的为:
(
)
A.a
>
c
>
d
>
b
B.d
>
a
>
b
>
c
C.d
>
b
>
a
>
c
D.b
>
a
>
d
>
c
B
5、下列叙述正确的是(
)
A.锌跟稀硫酸反应制取氢气,加入少量硫酸铜溶液能加快反应速率
B.镀层破损后,白口铁(镀锌的铁)比马口铁(镀锡的铁)更易腐蚀
C.家用炒菜铁锅出现锈斑的原因是发生了化学腐蚀
D.吸氧腐蚀时正极放出氧气,析氢腐蚀时正极放出氢气
E.化学腐蚀速率超过电化学腐蚀速率,析氢腐蚀比吸氧腐蚀普遍
A
6、以下现象与电化学腐蚀无关的是(
)
A.黄铜(铜锌合金)制作的铜制品不易被腐蚀
B.生铁比纯铁容易腐蚀
C.铁质器件附有铜质配件,在接触处易生铁锈
D.银制奖牌久置后表面变暗
7、下列事实不能用电化学理论解释的是(
)
A.轮船水线下船壳上装一偶一定数量的锌块
B.铝片不用特殊方法保存
C.纯锌与稀硫酸反应时,滴入少量的硫酸铜后速率加快
D.镀锌铁比镀锡铁耐用
D
B
8、下列防腐措施中,属于电化学保护法的是(
)
A.用氧化剂使金属表面生成一层致密稳定的氧化物保护膜
B.在金属中加入一些铬或镍制成合金
C.在轮船的船壳水线以下部分装上一些锌
D.金属表面喷漆
9、下列事实不能用电化学理论解释的是(
)
A.在轮船的船壳水线以下部分装有一定量的锌块
B.镀锌的铁制品比镀锡的铁制品耐用
C.铝片不用特殊方法保护
D.粗锌跟稀硫酸反应比纯锌更快
C
C
10、埋在地下的铸铁输油管道,在下列各种情况下,腐蚀最慢的是(
)
A.在含铁元素较多的酸性土壤中
B.在潮湿疏松透气的土壤中
C.在干燥致密不透气的土壤中
D.在含碳粒较多的潮湿透气的中性土壤中
11、(2007广东)为了避免青铜器生成铜绿,以下方法正确的是(
)
A.将青铜器放在银质托盘上
B.将青铜器保存在干燥的环境中
C.将青铜器保存在潮湿的空气中
D.在青铜器的表面覆盖一层防渗的高分子膜
C
BD
12、下列金属防护的方法不正确的是(
)
A.对健身器材刷油漆以防锈
B.对某些工具的“机械转动部位”选用刷油漆方法来防锈
C.用牺牲锌块的方法来保护船身
D.自行车的钢圈上镀上一层Cr防锈
B
13、下列各组金属均有导线相连,并插入对应的液体中,其中能组成原电池的是(
)
A.
Cu
|
H2SO4(稀)
|
C
B.
Cu
|
AgNO3(aq)
|
Ag
C.
Zn
|
CCl4(稀)
|
Cu
D.
Fe
|
H2SO4(稀)
|
Fe
14、下列各组金属均有导线相连,并插入稀硫酸溶液中,其中铁被腐蚀的速度由快到慢的顺序是(
)
①Fe-Fe
②Fe-Sn
③Fe-Zn
④Cu-Fe
A.
②①③④
B.
③②④①
C.
④②③①
D.
④②①③
B
D
15、烧过菜的铁锅未及时洗去含有NaCl的残液,过一段时间算便出现红棕色的铁锈斑点,已知该锈斑为Fe(OH)3失水的产物。表示Fe(OH)3生成的电极反应式、离子方程式和化学方程式分别为:
①负极反应式:_________________________
正极反应式:_________________________
②离子方程式:_________________________
③
化学方程式:_________________________
16、电工操作中规定,不能把铜线和铝线拧在一起连接线路,这是因为:
铜线与铝线拧在一起时,铜与铝组成原电池,铝线被腐蚀而失去导电能力
