人教版九年级化学下册第九单元溶液 达标测试卷(word版 含答案)
文档属性
| 名称 | 人教版九年级化学下册第九单元溶液 达标测试卷(word版 含答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 195.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-09-17 00:00:00 | ||
图片预览



文档简介
第九单元达标测试卷
可能用到的相对原子质量:H:1 O:16
一、选择题(本题包括12小题,每小题1分,共12分。每小题的4个选项中只有1个符合题意)
1.把少量下列物质分别放入水中,充分搅拌,可以形成溶液的是( )
A.碘 B.汽油 C.高锰酸钾 D.面粉
2.下列有关溶液的说法正确的是( )
A.所有溶液都能导电 B.无色澄清液体一定是溶液
C.只有固体能作溶质 D.水和酒精等都可用作溶剂
3.“美林”主要成分是布洛芬,“小儿开塞露”主要成分是甘油和山梨醇。两者都是儿科常用药,且都是药物分散在水中制成。“美林”即使密封保存放久了也会产生白色沉淀,“小儿开塞露”则久置不会分层。“美林”、“小儿开塞露”分别属于( )
A.乳浊液、乳浊液 B.悬浊液、溶液
C.乳浊液、溶液 D.悬浊液、乳浊液
4.乳化现象在生产和生活中很常见,下列常用的清洗方法中,用到乳化作用的是( )
A.用洗洁精除去盘子上的油污 B.用清水洗手
C.用洗衣粉洗去衣服上的泥渍 D.用盐酸除铁锈
5.在t ℃时,某物质X、Y分别完全溶于水,溶液中X、Y与水的质量关系分别如图a、图b所示。下列说法正确的是( )
A.X、Y都只能是固体 B.两种溶液一定是饱和溶液
C.图示溶液的浓度:X6.海水、河水或湖水中,都溶解了一定量的氧气,但养鱼池中常常由于鱼多而缺氧,因此,要设法增加水中的氧气含量。下列做法不能增加水中氧气含量的是( )
A.增加日晒时间 B.把水搅动起来
C.把水喷向空中 D.向养鱼池中通入空气或者氧气
7.硝酸钾的溶解度随温度升高而增大。如图是有关硝酸钾溶液的实验操作及变化情况。下列说法正确的是( )
A.整个实验过程中硝酸钾的溶解度一定不变
B.①与②的溶液质量一定相等
C.①与③的溶质质量一定相等
D.②与③的溶质质量分数一定相等
8.下列关于溶液的说法不正确的是( )
A.与乳化作用相比,溶解能使物质混合得更均匀
B. 20 ℃时,50 g水中溶解了15 g硝酸钾,则20 ℃时硝酸钾的溶解度是30 g
C.一定温度下,固体物质的溶解度不随水的质量改变而改变
D.硝酸钾的饱和溶液恒温蒸发部分水后,剩余溶液溶质质量分数不变
9.20 ℃时,向一盛有30 g某物质的烧杯内加入100 g水,充分搅拌后静置,烧杯底部仍有未溶解的固体,过滤得到5 g固体和澄清溶液。下列有关叙述错误的是( )
A.该溶液中溶质的质量等于25 g
B.该溶液中溶质的质量分数等于20%
C.该温度下,再加20 g水后该溶液变为不饱和溶液
D.该温度下,再加30 g水后该溶液变为不饱和溶液
10.现有100 g溶质质量分数为10%的硝酸钠溶液,要将其溶质质量分数变为20%,可采用的方法是( )
①蒸发掉2/3溶剂 ②蒸发掉50 g溶剂 ③加入10 g硝酸钠
④加入12.5 g硝酸钠
A.①③ B.②③ C.①④ D.②④
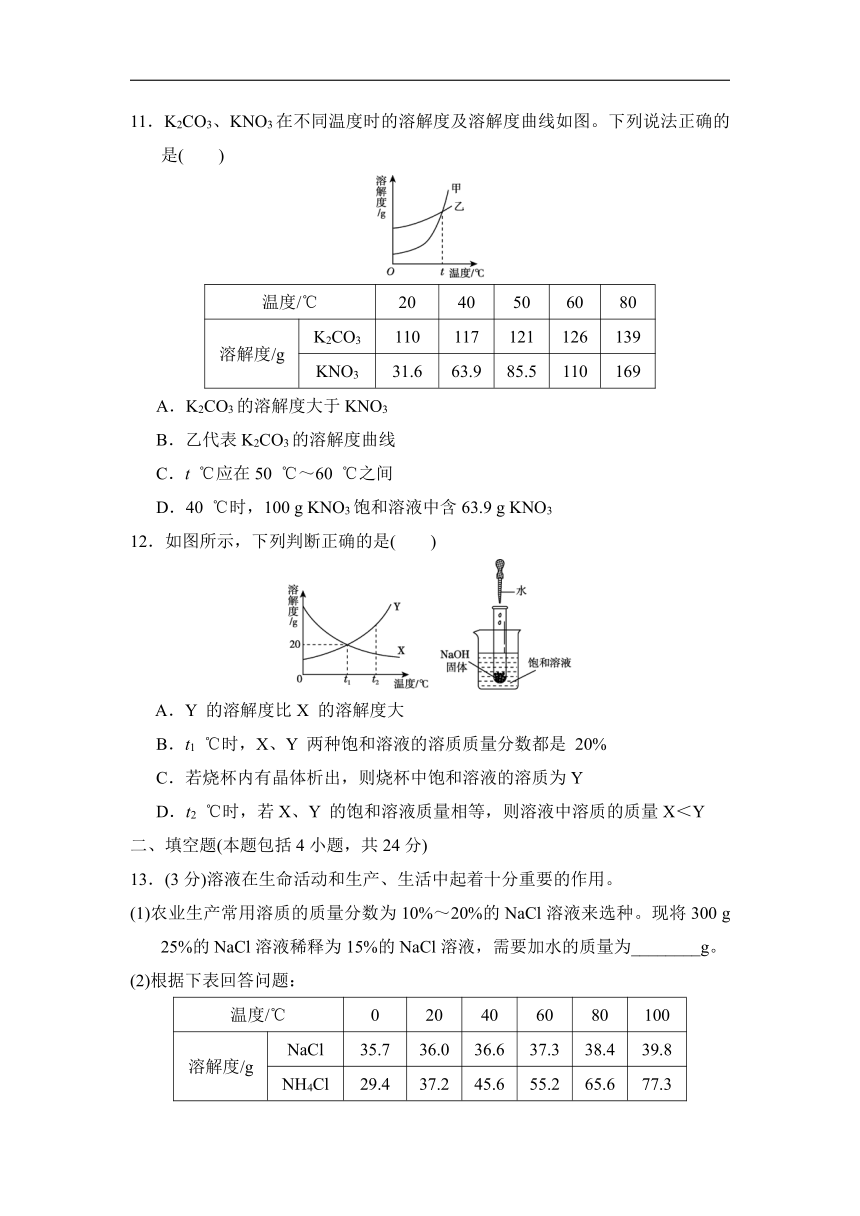
11.K2CO3、KNO3在不同温度时的溶解度及溶解度曲线如图。下列说法正确的是( )
温度/℃ 20 40 50 60 80
溶解度/g K2CO3 110 117 121 126 139
KNO3 31.6 63.9 85.5 110 169
A.K2CO3的溶解度大于KNO3
B.乙代表K2CO3的溶解度曲线
C.t ℃应在50 ℃~60 ℃之间
D.40 ℃时,100 g KNO3饱和溶液中含63.9 g KNO3
12.如图所示,下列判断正确的是( )
A.Y 的溶解度比X 的溶解度大
B.t1 ℃时,X、Y 两种饱和溶液的溶质质量分数都是 20%
C.若烧杯内有晶体析出,则烧杯中饱和溶液的溶质为Y
D.t2 ℃时,若X、Y 的饱和溶液质量相等,则溶液中溶质的质量X<Y
二、填空题(本题包括4小题,共24分)
13.(3分)溶液在生命活动和生产、生活中起着十分重要的作用。
(1)农业生产常用溶质的质量分数为10%~20%的NaCl溶液来选种。现将300 g 25%的NaCl溶液稀释为15%的NaCl溶液,需要加水的质量为________g。
(2)根据下表回答问题:
温度/℃ 0 20 40 60 80 100
溶解度/g NaCl 35.7 36.0 36.6 37.3 38.4 39.8
NH4Cl 29.4 37.2 45.6 55.2 65.6 77.3
①60 ℃时,向两个分别盛有50 g NaCl和NH4Cl的烧杯中,各加入100 g的水,充分溶解后,为饱和溶液的是________溶液;
②采用一种操作方法,将上述烧杯中的剩余固体全部溶解,变为不饱和溶液。下列说法正确的是________(填字母)。
A.溶质的质量不变 B.溶液中溶质的质量分数一定减小
C.溶液质量可能不变 D.可升高温度或增加溶剂
14.(5分)如图1是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线。回答下列问题:
(1)t1 ℃时,甲、乙、丙三种物质的溶解度由小到大的顺序是______________。
(2)P点表示t2 ℃时甲、丙两种物质的溶解度________(填“相等”或“不相等”)。
(3)t2 ℃时,取甲、乙两种固体各20 g分别加入50 g水中充分溶解,实验现象如图2所示,则烧杯a中溶解的物质是______(填“甲”或“乙”),未溶解固体的质量是________g。
(4)当甲中含有少量的乙和丙(甲、乙、丙相互间均不发生化学反应)时,可采用________(填“降温”或“蒸发”)结晶的方法提纯甲物质。
15.(6分)食盐是生活中必备的调味品。通过学习和生活体验,我们发现多种因素都能影响食盐在水中的溶解速率。
(1)写出两个你认为可能影响食盐在水中溶解速率的因素,并预测其对食盐溶解速率的影响。
因素①:______________,你的预测是____________________________________;
因素②:______________,你的预测是__________________________________。
(2)从你所列因素中选出一个,通过实验验证你的预测,你设计的实验方案是_________________________________________________________________________________________________________________________________。
(3)要使验证实验达到预测的效果,必须控制____________________________。
16.(10分)如图1是配制50 g溶质质量分数为5%的NaCl溶液的实验操作示意图。结合图示回答下列问题:
(第16题图1)
(1)请找出图中的错误加以改正(写出三处即可):
①______________________________________________________;
②______________________________________________________;
③______________________________________________________。
(2)需要称量的氯化钠的质量是________g,在用托盘天平称量氯化钠固体时,1 g以下使用游码。如果甲同学按照B操作,其他操作都正确,所配得溶液的溶质质量分数为__________(计算结果精确至0.1%)。
(3)需要水的质量是________g,配制时应选择________(填“10”或“50”)mL的量筒。量取水时,如果乙同学按照图D读数,配制的其余操作准确规范,则所得溶液的溶质质量分数________ (填“小于”“等于”或“大于”)5%。
(4)①丙同学配制的上述溶液,经测定其氯化钠质量分数大于5%,下列可能的原因有__________(填字母序号)。
A.用量筒量取水时俯视读数
B.用来配制溶液的烧杯刚用少量蒸馏水润洗过
C.用托盘天平称取氯化钠时,将氯化钠放在右盘,且称量时使用了游码
D.把量好的水倒入烧杯时,有少量水溅出烧杯
②通过以上过程可知,配制一定溶质质量分数的溶液,五个主要步骤依次是________、________、________、________、装瓶并贴标签。
【注意:答对下列问题奖励3分,卷面总分不超过40分】
(5)如图2所示,在氯化钠的溶解过程中发生了两种变化:一种是离子向水中扩散,这一过程吸收热量Q1;另一种是离子和水分子作用,形成水合离子,这一过程放出热量Q2。
(第16题图2)
①氯化钠溶解时溶液的温度略微降低,原因是Q1______Q2(填“>”或“<”)。
②若氯化钠溶解于水的微观过程如图2所示,则形成的水合钠离子中,钠离子与水分子的个数比为____________________________________________。
三、计算题(本题包括1小题,共4分)
17.(4分)某化学兴趣小组欲测定一瓶过氧化氢溶液中过氧化氢的质量分数,取2 g二氧化锰和68 g过氧化氢溶液在烧杯中混合,完全反应后烧杯内剩余物质的总质量为68.4 g,求:
(1)反应中生成氧气的总质量________g。
(2)这瓶过氧化氢溶液中过氧化氢的质量分数。
答案
一、1.C 2.D 3.B 4.A
5.C 6.A 7.D
8.B 点拨:乳化形成的乳浊液不均一、不稳定,溶解形成的溶液均一、稳定,故溶解比乳化混合更均匀;在一定温度下,某固态物质在100 g溶剂中达到饱和状态时所溶解的溶质的质量,叫做这种物质在这种溶剂中的溶解度,20 ℃时,50 g水中溶解了15 g硝酸钾,没有说明是否饱和,则无法确定20 ℃时硝酸钾的溶解度是30 g;物质溶解度的大小,一方面与物质(指的是溶剂和溶质)本身有关;另一方面也与外界条件如温度、压强、溶剂种类等有关,与溶剂的多少没有关系;硝酸钾溶液恒温蒸发部分水,溶液仍饱和,溶质质量分数=×100%,温度不变溶解度不变,剩余溶液溶质质量分数不变。
9.C
10.D 点拨:设加入硝酸钠的质量为x,100 g×10%+x=(100 g+x)×20%,计算得出x=12.5 g。设蒸发水的质量为y,100 g×10%=(100 g-y)×20%,计算得出y=50 g,故②④正确。
11.B 点拨:A.不指明温度,不能比较两种物质的溶解度大小,该选项说法不正确;B.由表中信息可知,碳酸钾溶解度受温度变化影响较小,硝酸钾溶解度受温度变化影响较大,乙代表K2CO3的溶解度曲线,该选项说法正确;C.50 ℃~60 ℃之间,硝酸钾和碳酸钾的溶解度不可能相等,该选项说法不正确;D.40 ℃时,100 g水中溶解63.9 g硝酸钾恰好饱和,因此100 g KNO3饱和溶液中含硝酸钾的质量小于63.9 g,该选项说法不正确。故选B。
12.D
二、13.(1)200
(2)①NaCl ②B
14.(1)甲<乙<丙
(2)相等
(3)甲;7.5
(4)降温
15.(1)①温度;温度升高(或降低),食盐溶解速率加快(或减慢)
②晶体颗粒大小;食盐颗粒越小,溶解速率越快
(2)分别称取2 g颗粒大小相同的食盐,同时放进盛有等质量的不同温度(20 ℃和100 ℃)水的烧杯中,观察并记录两个烧杯中的食盐完全溶解所需的时间
(3)除验证条件外其他条件
16.(1)①A中瓶塞正放在桌面上,应倒放在桌面上
②B中NaCl与砝码放反了,应采用“左物右码”,称量NaCl
③F中用温度计搅拌,应用玻璃棒搅拌
④D中读数时仰视,应视线与凹液面最低处相平(以上四个任写三个即可)
(2)2.5;3.1%
(3)47.5;50;小于
(4)①A、D ②计算;称量;量取;溶解
(5)①> ②1?6
三、17.(1)1.6
(2)解:设68 g过氧化氢溶液中含有的过氧化氢的质量为x。
68 32
x 1.6 g
= x=3.4 g
则这瓶过氧化氢溶液中过氧化氢的质量分数为×100%=5%。
答:略。
点拨:根据氧气的实验室制法可知,二氧化锰是催化剂。其质量在化学反应前后不变;依据质量守恒定律可知氧气的质量=68 g+2 g-68.4 g=1.6 g。
可能用到的相对原子质量:H:1 O:16
一、选择题(本题包括12小题,每小题1分,共12分。每小题的4个选项中只有1个符合题意)
1.把少量下列物质分别放入水中,充分搅拌,可以形成溶液的是( )
A.碘 B.汽油 C.高锰酸钾 D.面粉
2.下列有关溶液的说法正确的是( )
A.所有溶液都能导电 B.无色澄清液体一定是溶液
C.只有固体能作溶质 D.水和酒精等都可用作溶剂
3.“美林”主要成分是布洛芬,“小儿开塞露”主要成分是甘油和山梨醇。两者都是儿科常用药,且都是药物分散在水中制成。“美林”即使密封保存放久了也会产生白色沉淀,“小儿开塞露”则久置不会分层。“美林”、“小儿开塞露”分别属于( )
A.乳浊液、乳浊液 B.悬浊液、溶液
C.乳浊液、溶液 D.悬浊液、乳浊液
4.乳化现象在生产和生活中很常见,下列常用的清洗方法中,用到乳化作用的是( )
A.用洗洁精除去盘子上的油污 B.用清水洗手
C.用洗衣粉洗去衣服上的泥渍 D.用盐酸除铁锈
5.在t ℃时,某物质X、Y分别完全溶于水,溶液中X、Y与水的质量关系分别如图a、图b所示。下列说法正确的是( )
A.X、Y都只能是固体 B.两种溶液一定是饱和溶液
C.图示溶液的浓度:X
A.增加日晒时间 B.把水搅动起来
C.把水喷向空中 D.向养鱼池中通入空气或者氧气
7.硝酸钾的溶解度随温度升高而增大。如图是有关硝酸钾溶液的实验操作及变化情况。下列说法正确的是( )
A.整个实验过程中硝酸钾的溶解度一定不变
B.①与②的溶液质量一定相等
C.①与③的溶质质量一定相等
D.②与③的溶质质量分数一定相等
8.下列关于溶液的说法不正确的是( )
A.与乳化作用相比,溶解能使物质混合得更均匀
B. 20 ℃时,50 g水中溶解了15 g硝酸钾,则20 ℃时硝酸钾的溶解度是30 g
C.一定温度下,固体物质的溶解度不随水的质量改变而改变
D.硝酸钾的饱和溶液恒温蒸发部分水后,剩余溶液溶质质量分数不变
9.20 ℃时,向一盛有30 g某物质的烧杯内加入100 g水,充分搅拌后静置,烧杯底部仍有未溶解的固体,过滤得到5 g固体和澄清溶液。下列有关叙述错误的是( )
A.该溶液中溶质的质量等于25 g
B.该溶液中溶质的质量分数等于20%
C.该温度下,再加20 g水后该溶液变为不饱和溶液
D.该温度下,再加30 g水后该溶液变为不饱和溶液
10.现有100 g溶质质量分数为10%的硝酸钠溶液,要将其溶质质量分数变为20%,可采用的方法是( )
①蒸发掉2/3溶剂 ②蒸发掉50 g溶剂 ③加入10 g硝酸钠
④加入12.5 g硝酸钠
A.①③ B.②③ C.①④ D.②④
11.K2CO3、KNO3在不同温度时的溶解度及溶解度曲线如图。下列说法正确的是( )
温度/℃ 20 40 50 60 80
溶解度/g K2CO3 110 117 121 126 139
KNO3 31.6 63.9 85.5 110 169
A.K2CO3的溶解度大于KNO3
B.乙代表K2CO3的溶解度曲线
C.t ℃应在50 ℃~60 ℃之间
D.40 ℃时,100 g KNO3饱和溶液中含63.9 g KNO3
12.如图所示,下列判断正确的是( )
A.Y 的溶解度比X 的溶解度大
B.t1 ℃时,X、Y 两种饱和溶液的溶质质量分数都是 20%
C.若烧杯内有晶体析出,则烧杯中饱和溶液的溶质为Y
D.t2 ℃时,若X、Y 的饱和溶液质量相等,则溶液中溶质的质量X<Y
二、填空题(本题包括4小题,共24分)
13.(3分)溶液在生命活动和生产、生活中起着十分重要的作用。
(1)农业生产常用溶质的质量分数为10%~20%的NaCl溶液来选种。现将300 g 25%的NaCl溶液稀释为15%的NaCl溶液,需要加水的质量为________g。
(2)根据下表回答问题:
温度/℃ 0 20 40 60 80 100
溶解度/g NaCl 35.7 36.0 36.6 37.3 38.4 39.8
NH4Cl 29.4 37.2 45.6 55.2 65.6 77.3
①60 ℃时,向两个分别盛有50 g NaCl和NH4Cl的烧杯中,各加入100 g的水,充分溶解后,为饱和溶液的是________溶液;
②采用一种操作方法,将上述烧杯中的剩余固体全部溶解,变为不饱和溶液。下列说法正确的是________(填字母)。
A.溶质的质量不变 B.溶液中溶质的质量分数一定减小
C.溶液质量可能不变 D.可升高温度或增加溶剂
14.(5分)如图1是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线。回答下列问题:
(1)t1 ℃时,甲、乙、丙三种物质的溶解度由小到大的顺序是______________。
(2)P点表示t2 ℃时甲、丙两种物质的溶解度________(填“相等”或“不相等”)。
(3)t2 ℃时,取甲、乙两种固体各20 g分别加入50 g水中充分溶解,实验现象如图2所示,则烧杯a中溶解的物质是______(填“甲”或“乙”),未溶解固体的质量是________g。
(4)当甲中含有少量的乙和丙(甲、乙、丙相互间均不发生化学反应)时,可采用________(填“降温”或“蒸发”)结晶的方法提纯甲物质。
15.(6分)食盐是生活中必备的调味品。通过学习和生活体验,我们发现多种因素都能影响食盐在水中的溶解速率。
(1)写出两个你认为可能影响食盐在水中溶解速率的因素,并预测其对食盐溶解速率的影响。
因素①:______________,你的预测是____________________________________;
因素②:______________,你的预测是__________________________________。
(2)从你所列因素中选出一个,通过实验验证你的预测,你设计的实验方案是_________________________________________________________________________________________________________________________________。
(3)要使验证实验达到预测的效果,必须控制____________________________。
16.(10分)如图1是配制50 g溶质质量分数为5%的NaCl溶液的实验操作示意图。结合图示回答下列问题:
(第16题图1)
(1)请找出图中的错误加以改正(写出三处即可):
①______________________________________________________;
②______________________________________________________;
③______________________________________________________。
(2)需要称量的氯化钠的质量是________g,在用托盘天平称量氯化钠固体时,1 g以下使用游码。如果甲同学按照B操作,其他操作都正确,所配得溶液的溶质质量分数为__________(计算结果精确至0.1%)。
(3)需要水的质量是________g,配制时应选择________(填“10”或“50”)mL的量筒。量取水时,如果乙同学按照图D读数,配制的其余操作准确规范,则所得溶液的溶质质量分数________ (填“小于”“等于”或“大于”)5%。
(4)①丙同学配制的上述溶液,经测定其氯化钠质量分数大于5%,下列可能的原因有__________(填字母序号)。
A.用量筒量取水时俯视读数
B.用来配制溶液的烧杯刚用少量蒸馏水润洗过
C.用托盘天平称取氯化钠时,将氯化钠放在右盘,且称量时使用了游码
D.把量好的水倒入烧杯时,有少量水溅出烧杯
②通过以上过程可知,配制一定溶质质量分数的溶液,五个主要步骤依次是________、________、________、________、装瓶并贴标签。
【注意:答对下列问题奖励3分,卷面总分不超过40分】
(5)如图2所示,在氯化钠的溶解过程中发生了两种变化:一种是离子向水中扩散,这一过程吸收热量Q1;另一种是离子和水分子作用,形成水合离子,这一过程放出热量Q2。
(第16题图2)
①氯化钠溶解时溶液的温度略微降低,原因是Q1______Q2(填“>”或“<”)。
②若氯化钠溶解于水的微观过程如图2所示,则形成的水合钠离子中,钠离子与水分子的个数比为____________________________________________。
三、计算题(本题包括1小题,共4分)
17.(4分)某化学兴趣小组欲测定一瓶过氧化氢溶液中过氧化氢的质量分数,取2 g二氧化锰和68 g过氧化氢溶液在烧杯中混合,完全反应后烧杯内剩余物质的总质量为68.4 g,求:
(1)反应中生成氧气的总质量________g。
(2)这瓶过氧化氢溶液中过氧化氢的质量分数。
答案
一、1.C 2.D 3.B 4.A
5.C 6.A 7.D
8.B 点拨:乳化形成的乳浊液不均一、不稳定,溶解形成的溶液均一、稳定,故溶解比乳化混合更均匀;在一定温度下,某固态物质在100 g溶剂中达到饱和状态时所溶解的溶质的质量,叫做这种物质在这种溶剂中的溶解度,20 ℃时,50 g水中溶解了15 g硝酸钾,没有说明是否饱和,则无法确定20 ℃时硝酸钾的溶解度是30 g;物质溶解度的大小,一方面与物质(指的是溶剂和溶质)本身有关;另一方面也与外界条件如温度、压强、溶剂种类等有关,与溶剂的多少没有关系;硝酸钾溶液恒温蒸发部分水,溶液仍饱和,溶质质量分数=×100%,温度不变溶解度不变,剩余溶液溶质质量分数不变。
9.C
10.D 点拨:设加入硝酸钠的质量为x,100 g×10%+x=(100 g+x)×20%,计算得出x=12.5 g。设蒸发水的质量为y,100 g×10%=(100 g-y)×20%,计算得出y=50 g,故②④正确。
11.B 点拨:A.不指明温度,不能比较两种物质的溶解度大小,该选项说法不正确;B.由表中信息可知,碳酸钾溶解度受温度变化影响较小,硝酸钾溶解度受温度变化影响较大,乙代表K2CO3的溶解度曲线,该选项说法正确;C.50 ℃~60 ℃之间,硝酸钾和碳酸钾的溶解度不可能相等,该选项说法不正确;D.40 ℃时,100 g水中溶解63.9 g硝酸钾恰好饱和,因此100 g KNO3饱和溶液中含硝酸钾的质量小于63.9 g,该选项说法不正确。故选B。
12.D
二、13.(1)200
(2)①NaCl ②B
14.(1)甲<乙<丙
(2)相等
(3)甲;7.5
(4)降温
15.(1)①温度;温度升高(或降低),食盐溶解速率加快(或减慢)
②晶体颗粒大小;食盐颗粒越小,溶解速率越快
(2)分别称取2 g颗粒大小相同的食盐,同时放进盛有等质量的不同温度(20 ℃和100 ℃)水的烧杯中,观察并记录两个烧杯中的食盐完全溶解所需的时间
(3)除验证条件外其他条件
16.(1)①A中瓶塞正放在桌面上,应倒放在桌面上
②B中NaCl与砝码放反了,应采用“左物右码”,称量NaCl
③F中用温度计搅拌,应用玻璃棒搅拌
④D中读数时仰视,应视线与凹液面最低处相平(以上四个任写三个即可)
(2)2.5;3.1%
(3)47.5;50;小于
(4)①A、D ②计算;称量;量取;溶解
(5)①> ②1?6
三、17.(1)1.6
(2)解:设68 g过氧化氢溶液中含有的过氧化氢的质量为x。
68 32
x 1.6 g
= x=3.4 g
则这瓶过氧化氢溶液中过氧化氢的质量分数为×100%=5%。
答:略。
点拨:根据氧气的实验室制法可知,二氧化锰是催化剂。其质量在化学反应前后不变;依据质量守恒定律可知氧气的质量=68 g+2 g-68.4 g=1.6 g。
同课章节目录
