鲁教版九年级化学上册5.3化学反应中的计算(ppt 共18张)
文档属性
| 名称 | 鲁教版九年级化学上册5.3化学反应中的计算(ppt 共18张) |

|
|
| 格式 | ppt | ||
| 文件大小 | 656.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-10-28 00:00:00 | ||
图片预览






文档简介
5.3 化学方程式的简单计算
想一想,你能获取哪些信息?
化学方程式的意义:
4 : 32 : 36
(相对分子质量×化学计量数)之比
(1)反应物、生成物、反应条件
2H2 + O2 2H2O
点燃
(3)各物质质量比
(2)各微粒个数比
2 : 1 : 2
2个水分子分解 ( ) ( ) ( )
2×18 2×2 1×32
10个水分子分解( ) ( ) ( )
10×18 10×2 5×32
n个水分子分解
9:1:8
9:1:8
9:1:8
2H2O = 2 H2 + O2
通电
反应物和生成物各物质质量比恒定
在电解水的反应中反应物与生成物之间的质量比可表示为:
2×18 :2×2 : 2 × 16
若: 36g : ( )g : ( )g
若: ( )g : ( )g : 16 g
36 : 4 : 32
4
32
18
2
36
18g
4
2g
32
16g
=
=
2H2O = 2 H2 + O2
通电
说明:在化学反应中,反应物与生成物之间的质量比是成正比例关系。因此,利用正比例关系根据化学方程式和已知的一种反应 物(或生成物)的质量,可求生成物(反应物)。
已知反应物水的质量求生成物氢气的质量
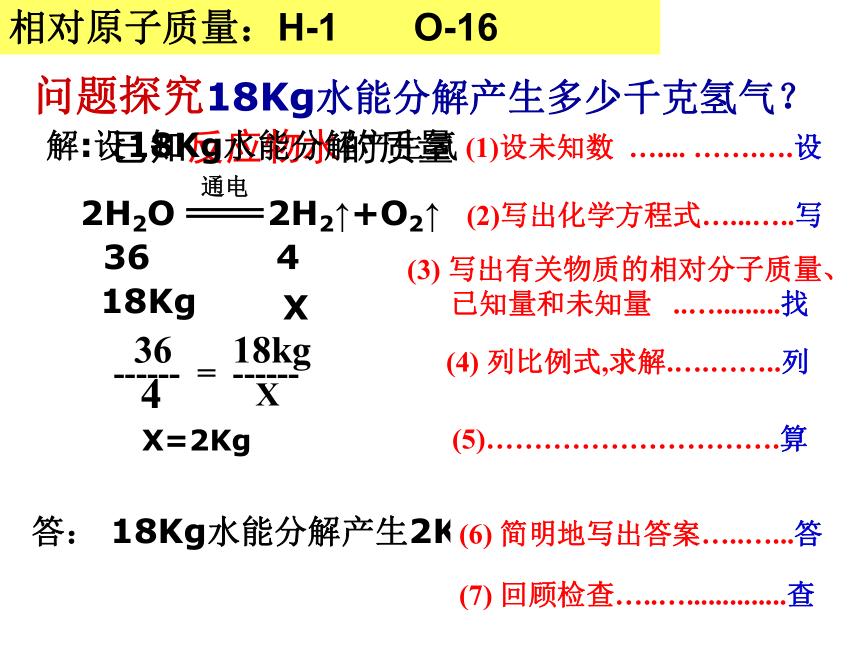
问题探究18Kg水能分解产生多少千克氢气?
解:设18Kg水能分解产生氢气的质量为X.
2H2O 2H2↑+O2↑
通电
36 4
X
18Kg
X=2Kg
答: 18Kg水能分解产生2Kg氢气.
相对原子质量:H-1 O-16
(1)设未知数 ….... …….….设
(2)写出化学方程式…...…..写
(3) 写出有关物质的相对分子质量、
已知量和未知量 ..….........找
(4) 列比例式,求解.….……..列
(5)………………………….算
(6) 简明地写出答案…..…...答
(7) 回顾检查…..…..............查
------ = ------
4
18kg
X
36
工业上电解氧化铝制取金属铝,反应的化学方程式为:
2Al2O3 4Al+3O2
如果加工一个铝锅需要1kg铝,至少需要电解多少多少千克的氧化铝(Al2O3 )才能制成这个铝锅?
通电
↑
(相对原子质量:Al-27 O-16)
你会了吗
解:设需要氧化铝的质量为X
204
X
1kg
答:需要氧化铝的质量为1.9kg
204 X
108 1kg
=
108
1.9kg
X=
204 X 1kg
108
=
你在解题中出现错误了吗?
2Al2O3 = 4Al+3O2↑
通电
下面是某同学做的根据化学方程式的计算题,请你会会诊,指出他的错误。
解:设需要氧化铝的质量为Xg
=
102
Xg
1kg
102 Xg
27 1kg
=
27
3.8
X=
102 X 1kg
27
Al2O3 = Al+3O2↑
通电
解:设需要氧化铝的质量为X
=
102 X2
X
1kg
204 X
108 1kg
=
27X4
1.9kg
X=
204 X 1kg
108
2Al2O3 = 4Al+3O2↑
通电
答:需要氧化铝的质量为1.9kg
×
×
×
×
×
×
×
1、 实验室要制取0.8g氧气,则需要过氧化氢的质量是多少克?(H-1 O-16)
2、 用3g碳与足量的氧气完全反应,生成二氧化碳多少?(C-12 O-16)
巩固训练:
小结:
化学方程式计算的三个要领和三个关键
三个要领:
①步骤要完整;
②格式要规范;
③得数要准确。
三个关键:
①准确书写化学式;
②化学方程式要配平;
③准确计算相对分子质量。
讨论1:
?从中你受到的启示是什么?
H:1 O:16
若将1g氢气和10g氧气混合在一密闭的容器中使之充分反应,生成水的质量为多少?
(思考: 你代入的应是氢气的质量还是氧气的质量)
2H2 + O2 ===== 2H2O
4 32 36
3、某同学把3g碳放在给定的氧气中充分燃烧,实验数据如下:
第一次
第二次
第三次
给定氧气的质量
4g
13g
8g
生成二氧化碳的质量
5.5g
11g
11g
(1)从以上数据说明,这三次实验中第 次恰好完全反应。
(2)第 次实验碳有剩余,剩余 g。
(3)第 次实验中氧气有剩余,剩余 g。
三
一
1.5
二
5
提高题: C:12 O:16
第二课时
反思回顾
实验室用含6.8g 过氧化氢的双氧水溶液在二氧化锰催化下制取氧气,完全反应后可生成氧气的质量是多少克?
2、 如果实验室中双氧水中过氧化氢的质量分数为5%,现有34克过氧化氢溶液,最多可制得氧气的质量为多少?
3、 如果实验室中双氧水中过氧化氢的质量分数为5%,要制取3.2g氧气,则需要这种双氧水的质量为多少?
交流讨论:
练习:医学上常用双氧水来清洗创口和局部抗菌。小美同学为了测定一瓶医用双氧水溶液的溶质质量分数,取该双氧水69g放入烧杯中,然后加入2g二氧化锰,完全反应后,称得烧杯内剩余物质的总质量为69.04g。请回答下列问题;
?(1)二氧化锰在反应中的作用是????? ,生成的氧气为?? ???g。
?(2)该双氧水溶液的溶质质量分数。(写出计算过程)
【2016年江苏省淮安市】(6分)
为测定某黄铜(铜、锌合金)中铜的质量分数,某同学取20g黄铜样品放入盛有200g稀硫酸的烧杯中,恰好完全反应(铜与稀硫酸不反应),测得烧杯中剩余物质的总质量为219.8g,试计算:
(1)生成氢气的质量 g。
(2)该黄铜样品中铜的质量分数和所用稀硫酸的溶质质量分数。(写出计算过程)
小提示:
Zn + H2SO4 ==ZnSO4 +H2
根据化学方程式的计算步骤及注意事项(韵语)
化学式子要配平,需将纯量代方程;
遇到体积换质量,上下单位要相同;
关系量间成比例,计算格式要完整。
想一想,你能获取哪些信息?
化学方程式的意义:
4 : 32 : 36
(相对分子质量×化学计量数)之比
(1)反应物、生成物、反应条件
2H2 + O2 2H2O
点燃
(3)各物质质量比
(2)各微粒个数比
2 : 1 : 2
2个水分子分解 ( ) ( ) ( )
2×18 2×2 1×32
10个水分子分解( ) ( ) ( )
10×18 10×2 5×32
n个水分子分解
9:1:8
9:1:8
9:1:8
2H2O = 2 H2 + O2
通电
反应物和生成物各物质质量比恒定
在电解水的反应中反应物与生成物之间的质量比可表示为:
2×18 :2×2 : 2 × 16
若: 36g : ( )g : ( )g
若: ( )g : ( )g : 16 g
36 : 4 : 32
4
32
18
2
36
18g
4
2g
32
16g
=
=
2H2O = 2 H2 + O2
通电
说明:在化学反应中,反应物与生成物之间的质量比是成正比例关系。因此,利用正比例关系根据化学方程式和已知的一种反应 物(或生成物)的质量,可求生成物(反应物)。
已知反应物水的质量求生成物氢气的质量
问题探究18Kg水能分解产生多少千克氢气?
解:设18Kg水能分解产生氢气的质量为X.
2H2O 2H2↑+O2↑
通电
36 4
X
18Kg
X=2Kg
答: 18Kg水能分解产生2Kg氢气.
相对原子质量:H-1 O-16
(1)设未知数 ….... …….….设
(2)写出化学方程式…...…..写
(3) 写出有关物质的相对分子质量、
已知量和未知量 ..….........找
(4) 列比例式,求解.….……..列
(5)………………………….算
(6) 简明地写出答案…..…...答
(7) 回顾检查…..…..............查
------ = ------
4
18kg
X
36
工业上电解氧化铝制取金属铝,反应的化学方程式为:
2Al2O3 4Al+3O2
如果加工一个铝锅需要1kg铝,至少需要电解多少多少千克的氧化铝(Al2O3 )才能制成这个铝锅?
通电
↑
(相对原子质量:Al-27 O-16)
你会了吗
解:设需要氧化铝的质量为X
204
X
1kg
答:需要氧化铝的质量为1.9kg
204 X
108 1kg
=
108
1.9kg
X=
204 X 1kg
108
=
你在解题中出现错误了吗?
2Al2O3 = 4Al+3O2↑
通电
下面是某同学做的根据化学方程式的计算题,请你会会诊,指出他的错误。
解:设需要氧化铝的质量为Xg
=
102
Xg
1kg
102 Xg
27 1kg
=
27
3.8
X=
102 X 1kg
27
Al2O3 = Al+3O2↑
通电
解:设需要氧化铝的质量为X
=
102 X2
X
1kg
204 X
108 1kg
=
27X4
1.9kg
X=
204 X 1kg
108
2Al2O3 = 4Al+3O2↑
通电
答:需要氧化铝的质量为1.9kg
×
×
×
×
×
×
×
1、 实验室要制取0.8g氧气,则需要过氧化氢的质量是多少克?(H-1 O-16)
2、 用3g碳与足量的氧气完全反应,生成二氧化碳多少?(C-12 O-16)
巩固训练:
小结:
化学方程式计算的三个要领和三个关键
三个要领:
①步骤要完整;
②格式要规范;
③得数要准确。
三个关键:
①准确书写化学式;
②化学方程式要配平;
③准确计算相对分子质量。
讨论1:
?从中你受到的启示是什么?
H:1 O:16
若将1g氢气和10g氧气混合在一密闭的容器中使之充分反应,生成水的质量为多少?
(思考: 你代入的应是氢气的质量还是氧气的质量)
2H2 + O2 ===== 2H2O
4 32 36
3、某同学把3g碳放在给定的氧气中充分燃烧,实验数据如下:
第一次
第二次
第三次
给定氧气的质量
4g
13g
8g
生成二氧化碳的质量
5.5g
11g
11g
(1)从以上数据说明,这三次实验中第 次恰好完全反应。
(2)第 次实验碳有剩余,剩余 g。
(3)第 次实验中氧气有剩余,剩余 g。
三
一
1.5
二
5
提高题: C:12 O:16
第二课时
反思回顾
实验室用含6.8g 过氧化氢的双氧水溶液在二氧化锰催化下制取氧气,完全反应后可生成氧气的质量是多少克?
2、 如果实验室中双氧水中过氧化氢的质量分数为5%,现有34克过氧化氢溶液,最多可制得氧气的质量为多少?
3、 如果实验室中双氧水中过氧化氢的质量分数为5%,要制取3.2g氧气,则需要这种双氧水的质量为多少?
交流讨论:
练习:医学上常用双氧水来清洗创口和局部抗菌。小美同学为了测定一瓶医用双氧水溶液的溶质质量分数,取该双氧水69g放入烧杯中,然后加入2g二氧化锰,完全反应后,称得烧杯内剩余物质的总质量为69.04g。请回答下列问题;
?(1)二氧化锰在反应中的作用是????? ,生成的氧气为?? ???g。
?(2)该双氧水溶液的溶质质量分数。(写出计算过程)
【2016年江苏省淮安市】(6分)
为测定某黄铜(铜、锌合金)中铜的质量分数,某同学取20g黄铜样品放入盛有200g稀硫酸的烧杯中,恰好完全反应(铜与稀硫酸不反应),测得烧杯中剩余物质的总质量为219.8g,试计算:
(1)生成氢气的质量 g。
(2)该黄铜样品中铜的质量分数和所用稀硫酸的溶质质量分数。(写出计算过程)
小提示:
Zn + H2SO4 ==ZnSO4 +H2
根据化学方程式的计算步骤及注意事项(韵语)
化学式子要配平,需将纯量代方程;
遇到体积换质量,上下单位要相同;
关系量间成比例,计算格式要完整。
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
