3.2原子的结构 第三课时(课件16页)
图片预览





文档简介
(共16张PPT)
课题2
原子的结构
第3课时
人教版
初中化学
学习目标
1、认识离子是构成物质的一种微粒。
2、知道离子结构示意图的画法以及离子符号的书写。
3、了解分子、原子和离子之间的关系。
新课引入
由于金属原子、非金属原子的原子核外最外层没有达到稳定结构,在化学反应中容易得失电子,从而达到稳定结构,那么,得失电子的结果怎样呢?
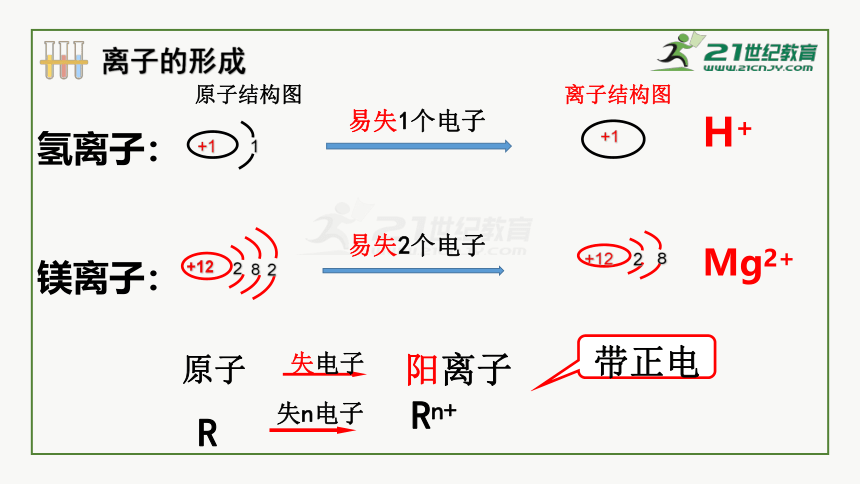
离子的形成
+1
1
+1
+12
2
8
2
+12
8
2
易失1个电子
易失2个电子
原子
阳离子
失电子
R
失n电子
Rn+
带正电
H+
原子结构图
离子结构图
Mg2+
氢离子:
镁离子:
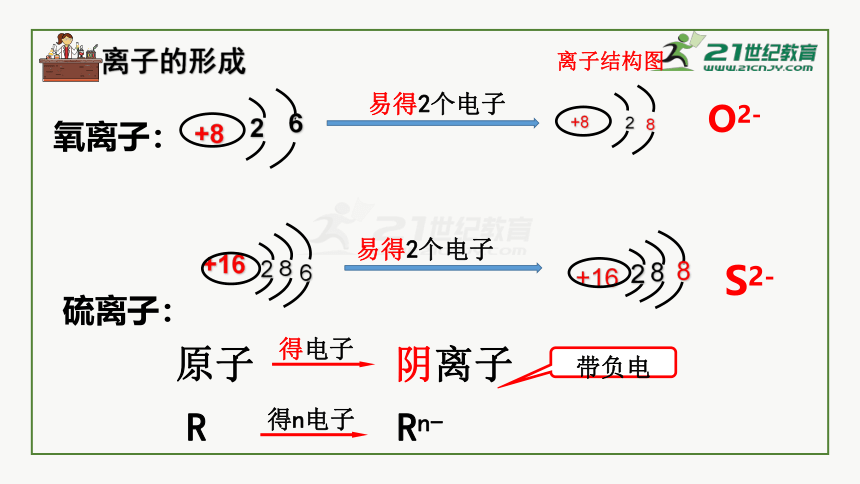
离子的形成
2
+8
6
2
+8
8
8
+16
6
2
8
+16
8
2
易得2个电子
易得2个电子
原子
得电子
阴离子
R
得n电子
Rn-
带负电
O2-
S2-
氧离子:
硫离子:
离子结构图
离子的定义
离子:带电荷的原子或原子团叫做离子。
阳离子——带正电荷的原子
阴离子——带负电荷的原子
Na+
、
Ca2+
、Mg2+
、Al3+
、H+
、NH4+
Cl-
、
O2-
、OH-
、
SO42-
、NO3-
、
CO32-
带电的原子团
阳离子(1个)
NH4+铵根离子
阴离子(5个)
OH-氢氧根离子
NO3-硝酸根离子
CO32-碳酸根离子
SO42-硫酸根离子
PO43-磷酸根离子
书写离子符号的方法
Mg2+
镁离子
Cl-
氯离子
氧离子
O2-
离子用离子符号表示:
在元素符号的右上角标出离子所带的电荷的多少及电荷的正负,当离子所带电荷数为1时,1可以不写。
离子符号表示的意义
Fe
3+
Fe
表示铁元素。
表示一个铁原子
这样你还会做吗?
Fe3+
表示一个铁离子。
3
加了一个3你还会做吗?
表示3个铁离子
表示每个铁离子带3个单位的正电荷
3
练习
用化学用语表示或写出符号的意义:
⑴钠离子
⑵氢离子
⑶2个氢离子
⑷氢原子
⑸氢分子
⑹2H
⑺2H2
⑻S2-
⑼2Al3+
⑽2Al
H+
2H+
H
H2
2个氢原子
2个氢分子
硫离子
2个铝离子
2个铝原子
Na+
原子和离子的联系和区别
原子
阳离子
阴离子
失电子
得电子
原子中:质子数=电子数(原子不带电)
2、区别:
1、联系:
区分原子、离子
阳离子中:质子数>电子数(带正电)
阴离子中:质子数<电子数(带负电)
练习
1.要能够分清原子结构示意图、离子结构示意图,要能够根据示意图写出对应的符号。
Na
Mg
2
1
8
+11
2
2
8
+12
2
8
+11
2
8
+12
2
8
8
+16
2
8
8
+17
原子:核电荷数=核外电子数
离子:核电荷数≠核外电子数
Mg2+
S2-
Cl-
2
6
8
+16
2
7
8
+17
Cl
S
Na+
练习
2.判断下列原子结构示意图是否正确?
+16
2
6
8
+8
2
8
+12
2
8
2
3.请写出下列示意图的名称
+2
2
+8
2
8
+17
2
8
7
+13
2
8
硫原子
氧原子
镁原子
氦原子
氧离子
氯原子
铝离子
课堂小结
原子
结合
物质
,如
金属
稀有气体
分子
结合
分解
聚集
物质
失或得电子
离子
得或失电子
结合
物质,如氯化钠
某些非金属固体
作业布置
1、复习本节课的内容
2、完成练习册对应的习题
3、预习下一节课的内容
https://www.21cnjy.com/help/help_extract.php
课题2
原子的结构
第3课时
人教版
初中化学
学习目标
1、认识离子是构成物质的一种微粒。
2、知道离子结构示意图的画法以及离子符号的书写。
3、了解分子、原子和离子之间的关系。
新课引入
由于金属原子、非金属原子的原子核外最外层没有达到稳定结构,在化学反应中容易得失电子,从而达到稳定结构,那么,得失电子的结果怎样呢?
离子的形成
+1
1
+1
+12
2
8
2
+12
8
2
易失1个电子
易失2个电子
原子
阳离子
失电子
R
失n电子
Rn+
带正电
H+
原子结构图
离子结构图
Mg2+
氢离子:
镁离子:
离子的形成
2
+8
6
2
+8
8
8
+16
6
2
8
+16
8
2
易得2个电子
易得2个电子
原子
得电子
阴离子
R
得n电子
Rn-
带负电
O2-
S2-
氧离子:
硫离子:
离子结构图
离子的定义
离子:带电荷的原子或原子团叫做离子。
阳离子——带正电荷的原子
阴离子——带负电荷的原子
Na+
、
Ca2+
、Mg2+
、Al3+
、H+
、NH4+
Cl-
、
O2-
、OH-
、
SO42-
、NO3-
、
CO32-
带电的原子团
阳离子(1个)
NH4+铵根离子
阴离子(5个)
OH-氢氧根离子
NO3-硝酸根离子
CO32-碳酸根离子
SO42-硫酸根离子
PO43-磷酸根离子
书写离子符号的方法
Mg2+
镁离子
Cl-
氯离子
氧离子
O2-
离子用离子符号表示:
在元素符号的右上角标出离子所带的电荷的多少及电荷的正负,当离子所带电荷数为1时,1可以不写。
离子符号表示的意义
Fe
3+
Fe
表示铁元素。
表示一个铁原子
这样你还会做吗?
Fe3+
表示一个铁离子。
3
加了一个3你还会做吗?
表示3个铁离子
表示每个铁离子带3个单位的正电荷
3
练习
用化学用语表示或写出符号的意义:
⑴钠离子
⑵氢离子
⑶2个氢离子
⑷氢原子
⑸氢分子
⑹2H
⑺2H2
⑻S2-
⑼2Al3+
⑽2Al
H+
2H+
H
H2
2个氢原子
2个氢分子
硫离子
2个铝离子
2个铝原子
Na+
原子和离子的联系和区别
原子
阳离子
阴离子
失电子
得电子
原子中:质子数=电子数(原子不带电)
2、区别:
1、联系:
区分原子、离子
阳离子中:质子数>电子数(带正电)
阴离子中:质子数<电子数(带负电)
练习
1.要能够分清原子结构示意图、离子结构示意图,要能够根据示意图写出对应的符号。
Na
Mg
2
1
8
+11
2
2
8
+12
2
8
+11
2
8
+12
2
8
8
+16
2
8
8
+17
原子:核电荷数=核外电子数
离子:核电荷数≠核外电子数
Mg2+
S2-
Cl-
2
6
8
+16
2
7
8
+17
Cl
S
Na+
练习
2.判断下列原子结构示意图是否正确?
+16
2
6
8
+8
2
8
+12
2
8
2
3.请写出下列示意图的名称
+2
2
+8
2
8
+17
2
8
7
+13
2
8
硫原子
氧原子
镁原子
氦原子
氧离子
氯原子
铝离子
课堂小结
原子
结合
物质
,如
金属
稀有气体
分子
结合
分解
聚集
物质
失或得电子
离子
得或失电子
结合
物质,如氯化钠
某些非金属固体
作业布置
1、复习本节课的内容
2、完成练习册对应的习题
3、预习下一节课的内容
https://www.21cnjy.com/help/help_extract.php
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
