第二节探索酸的性质复习
图片预览






文档简介
(共17张PPT)
国家环保部通报2010年上半年温州酸雨频率达到100%
酸雨:PH值小于5.6的降水
检测是否是酸雨?
硫酸能使酸碱指示剂变色
降低这杯酸雨的酸性,有哪些方法?以硫酸为例
同桌合作,用化学方程式表示你的方法
硫酸能使酸碱指示剂变色
硫酸+某些金属=盐+氢气
硫酸+某些金属氧化物=盐+水
硫酸+碱=盐+水
硫酸+某些盐=盐+酸
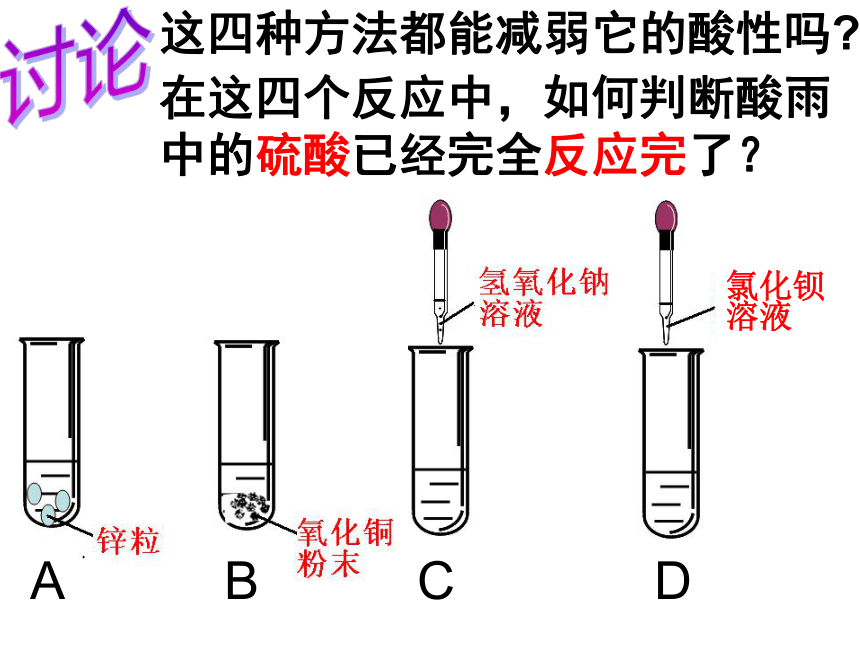
在这四个反应中,如何判断酸雨中的硫酸已经完全反应完了?
A
B
C
D
氯化钡
溶液
这四种方法都能减弱它的酸性吗
硫酸能使酸碱指示剂变色
硫酸+某些金属=盐+氢气
硫酸+某些金属氧化物=盐+水
硫酸+碱=盐+水
硫酸+某些盐=盐+酸
酸电离时生成的阳离子全部是氢离子
HCl = H+ + Cl-
H2SO4= 2H+ + SO42-
氯化钡
溶液
A
B
C
D
用盐酸来取代硫酸,下列反应是否都能够发生呢?
怎么去区别盐酸和硫酸?
HCl = H+ + Cl-
H2SO4= 2H+ + SO42-
酸根离子
实验二:
干燥某些气体
实验一:
白糖变黑炭
浓硫酸
实验三:浓硫酸稀释
A
B
如果是鱼塘中的水受酸雨污染,下列方案可行吗
方案一:倒入大量氢氧化钠(NaOH)
方案二:倒入大量石灰石粉末(CaCO3)
方案三:倒入大量氧化铜粉末(CuO)
请设计实验探究稀硫酸中哪种微粒(H+、 SO42- 、 H2O )能使氧化铜溶解,请设计实验方案。
谢谢指导
国家环保部通报2010年上半年温州酸雨频率达到100%
酸雨:PH值小于5.6的降水
检测是否是酸雨?
硫酸能使酸碱指示剂变色
降低这杯酸雨的酸性,有哪些方法?以硫酸为例
同桌合作,用化学方程式表示你的方法
硫酸能使酸碱指示剂变色
硫酸+某些金属=盐+氢气
硫酸+某些金属氧化物=盐+水
硫酸+碱=盐+水
硫酸+某些盐=盐+酸
在这四个反应中,如何判断酸雨中的硫酸已经完全反应完了?
A
B
C
D
氯化钡
溶液
这四种方法都能减弱它的酸性吗
硫酸能使酸碱指示剂变色
硫酸+某些金属=盐+氢气
硫酸+某些金属氧化物=盐+水
硫酸+碱=盐+水
硫酸+某些盐=盐+酸
酸电离时生成的阳离子全部是氢离子
HCl = H+ + Cl-
H2SO4= 2H+ + SO42-
氯化钡
溶液
A
B
C
D
用盐酸来取代硫酸,下列反应是否都能够发生呢?
怎么去区别盐酸和硫酸?
HCl = H+ + Cl-
H2SO4= 2H+ + SO42-
酸根离子
实验二:
干燥某些气体
实验一:
白糖变黑炭
浓硫酸
实验三:浓硫酸稀释
A
B
如果是鱼塘中的水受酸雨污染,下列方案可行吗
方案一:倒入大量氢氧化钠(NaOH)
方案二:倒入大量石灰石粉末(CaCO3)
方案三:倒入大量氧化铜粉末(CuO)
请设计实验探究稀硫酸中哪种微粒(H+、 SO42- 、 H2O )能使氧化铜溶解,请设计实验方案。
谢谢指导
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
