沪教课标版九年级化学上册2.3化学变化中的质量守恒(36张ppt)
文档属性
| 名称 | 沪教课标版九年级化学上册2.3化学变化中的质量守恒(36张ppt) |

|
|
| 格式 | ppt | ||
| 文件大小 | 1.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版(试用本) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-10-06 00:00:00 | ||
图片预览






文档简介
(共36张PPT)
质量减小
质量守恒定律
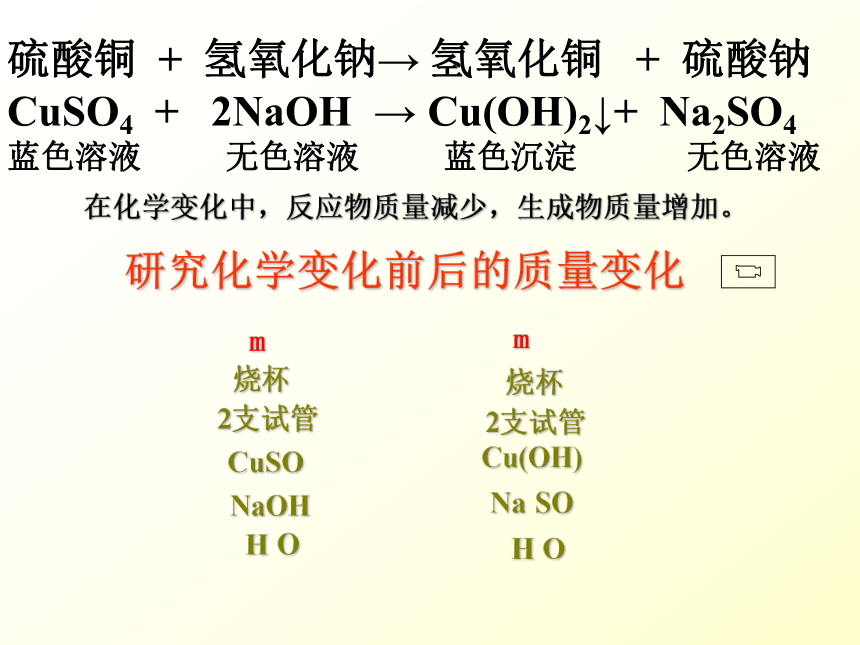
硫酸铜
+
氢氧化钠→
氢氧化铜
+
硫酸钠CuSO4
+
2NaOH
→
Cu(OH)2↓+
Na2SO4
蓝色溶液
无色溶液
蓝色沉淀
无色溶液
在化学变化中,反应物质量减少,生成物质量增加。
研究化学变化前后的质量变化
m1
m2
烧杯
2支试管
CuSO4
NaOH
H2O
烧杯
2支试管
Na2SO4
Cu(OH)2
H2O
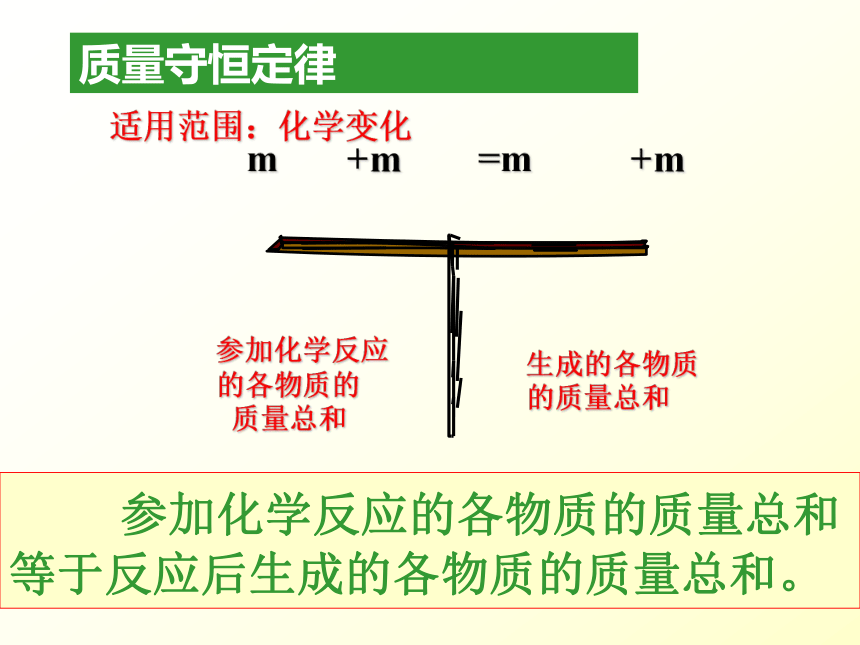
质量守恒定律
参加化学反应
的各物质的
质量总和
生成的各物质的质量总和
参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。
mNaOH+mCuSO4=mCu(OH)2+mNa2SO4
适用范围:化学变化
为什么化学反应前后的物质的质量总和相等?
试用分子、原子的观点解释质量守恒的原因。
想一想:
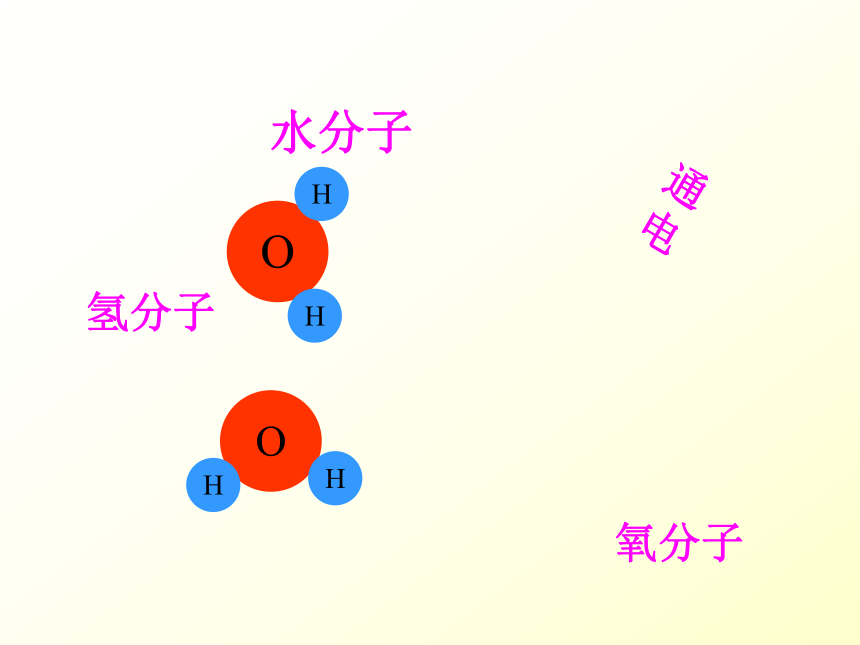
O
H
H
O
H
H
水分子
通电
氢分子
氧分子
O
H
H
O
O
O
H
H
H
H
H
H
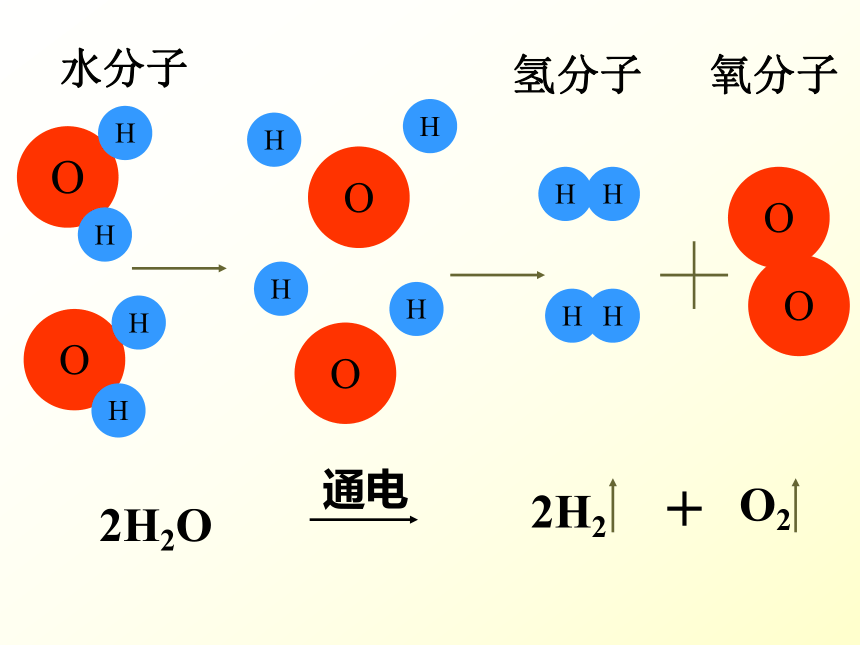
水分子
氢分子
氧分子
H
H
H
H
O
O
+
2H2O
2H2
O2
通电
质量守恒的原因:
宏观:反应前后元素种类、质量不变。
微观:
原子种类不变。
原子数目不变。
原子质量不变。
是否存在违背质量守恒定律的化学反应呢?
质量减小
C
+
O2
CO2
点燃
1、为什么质量会变小?
是由于反应有气体生成的缘故。
一定要在密闭容器内进行。
活
动
与
探
究
2、若选择有气体参加或有气体生成的化学反应来证明质量守恒定律,对反应环境有什么要求?
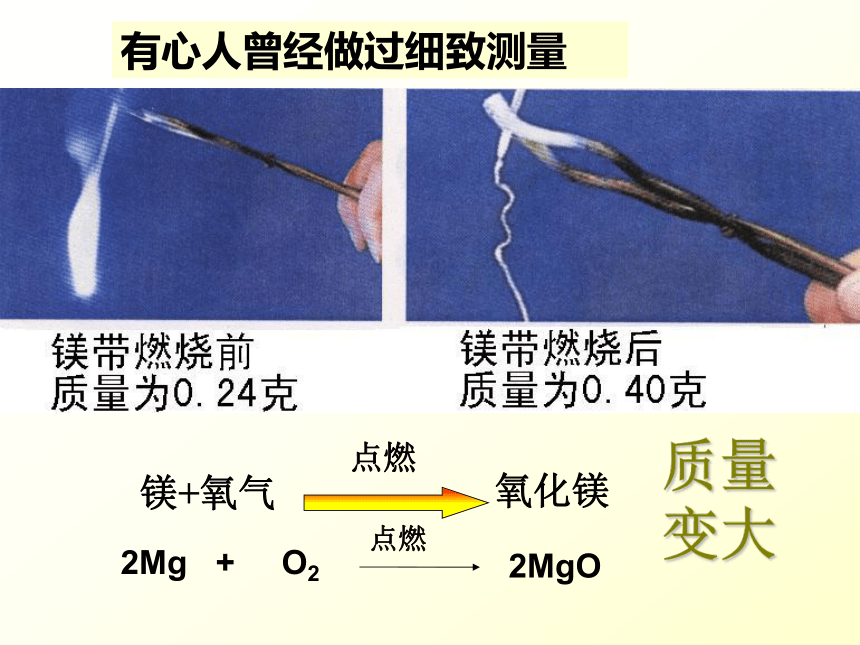
有心人曾经做过细致测量
镁+氧气
氧化镁
点燃
2Mg
+
O2
2MgO
点燃
质量变大
“水变含碳元素的高价的汽油、柴油,经济收入惊人,技术转让,请有识之士加盟。”同学们,假如你是老板,你是否会加盟呢?请谈一谈你的想法?
廣而告之
想一想:
2、质量守恒的原因:
宏观:反应前后元素种类、质量不变。
微观:
原子种类不变。
原子数目不变。
原子质量不变。
1、质量守恒定律
小结
2011年中考
22.联合国将2011年定为“国际化学年”以彰显化学对知识进步、环境保护和经济发展的重要贡献。
①拉瓦锡通过实验揭示了质量守恒定律。根据质量守恒定律推断,在化学反应
,X的化学式
是________。
H2
考试链接
2014年浦东一模
47
.化学与生活息息相关。
47
.化学与生活息息相关。
47.化学与生活息息相关。
③NH2Cl消毒时发生反应:NH2Cl+X→NH3+HClO,
其中X的化学式为_________.
H2O
47.化学与生产生活、社会发展息息相关,请回答。
⑤
为提高煤的利用率,可将碳与水蒸气反应得到两种可燃性气体,其微观示意图如下:
Ⅰ.根据质量守恒定律判断,上述微观示意图中缺少的微粒是____。
D
2012年浦东一模
2015中考
50)实验室用氯酸钾和二氧化锰的混合物制取氧气,某次实验中固体的质量变化如下:
①生成氧气的质量是
g。
4.8
15+5-15.2
2015年浦东一模
46.在一定条件下,甲、乙、丙、丁在某密闭
容器中发生反应,测得反应前后各物质的
质量分数如右图所示。正确的说法是(
)
A.该反应是分解反应
B.若消耗3
g乙,则生成17
g丙
C.丁一定是该反应的催化剂
D.甲、乙的质量之和一定等于生成丙的质量
B
2013浦东一模
46.密闭容器中有甲~丁四种物质,右图为反应前后各物质的质量分数,说法错误的是(
)
A.丙是化合物
B.该反应是化合反应
C.参加反应的甲、乙质量比是21:4
D.反应前甲和乙的质量之和大于生成丙的质量
C
布置作业
练习册P21~P22的第4题
谢
谢!
化学方程式
木炭在氧气中燃烧生成二氧化碳的反应
可以用文字表示为
:
碳
点燃
二氧化碳
+
氧气
“
和
”
“
反应条件
”
“
生成
”
反应物
生成物
↓
1、定义:用化学式来表示化学反应的式子,叫做化学方程式。
2、书写
(1)原则:
以客观事实为依据
遵循质量守恒定律---箭头两边的各原子数目相等
(2)、书写化学方程式的步骤
①写:正确书写化学式和反应条件
②配:配平化学方程式
方法1:奇数偶配法(找到氧原子是奇数的化学式)
Mg
+
O2
点燃
MgO
点燃
P
+
O2
点燃
P2O5
2
2
4
2
5
Fe
+
O2
3
2
Fe3O4
方法2:待定系数法(找到元素种类最多的化学式)
P
+
O2
点燃
P2O5
2
2
5
4
2
1
H2O
通电
H2+
O2
1
1
2
2
1
2
C
+
O2
点燃
CO2
H2
+
O2
点燃
H2O
Ca(OH)2+CO2
CaCO3
+
H2O
KClO3
KCl
+
O2
MnO2
△
H2O2
MnO2
H2O
+
O2
2
2
2
3
2
2
2
2
如果反应物和生成物中都有气体,气体生成物就不需注“↑”;
③注:用“↑”和“↓”来注明产生的气体和沉淀
“↑”和“↓”是表示生成物状态的符号,在反应物中即使是气体、固体也决不能注;
↑
↑
↓
C
+
O2
点燃
CO2
H2
+
O2
点燃
H2O
Ca(OH)2+CO2
CaCO3
+
H2O
KClO3
KCl
+
O2
MnO2
△
H2O2
MnO2
H2O
+
O2
H2O
通电
H2
+
O2
2
2
2
3
2
2
2
2
2
2
↑
↑
↑
↑
↓
写出盐酸滴在大理石上的化学方程式
C
O
O
C
O
O
12
(16×2)
32
44
:
:
:
:
(12+16
×
2)
12
3、化学方程式的意义和读法
(1)宏观读法:
每12g碳跟32g氧气在点燃的条件下反应生成44g二氧化碳气体。
(2)微观读法:
每1mol碳和1mol氧气在点燃的条件下反应生成1mol二氧化碳气体。
36
4
32
②表示每2mol水在通电的条件下能反应生成2mol氢气和1mol氧气。
①表示每36g水在通电的条件下能反应生成4g氢气和32g氧气。
4、化学方程式的简单计算
例:1、实验室常用过氧化氢制取少量氧气,试问每摩尔过氧化氢能得到氧气多少摩尔?
2、工业上可用电解水得到氧气,每摩尔水能得到氧气多少摩尔?
3、制取1mol氧气,需要氯酸钾多少摩尔?
2、用电解水的方法制1mol氧气,需要多少摩尔水?
1、3mol镁跟多少摩尔氧气恰好完全反应?生成氧化镁多少摩尔?
练一练:
再见
质量减小
质量守恒定律
硫酸铜
+
氢氧化钠→
氢氧化铜
+
硫酸钠CuSO4
+
2NaOH
→
Cu(OH)2↓+
Na2SO4
蓝色溶液
无色溶液
蓝色沉淀
无色溶液
在化学变化中,反应物质量减少,生成物质量增加。
研究化学变化前后的质量变化
m1
m2
烧杯
2支试管
CuSO4
NaOH
H2O
烧杯
2支试管
Na2SO4
Cu(OH)2
H2O
质量守恒定律
参加化学反应
的各物质的
质量总和
生成的各物质的质量总和
参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。
mNaOH+mCuSO4=mCu(OH)2+mNa2SO4
适用范围:化学变化
为什么化学反应前后的物质的质量总和相等?
试用分子、原子的观点解释质量守恒的原因。
想一想:
O
H
H
O
H
H
水分子
通电
氢分子
氧分子
O
H
H
O
O
O
H
H
H
H
H
H
水分子
氢分子
氧分子
H
H
H
H
O
O
+
2H2O
2H2
O2
通电
质量守恒的原因:
宏观:反应前后元素种类、质量不变。
微观:
原子种类不变。
原子数目不变。
原子质量不变。
是否存在违背质量守恒定律的化学反应呢?
质量减小
C
+
O2
CO2
点燃
1、为什么质量会变小?
是由于反应有气体生成的缘故。
一定要在密闭容器内进行。
活
动
与
探
究
2、若选择有气体参加或有气体生成的化学反应来证明质量守恒定律,对反应环境有什么要求?
有心人曾经做过细致测量
镁+氧气
氧化镁
点燃
2Mg
+
O2
2MgO
点燃
质量变大
“水变含碳元素的高价的汽油、柴油,经济收入惊人,技术转让,请有识之士加盟。”同学们,假如你是老板,你是否会加盟呢?请谈一谈你的想法?
廣而告之
想一想:
2、质量守恒的原因:
宏观:反应前后元素种类、质量不变。
微观:
原子种类不变。
原子数目不变。
原子质量不变。
1、质量守恒定律
小结
2011年中考
22.联合国将2011年定为“国际化学年”以彰显化学对知识进步、环境保护和经济发展的重要贡献。
①拉瓦锡通过实验揭示了质量守恒定律。根据质量守恒定律推断,在化学反应
,X的化学式
是________。
H2
考试链接
2014年浦东一模
47
.化学与生活息息相关。
47
.化学与生活息息相关。
47.化学与生活息息相关。
③NH2Cl消毒时发生反应:NH2Cl+X→NH3+HClO,
其中X的化学式为_________.
H2O
47.化学与生产生活、社会发展息息相关,请回答。
⑤
为提高煤的利用率,可将碳与水蒸气反应得到两种可燃性气体,其微观示意图如下:
Ⅰ.根据质量守恒定律判断,上述微观示意图中缺少的微粒是____。
D
2012年浦东一模
2015中考
50)实验室用氯酸钾和二氧化锰的混合物制取氧气,某次实验中固体的质量变化如下:
①生成氧气的质量是
g。
4.8
15+5-15.2
2015年浦东一模
46.在一定条件下,甲、乙、丙、丁在某密闭
容器中发生反应,测得反应前后各物质的
质量分数如右图所示。正确的说法是(
)
A.该反应是分解反应
B.若消耗3
g乙,则生成17
g丙
C.丁一定是该反应的催化剂
D.甲、乙的质量之和一定等于生成丙的质量
B
2013浦东一模
46.密闭容器中有甲~丁四种物质,右图为反应前后各物质的质量分数,说法错误的是(
)
A.丙是化合物
B.该反应是化合反应
C.参加反应的甲、乙质量比是21:4
D.反应前甲和乙的质量之和大于生成丙的质量
C
布置作业
练习册P21~P22的第4题
谢
谢!
化学方程式
木炭在氧气中燃烧生成二氧化碳的反应
可以用文字表示为
:
碳
点燃
二氧化碳
+
氧气
“
和
”
“
反应条件
”
“
生成
”
反应物
生成物
↓
1、定义:用化学式来表示化学反应的式子,叫做化学方程式。
2、书写
(1)原则:
以客观事实为依据
遵循质量守恒定律---箭头两边的各原子数目相等
(2)、书写化学方程式的步骤
①写:正确书写化学式和反应条件
②配:配平化学方程式
方法1:奇数偶配法(找到氧原子是奇数的化学式)
Mg
+
O2
点燃
MgO
点燃
P
+
O2
点燃
P2O5
2
2
4
2
5
Fe
+
O2
3
2
Fe3O4
方法2:待定系数法(找到元素种类最多的化学式)
P
+
O2
点燃
P2O5
2
2
5
4
2
1
H2O
通电
H2+
O2
1
1
2
2
1
2
C
+
O2
点燃
CO2
H2
+
O2
点燃
H2O
Ca(OH)2+CO2
CaCO3
+
H2O
KClO3
KCl
+
O2
MnO2
△
H2O2
MnO2
H2O
+
O2
2
2
2
3
2
2
2
2
如果反应物和生成物中都有气体,气体生成物就不需注“↑”;
③注:用“↑”和“↓”来注明产生的气体和沉淀
“↑”和“↓”是表示生成物状态的符号,在反应物中即使是气体、固体也决不能注;
↑
↑
↓
C
+
O2
点燃
CO2
H2
+
O2
点燃
H2O
Ca(OH)2+CO2
CaCO3
+
H2O
KClO3
KCl
+
O2
MnO2
△
H2O2
MnO2
H2O
+
O2
H2O
通电
H2
+
O2
2
2
2
3
2
2
2
2
2
2
↑
↑
↑
↑
↓
写出盐酸滴在大理石上的化学方程式
C
O
O
C
O
O
12
(16×2)
32
44
:
:
:
:
(12+16
×
2)
12
3、化学方程式的意义和读法
(1)宏观读法:
每12g碳跟32g氧气在点燃的条件下反应生成44g二氧化碳气体。
(2)微观读法:
每1mol碳和1mol氧气在点燃的条件下反应生成1mol二氧化碳气体。
36
4
32
②表示每2mol水在通电的条件下能反应生成2mol氢气和1mol氧气。
①表示每36g水在通电的条件下能反应生成4g氢气和32g氧气。
4、化学方程式的简单计算
例:1、实验室常用过氧化氢制取少量氧气,试问每摩尔过氧化氢能得到氧气多少摩尔?
2、工业上可用电解水得到氧气,每摩尔水能得到氧气多少摩尔?
3、制取1mol氧气,需要氯酸钾多少摩尔?
2、用电解水的方法制1mol氧气,需要多少摩尔水?
1、3mol镁跟多少摩尔氧气恰好完全反应?生成氧化镁多少摩尔?
练一练:
再见
