2020年人教版第五单元《化学方程式》5.1质量守恒定律最新中考真题练习
文档属性
| 名称 | 2020年人教版第五单元《化学方程式》5.1质量守恒定律最新中考真题练习 |

|
|
| 格式 | doc | ||
| 文件大小 | 73.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-10-07 00:00:00 | ||
图片预览


文档简介
第五单元《化学方程式》5.1质量守恒定律
一、选择题:
1、(2020?黑龙江)漂白粉可用于自来水的杀菌消毒,其有效成分是次氯酸钙[化学式为Ca(ClO)2].次氯酸钙可发生如下反应:Ca(ClO)2+X+H2O═CaCO3↓+2HClO,则X的化学式为( )
A.Cl2 B.CO2 C.CaCl2 D.O2
2、(2020?沈阳)氮化硅是一种性能优异的无机非金属材料,可通过以下反应来制备:3SiO2+6C+2XSi3N4+6CO,此化学方程式中X的化学式是( )
A.N2 B.Si C.NO D.CO2
3、(2020?恩施州)下列选项中,不利于培养化学学科核心素养的是( )
A.变化与守恒:某物质R燃烧后生成CO2和H2O,则R中一定含C、H元素,可能含O元素
B.模型与推理:氧化物一定含有氧元素,但含有氧元素的化合物不一定是氧化物
C.宏观与微观:品红在水中扩散,说明分子总在不停地运动
D.探究与创新:探究红砖粉是否为过氧化氢分解的催化剂,只需设计实验证明红砖粉能否改变反应速率即可
4、(2020?东莞市)化学方程式2Mg+O22MgO可读作( )
A.镁加氧气等于氧化镁
B.2个镁加1个氧气等于2个氯化镁
C.镁和氧气在点燃条件下生成氧化镁
D.镁加氧气点燃等于氧化镁
5、(2020?徐州)下列关于有机物的叙述中正确的是( )
A.甲醇(CH4O)中氧元素的质量分数最大
B.葡萄糖(C6H12O6)中C、H、O的质量比为1:2:1
C.醋酸(C2H4O2)由2个碳元素,4个氢元素、2个氧元素组成
D.某有机物在O2中完全燃烧只生成CO2和H2O,则该物质只含碳、氢元素
6、(2020?怀化)将甲、乙、丙、丁四种物质置于一个完全密闭的容器中,在一定条件下反应,已知反应前后各物质的质量如下:
物质 甲 乙 丙 丁
反应前的质量/g 30 10 5 5
反应后的质量/g 2 4 m 39
下列有关说法正确的是( )
A.m=0
B.发生反应的甲、乙质量比为3:1
C.该反应是化合反应
D.丙一定作催化剂
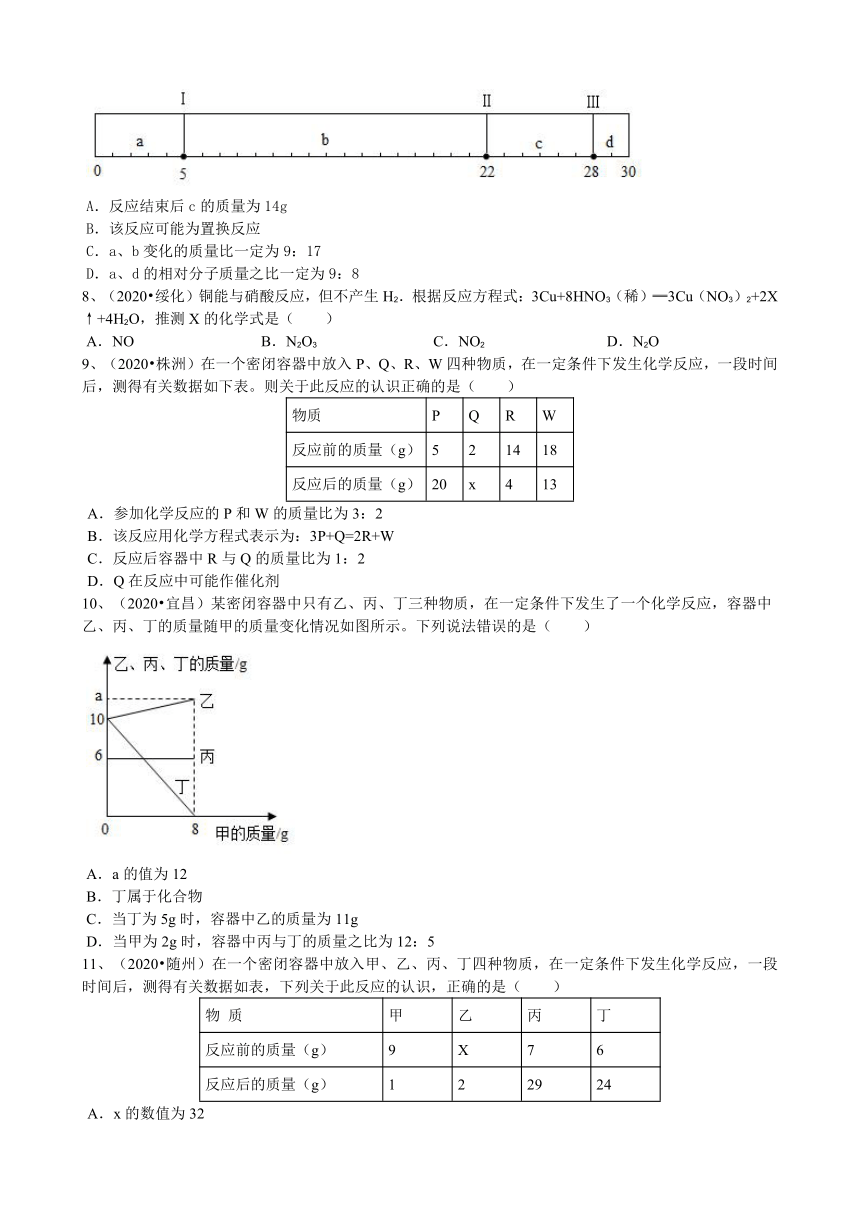
7、(2020?昆明)在一个密闭容器中,有a、b、c、d四种物质,反应前各物质的质量关系如图刻度纸所示(例如:d的质量为2g)。在一定条件下发生反应,反应结束后,再次测得各物质的质量变化,并通过刻度的移动来表示,且记录在同一张刻度纸上:刻度线Ⅰ向右移动9格;刻度线Ⅱ向左移动8格;刻度线Ⅲ向左移动8格。下列说法正确的是( )
A.反应结束后c的质量为14g
B.该反应可能为置换反应
C.a、b变化的质量比一定为9:17
D.a、d的相对分子质量之比一定为9:8
8、(2020?绥化)铜能与硝酸反应,但不产生H2.根据反应方程式:3Cu+8HNO3(稀)═3Cu(NO3)2+2X↑+4H2O,推测X的化学式是( )
A.NO B.N2O3 C.NO2 D.N2O
9、(2020?株洲)在一个密闭容器中放入P、Q、R、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表。则关于此反应的认识正确的是( )
物质 P Q R W
反应前的质量(g) 5 2 14 18
反应后的质量(g) 20 x 4 13
A.参加化学反应的P和W的质量比为3:2
B.该反应用化学方程式表示为:3P+Q=2R+W
C.反应后容器中R与Q的质量比为1:2
D.Q在反应中可能作催化剂
10、(2020?宜昌)某密闭容器中只有乙、丙、丁三种物质,在一定条件下发生了一个化学反应,容器中乙、丙、丁的质量随甲的质量变化情况如图所示。下列说法错误的是( )
A.a的值为12
B.丁属于化合物
C.当丁为5g时,容器中乙的质量为11g
D.当甲为2g时,容器中丙与丁的质量之比为12:5
11、(2020?随州)在一个密闭容器中放入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如表,下列关于此反应的认识,正确的是( )
物??质 甲 乙 丙 丁
反应前的质量(g) 9 X 7 6
反应后的质量(g) 1 2 29 24
A.x的数值为32
B.若甲为化合物,乙为单质,则该反应一定为置换反应
C.该反应中丙和丁的质量变化之比为11:9
D.若丁为水,则甲或乙必定为酸或碱
12、(2020?青海)氢气与四氯化硅反应制取硅的化学方程式为:2H2+SiCl4Si+4X,其中X的化学式是( )
A.Cl2 B.H2O C.HCl D.SiH4
13、(2020?扬州)潜艇供氧的一种反应原理为2X+2CO2═2Na2CO3+O2,其中X的化学式是( )
A.Na B.Na2O C.Na2O2 D.NaOH
14、(2020?郴州)一定质量的某化合物完全燃烧,需要3.2g氧气,生成4.4g二氧化碳和1.8g水。下列判断错误的是( )
A.该化合物的质量为3.0g
B.该化合物一定含有碳、氢、氧三种元素
C.该化合物中碳、氢、氧的原子个数比为2:4:1
D.该化合物中碳元素的质量分数是40%
15、(2020?湘西州)煤中含有少量的硫元素,在煤中加入X可有效防止煤燃烧时生成的SO2对大气造成污染,发生反应的化学方程式是2X+2SO2+O2═2CaSO4+2CO2,则X的化学式是( )
A.CaO B.Na2CO3?? C.Ca(HCO3)2? D.CaCO3
16、(2020?黄冈)将69g酒精(C2H5OH)点燃,酒精燃烧全部变为CO、CO2和H2O,恢复到室温,测得所得气体中氧元素质量分数为64%,则燃烧所耗氧气的质量为( )
A.136g B.64g C.112g D.48g
17、(2020?凉山州)某物质1.6克在空气中充分燃烧共生成4.4克二氧化碳和3.6克水。则下列说法正确的是( )
①该物质中一定含有氧元素;
②该物质中一定不含氧元素;
③该物质中一定含有碳、氢元素;
④该物质的一个分子中碳、氢原子的个数比为1:4;
⑤该物质中氢元素的质量分数最大。
A.①②③④⑤ B.②③④ C.③④⑤ D.②③④⑤
18、(2020?抚顺)在实验室和化工生产中常用到硝酸。硝酸是一种强氧化剂,能与碳发生氧化还原反应,化学方程式为4HNO3+C═2H2O+4X↑+CO2↑.则X是( )
A.NO2 B.CO C.NO D.N2O5
19、(2020?邵阳)已知某纯净物4.6g在足量的氧气中充分燃烧后,生成8.8g二氧化碳和5.4g水。下列关于该纯净物组成的说法正确的是( )
A.只含有碳、氢元素
B.一定含有碳、氢、氧三种元素
C.一定含有碳、氢元素,可能含有氧元素
D.一定含有碳元素,可能含有氢、氧元素
20、(2020?天津)现将20g A和足量B在一定条件下充分反应,生成16g C和11g D,则参加反应的A和B的质量比是( )
A.20:11 B.20:7 C.5:4 D.16:11
21、(2020?湘潭)为及时发现燃气泄漏,常在燃气中加入微量具有难闻气味的乙硫醇(C2H5SH),乙碳醇燃烧的化学方程式为:2C2H5SH+9O24CO2+2X+6H2O,其中X的化学式为( )
A.SO2 B.H2S C.CO D.H2
22、(2020?盐城)将一定质量的甲醇(CH3OH)和氧气(O2)置于密闭容器中点燃,一段时间后反应停止,冷却、测得反应后各物质的质量,相关数据如下表所示。下列说法不符合事实的是( )
物质 CH3OH O2 H2O CO2 X
反应前质量/g m 12.8 0 0 0
反应后质量/g 0 0 10.8 8.8 n
A.m>n
B.X中一定含有碳元素
C.无法判断X中是否含有氧元素
D.生成物中C、H两种元素的质量比为3:1
23、(2020?齐齐哈尔)学校防控新冠肺炎所用消毒液成分之一是次氯酸钠,以下反应可生成次氯酸钠,Cl2+2NaOH═NaCl+X+H2O,其中X的化学式为( )
A.NaClO B.Na2O C.NaOH D.NaClO3
24、(2020?衡阳)“84消毒液”可用于新冠状病毒肺炎的防疫,制备其主要成分次氯酸钠(NaClO)的化学方程式为:2NaOH+Cl2═NaClO+NaCl+X.则X的化学式是( )
A.ClO2 B.H2 C.H2O D.Na2O
25、(2020?乐山)将20g镁、铁的金属混合物加入到一定质量的稀硫酸中,恰好完全反应后,经测定溶液质量增加了19g,将反应后的溶液蒸干,得到固体的质量为( )
A.39g B.60g C.68g D.73g
26、(2020?河南)氯碱工业是以电解食盐水为基础的基本化学工业,电解食盐水不可能生成的是( )
A.H2 B.Cl2 C.NaOH D.NaNO3
27、工业上可以将一氧化碳转化为甲烷,反应的微观示意图如图,下列说法不正确的是( )
A.丁的相对分子质量为18
B.丙中碳、氢原子个数比为1:4
C.28g甲完全反应至少需要2g乙
D.反应前后原子种类不变
28、(2020?湘潭)某固体由镁、锌、铁三种金属中的一种或几种组成,现取ag固体于烧杯中,再加入足量稀盐酸,充分反应后,将所得溶液小心蒸干(不考虑操作过程中物质的损耗),得到(a+14.2)g不含结晶水的固体,则a的取值范围是( )
A.4.8≤a≤13.0 B.11.2<a≤13.0
C.3.6≤a≤11.2 D.4.8≤a<11.2
二、填空题:
1、(2020海南)2020年5月5日,长征五号B运载火箭在海南文昌成功发射,该火箭采用无毒无污染的液氧、液氢和煤油作为推进剂,正式拉开我国载人航天工程“第三步”任务的序幕。
(1)液氢属于 (填“单质”、“氧化物”或“混合物”);
(2)火箭用到了钛合金。工业制钛的一个反应为:TiF4+2H2SO44HF+2X+TiO2,X的化学式为 ,TiO2中Ti的化合价为
2、(2020毕节市)在距地面10~50km的高空有一层臭氧(O3),它能吸收大部分紫外线,保护地球生物。臭氧与氧气在一定条件下能相互转化,在此过程中改变的是 (填选项序号)。
a.总质量 b.原子数 c.分子数
3、(2020?衢州)利用加热高锰酸钾的方法,验证化学反应中质量守恒定律。如图,小科将适量高锰酸钾装入试管,塞入一团棉花并测出试管、棉花与药品的总质量为m1.加热使之充分反应后,测得量筒中气体体积为V,再次测得反应装置与物质总质量为m2,已知常温常压下氧气密度为ρ.据此请回答:
(1)实验中用量筒收集气体的好处是
(2)实验中,试管口内壁附着紫红色小液滴,请解释产生该现象的原因
(3)根据实验数据计算发现:m1-m2≠ρV,与质量守恒定律不符。造成这一实验结果的原因分析正确的是
A、试管中高锰酸钾没有完全分解
B、导管口连续均匀冒气泡时才收集气体
C、未调节量筒内外液面相平就读数
D、停止加热时,先将导管移出水面,再熄灭酒精灯
参考答案
一、选择题:
1 2 3 4 5 6 7 8 9 10
B A D C A C C A D D
11 12 13 14 15 16 17 18 19 20
C C C C D C B A B B
21 22 23 24 25 26 27 28
A C A C C D C A
二、填空题:
1、答案为:
(1)单质;
(2)SO3;+4。
2、答案为:
c。
3、解:(1)实验中用量筒收集气体的好处是便于直接读出氧气的体积;故填:便于直接读出氧气的体积;
(2)高锰酸钾粉末溶于冷凝水后形成高锰酸钾溶液,高锰酸钾溶液是紫红色的,所以实验中,试管口内壁附着紫红色小液滴,故填:高锰酸钾粉末溶于冷凝水后形成溶液;
(3)A.试管中高锰酸钾没有完全分解不会造成m1-m2≠ρV,不合题意;
B.导管口连续均匀冒气泡时才收集气体导致部分氧气没有收集起来,会造成m1-m2≠ρV,符合题意;
C.未调节量筒内外液面相平就读数会造成氧气的体积读数不准确,造成m1-m2≠ρV,符合题意;
D.停止加热时,先将导管移出水面,再熄灭酒精灯造成继续加热过程中生成的氧气逸散到空气中,没有收集在量筒内,会造成m1-m2≠ρV,符合题意;
故选BCD。
一、选择题:
1、(2020?黑龙江)漂白粉可用于自来水的杀菌消毒,其有效成分是次氯酸钙[化学式为Ca(ClO)2].次氯酸钙可发生如下反应:Ca(ClO)2+X+H2O═CaCO3↓+2HClO,则X的化学式为( )
A.Cl2 B.CO2 C.CaCl2 D.O2
2、(2020?沈阳)氮化硅是一种性能优异的无机非金属材料,可通过以下反应来制备:3SiO2+6C+2XSi3N4+6CO,此化学方程式中X的化学式是( )
A.N2 B.Si C.NO D.CO2
3、(2020?恩施州)下列选项中,不利于培养化学学科核心素养的是( )
A.变化与守恒:某物质R燃烧后生成CO2和H2O,则R中一定含C、H元素,可能含O元素
B.模型与推理:氧化物一定含有氧元素,但含有氧元素的化合物不一定是氧化物
C.宏观与微观:品红在水中扩散,说明分子总在不停地运动
D.探究与创新:探究红砖粉是否为过氧化氢分解的催化剂,只需设计实验证明红砖粉能否改变反应速率即可
4、(2020?东莞市)化学方程式2Mg+O22MgO可读作( )
A.镁加氧气等于氧化镁
B.2个镁加1个氧气等于2个氯化镁
C.镁和氧气在点燃条件下生成氧化镁
D.镁加氧气点燃等于氧化镁
5、(2020?徐州)下列关于有机物的叙述中正确的是( )
A.甲醇(CH4O)中氧元素的质量分数最大
B.葡萄糖(C6H12O6)中C、H、O的质量比为1:2:1
C.醋酸(C2H4O2)由2个碳元素,4个氢元素、2个氧元素组成
D.某有机物在O2中完全燃烧只生成CO2和H2O,则该物质只含碳、氢元素
6、(2020?怀化)将甲、乙、丙、丁四种物质置于一个完全密闭的容器中,在一定条件下反应,已知反应前后各物质的质量如下:
物质 甲 乙 丙 丁
反应前的质量/g 30 10 5 5
反应后的质量/g 2 4 m 39
下列有关说法正确的是( )
A.m=0
B.发生反应的甲、乙质量比为3:1
C.该反应是化合反应
D.丙一定作催化剂
7、(2020?昆明)在一个密闭容器中,有a、b、c、d四种物质,反应前各物质的质量关系如图刻度纸所示(例如:d的质量为2g)。在一定条件下发生反应,反应结束后,再次测得各物质的质量变化,并通过刻度的移动来表示,且记录在同一张刻度纸上:刻度线Ⅰ向右移动9格;刻度线Ⅱ向左移动8格;刻度线Ⅲ向左移动8格。下列说法正确的是( )
A.反应结束后c的质量为14g
B.该反应可能为置换反应
C.a、b变化的质量比一定为9:17
D.a、d的相对分子质量之比一定为9:8
8、(2020?绥化)铜能与硝酸反应,但不产生H2.根据反应方程式:3Cu+8HNO3(稀)═3Cu(NO3)2+2X↑+4H2O,推测X的化学式是( )
A.NO B.N2O3 C.NO2 D.N2O
9、(2020?株洲)在一个密闭容器中放入P、Q、R、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表。则关于此反应的认识正确的是( )
物质 P Q R W
反应前的质量(g) 5 2 14 18
反应后的质量(g) 20 x 4 13
A.参加化学反应的P和W的质量比为3:2
B.该反应用化学方程式表示为:3P+Q=2R+W
C.反应后容器中R与Q的质量比为1:2
D.Q在反应中可能作催化剂
10、(2020?宜昌)某密闭容器中只有乙、丙、丁三种物质,在一定条件下发生了一个化学反应,容器中乙、丙、丁的质量随甲的质量变化情况如图所示。下列说法错误的是( )
A.a的值为12
B.丁属于化合物
C.当丁为5g时,容器中乙的质量为11g
D.当甲为2g时,容器中丙与丁的质量之比为12:5
11、(2020?随州)在一个密闭容器中放入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如表,下列关于此反应的认识,正确的是( )
物??质 甲 乙 丙 丁
反应前的质量(g) 9 X 7 6
反应后的质量(g) 1 2 29 24
A.x的数值为32
B.若甲为化合物,乙为单质,则该反应一定为置换反应
C.该反应中丙和丁的质量变化之比为11:9
D.若丁为水,则甲或乙必定为酸或碱
12、(2020?青海)氢气与四氯化硅反应制取硅的化学方程式为:2H2+SiCl4Si+4X,其中X的化学式是( )
A.Cl2 B.H2O C.HCl D.SiH4
13、(2020?扬州)潜艇供氧的一种反应原理为2X+2CO2═2Na2CO3+O2,其中X的化学式是( )
A.Na B.Na2O C.Na2O2 D.NaOH
14、(2020?郴州)一定质量的某化合物完全燃烧,需要3.2g氧气,生成4.4g二氧化碳和1.8g水。下列判断错误的是( )
A.该化合物的质量为3.0g
B.该化合物一定含有碳、氢、氧三种元素
C.该化合物中碳、氢、氧的原子个数比为2:4:1
D.该化合物中碳元素的质量分数是40%
15、(2020?湘西州)煤中含有少量的硫元素,在煤中加入X可有效防止煤燃烧时生成的SO2对大气造成污染,发生反应的化学方程式是2X+2SO2+O2═2CaSO4+2CO2,则X的化学式是( )
A.CaO B.Na2CO3?? C.Ca(HCO3)2? D.CaCO3
16、(2020?黄冈)将69g酒精(C2H5OH)点燃,酒精燃烧全部变为CO、CO2和H2O,恢复到室温,测得所得气体中氧元素质量分数为64%,则燃烧所耗氧气的质量为( )
A.136g B.64g C.112g D.48g
17、(2020?凉山州)某物质1.6克在空气中充分燃烧共生成4.4克二氧化碳和3.6克水。则下列说法正确的是( )
①该物质中一定含有氧元素;
②该物质中一定不含氧元素;
③该物质中一定含有碳、氢元素;
④该物质的一个分子中碳、氢原子的个数比为1:4;
⑤该物质中氢元素的质量分数最大。
A.①②③④⑤ B.②③④ C.③④⑤ D.②③④⑤
18、(2020?抚顺)在实验室和化工生产中常用到硝酸。硝酸是一种强氧化剂,能与碳发生氧化还原反应,化学方程式为4HNO3+C═2H2O+4X↑+CO2↑.则X是( )
A.NO2 B.CO C.NO D.N2O5
19、(2020?邵阳)已知某纯净物4.6g在足量的氧气中充分燃烧后,生成8.8g二氧化碳和5.4g水。下列关于该纯净物组成的说法正确的是( )
A.只含有碳、氢元素
B.一定含有碳、氢、氧三种元素
C.一定含有碳、氢元素,可能含有氧元素
D.一定含有碳元素,可能含有氢、氧元素
20、(2020?天津)现将20g A和足量B在一定条件下充分反应,生成16g C和11g D,则参加反应的A和B的质量比是( )
A.20:11 B.20:7 C.5:4 D.16:11
21、(2020?湘潭)为及时发现燃气泄漏,常在燃气中加入微量具有难闻气味的乙硫醇(C2H5SH),乙碳醇燃烧的化学方程式为:2C2H5SH+9O24CO2+2X+6H2O,其中X的化学式为( )
A.SO2 B.H2S C.CO D.H2
22、(2020?盐城)将一定质量的甲醇(CH3OH)和氧气(O2)置于密闭容器中点燃,一段时间后反应停止,冷却、测得反应后各物质的质量,相关数据如下表所示。下列说法不符合事实的是( )
物质 CH3OH O2 H2O CO2 X
反应前质量/g m 12.8 0 0 0
反应后质量/g 0 0 10.8 8.8 n
A.m>n
B.X中一定含有碳元素
C.无法判断X中是否含有氧元素
D.生成物中C、H两种元素的质量比为3:1
23、(2020?齐齐哈尔)学校防控新冠肺炎所用消毒液成分之一是次氯酸钠,以下反应可生成次氯酸钠,Cl2+2NaOH═NaCl+X+H2O,其中X的化学式为( )
A.NaClO B.Na2O C.NaOH D.NaClO3
24、(2020?衡阳)“84消毒液”可用于新冠状病毒肺炎的防疫,制备其主要成分次氯酸钠(NaClO)的化学方程式为:2NaOH+Cl2═NaClO+NaCl+X.则X的化学式是( )
A.ClO2 B.H2 C.H2O D.Na2O
25、(2020?乐山)将20g镁、铁的金属混合物加入到一定质量的稀硫酸中,恰好完全反应后,经测定溶液质量增加了19g,将反应后的溶液蒸干,得到固体的质量为( )
A.39g B.60g C.68g D.73g
26、(2020?河南)氯碱工业是以电解食盐水为基础的基本化学工业,电解食盐水不可能生成的是( )
A.H2 B.Cl2 C.NaOH D.NaNO3
27、工业上可以将一氧化碳转化为甲烷,反应的微观示意图如图,下列说法不正确的是( )
A.丁的相对分子质量为18
B.丙中碳、氢原子个数比为1:4
C.28g甲完全反应至少需要2g乙
D.反应前后原子种类不变
28、(2020?湘潭)某固体由镁、锌、铁三种金属中的一种或几种组成,现取ag固体于烧杯中,再加入足量稀盐酸,充分反应后,将所得溶液小心蒸干(不考虑操作过程中物质的损耗),得到(a+14.2)g不含结晶水的固体,则a的取值范围是( )
A.4.8≤a≤13.0 B.11.2<a≤13.0
C.3.6≤a≤11.2 D.4.8≤a<11.2
二、填空题:
1、(2020海南)2020年5月5日,长征五号B运载火箭在海南文昌成功发射,该火箭采用无毒无污染的液氧、液氢和煤油作为推进剂,正式拉开我国载人航天工程“第三步”任务的序幕。
(1)液氢属于 (填“单质”、“氧化物”或“混合物”);
(2)火箭用到了钛合金。工业制钛的一个反应为:TiF4+2H2SO44HF+2X+TiO2,X的化学式为 ,TiO2中Ti的化合价为
2、(2020毕节市)在距地面10~50km的高空有一层臭氧(O3),它能吸收大部分紫外线,保护地球生物。臭氧与氧气在一定条件下能相互转化,在此过程中改变的是 (填选项序号)。
a.总质量 b.原子数 c.分子数
3、(2020?衢州)利用加热高锰酸钾的方法,验证化学反应中质量守恒定律。如图,小科将适量高锰酸钾装入试管,塞入一团棉花并测出试管、棉花与药品的总质量为m1.加热使之充分反应后,测得量筒中气体体积为V,再次测得反应装置与物质总质量为m2,已知常温常压下氧气密度为ρ.据此请回答:
(1)实验中用量筒收集气体的好处是
(2)实验中,试管口内壁附着紫红色小液滴,请解释产生该现象的原因
(3)根据实验数据计算发现:m1-m2≠ρV,与质量守恒定律不符。造成这一实验结果的原因分析正确的是
A、试管中高锰酸钾没有完全分解
B、导管口连续均匀冒气泡时才收集气体
C、未调节量筒内外液面相平就读数
D、停止加热时,先将导管移出水面,再熄灭酒精灯
参考答案
一、选择题:
1 2 3 4 5 6 7 8 9 10
B A D C A C C A D D
11 12 13 14 15 16 17 18 19 20
C C C C D C B A B B
21 22 23 24 25 26 27 28
A C A C C D C A
二、填空题:
1、答案为:
(1)单质;
(2)SO3;+4。
2、答案为:
c。
3、解:(1)实验中用量筒收集气体的好处是便于直接读出氧气的体积;故填:便于直接读出氧气的体积;
(2)高锰酸钾粉末溶于冷凝水后形成高锰酸钾溶液,高锰酸钾溶液是紫红色的,所以实验中,试管口内壁附着紫红色小液滴,故填:高锰酸钾粉末溶于冷凝水后形成溶液;
(3)A.试管中高锰酸钾没有完全分解不会造成m1-m2≠ρV,不合题意;
B.导管口连续均匀冒气泡时才收集气体导致部分氧气没有收集起来,会造成m1-m2≠ρV,符合题意;
C.未调节量筒内外液面相平就读数会造成氧气的体积读数不准确,造成m1-m2≠ρV,符合题意;
D.停止加热时,先将导管移出水面,再熄灭酒精灯造成继续加热过程中生成的氧气逸散到空气中,没有收集在量筒内,会造成m1-m2≠ρV,符合题意;
故选BCD。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
