物质的分类学案及过关检测
图片预览


文档简介
第一节 物质的分类(1)
学习目标】1.了解分类的方法:交叉分类法和树状分类法。
2.学会对常见的化学物质进行分类。
学习重点】化合物的分类
【基础知识】
分类是把____________________物体归类到一起的方法。
对于若干种同样的物质,若分类的依据不同,则得到的分类结果_______________。
运用分类的方法不仅能使有关化学物质及其变化的知识_________,还可以分门别类的研究,发现物质变化的规律。
4、分类方法有_________________和__________________。
[课堂练习1]
把以下物质分类
H2,CaO,Ba(OH)2, Fe2O3,Al,浑浊的河水,CH3CH2OH,NH3·H2O,Ar,NaHSO4,Cu(OH)2,HCl,HNO3,H2SO4,CO2,H3PO4,NaOH, CuSO4,Cu2(OH)2CO3,NaHCO3,空气,盐酸,CO,CH4,H2CO3,MgCl2,MgSO4
(1)属于单质的是:________________________________________________;
(2)属于金属单质的是:__________________________________________;
(3)属于非金属单质的是:__________________________________________;
(4)属于稀有气体的是:___________________________________________________;
(5)属于有机化合物的是:_________________________________________________;
(6)属于氧化物:_________________________________________________________;
(7)属于酸:_____________________________________________________________;
(8)属于碱:_____________________________________________________________;
(9)属于盐:_____________________________________________________________;
(10)属于混合物:_________________________________________________________
化合物分为氧化物,酸,碱,盐:
氧化物分为酸性氧化物和碱性氧化物等。
酸:___________________________________________________________
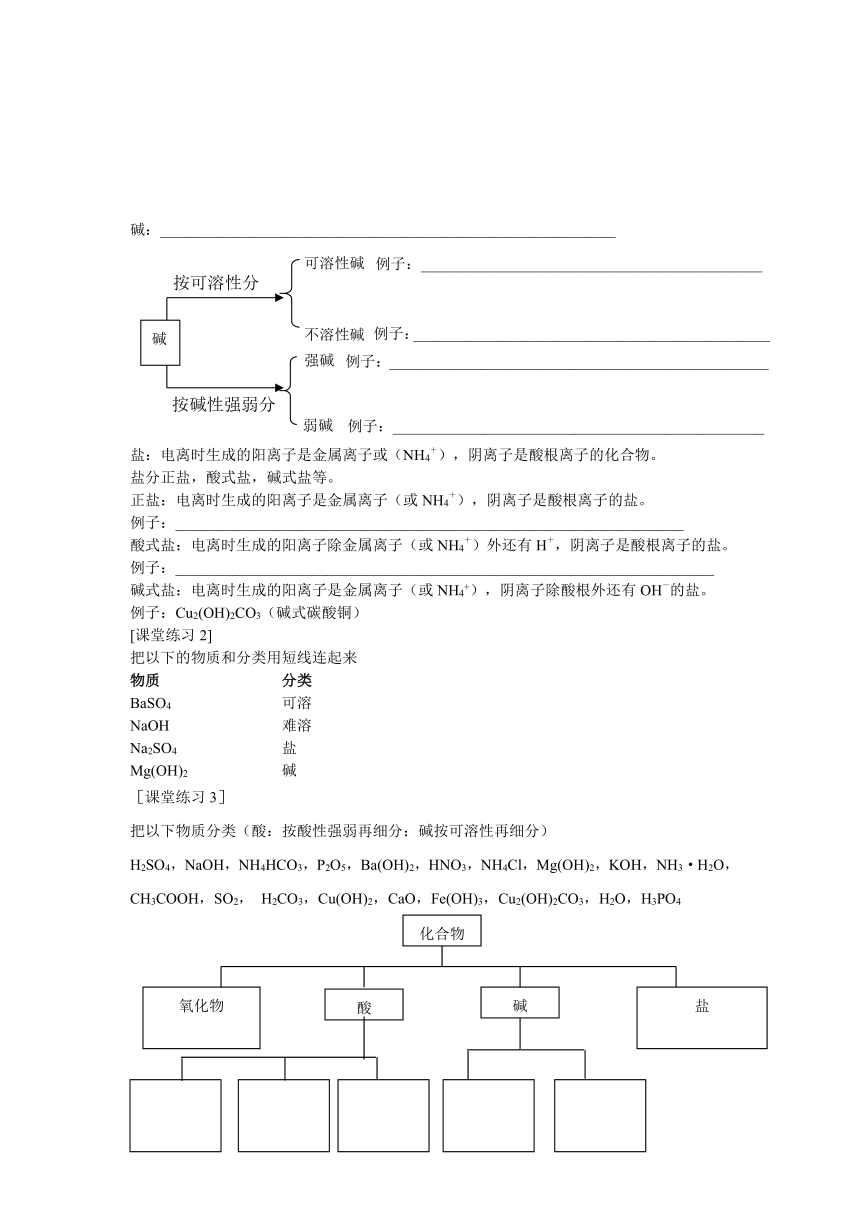
碱:____________________________________________________________
盐:电离时生成的阳离子是金属离子或(NH4+),阴离子是酸根离子的化合物。
盐分正盐,酸式盐,碱式盐等。
正盐:电离时生成的阳离子是金属离子(或NH4+),阴离子是酸根离子的盐。
例子:___________________________________________________________________
酸式盐:电离时生成的阳离子除金属离子(或NH4+)外还有H+,阴离子是酸根离子的盐。
例子:_______________________________________________________________________
碱式盐:电离时生成的阳离子是金属离子(或NH4+),阴离子除酸根外还有OH-的盐。
例子:Cu2(OH)2CO3(碱式碳酸铜)
[课堂练习2]
把以下的物质和分类用短线连起来
物质 分类
BaSO4 可溶
NaOH 难溶
Na2SO4 盐
Mg(OH)2 碱
[课堂练习3]
把以下物质分类(酸:按酸性强弱再细分;碱按可溶性再细分)
H2SO4,NaOH,NH4HCO3,P2O5,Ba(OH)2,HNO3,NH4Cl,Mg(OH)2,KOH,NH3·H2O,CH3COOH,SO2, H2CO3,Cu(OH)2,CaO,Fe(OH)3,Cu2(OH)2CO3,H2O,H3PO4
【过关训练】
1、分类法是一种行之有效,简单易行的科学方法,人们在认识事物时可以采取多种分类方法,下列关于“Na2CO3”的分类不正确的是 A、化合物 B、氧化物 C、碳酸盐 D、钠盐
2、下列物质中都含有氢元素,按照已学知识判断其中属于酸的是
A、NH3 B、CH4 C、NaHCO3 D、HClO3
3、下列各物质中,均为纯净物的一组是: ( )
A、碘酒,干冰 B、石油,液氨
C、Na2CO3·10H2O,Na2CO3 D、石灰石,氨水
4、下列物质中,前一种是化合物,后一种是混合物的是 ( )
A、氧化钙,洁净的雨水
B、氢氧化钾,含铜80%的氧化铜 (Cu相对原子质量64)
C、澄清的石灰水,粗盐
D、红磷,空气
5、将下列各组物质按酸、碱、盐分类顺序排列,正确的是 ( )
A、硫酸、纯碱、石膏 B、氢硫酸、烧碱、绿矾
C、碳酸、乙醇、醋酸钠 D、磷酸、熟石灰、苛性钾
6、物质分类的正确组合是 ( )
碱 酸 盐 酸性氧化物
A 纯碱 盐酸 烧碱 二氧化硫
B 烧碱 硫酸 食盐 一氧化碳
C 苛性钠 醋酸 石灰石 水
D 苛性钾 碳酸 苏打 三氧化硫
7、现有下列物质:①Na2CO3 ②Na2O ③SiO2 ④铁 ⑤O2 ⑥Ca(OH)2
⑦H2SO4 ⑧海水 ⑨新鲜的空气 ⑩Ba(OH)2 NaBr Fe3O4 H2O AgNO3
请将上述物质按下列要求分类,并将其序号填入空白处:
(1)按组成分类,属于混合物的是________________,属于单质的是_________________,属于氧化物的是______________,属于酸的是_________________,属于碱的是__________________,属于盐的是________________。
(2)按溶解性分类,属于易溶物的是______________,属于难溶物的是________________属于微溶物的是___________。
(3)按常温状态分类,属于固态的是____________,属于液态的是_____________,属于气态的是_________。
8、按照物质的树状分类和交叉分类,HNO3属于 ( )
①酸 ②氢化物 ③氧化物 ④含氧酸 ⑤难挥发性酸
⑥强氧化性酸 ⑦一元酸 ⑧化合物 ⑨混合物
A、①②③④⑤⑥⑦⑧ B、①④⑥⑦⑧ C、①⑨ D、①④⑤⑥⑦
9、以下哪一个化合物是正盐 ( )
A.KHSO4 B.Cu2(OH)2CO3 C.Ca(H2PO4)2 D.NH4NO3
10、科学家在研究化学物质时,常常对物质进行分类,以便对同类物质的组成和性能进行深入的研究.下列各组物质中有一种物质与其它物质不属于同一类,请将其挑出来,并说明理由。
物质组 不属于同一类的物质 理由
(1)Mg、O2、N2、NO
(2)NaOH、Na2CO3、CH4、KCl
(3)H2CO3、H2SO4、NH3·H2O、H2SiO3
(4)CaO、SO2、CO2、SiO2
物质的分类(2)
[学习目标]
知道胶体是一种常见的分散系,了解丁达尔效应。
了解胶体和分散系的概念,了解胶体和其他分散系的区别。
[学习重点]分散系的概念,区分溶液和胶体的方法
[基础知识]
分散系是________________________________________________________
前者属于被分散的物质,叫___________;后者起容纳分散质的作用,叫_____________。
问题一:分别指出CuSO4溶液和碘酒中的分散质和分散剂。
________________________________________________________________________
按分散质或分散剂的聚集状态(气态、液态、固态)来分,有9种组合方式。
分散质 分散剂 实例
气 气 空气
液 气 云、雾
固 气 烟灰尘
气 液 泡沫
液 液 牛奶、酒精的水溶液
固 液 油漆
气 固 泡沫塑料
液 固 珍珠(包藏着水的碳酸钙)
固 固 有色玻璃、合金
3、根据分散质___________不同,可将分散系分为________、_______和_______三大类。
4、胶体的制备及性质:A.Fe(OH)3胶体的制备
【问题】现在有FeCl3饱和溶液,问如何制备Fe(OH)3胶体?
实验:将一定量的FeCl3饱和溶液加入NaOH溶液,得到______________________。
【对比实验】
实验过程 冷水中滴加FeCl3饱和溶液 沸水中滴加FeCl3饱和溶液
现象
结论
B.胶体的性质
(1)比较溶液、浊液和胶体,通过观察胶体的外观,说明胶体_____________、_____________。(2)胶体微粒________通过滤纸
【实验】CuSO4,Fe(OH)3胶体,泥水能否透过滤纸
物质 CuSO4溶液 Fe(OH)3胶体 泥水
实验过程 把三种物质分别倒入放了滤纸的漏斗中
现象
结论
问题二:能否用过滤的方法分离胶体
___________________________________________________________________________
(3)丁达尔效应:
【实验】
物质 CuSO4 溶液 Fe(OH)3胶体 泥水
实验过程 分别将盛有以上两种物质的烧杯置于较暗的环境中,用电筒照射,观察现象。
现象
结论
问题三:溶液,浊液是否会发生丁达尔效应?这一性质有什么用途?
___________________________________________________________________________
【小结】溶液、胶体和浊液的比较
物质 溶液 胶体 浊液
分散质粒子直径大小
分散质粒子能否透过滤纸
稳定性
稳定性顺序
均一性
能否发生丁达尔效应
实例
【思考题】溶液、胶体和浊液这三种分散系的根本区别是 ( )
A、是否能发生丁达尔效应 B、分散质微粒直径的大小
C、能否透过滤纸 D、是否均一、较稳定、透明
[过关训练]
A组
1. 下列分散系中最稳定的是
A. 悬浊液 B. 乳液 C. 胶体 D. 溶液
2.下列关于胶体的说法中,正确的是
A. 胶体都是不透明的 B. 胶体不能通过滤纸
C. 胶体能够发生丁达尔效应 D. 胶体不稳定,静置后容易产生沉淀
3.能够将溶液和胶体区分开的方法是 ( )
A. 过滤 B.观察颜色、状态 C. 利用丁达尔效应 D. 闻气味
4.下列分散系能产生丁达尔效应的是
A. 食盐水 B. 酒精溶液 C. 淀粉溶液 D. Fe(OH)3胶体
5.FeCl3溶液与Fe(OH)3胶体共同具备的性质是
A. 分散质的粒子都可以通过滤纸 B. 都比较稳定,密封一段时间也不会产生沉淀
C. 都产生丁达尔效应 D. 加入盐酸先产生沉淀,然后沉淀溶解
6.“纳米材料”是粒子直径为1~ 100nm的材料,纳米碳就是其中的一种,若将纳米碳均匀地分散到蒸馏水中,所形成的物质 ( )
①是溶液 ②是胶体 ③能产生丁达尔效应 ④能透过滤纸 ⑤不能透过滤纸 ⑥静置后,会析出黑色沉淀
A. ①④⑥ B. ②③④ C. ②③⑤ D. ①③④⑥
7、今有下列各种物质:A.碘酒 B.豆浆 C.泥水 D.Fe(OH)3胶体 E.淀粉溶液 F.氨水 G..盐水,
按要求填写物质的代号:
(1)属于溶液的是________________________。
(2)属于浊液的是________________________。
(3)具有丁达尔效应的是__________________________。
(4)属于介稳体系的是____________________________。
(5)均一、稳定的混合物是_____________________________。
氧化物
酸性氧化物
例子:________________________________________________________
碱性氧化物
例子:________________________________________________________
其他
例子:CO,Al2O3
二元酸
例子:______________________________________
三元酸
例子:______________________________________
一元酸
例子:______________________________________
酸
按酸性强弱分
按所含H+个数分
弱酸
例子:______________________________________
强酸
例子:______________________________________
中强酸
例子:______________________________________
按可溶性分
强碱
弱碱
碱
例子:_________________________________________________
可溶性碱
不溶性碱
例子:_____________________________________________
例子:__________________________________________________
例子:_______________________________________________
按碱性强弱分
化合物
氧化物
酸
碱
盐
学习目标】1.了解分类的方法:交叉分类法和树状分类法。
2.学会对常见的化学物质进行分类。
学习重点】化合物的分类
【基础知识】
分类是把____________________物体归类到一起的方法。
对于若干种同样的物质,若分类的依据不同,则得到的分类结果_______________。
运用分类的方法不仅能使有关化学物质及其变化的知识_________,还可以分门别类的研究,发现物质变化的规律。
4、分类方法有_________________和__________________。
[课堂练习1]
把以下物质分类
H2,CaO,Ba(OH)2, Fe2O3,Al,浑浊的河水,CH3CH2OH,NH3·H2O,Ar,NaHSO4,Cu(OH)2,HCl,HNO3,H2SO4,CO2,H3PO4,NaOH, CuSO4,Cu2(OH)2CO3,NaHCO3,空气,盐酸,CO,CH4,H2CO3,MgCl2,MgSO4
(1)属于单质的是:________________________________________________;
(2)属于金属单质的是:__________________________________________;
(3)属于非金属单质的是:__________________________________________;
(4)属于稀有气体的是:___________________________________________________;
(5)属于有机化合物的是:_________________________________________________;
(6)属于氧化物:_________________________________________________________;
(7)属于酸:_____________________________________________________________;
(8)属于碱:_____________________________________________________________;
(9)属于盐:_____________________________________________________________;
(10)属于混合物:_________________________________________________________
化合物分为氧化物,酸,碱,盐:
氧化物分为酸性氧化物和碱性氧化物等。
酸:___________________________________________________________
碱:____________________________________________________________
盐:电离时生成的阳离子是金属离子或(NH4+),阴离子是酸根离子的化合物。
盐分正盐,酸式盐,碱式盐等。
正盐:电离时生成的阳离子是金属离子(或NH4+),阴离子是酸根离子的盐。
例子:___________________________________________________________________
酸式盐:电离时生成的阳离子除金属离子(或NH4+)外还有H+,阴离子是酸根离子的盐。
例子:_______________________________________________________________________
碱式盐:电离时生成的阳离子是金属离子(或NH4+),阴离子除酸根外还有OH-的盐。
例子:Cu2(OH)2CO3(碱式碳酸铜)
[课堂练习2]
把以下的物质和分类用短线连起来
物质 分类
BaSO4 可溶
NaOH 难溶
Na2SO4 盐
Mg(OH)2 碱
[课堂练习3]
把以下物质分类(酸:按酸性强弱再细分;碱按可溶性再细分)
H2SO4,NaOH,NH4HCO3,P2O5,Ba(OH)2,HNO3,NH4Cl,Mg(OH)2,KOH,NH3·H2O,CH3COOH,SO2, H2CO3,Cu(OH)2,CaO,Fe(OH)3,Cu2(OH)2CO3,H2O,H3PO4
【过关训练】
1、分类法是一种行之有效,简单易行的科学方法,人们在认识事物时可以采取多种分类方法,下列关于“Na2CO3”的分类不正确的是 A、化合物 B、氧化物 C、碳酸盐 D、钠盐
2、下列物质中都含有氢元素,按照已学知识判断其中属于酸的是
A、NH3 B、CH4 C、NaHCO3 D、HClO3
3、下列各物质中,均为纯净物的一组是: ( )
A、碘酒,干冰 B、石油,液氨
C、Na2CO3·10H2O,Na2CO3 D、石灰石,氨水
4、下列物质中,前一种是化合物,后一种是混合物的是 ( )
A、氧化钙,洁净的雨水
B、氢氧化钾,含铜80%的氧化铜 (Cu相对原子质量64)
C、澄清的石灰水,粗盐
D、红磷,空气
5、将下列各组物质按酸、碱、盐分类顺序排列,正确的是 ( )
A、硫酸、纯碱、石膏 B、氢硫酸、烧碱、绿矾
C、碳酸、乙醇、醋酸钠 D、磷酸、熟石灰、苛性钾
6、物质分类的正确组合是 ( )
碱 酸 盐 酸性氧化物
A 纯碱 盐酸 烧碱 二氧化硫
B 烧碱 硫酸 食盐 一氧化碳
C 苛性钠 醋酸 石灰石 水
D 苛性钾 碳酸 苏打 三氧化硫
7、现有下列物质:①Na2CO3 ②Na2O ③SiO2 ④铁 ⑤O2 ⑥Ca(OH)2
⑦H2SO4 ⑧海水 ⑨新鲜的空气 ⑩Ba(OH)2 NaBr Fe3O4 H2O AgNO3
请将上述物质按下列要求分类,并将其序号填入空白处:
(1)按组成分类,属于混合物的是________________,属于单质的是_________________,属于氧化物的是______________,属于酸的是_________________,属于碱的是__________________,属于盐的是________________。
(2)按溶解性分类,属于易溶物的是______________,属于难溶物的是________________属于微溶物的是___________。
(3)按常温状态分类,属于固态的是____________,属于液态的是_____________,属于气态的是_________。
8、按照物质的树状分类和交叉分类,HNO3属于 ( )
①酸 ②氢化物 ③氧化物 ④含氧酸 ⑤难挥发性酸
⑥强氧化性酸 ⑦一元酸 ⑧化合物 ⑨混合物
A、①②③④⑤⑥⑦⑧ B、①④⑥⑦⑧ C、①⑨ D、①④⑤⑥⑦
9、以下哪一个化合物是正盐 ( )
A.KHSO4 B.Cu2(OH)2CO3 C.Ca(H2PO4)2 D.NH4NO3
10、科学家在研究化学物质时,常常对物质进行分类,以便对同类物质的组成和性能进行深入的研究.下列各组物质中有一种物质与其它物质不属于同一类,请将其挑出来,并说明理由。
物质组 不属于同一类的物质 理由
(1)Mg、O2、N2、NO
(2)NaOH、Na2CO3、CH4、KCl
(3)H2CO3、H2SO4、NH3·H2O、H2SiO3
(4)CaO、SO2、CO2、SiO2
物质的分类(2)
[学习目标]
知道胶体是一种常见的分散系,了解丁达尔效应。
了解胶体和分散系的概念,了解胶体和其他分散系的区别。
[学习重点]分散系的概念,区分溶液和胶体的方法
[基础知识]
分散系是________________________________________________________
前者属于被分散的物质,叫___________;后者起容纳分散质的作用,叫_____________。
问题一:分别指出CuSO4溶液和碘酒中的分散质和分散剂。
________________________________________________________________________
按分散质或分散剂的聚集状态(气态、液态、固态)来分,有9种组合方式。
分散质 分散剂 实例
气 气 空气
液 气 云、雾
固 气 烟灰尘
气 液 泡沫
液 液 牛奶、酒精的水溶液
固 液 油漆
气 固 泡沫塑料
液 固 珍珠(包藏着水的碳酸钙)
固 固 有色玻璃、合金
3、根据分散质___________不同,可将分散系分为________、_______和_______三大类。
4、胶体的制备及性质:A.Fe(OH)3胶体的制备
【问题】现在有FeCl3饱和溶液,问如何制备Fe(OH)3胶体?
实验:将一定量的FeCl3饱和溶液加入NaOH溶液,得到______________________。
【对比实验】
实验过程 冷水中滴加FeCl3饱和溶液 沸水中滴加FeCl3饱和溶液
现象
结论
B.胶体的性质
(1)比较溶液、浊液和胶体,通过观察胶体的外观,说明胶体_____________、_____________。(2)胶体微粒________通过滤纸
【实验】CuSO4,Fe(OH)3胶体,泥水能否透过滤纸
物质 CuSO4溶液 Fe(OH)3胶体 泥水
实验过程 把三种物质分别倒入放了滤纸的漏斗中
现象
结论
问题二:能否用过滤的方法分离胶体
___________________________________________________________________________
(3)丁达尔效应:
【实验】
物质 CuSO4 溶液 Fe(OH)3胶体 泥水
实验过程 分别将盛有以上两种物质的烧杯置于较暗的环境中,用电筒照射,观察现象。
现象
结论
问题三:溶液,浊液是否会发生丁达尔效应?这一性质有什么用途?
___________________________________________________________________________
【小结】溶液、胶体和浊液的比较
物质 溶液 胶体 浊液
分散质粒子直径大小
分散质粒子能否透过滤纸
稳定性
稳定性顺序
均一性
能否发生丁达尔效应
实例
【思考题】溶液、胶体和浊液这三种分散系的根本区别是 ( )
A、是否能发生丁达尔效应 B、分散质微粒直径的大小
C、能否透过滤纸 D、是否均一、较稳定、透明
[过关训练]
A组
1. 下列分散系中最稳定的是
A. 悬浊液 B. 乳液 C. 胶体 D. 溶液
2.下列关于胶体的说法中,正确的是
A. 胶体都是不透明的 B. 胶体不能通过滤纸
C. 胶体能够发生丁达尔效应 D. 胶体不稳定,静置后容易产生沉淀
3.能够将溶液和胶体区分开的方法是 ( )
A. 过滤 B.观察颜色、状态 C. 利用丁达尔效应 D. 闻气味
4.下列分散系能产生丁达尔效应的是
A. 食盐水 B. 酒精溶液 C. 淀粉溶液 D. Fe(OH)3胶体
5.FeCl3溶液与Fe(OH)3胶体共同具备的性质是
A. 分散质的粒子都可以通过滤纸 B. 都比较稳定,密封一段时间也不会产生沉淀
C. 都产生丁达尔效应 D. 加入盐酸先产生沉淀,然后沉淀溶解
6.“纳米材料”是粒子直径为1~ 100nm的材料,纳米碳就是其中的一种,若将纳米碳均匀地分散到蒸馏水中,所形成的物质 ( )
①是溶液 ②是胶体 ③能产生丁达尔效应 ④能透过滤纸 ⑤不能透过滤纸 ⑥静置后,会析出黑色沉淀
A. ①④⑥ B. ②③④ C. ②③⑤ D. ①③④⑥
7、今有下列各种物质:A.碘酒 B.豆浆 C.泥水 D.Fe(OH)3胶体 E.淀粉溶液 F.氨水 G..盐水,
按要求填写物质的代号:
(1)属于溶液的是________________________。
(2)属于浊液的是________________________。
(3)具有丁达尔效应的是__________________________。
(4)属于介稳体系的是____________________________。
(5)均一、稳定的混合物是_____________________________。
氧化物
酸性氧化物
例子:________________________________________________________
碱性氧化物
例子:________________________________________________________
其他
例子:CO,Al2O3
二元酸
例子:______________________________________
三元酸
例子:______________________________________
一元酸
例子:______________________________________
酸
按酸性强弱分
按所含H+个数分
弱酸
例子:______________________________________
强酸
例子:______________________________________
中强酸
例子:______________________________________
按可溶性分
强碱
弱碱
碱
例子:_________________________________________________
可溶性碱
不溶性碱
例子:_____________________________________________
例子:__________________________________________________
例子:_______________________________________________
按碱性强弱分
化合物
氧化物
酸
碱
盐
