【8年级上册同步重难点集训】03 第一章 第4—5节溶液的性质与计算(含答案)
文档属性
| 名称 | 【8年级上册同步重难点集训】03 第一章 第4—5节溶液的性质与计算(含答案) |  | |
| 格式 | zip | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2020-10-11 09:51:43 | ||
图片预览

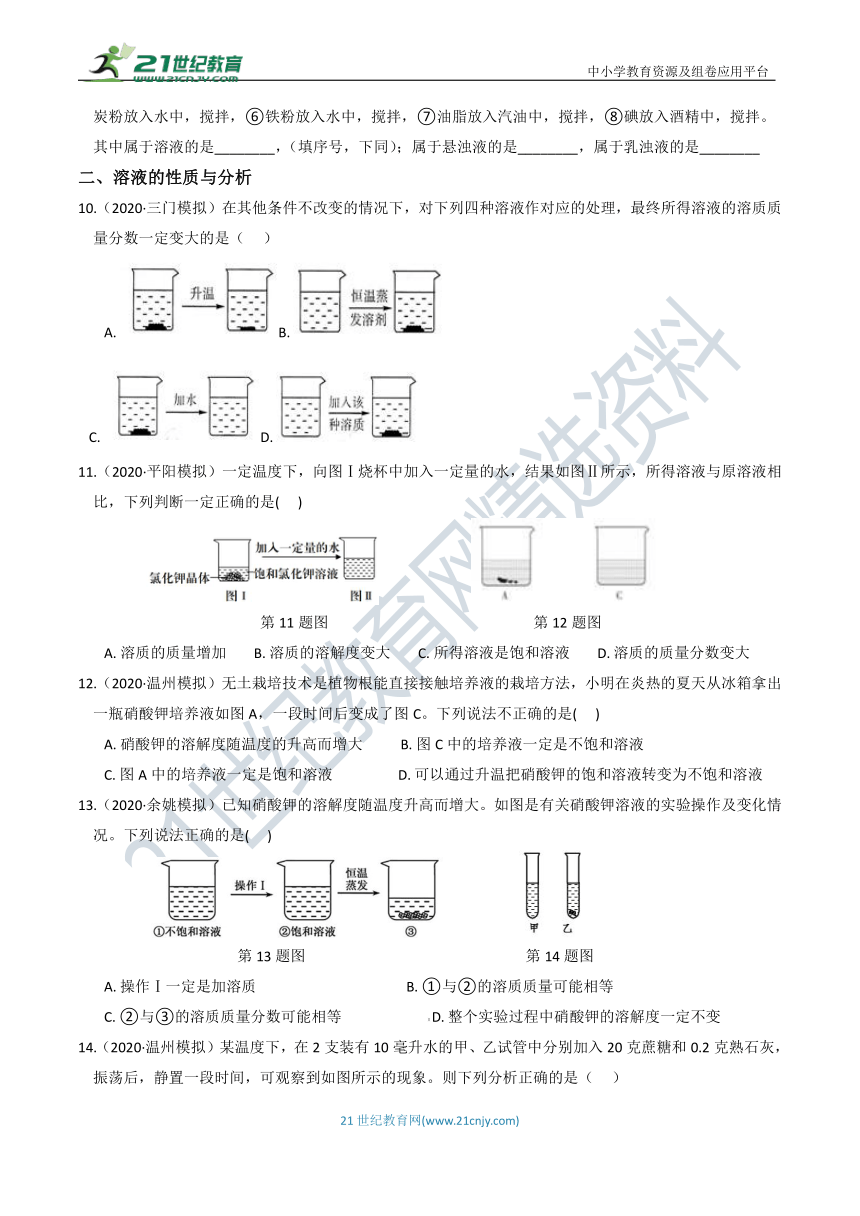


文档简介
中小学教育资源及组卷应用平台
【8年级上册同步重难点集训】03
第一章
第4—5节溶液的性质与计算
一、物质在水中的分散情况
1.(2020七下·余姚期末)下列物质属于溶液的是(???
)
A.?纯净水?????????????????????????????????B.?牛奶?????????????????????????????????C.?豆浆?????????????????????????????????D.?生理盐水
2.(2020七下·慈溪期中)衣服上沾有碘很难洗净,碘在下列四种不同溶剂中的溶解性如下表所示:
溶质
碘
溶剂
水
酒精
汽油
苯(有毒)
溶解性
微溶
可溶
易溶
易溶
由表中提供的信息判断,能最快洗净衣服上的碘污渍且对人体无害的是(???
)
A.?水???????????????????????????????????????B.?酒精???????????????????????????????????????C.?汽油???????????????????????????????????????D.?苯
3.(2020七下·慈溪期中)如图所示将一种物质加入另一种物质中,其中能得到乳浊液的是(???
)
A.????????????????????????B.????????????????????????C.????????????????????????D.?
4.(2019八上·柯桥月考)下列一些生活中常见的液体,属于溶液的是(
???)
A.?牛奶?????????????????????????????????????B.?碘酒?????????????????????????????????????C.?泥水?????????????????????????????????????D.?墨汁
5.(2019八上·浙江期中)下表是某同学的实验记录,以下说法不正确的是(????
)
溶质
碘
高锰酸钾
溶剂
水
汽油
酒精
水
汽油
溶解性
不溶
易溶
可溶
易溶
不溶
A.?衣服不慎沾上碘酒,可用汽油擦洗??????????????????????B.?溶液都是均一、稳定、无色的混合物
C.?水、汽油、酒精都可以做溶剂?????????????????????????????D.?同一物质在不同溶剂中溶解性不同
6.(2019八上·新昌期中)小明周六去郊游,出发前到超市买了下列4种饮品,其中属于溶液的是(???
)
A.?“永和”豆浆????????????B.?“娃哈哈”矿泉水????????????C.?“美汁源”果粒橙????????????D.?“伊利”纯牛奶
7.(2019八上·天台期中)给下列混合物归类:①食盐水,②牛奶,③色拉油和汽油混合后的液体,④肥皂水,⑤泥水,⑥色拉油和水混合后的液体;属于溶液的是________,属于乳浊液的是________,属于悬浊液的是________。
8.(2019八上·余杭期中)请你各举一个实例,说明下列有关溶液的叙述是错误的。
(1)溶液一定是无色的。实例:________溶液不是无色的。
(2)均一的、稳定的液体都是溶液。实例:________是均一的、稳定的液体,但不是溶液。
9.(2019八上·诸暨月考)下列物质:①冰水混合物,②食用油滴入水中,搅拌,③白酒,④钡餐⑤木炭粉放入水中,搅拌,⑥铁粉放入水中,搅拌,⑦油脂放入汽油中,搅拌,⑧碘放入酒精中,搅拌。其中属于溶液的是________,(填序号,下同);属于悬浊液的是________,属于乳浊液的是________
二、溶液的性质与分析
10.(2020·三门模拟)在其他条件不改变的情况下,对下列四种溶液作对应的处理,最终所得溶液的溶质质量分数一定变大的是(???
)
A.?B.?
C.?D.?
11.(2020·平阳模拟)一定温度下,向图Ⅰ烧杯中加入一定量的水,结果如图Ⅱ所示,所得溶液与原溶液相比,下列判断一定正确的是(???
)
第11题图
第12题图
A.?溶质的质量增加????????B.?溶质的溶解度变大????????C.?所得溶液是饱和溶液????????D.?溶质的质量分数变大
12.(2020·温州模拟)无土栽培技术是植物根能直接接触培养液的栽培方法,小明在炎热的夏天从冰箱拿出一瓶硝酸钾培养液如图A,一段时间后变成了图C。下列说法不正确的是(???
)
A.?硝酸钾的溶解度随温度的升高而增大???????????B.?图C中的培养液一定是不饱和溶液
C.?图A中的培养液一定是饱和溶液???????????????????D.?可以通过升温把硝酸钾的饱和溶液转变为不饱和溶液
13.(2020·余姚模拟)已知硝酸钾的溶解度随温度升高而增大。如图是有关硝酸钾溶液的实验操作及变化情况。下列说法正确的是(???
)
第13题图
第14题图
A.?操作Ⅰ一定是加溶质???????????????????????????????????????????B.?①与②的溶质质量可能相等
C.?②与③的溶质质量分数可能相等?????????????????????????D.?整个实验过程中硝酸钾的溶解度一定不变
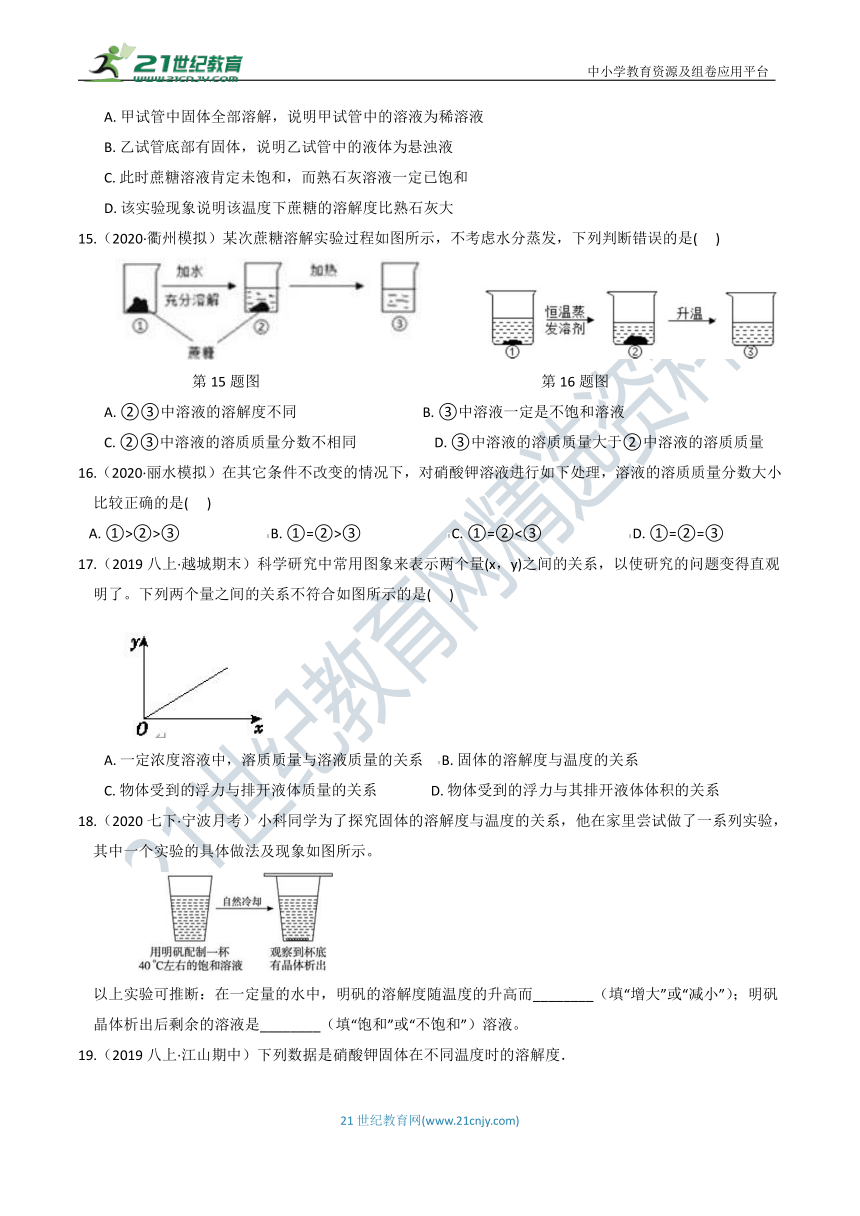
14.(2020·温州模拟)某温度下,在2支装有10毫升水的甲、乙试管中分别加入20克蔗糖和0.2克熟石灰,振荡后,静置一段时间,可观察到如图所示的现象。则下列分析正确的是(???
)
A.?甲试管中固体全部溶解,说明甲试管中的溶液为稀溶液
B.?乙试管底部有固体,说明乙试管中的液体为悬浊液
C.?此时蔗糖溶液肯定未饱和,而熟石灰溶液一定已饱和
D.?该实验现象说明该温度下蔗糖的溶解度比熟石灰大
15.(2020·衢州模拟)某次蔗糖溶解实验过程如图所示,不考虑水分蒸发,下列判断错误的是(???
)
第15题图
第16题图
A.?②③中溶液的溶解度不同????????????????????????????????????B.?③中溶液一定是不饱和溶液
C.?②③中溶液的溶质质量分数不相同??????????????????????D.?③中溶液的溶质质量大于②中溶液的溶质质量
16.(2020·丽水模拟)在其它条件不改变的情况下,对硝酸钾溶液进行如下处理,溶液的溶质质量分数大小比较正确的是(???
)
A.?①>②>③?????????????????????????B.?①=②>③?????????????????????????C.?①=②<③?????????????????????????D.?①=②=③
17.(2019八上·越城期末)科学研究中常用图象来表示两个量(x,y)之间的关系,以使研究的问题变得直观明了。下列两个量之间的关系不符合如图所示的是(?
??)
A.?一定浓度溶液中,溶质质量与溶液质量的关系????B.?固体的溶解度与温度的关系
C.?物体受到的浮力与排开液体质量的关系???????????????D.?物体受到的浮力与其排开液体体积的关系
18.(2020七下·宁波月考)小科同学为了探究固体的溶解度与温度的关系,他在家里尝试做了一系列实验,其中一个实验的具体做法及现象如图所示。
以上实验可推断:在一定量的水中,明矾的溶解度随温度的升高而________(填“增大”或“减小”);明矾晶体析出后剩余的溶液是________(填“饱和”或“不饱和”)溶液。
19.(2019八上·江山期中)下列数据是硝酸钾固体在不同温度时的溶解度.
(1)20℃时,向100g水中加入31.6g硝酸钾,充分溶解后得到________(填“饱和”或“不饱和”溶液。
(2)20℃时,向100g水中加入40g硝酸钾,若使硝酸钾完全溶解,可以采用的方法是________。
(3)如图所示,小烧杯中盛放的是上述(1)中所得硝酸钾溶液,若将少量的下列物质分别放入大烧杯中的水中,不断搅拌,则小烧杯中一定有硝酸钾晶体析出的是???????????(填字母)。
A.冰
B.氢氧化钠
C.硝酸按
D.干冰
20.(2019八上·义乌期中)配制一定质量的硝酸钾溶液,将一木块漂浮于50℃时的硝酸钾的饱和溶液中,(如图a所示)当温度改变时(不考虑由此引起的木块和溶液体积的变化),木块排开液体的体积V排随时间t发生了如图b所示的变化。
(1)由此推测出温度的改变是________?(填“升温”或“降温”)。
(2)同时观察到烧杯底部硝酸钾晶体________?(填“增多”或“减少”)。
(3)如果在配制硝酸钾溶液的过程中出现以下情况,可能造成对所配溶液的溶质质量分数的误差(填“偏高”、“偏低”、“无影响”):
①所用硝酸钾药品不纯________;
②量取水时仰视读数________;
③配制完后将溶液转移至试剂瓶时洒出了一些________。
21.(2017八上·杭州月考)为了探究影响固体溶解性的因素,某同学设计了如下三组实验:
因素
第一组
第二组
第三组
实验温度
20℃
20℃
20℃
20℃
80℃
加入溶剂种类
水
酒精
水
水
水
加入溶剂质量
20g
20g
10g
10g
10g
加入固体种类
硝酸钾
硝酸钾
硝酸钾
食盐
硝酸钾
加入固体质量
10g
10g
10g
10g
10g
溶解固体质量
6.2g
0g
3.1g
3.6g
10g
(1)分析上表,第一组实验研究的因素是________;
(2)由上述实验可知,影响固体溶解性的因素是________(填序号)
①温度
②加入溶剂种类
③加入溶剂质量
④加入固体种类
⑤加入固体质量
(3)在第二组实验中,该同学按照如下步骤进行实验(假设溶液损失不计)
①用电子天平称取
10.0g
硝酸钾,放入烧杯中;
②量取
10.0mL
水,倒入上述烧杯中,称量烧杯、硝酸钾和水的总质量为
m1g;
③搅拌至硝酸钾不再溶解为止;
④过滤,称量所得硝酸钾溶液和烧杯的总质量为
m2g;
⑤计算:m1-m2=______g(结合第二组实验数据进行分析)。
将溶质改为食盐,重复上述步骤进行实验。
由实验可知,20℃时食盐的溶解性________(填“>”“﹦”“<”)硝酸钾的溶解性。
(4)根据上述实验,以下推论正确的是
?????????????????????。
A.20℃时,氯化钠的溶解度为
36g/100g
水
B.20℃时,硝酸钾饱和溶液的溶质质量分数为
31%
C.第三组实验中的硝酸钾溶液为
80℃时的饱和溶液
D.20℃的任意一杯饱和硝酸钾溶液中,溶质与溶剂的质量比一定相等
三、定量计算与配置溶液
22.(2020·金东模拟)实验室用氯化钠配制50g质量分数为6%的氯化钠溶液,下列说法不正确的是(???
)
A.?所需氯化钠的质量为3g???????????????????????????????????????B.?氯化钠放在托盘天平的左盘称量
C.?俯视量筒读数会使所配溶液偏稀?????????????????????????D.?所需玻璃仪器有烧杯、玻璃棒、量筒等
23.(2020九下·宁波保送考试)某容器中装有盐水若干,老师让小科倒入质量分数1%的盐水100克以配成质量分数2%的盐水,但小科却错误的倒入100克水,老师发现后说你再将第三种盐水40克倒入水中就可得到2%的盐水了,那么第三种盐水的质量分数为(???
)
A.?2.5%??????????????????????????????????????B.?4.5%??????????????????????????????????????C.?5%??????????????????????????????????????D.?7%
温度(℃)
t0
t1
t2
硝酸钾溶解度/克
31.6
44
60
氯化铵溶解度/克
37.6
40
41
24.(2020八上·苍南期末)M是硝酸钾或氯化铵其中的一种,硝酸钾和氯化铵在不同温度(t0某科学兴趣小组用物质M进行了如图所示实验。下列说法不正确的是(???
)
A.?物质M是硝酸钾????????????????????????????????????????????????B.?溶液①为不饱和溶液,溶液②和③为饱和溶液
C.?溶液②中溶质质量分数为37.5%????????????????????????D.?溶液①②③中,溶质质量分数的关系是②>③>①
25.用溶质质量分数为98%、密度为1.84g/cm3的浓硫酸配制溶质质量分数为10%的稀硫酸100mL,计算时必须查阅的数据是________。配制过程中除了使用量筒、玻璃棒和胶头滴管外,还需要的一种玻璃仪器是________。
26.(2020·瑞安模拟)t1℃时,将质量均为35克的氯化钾和硝酸钾分别加入到各盛有100g水的两个烧杯中,充分搅拌后现象如图所示(t1℃时,硝酸钾的溶解度小于氯化钾的溶解度)。
(1)据图分析烧杯A中溶解的溶质为________;
(2)将t1℃时烧杯B中的溶液稀释成10%的溶液,需加水________克。
27.如图是配制50克质量分数为5%的氯化钠溶液的操作过程示意图
(1)B操作,在称量中发现指针偏向右边,接下来的操作是________;
(2)E操作中玻璃棒的作用是________。
(3)如果配制过程中出现以下情况,可能导致所配溶液的溶质质量分数偏大的是????
。
A.所用氯化钠药品不纯
B.量取水时俯视读数
C.配完后将溶液转移至试剂瓶时洒出了一些
D.将量好的水从量筒里倒入烧杯时,酒出一些水
28.(2019八上·嵊州月考)在一定温度下,向100g水中依次加入一定质量的氯化钾(即KCl)固体,充分溶解。加入氯化钾的质量与得到相应溶液质量的关系如图所示:
(1)该温度下氯化钾的溶解度为________克。
(2)实验①、②、③的溶液,溶质的质量分数分别为a、b、c,则它们的大小关系是________(用“>”“<”或“=”表示出来)。
29.(2019八上·嵊州月考)实验室配置质量分数为10%的食盐溶液。如图1是某同学的实验操作过程:
(1)玻璃棒a在④中所起的作用是________。
(2)若③中游码读数为1.2,则他称氯化钠的质量是________?g。
(3)该同学如果操作正确,则需要用水的体积是________?mL。(水的密度为1.0g/cm3)
(4)下列操作会导致溶液溶质质量分数偏小的是
?????。
A.搅拌溶解时有少量水溅出
B.量取水的体积时,如图2所示操作
C.所用的托盘天平游码生锈了
D.用4g食盐和100g水配制溶液
30.(2020八下·天台月考)实验室保存﹣瓶浓盐酸,瓶上的标签部分内容如图所示,请根据标签上的信息回答下列各问:
(1)这一瓶浓盐酸中溶质的质量是多少克?(结果精确到0.1)
(2)取200克此瓶内的浓盐酸可以稀释成1.85%的稀盐酸多少克?同时加水多少克?
31.(2019八上·柯桥月考)如图为某医用生理盐水注射液的标签中的部分内容。计算:
(1)该瓶盐水能给病人体内提供氯化钠的质量是多少?
(2)若用溶质质量分数为18%的氯化钠溶液配制该瓶生理盐水,需要18%的氯化钠溶液多少克?需蒸馏水多少毫升?(ρ水=1×103Kg/m3)
32.(2019八上·天台月考)氯化钠俗名食盐是工业生产和生活的一种重要原料,也是实验室里常见的一种药品。下表是20℃时,氯化钠溶解于水的实验数据,回答下列问题;
实验序号
水的质量(g)
加入氯化钠的质量(g)
溶液的质量(g)
①
10
2
12
②
10
3
13
③
10
4
13.6
④
10
5
m
(1)表中m=________;
(2)在这4次实验中,得到的是20℃氯化钠溶液属于饱和溶液的是________(填实验序号)
(3)计算第3次实验得到的氯化钠溶液的溶质质量分数。(写出过程)
(4)20℃时,实验室把100克溶质质量分数为20%的氯化钠溶液释成5%的氯化钠溶液,需加水多少毫升?(写出过程)
33.(2019八上·杭州期中)预防流感现在最有效的方法之一就是用消毒液对空气消毒。二氧化氯消毒液能够迅速彻底地杀灭各种细菌(大肠杆菌、白色念珠菌等)和病毒(肝炎病毒、流感病毒等)。某校决定放学后对全校教室、寝室全面消毒。小陈观察到瓶上的标签如下表所示。
二氧化氯消毒液(ClO2)1000毫升
溶质的质量分数
80%
密度
1.2
克/厘米
3
相对分子质量
67.5
强腐蚀性,阴冷、密封储藏
求:
(1)这1000毫升二氧化氯消毒液含溶质二氧化氯?
________?克。
(2)若将这1000毫升二氧化氯消毒液与5000克水均匀混合,所得稀二氧化氯消毒液中二氧化氯的质量分数是________。(保留1位小数)
(3)我校欲配制30千克质量分数为20%的稀二氧化氯消毒液用来消毒,需要多少千克这种二氧化氯消毒液和多少升水?(写出计算过程)
34.(2019八上·衢州期中)下表列出了硝酸钾与氯化钠在不同温度下的溶解度:
温度/℃
0
10
20
40
60
80
100
硝酸钾的溶解度/g
13.3
20.9
31.6
63.9
110
169
246
氯化钠的溶解度/g
35.7
35.8
36.0
36.6
37.3
38.4
39.8
(1)20℃时,在装有15g硝酸钾晶体的试管中,加入10g水并充分振荡,将所得溶液放入盛有热水的烧杯中,将溶液温度升至60℃,此时试管内的溶液中溶质与溶剂质量比为________。
(2)取25g氯化钠晶体加入70g水中,加热溶解。在100℃时蒸发掉
20g水,维持该温度过滤,得到的晶体质量为________g。
(3)现有硝酸钾和氯化钠晶体各40g,分别加到100g、80℃的水中充分溶解得到溶液A、B,其中________溶液为饱和溶液,若要使A、B两种溶液的溶质质量分数相等,则应将A、B两溶液的温度至少降至________的范围内。
35.(2019八上·衢州期中)下表为硫酸密度与硫酸溶液中的溶质的质量分数对照表(20℃)
密度(g/ml)
1.01
1.07
1.14
1.22
1.30
1.40
1.50
1.61
1.73
1.81
1.84
质量分数(%)
1
10
20
30
40
50
60
70
80
90
98
有一物块A,其体积为250cm3,密度为1.30g/cm3。一只容器中盛有某硫酸溶液5千克,将物块A放入该溶液中静止后如图所示,此时物块A有2/15的体积露出液面。
(1)求物块A静止时受到的浮力大小?
(2)求这种硫酸溶液的溶质质量分数是多少?
(3)要使物块A全部浸入溶液中,至少需要往容器中加水多少千克?(容器足够大,加水后溶液不溢出。)
答案解析部分
一、物质在水中的分散情况
1.【答案】
D
2.【答案】
C
3.【答案】
D
4.【答案】
B
5.【答案】
B
6.【答案】
B
7.【答案】
①③;②④⑥;⑤
8.【答案】
(1)高锰酸钾(2)蒸馏水
9.【答案】
③⑧⑦;④⑤⑥;②
二、溶液的性质与分析
10.【答案】
A
11.【答案】
A
12.【答案】
B
13.【答案】
B
14.【答案】
D
15.【答案】
B
16.【答案】
C
17.【答案】
B
18.【答案】
增大;饱和
19.【答案】
(1)饱和(2)升高温度或加水(3)A,C,D
20.【答案】
(1)降温(2)增多(3)偏低;偏低;无影响
21.【答案】
(1)溶剂种类(2)①②④(3)6.9;>(4)A,D
三、定量计算与配置溶液
22.【答案】
C
23.【答案】
B
24.【答案】
D
25.【答案】
溶质质量分数为10%的稀硫酸的密度;烧杯
26.【答案】
(1)硝酸钾(2)215
27.【答案】
(1)继续向左盘加药品直到天平平衡(2)搅拌,加快食盐的溶解(3)B,D
28.【答案】
(1)40(2)a29.【答案】
(1)搅拌,加快溶解速(2)5.8(3)52.2(4)B,D
30.【答案】
(1)解:500mL=500cm3
,
这一瓶浓盐酸中溶质的质量是1.19g/cm3×500cm3×37%≈220.2g
(2)设可以稀释成1.85%的稀盐酸的质量为x,根据溶液稀释前后溶质的质量不变,则200g×37%=x×1.85%?
?x=4000g。
同时加水的质量为4000g﹣200g=3800g。
31.【答案】
(1)该瓶盐水能给病人体内提供氯化钠的质:500g×0.9%=4.5g;
(2)需要18%的氯化钠溶液质量:4.5g÷18%=25g;
那么需要加水的质量:500g-25g=475g;
需要加水的体积:。
32.【答案】
(1)13.6(2)③④(3)第3次实验得到的氯化钠溶液的溶质质量分数为;
(4)设释成5%的氯化钠溶液擀质量为x
?100×20%
=5%x
x=400g,所以所用水的质量为400g-100g=300g。
33.【答案】
(1)960(2)15.48%(3)7.5千克;22.5升
34.【答案】
(1)11:10(2)5.1(3)B;20—40℃
35.【答案】
(1)解:因为物体漂浮
所以F浮=G物=ρVg=1.30×103kg/m3×2.50×10-6m3×10N/kg=3.25N
(2)F浮=ρgV排
所以ρ液=F浮/gV排=3.25N/(10N/kg×13/15×250×10-6m3)=1.5×103kg/m3=1.5g/cm3
查表为这种硫酸溶液的溶质质量分数60%
(3)解:物块A全浸,则ρ液=ρ物=1.30g/cm3
,
p%=40%
5kg×60%=(5kg+m)×40%
m=2.5kg
21世纪教育网(www.21cnjy.com)
【8年级上册同步重难点集训】03
第一章
第4—5节溶液的性质与计算
一、物质在水中的分散情况
1.(2020七下·余姚期末)下列物质属于溶液的是(???
)
A.?纯净水?????????????????????????????????B.?牛奶?????????????????????????????????C.?豆浆?????????????????????????????????D.?生理盐水
2.(2020七下·慈溪期中)衣服上沾有碘很难洗净,碘在下列四种不同溶剂中的溶解性如下表所示:
溶质
碘
溶剂
水
酒精
汽油
苯(有毒)
溶解性
微溶
可溶
易溶
易溶
由表中提供的信息判断,能最快洗净衣服上的碘污渍且对人体无害的是(???
)
A.?水???????????????????????????????????????B.?酒精???????????????????????????????????????C.?汽油???????????????????????????????????????D.?苯
3.(2020七下·慈溪期中)如图所示将一种物质加入另一种物质中,其中能得到乳浊液的是(???
)
A.????????????????????????B.????????????????????????C.????????????????????????D.?
4.(2019八上·柯桥月考)下列一些生活中常见的液体,属于溶液的是(
???)
A.?牛奶?????????????????????????????????????B.?碘酒?????????????????????????????????????C.?泥水?????????????????????????????????????D.?墨汁
5.(2019八上·浙江期中)下表是某同学的实验记录,以下说法不正确的是(????
)
溶质
碘
高锰酸钾
溶剂
水
汽油
酒精
水
汽油
溶解性
不溶
易溶
可溶
易溶
不溶
A.?衣服不慎沾上碘酒,可用汽油擦洗??????????????????????B.?溶液都是均一、稳定、无色的混合物
C.?水、汽油、酒精都可以做溶剂?????????????????????????????D.?同一物质在不同溶剂中溶解性不同
6.(2019八上·新昌期中)小明周六去郊游,出发前到超市买了下列4种饮品,其中属于溶液的是(???
)
A.?“永和”豆浆????????????B.?“娃哈哈”矿泉水????????????C.?“美汁源”果粒橙????????????D.?“伊利”纯牛奶
7.(2019八上·天台期中)给下列混合物归类:①食盐水,②牛奶,③色拉油和汽油混合后的液体,④肥皂水,⑤泥水,⑥色拉油和水混合后的液体;属于溶液的是________,属于乳浊液的是________,属于悬浊液的是________。
8.(2019八上·余杭期中)请你各举一个实例,说明下列有关溶液的叙述是错误的。
(1)溶液一定是无色的。实例:________溶液不是无色的。
(2)均一的、稳定的液体都是溶液。实例:________是均一的、稳定的液体,但不是溶液。
9.(2019八上·诸暨月考)下列物质:①冰水混合物,②食用油滴入水中,搅拌,③白酒,④钡餐⑤木炭粉放入水中,搅拌,⑥铁粉放入水中,搅拌,⑦油脂放入汽油中,搅拌,⑧碘放入酒精中,搅拌。其中属于溶液的是________,(填序号,下同);属于悬浊液的是________,属于乳浊液的是________
二、溶液的性质与分析
10.(2020·三门模拟)在其他条件不改变的情况下,对下列四种溶液作对应的处理,最终所得溶液的溶质质量分数一定变大的是(???
)
A.?B.?
C.?D.?
11.(2020·平阳模拟)一定温度下,向图Ⅰ烧杯中加入一定量的水,结果如图Ⅱ所示,所得溶液与原溶液相比,下列判断一定正确的是(???
)
第11题图
第12题图
A.?溶质的质量增加????????B.?溶质的溶解度变大????????C.?所得溶液是饱和溶液????????D.?溶质的质量分数变大
12.(2020·温州模拟)无土栽培技术是植物根能直接接触培养液的栽培方法,小明在炎热的夏天从冰箱拿出一瓶硝酸钾培养液如图A,一段时间后变成了图C。下列说法不正确的是(???
)
A.?硝酸钾的溶解度随温度的升高而增大???????????B.?图C中的培养液一定是不饱和溶液
C.?图A中的培养液一定是饱和溶液???????????????????D.?可以通过升温把硝酸钾的饱和溶液转变为不饱和溶液
13.(2020·余姚模拟)已知硝酸钾的溶解度随温度升高而增大。如图是有关硝酸钾溶液的实验操作及变化情况。下列说法正确的是(???
)
第13题图
第14题图
A.?操作Ⅰ一定是加溶质???????????????????????????????????????????B.?①与②的溶质质量可能相等
C.?②与③的溶质质量分数可能相等?????????????????????????D.?整个实验过程中硝酸钾的溶解度一定不变
14.(2020·温州模拟)某温度下,在2支装有10毫升水的甲、乙试管中分别加入20克蔗糖和0.2克熟石灰,振荡后,静置一段时间,可观察到如图所示的现象。则下列分析正确的是(???
)
A.?甲试管中固体全部溶解,说明甲试管中的溶液为稀溶液
B.?乙试管底部有固体,说明乙试管中的液体为悬浊液
C.?此时蔗糖溶液肯定未饱和,而熟石灰溶液一定已饱和
D.?该实验现象说明该温度下蔗糖的溶解度比熟石灰大
15.(2020·衢州模拟)某次蔗糖溶解实验过程如图所示,不考虑水分蒸发,下列判断错误的是(???
)
第15题图
第16题图
A.?②③中溶液的溶解度不同????????????????????????????????????B.?③中溶液一定是不饱和溶液
C.?②③中溶液的溶质质量分数不相同??????????????????????D.?③中溶液的溶质质量大于②中溶液的溶质质量
16.(2020·丽水模拟)在其它条件不改变的情况下,对硝酸钾溶液进行如下处理,溶液的溶质质量分数大小比较正确的是(???
)
A.?①>②>③?????????????????????????B.?①=②>③?????????????????????????C.?①=②<③?????????????????????????D.?①=②=③
17.(2019八上·越城期末)科学研究中常用图象来表示两个量(x,y)之间的关系,以使研究的问题变得直观明了。下列两个量之间的关系不符合如图所示的是(?
??)
A.?一定浓度溶液中,溶质质量与溶液质量的关系????B.?固体的溶解度与温度的关系
C.?物体受到的浮力与排开液体质量的关系???????????????D.?物体受到的浮力与其排开液体体积的关系
18.(2020七下·宁波月考)小科同学为了探究固体的溶解度与温度的关系,他在家里尝试做了一系列实验,其中一个实验的具体做法及现象如图所示。
以上实验可推断:在一定量的水中,明矾的溶解度随温度的升高而________(填“增大”或“减小”);明矾晶体析出后剩余的溶液是________(填“饱和”或“不饱和”)溶液。
19.(2019八上·江山期中)下列数据是硝酸钾固体在不同温度时的溶解度.
(1)20℃时,向100g水中加入31.6g硝酸钾,充分溶解后得到________(填“饱和”或“不饱和”溶液。
(2)20℃时,向100g水中加入40g硝酸钾,若使硝酸钾完全溶解,可以采用的方法是________。
(3)如图所示,小烧杯中盛放的是上述(1)中所得硝酸钾溶液,若将少量的下列物质分别放入大烧杯中的水中,不断搅拌,则小烧杯中一定有硝酸钾晶体析出的是???????????(填字母)。
A.冰
B.氢氧化钠
C.硝酸按
D.干冰
20.(2019八上·义乌期中)配制一定质量的硝酸钾溶液,将一木块漂浮于50℃时的硝酸钾的饱和溶液中,(如图a所示)当温度改变时(不考虑由此引起的木块和溶液体积的变化),木块排开液体的体积V排随时间t发生了如图b所示的变化。
(1)由此推测出温度的改变是________?(填“升温”或“降温”)。
(2)同时观察到烧杯底部硝酸钾晶体________?(填“增多”或“减少”)。
(3)如果在配制硝酸钾溶液的过程中出现以下情况,可能造成对所配溶液的溶质质量分数的误差(填“偏高”、“偏低”、“无影响”):
①所用硝酸钾药品不纯________;
②量取水时仰视读数________;
③配制完后将溶液转移至试剂瓶时洒出了一些________。
21.(2017八上·杭州月考)为了探究影响固体溶解性的因素,某同学设计了如下三组实验:
因素
第一组
第二组
第三组
实验温度
20℃
20℃
20℃
20℃
80℃
加入溶剂种类
水
酒精
水
水
水
加入溶剂质量
20g
20g
10g
10g
10g
加入固体种类
硝酸钾
硝酸钾
硝酸钾
食盐
硝酸钾
加入固体质量
10g
10g
10g
10g
10g
溶解固体质量
6.2g
0g
3.1g
3.6g
10g
(1)分析上表,第一组实验研究的因素是________;
(2)由上述实验可知,影响固体溶解性的因素是________(填序号)
①温度
②加入溶剂种类
③加入溶剂质量
④加入固体种类
⑤加入固体质量
(3)在第二组实验中,该同学按照如下步骤进行实验(假设溶液损失不计)
①用电子天平称取
10.0g
硝酸钾,放入烧杯中;
②量取
10.0mL
水,倒入上述烧杯中,称量烧杯、硝酸钾和水的总质量为
m1g;
③搅拌至硝酸钾不再溶解为止;
④过滤,称量所得硝酸钾溶液和烧杯的总质量为
m2g;
⑤计算:m1-m2=______g(结合第二组实验数据进行分析)。
将溶质改为食盐,重复上述步骤进行实验。
由实验可知,20℃时食盐的溶解性________(填“>”“﹦”“<”)硝酸钾的溶解性。
(4)根据上述实验,以下推论正确的是
?????????????????????。
A.20℃时,氯化钠的溶解度为
36g/100g
水
B.20℃时,硝酸钾饱和溶液的溶质质量分数为
31%
C.第三组实验中的硝酸钾溶液为
80℃时的饱和溶液
D.20℃的任意一杯饱和硝酸钾溶液中,溶质与溶剂的质量比一定相等
三、定量计算与配置溶液
22.(2020·金东模拟)实验室用氯化钠配制50g质量分数为6%的氯化钠溶液,下列说法不正确的是(???
)
A.?所需氯化钠的质量为3g???????????????????????????????????????B.?氯化钠放在托盘天平的左盘称量
C.?俯视量筒读数会使所配溶液偏稀?????????????????????????D.?所需玻璃仪器有烧杯、玻璃棒、量筒等
23.(2020九下·宁波保送考试)某容器中装有盐水若干,老师让小科倒入质量分数1%的盐水100克以配成质量分数2%的盐水,但小科却错误的倒入100克水,老师发现后说你再将第三种盐水40克倒入水中就可得到2%的盐水了,那么第三种盐水的质量分数为(???
)
A.?2.5%??????????????????????????????????????B.?4.5%??????????????????????????????????????C.?5%??????????????????????????????????????D.?7%
温度(℃)
t0
t1
t2
硝酸钾溶解度/克
31.6
44
60
氯化铵溶解度/克
37.6
40
41
24.(2020八上·苍南期末)M是硝酸钾或氯化铵其中的一种,硝酸钾和氯化铵在不同温度(t0
)
A.?物质M是硝酸钾????????????????????????????????????????????????B.?溶液①为不饱和溶液,溶液②和③为饱和溶液
C.?溶液②中溶质质量分数为37.5%????????????????????????D.?溶液①②③中,溶质质量分数的关系是②>③>①
25.用溶质质量分数为98%、密度为1.84g/cm3的浓硫酸配制溶质质量分数为10%的稀硫酸100mL,计算时必须查阅的数据是________。配制过程中除了使用量筒、玻璃棒和胶头滴管外,还需要的一种玻璃仪器是________。
26.(2020·瑞安模拟)t1℃时,将质量均为35克的氯化钾和硝酸钾分别加入到各盛有100g水的两个烧杯中,充分搅拌后现象如图所示(t1℃时,硝酸钾的溶解度小于氯化钾的溶解度)。
(1)据图分析烧杯A中溶解的溶质为________;
(2)将t1℃时烧杯B中的溶液稀释成10%的溶液,需加水________克。
27.如图是配制50克质量分数为5%的氯化钠溶液的操作过程示意图
(1)B操作,在称量中发现指针偏向右边,接下来的操作是________;
(2)E操作中玻璃棒的作用是________。
(3)如果配制过程中出现以下情况,可能导致所配溶液的溶质质量分数偏大的是????
。
A.所用氯化钠药品不纯
B.量取水时俯视读数
C.配完后将溶液转移至试剂瓶时洒出了一些
D.将量好的水从量筒里倒入烧杯时,酒出一些水
28.(2019八上·嵊州月考)在一定温度下,向100g水中依次加入一定质量的氯化钾(即KCl)固体,充分溶解。加入氯化钾的质量与得到相应溶液质量的关系如图所示:
(1)该温度下氯化钾的溶解度为________克。
(2)实验①、②、③的溶液,溶质的质量分数分别为a、b、c,则它们的大小关系是________(用“>”“<”或“=”表示出来)。
29.(2019八上·嵊州月考)实验室配置质量分数为10%的食盐溶液。如图1是某同学的实验操作过程:
(1)玻璃棒a在④中所起的作用是________。
(2)若③中游码读数为1.2,则他称氯化钠的质量是________?g。
(3)该同学如果操作正确,则需要用水的体积是________?mL。(水的密度为1.0g/cm3)
(4)下列操作会导致溶液溶质质量分数偏小的是
?????。
A.搅拌溶解时有少量水溅出
B.量取水的体积时,如图2所示操作
C.所用的托盘天平游码生锈了
D.用4g食盐和100g水配制溶液
30.(2020八下·天台月考)实验室保存﹣瓶浓盐酸,瓶上的标签部分内容如图所示,请根据标签上的信息回答下列各问:
(1)这一瓶浓盐酸中溶质的质量是多少克?(结果精确到0.1)
(2)取200克此瓶内的浓盐酸可以稀释成1.85%的稀盐酸多少克?同时加水多少克?
31.(2019八上·柯桥月考)如图为某医用生理盐水注射液的标签中的部分内容。计算:
(1)该瓶盐水能给病人体内提供氯化钠的质量是多少?
(2)若用溶质质量分数为18%的氯化钠溶液配制该瓶生理盐水,需要18%的氯化钠溶液多少克?需蒸馏水多少毫升?(ρ水=1×103Kg/m3)
32.(2019八上·天台月考)氯化钠俗名食盐是工业生产和生活的一种重要原料,也是实验室里常见的一种药品。下表是20℃时,氯化钠溶解于水的实验数据,回答下列问题;
实验序号
水的质量(g)
加入氯化钠的质量(g)
溶液的质量(g)
①
10
2
12
②
10
3
13
③
10
4
13.6
④
10
5
m
(1)表中m=________;
(2)在这4次实验中,得到的是20℃氯化钠溶液属于饱和溶液的是________(填实验序号)
(3)计算第3次实验得到的氯化钠溶液的溶质质量分数。(写出过程)
(4)20℃时,实验室把100克溶质质量分数为20%的氯化钠溶液释成5%的氯化钠溶液,需加水多少毫升?(写出过程)
33.(2019八上·杭州期中)预防流感现在最有效的方法之一就是用消毒液对空气消毒。二氧化氯消毒液能够迅速彻底地杀灭各种细菌(大肠杆菌、白色念珠菌等)和病毒(肝炎病毒、流感病毒等)。某校决定放学后对全校教室、寝室全面消毒。小陈观察到瓶上的标签如下表所示。
二氧化氯消毒液(ClO2)1000毫升
溶质的质量分数
80%
密度
1.2
克/厘米
3
相对分子质量
67.5
强腐蚀性,阴冷、密封储藏
求:
(1)这1000毫升二氧化氯消毒液含溶质二氧化氯?
________?克。
(2)若将这1000毫升二氧化氯消毒液与5000克水均匀混合,所得稀二氧化氯消毒液中二氧化氯的质量分数是________。(保留1位小数)
(3)我校欲配制30千克质量分数为20%的稀二氧化氯消毒液用来消毒,需要多少千克这种二氧化氯消毒液和多少升水?(写出计算过程)
34.(2019八上·衢州期中)下表列出了硝酸钾与氯化钠在不同温度下的溶解度:
温度/℃
0
10
20
40
60
80
100
硝酸钾的溶解度/g
13.3
20.9
31.6
63.9
110
169
246
氯化钠的溶解度/g
35.7
35.8
36.0
36.6
37.3
38.4
39.8
(1)20℃时,在装有15g硝酸钾晶体的试管中,加入10g水并充分振荡,将所得溶液放入盛有热水的烧杯中,将溶液温度升至60℃,此时试管内的溶液中溶质与溶剂质量比为________。
(2)取25g氯化钠晶体加入70g水中,加热溶解。在100℃时蒸发掉
20g水,维持该温度过滤,得到的晶体质量为________g。
(3)现有硝酸钾和氯化钠晶体各40g,分别加到100g、80℃的水中充分溶解得到溶液A、B,其中________溶液为饱和溶液,若要使A、B两种溶液的溶质质量分数相等,则应将A、B两溶液的温度至少降至________的范围内。
35.(2019八上·衢州期中)下表为硫酸密度与硫酸溶液中的溶质的质量分数对照表(20℃)
密度(g/ml)
1.01
1.07
1.14
1.22
1.30
1.40
1.50
1.61
1.73
1.81
1.84
质量分数(%)
1
10
20
30
40
50
60
70
80
90
98
有一物块A,其体积为250cm3,密度为1.30g/cm3。一只容器中盛有某硫酸溶液5千克,将物块A放入该溶液中静止后如图所示,此时物块A有2/15的体积露出液面。
(1)求物块A静止时受到的浮力大小?
(2)求这种硫酸溶液的溶质质量分数是多少?
(3)要使物块A全部浸入溶液中,至少需要往容器中加水多少千克?(容器足够大,加水后溶液不溢出。)
答案解析部分
一、物质在水中的分散情况
1.【答案】
D
2.【答案】
C
3.【答案】
D
4.【答案】
B
5.【答案】
B
6.【答案】
B
7.【答案】
①③;②④⑥;⑤
8.【答案】
(1)高锰酸钾(2)蒸馏水
9.【答案】
③⑧⑦;④⑤⑥;②
二、溶液的性质与分析
10.【答案】
A
11.【答案】
A
12.【答案】
B
13.【答案】
B
14.【答案】
D
15.【答案】
B
16.【答案】
C
17.【答案】
B
18.【答案】
增大;饱和
19.【答案】
(1)饱和(2)升高温度或加水(3)A,C,D
20.【答案】
(1)降温(2)增多(3)偏低;偏低;无影响
21.【答案】
(1)溶剂种类(2)①②④(3)6.9;>(4)A,D
三、定量计算与配置溶液
22.【答案】
C
23.【答案】
B
24.【答案】
D
25.【答案】
溶质质量分数为10%的稀硫酸的密度;烧杯
26.【答案】
(1)硝酸钾(2)215
27.【答案】
(1)继续向左盘加药品直到天平平衡(2)搅拌,加快食盐的溶解(3)B,D
28.【答案】
(1)40(2)a
(1)搅拌,加快溶解速(2)5.8(3)52.2(4)B,D
30.【答案】
(1)解:500mL=500cm3
,
这一瓶浓盐酸中溶质的质量是1.19g/cm3×500cm3×37%≈220.2g
(2)设可以稀释成1.85%的稀盐酸的质量为x,根据溶液稀释前后溶质的质量不变,则200g×37%=x×1.85%?
?x=4000g。
同时加水的质量为4000g﹣200g=3800g。
31.【答案】
(1)该瓶盐水能给病人体内提供氯化钠的质:500g×0.9%=4.5g;
(2)需要18%的氯化钠溶液质量:4.5g÷18%=25g;
那么需要加水的质量:500g-25g=475g;
需要加水的体积:。
32.【答案】
(1)13.6(2)③④(3)第3次实验得到的氯化钠溶液的溶质质量分数为;
(4)设释成5%的氯化钠溶液擀质量为x
?100×20%
=5%x
x=400g,所以所用水的质量为400g-100g=300g。
33.【答案】
(1)960(2)15.48%(3)7.5千克;22.5升
34.【答案】
(1)11:10(2)5.1(3)B;20—40℃
35.【答案】
(1)解:因为物体漂浮
所以F浮=G物=ρVg=1.30×103kg/m3×2.50×10-6m3×10N/kg=3.25N
(2)F浮=ρgV排
所以ρ液=F浮/gV排=3.25N/(10N/kg×13/15×250×10-6m3)=1.5×103kg/m3=1.5g/cm3
查表为这种硫酸溶液的溶质质量分数60%
(3)解:物块A全浸,则ρ液=ρ物=1.30g/cm3
,
p%=40%
5kg×60%=(5kg+m)×40%
m=2.5kg
21世纪教育网(www.21cnjy.com)
同课章节目录
- 第1章 水和水的溶液
- 第1节 地球上的水
- 第2节 水的组成
- 第3节 水的浮力
- 第4节 物质在水中的分散状况
- 第5节 物质的溶解
- 第6节 物质的分离
- 第7节 水资源的利用、开发和保护
- 第2章 天气与气候
- 第1节 大气层
- 第2节 气温
- 第3节 大气的压强
- 第4节 风和降水
- 第5节 天气预报
- 第6节 气候和影响气候的因素
- 第7节 我国的气候特征与主要气象灾害
- 第3章 生命活动的调节
- 第1节 植物生命活动的调节
- 第2节 人体的激素调节
- 第3节 神经调节
- 第4节 动物的行为
- 第5节 体温的控制
- 第4章 电路探秘
- 第1节 电荷与电流
- 第2节 电流的测量
- 第3节 物质的导电性与电阻
- 第4节 变阻器
- 第5节 电压的测量
- 第6节 电流与电压、电阻的关系
- 第7节 电路分析与应用
- 研究性学习课题
- 一 测定本地区的“酸雨”情况及分析原因
- 二 太阳黑子活动与本地区降水的关系
- 三 训练小动物建立某种条件反射
- 四 调查在自然界或生命活动中的电现象
