华东师大版八年级科学上册第六章第五节《固态物质》(课件 共30张ppt)
文档属性
| 名称 | 华东师大版八年级科学上册第六章第五节《固态物质》(课件 共30张ppt) |

|
|
| 格式 | ppt | ||
| 文件大小 | 3.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 华东师大版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2020-10-12 00:00:00 | ||
图片预览








文档简介
(共30张PPT)
第六章
物质的构成
第5节
固态物质
1、掌握解晶体与非晶体的本质差异
2、掌握晶体的基本性质
3、知道获得晶体的几种途径
导入新课
构成物质的微粒有几种,分别是什么?
自然界中的物质一共有几种状态?
物质可以分为哪几类?
一、物质的状态
一、物质的状态
我们日常接触到的物质不是单个的分子、原子或离子,
而是大量分子、原子或离子聚集在一起的状态。
气态、液态与固态是物质常见的三种聚集状态。
常见物质的状态有哪些呢?
一、物质的状态
物质
常温常压下的状态
颜色
熔点/℃
沸点/℃
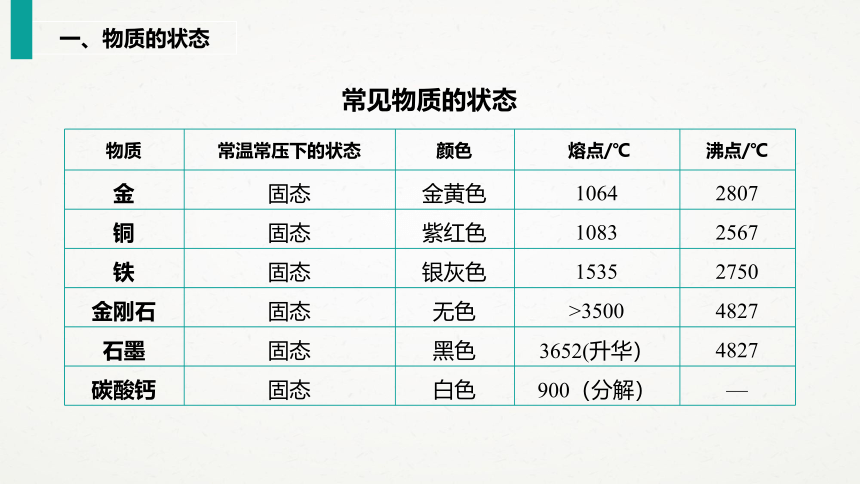
金
固态
金黄色
1064
2807
铜
固态
紫红色
1083
2567
铁
固态
银灰色
1535
2750
金刚石
固态
无色
>3500
4827
石墨
固态
黑色
3652(升华)
4827
碳酸钙
固态
白色
900(分解)
—
常见物质的状态
一、物质的状态
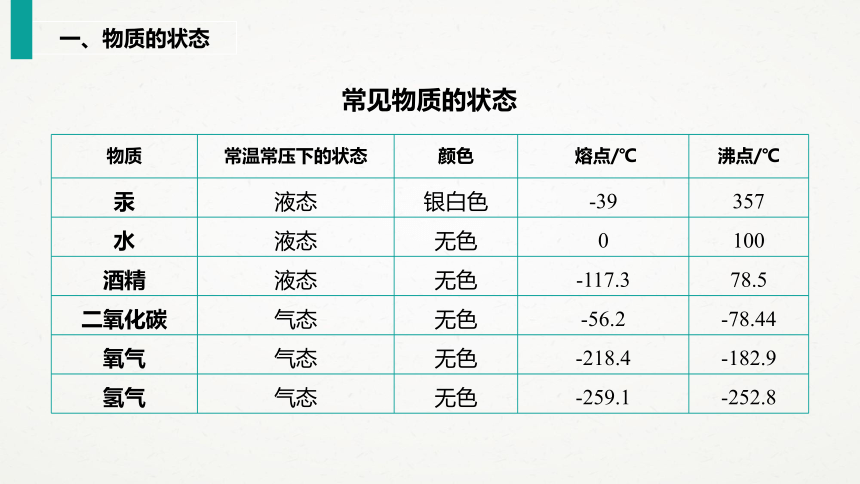
常见物质的状态
物质
常温常压下的状态
颜色
熔点/℃
沸点/℃
汞
液态
银白色
-39
357
水
液态
无色
0
100
酒精
液态
无色
-117.3
78.5
二氧化碳
气态
无色
-56.2
-78.44
氧气
气态
无色
-218.4
-182.9
氢气
气态
无色
-259.1
-252.8
二、晶体与非晶体
晶体:晶体内部的原子按一定规律排列。
由于构成晶体内部的微粒排列有序,犹如一支正待检阅的队伍,
因此晶体在生长过程中自然形成规则的多面体外形。
食盐
(氯化钠NaCl)、
冰
(H2O
)、
石英
(二氧化硅SiO2)、
石墨
(C)、
萤石
(氟化钙
CaF2)和金属等。
固体可以分成晶体与非晶体
二、晶体与非晶体
非晶体:非晶体内部的原子排列无规则。
由于构成非晶体的微粒排列无序,好像一群正在草坪上玩耍的孩子,因而没有规则的外形,故又称为无定形。
如:松香、玻璃、蜂蜡、琥珀等。
二、晶体与非晶体
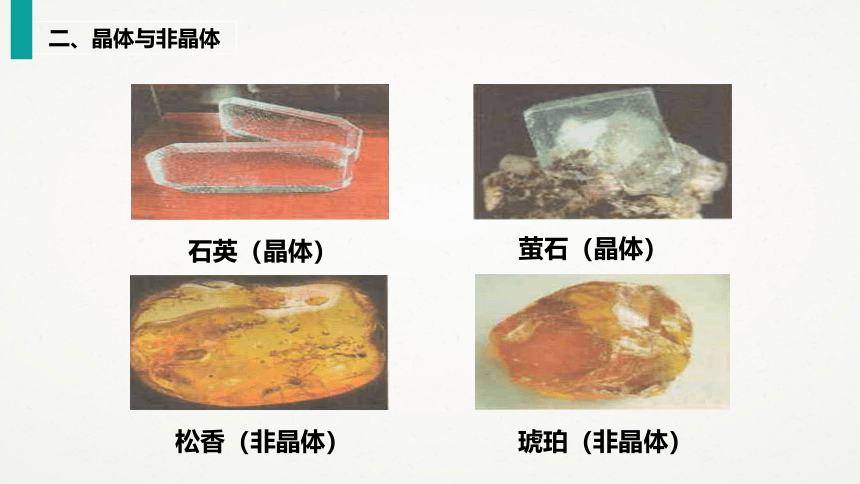
石英(晶体)
萤石(晶体)
松香(非晶体)
琥珀(非晶体)
二、晶体与非晶体
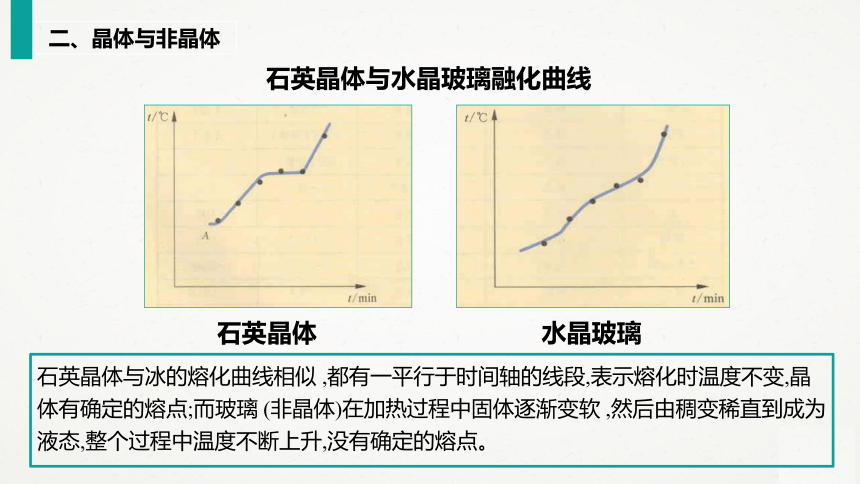
石英晶体与水晶玻璃融化曲线
石英晶体
水晶玻璃
石英晶体与冰的熔化曲线相似
,都有一平行于时间轴的线段,表示熔化时温度不变,晶体有确定的熔点;而玻璃
(非晶体)在加热过程中固体逐渐变软
,然后由稠变稀直到成为液态,整个过程中温度不断上升,没有确定的熔点。
二、晶体与非晶体
石英晶体和水晶玻璃虽然化学成分相同,都是二氧化硅,但是它们的结构与物理性质却不相同。
晶体有确定的熔点,非晶体没有确定的熔点。有没有确定的熔点,是晶体与非晶体的重要区别之一。
二、晶体与非晶体
标准大气压下冰的熔点为0
℃。
物质熔点和凝固点相同。
晶体有确定的熔点
二、晶体与非晶体
晶体熔化时的特点:
1、持续吸热
2、温度保持不变。
晶体有确定的熔点
AB段表示
;
BC段表示
;
CD段表示
;
冰块吸热,温度升高
冰块正在熔化,温度不变
水吸热,温度升高
二、晶体与非晶体
晶体融化的条件:
1、温度要达到熔点。
2、还要继续吸热。
晶体有确定的熔点
时间
温度
熔点
固态
D
C
B
A
液态
固液共存
二、晶体与非晶体
非晶体熔化时的特点:
1)持续吸热;
2)温度升高;
非晶体没有确定的熔点
非晶体受热就会开始熔化,
没有固定的熔化温度,即没有熔点。
二、晶体与非晶体
归纳总结
晶体:晶体内部的原子按一定规律排列。
非晶体:非晶体内部的原子排列无规则。
晶体熔化时的温度叫做熔点。
无论是晶体还是非晶体熔化时都要吸热。
晶体和非晶体的主要区别是:晶体有熔点,而非晶体没有熔点。
思考与讨论
不同种元素可以组成不同种物质,同种元素可否组成不同物质呢?
三、金刚石与石墨
金刚石
石墨
三、金刚石与石墨
常见的金刚石无色或略带颜色。金刚石是自然界中最硬的物质,常用于制作各种切割工具、钻探用的钻头等。导热性比铜还要优良。掺杂后的金刚石还是优良的半导体,宝石级的金刚石常称为钻石。
金刚石与石墨两种晶体都是碳的单质。
三、金刚石与石墨
性质
用途
金
刚
石
无色透明、正八面体形状的固体
经仔细琢磨后,成为装饰品──钻石
自然界中存在的最硬的物质
划玻璃、切割大理石、加工坚硬的金属,装在钻探机的钻头上钻凿坚硬的岩层等
。
金刚石的性质及其对应的用途
三、金刚石与石墨
纯净的石墨为黑灰色的不透明晶体,有金属光泽。
石墨质软,滑腻,轻轻摩擦便留下痕迹。
铅笔芯就是用石墨粉与黏土制成的,石墨粉多则软,用
“B”
表;
黏土掺多了则硬,用
“H”
表示。
石墨具有良好的导电性,广
泛用于制造电极、电刷等。
金刚石与石墨两种晶体都是碳的单质。
三、金刚石与石墨
性质
用途
石
墨
深灰色、有金属光泽、不透明的细磷片状固体
铅笔芯
能导电
电极
滑腻感
润滑剂
石墨的性质及其用途
思考与讨论
为什么金刚石和石墨的物理性质存在这么大的差异呢?
三、金刚石与石墨
C60是分子,C60分子的结构形似足球,每个C60的分子是由60个碳原子构成,又名足球烯。良好的超导体,使超导体的温度为12.8K。
其他碳单质
三、金刚石与石墨
同一类原子,排列方式不同,所形成的单质不同。
其他碳单质
三、金刚石与石墨
石墨烯与碳纳米管
三、金刚石与石墨
共同点:都能在氧气中燃烧只生成一种使澄清石灰水变浑浊的无色气体。
碳的几种单质物理性质不同,但化学性质相同。
小组活动
观察金刚石、石墨、C60、
碳纳米管的结构模型,
查
阅有关资料,比较这4种物质的结构。
晶体:晶体内部的原子按一定规律排列。
非晶体:非晶体内部的原子排列无规则。
晶体熔化时的温度叫做熔点。
无论是晶体还是非晶体熔化时都要吸热。
晶体和非晶体的主要区别是:晶体有熔点,而非晶体没有熔点。
金刚石与石墨两种晶体都是碳的单质。
同一类原子,排列方式不同,所形成的单质不同。
第六章
物质的构成
第5节
固态物质
1、掌握解晶体与非晶体的本质差异
2、掌握晶体的基本性质
3、知道获得晶体的几种途径
导入新课
构成物质的微粒有几种,分别是什么?
自然界中的物质一共有几种状态?
物质可以分为哪几类?
一、物质的状态
一、物质的状态
我们日常接触到的物质不是单个的分子、原子或离子,
而是大量分子、原子或离子聚集在一起的状态。
气态、液态与固态是物质常见的三种聚集状态。
常见物质的状态有哪些呢?
一、物质的状态
物质
常温常压下的状态
颜色
熔点/℃
沸点/℃
金
固态
金黄色
1064
2807
铜
固态
紫红色
1083
2567
铁
固态
银灰色
1535
2750
金刚石
固态
无色
>3500
4827
石墨
固态
黑色
3652(升华)
4827
碳酸钙
固态
白色
900(分解)
—
常见物质的状态
一、物质的状态
常见物质的状态
物质
常温常压下的状态
颜色
熔点/℃
沸点/℃
汞
液态
银白色
-39
357
水
液态
无色
0
100
酒精
液态
无色
-117.3
78.5
二氧化碳
气态
无色
-56.2
-78.44
氧气
气态
无色
-218.4
-182.9
氢气
气态
无色
-259.1
-252.8
二、晶体与非晶体
晶体:晶体内部的原子按一定规律排列。
由于构成晶体内部的微粒排列有序,犹如一支正待检阅的队伍,
因此晶体在生长过程中自然形成规则的多面体外形。
食盐
(氯化钠NaCl)、
冰
(H2O
)、
石英
(二氧化硅SiO2)、
石墨
(C)、
萤石
(氟化钙
CaF2)和金属等。
固体可以分成晶体与非晶体
二、晶体与非晶体
非晶体:非晶体内部的原子排列无规则。
由于构成非晶体的微粒排列无序,好像一群正在草坪上玩耍的孩子,因而没有规则的外形,故又称为无定形。
如:松香、玻璃、蜂蜡、琥珀等。
二、晶体与非晶体
石英(晶体)
萤石(晶体)
松香(非晶体)
琥珀(非晶体)
二、晶体与非晶体
石英晶体与水晶玻璃融化曲线
石英晶体
水晶玻璃
石英晶体与冰的熔化曲线相似
,都有一平行于时间轴的线段,表示熔化时温度不变,晶体有确定的熔点;而玻璃
(非晶体)在加热过程中固体逐渐变软
,然后由稠变稀直到成为液态,整个过程中温度不断上升,没有确定的熔点。
二、晶体与非晶体
石英晶体和水晶玻璃虽然化学成分相同,都是二氧化硅,但是它们的结构与物理性质却不相同。
晶体有确定的熔点,非晶体没有确定的熔点。有没有确定的熔点,是晶体与非晶体的重要区别之一。
二、晶体与非晶体
标准大气压下冰的熔点为0
℃。
物质熔点和凝固点相同。
晶体有确定的熔点
二、晶体与非晶体
晶体熔化时的特点:
1、持续吸热
2、温度保持不变。
晶体有确定的熔点
AB段表示
;
BC段表示
;
CD段表示
;
冰块吸热,温度升高
冰块正在熔化,温度不变
水吸热,温度升高
二、晶体与非晶体
晶体融化的条件:
1、温度要达到熔点。
2、还要继续吸热。
晶体有确定的熔点
时间
温度
熔点
固态
D
C
B
A
液态
固液共存
二、晶体与非晶体
非晶体熔化时的特点:
1)持续吸热;
2)温度升高;
非晶体没有确定的熔点
非晶体受热就会开始熔化,
没有固定的熔化温度,即没有熔点。
二、晶体与非晶体
归纳总结
晶体:晶体内部的原子按一定规律排列。
非晶体:非晶体内部的原子排列无规则。
晶体熔化时的温度叫做熔点。
无论是晶体还是非晶体熔化时都要吸热。
晶体和非晶体的主要区别是:晶体有熔点,而非晶体没有熔点。
思考与讨论
不同种元素可以组成不同种物质,同种元素可否组成不同物质呢?
三、金刚石与石墨
金刚石
石墨
三、金刚石与石墨
常见的金刚石无色或略带颜色。金刚石是自然界中最硬的物质,常用于制作各种切割工具、钻探用的钻头等。导热性比铜还要优良。掺杂后的金刚石还是优良的半导体,宝石级的金刚石常称为钻石。
金刚石与石墨两种晶体都是碳的单质。
三、金刚石与石墨
性质
用途
金
刚
石
无色透明、正八面体形状的固体
经仔细琢磨后,成为装饰品──钻石
自然界中存在的最硬的物质
划玻璃、切割大理石、加工坚硬的金属,装在钻探机的钻头上钻凿坚硬的岩层等
。
金刚石的性质及其对应的用途
三、金刚石与石墨
纯净的石墨为黑灰色的不透明晶体,有金属光泽。
石墨质软,滑腻,轻轻摩擦便留下痕迹。
铅笔芯就是用石墨粉与黏土制成的,石墨粉多则软,用
“B”
表;
黏土掺多了则硬,用
“H”
表示。
石墨具有良好的导电性,广
泛用于制造电极、电刷等。
金刚石与石墨两种晶体都是碳的单质。
三、金刚石与石墨
性质
用途
石
墨
深灰色、有金属光泽、不透明的细磷片状固体
铅笔芯
能导电
电极
滑腻感
润滑剂
石墨的性质及其用途
思考与讨论
为什么金刚石和石墨的物理性质存在这么大的差异呢?
三、金刚石与石墨
C60是分子,C60分子的结构形似足球,每个C60的分子是由60个碳原子构成,又名足球烯。良好的超导体,使超导体的温度为12.8K。
其他碳单质
三、金刚石与石墨
同一类原子,排列方式不同,所形成的单质不同。
其他碳单质
三、金刚石与石墨
石墨烯与碳纳米管
三、金刚石与石墨
共同点:都能在氧气中燃烧只生成一种使澄清石灰水变浑浊的无色气体。
碳的几种单质物理性质不同,但化学性质相同。
小组活动
观察金刚石、石墨、C60、
碳纳米管的结构模型,
查
阅有关资料,比较这4种物质的结构。
晶体:晶体内部的原子按一定规律排列。
非晶体:非晶体内部的原子排列无规则。
晶体熔化时的温度叫做熔点。
无论是晶体还是非晶体熔化时都要吸热。
晶体和非晶体的主要区别是:晶体有熔点,而非晶体没有熔点。
金刚石与石墨两种晶体都是碳的单质。
同一类原子,排列方式不同,所形成的单质不同。
同课章节目录
- 第1章 运动和力
- 1 机械运动
- 2 力
- 3 几种常见的力
- 4 运动和力
- 5 二力平衡的条件
- 第2章 压力 压强
- 1 压强
- 2 液体内部的压强
- 3 大气压强
- 4 流体的压强与流速的关系
- 第3章 浮力
- 1 密度
- 2 浮力
- 3 阿基米德原理
- 4 物体浮沉条件及其应用
- 第4章 植物的物质和能量的转化
- 1 绿色开花植物的营养器官
- 2 水在植物体中的代谢
- 3 无机盐在植物体内的代谢
- 4 植物的光合作用和呼吸作用
- 第5章 人体的物质和能量的转化
- 1 食物的消化和吸收
- 2 人体的呼吸
- 3 人体内的物质运输
- 4 人体的排泄
- 5 人体生命活动过程中物质和能量的转化
- 第6章 物质的构成
- 1 构成物质的微粒
- 2 元素
- 3 物质的分类
- 4 化学式
- 5 固态物质
