沪教版(上海)初中化学九年级第一学期第4章《燃料及其燃烧》检测题(含答案)
文档属性
| 名称 | 沪教版(上海)初中化学九年级第一学期第4章《燃料及其燃烧》检测题(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 133.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版(试用本) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-10-12 00:00:00 | ||
图片预览


文档简介
《燃料及其燃烧》检测题
一、单选题
1.下列实验方案及操作中,合理的是( )
A.除去CO2中少量CO:将混合气体点燃
B.实验室制取CO2:利用稀硫酸和大理石反应
C.鉴别甲烷、一氧化碳、氢气三种气体:分别燃烧,检验燃烧产物
D.比较空气和人体呼出气体中CO2含量:向分别装有两种气体集气瓶中伸入燃着小木条
2.有关金刚石、石墨和C60的说法正确的是
A.都属于单质
B.元素组成不同
C.硬度相同
D.碳原子排列方式相同
3.化学与生活密切相关。生活中的下列做法不合理的是(
)
A.煤炉火上放一盆水,就能防止一氧化碳中毒
B.冰箱中的异味,可用活性炭除去
C.电器着火,应先切断电源再灭火
D.为防止煤气泄漏引发危险,可在煤气中添加有刺激性气味的乙硫醇
4.某合作学习小组讨论辨析以下说法:①CO2和KClO3中都含有氧元素,都是氧化物;②生活中常用煮沸法来降低水的硬度③有的元素有变价,在同种化合物里也可能显不同的化合价;④推广使用无氟冰箱防止“臭氧空洞”;⑤加高工厂烟囱可减少废气对大气的污染;⑥在食品袋中填充氮气可延长食品的保质期。其中正确的一组是( )
A.①②③④⑤⑥
B.②③④⑤⑥
C.②③④⑥
D.②④⑤⑥
5.水是生命之源,下列有关水的说法正确的是
A.水是常用的溶质
B.水汽化时分子大小发生了变化
C.正常雨水呈酸性
D.电解水得到氢气与氧气的质量比为2:1
6.燃烧柴禾时,通常把柴禾架空一些,才能燃烧得更旺,这是因为
A.散热的速度加快
B.聚集的热量增加
C.柴禾的着火点降低
D.柴禾与空气的接触面积增大
7.二氧化碳常用来对电器灭火,与之无关的性质是( )
A.本身不能燃烧
B.不支持燃烧
C.能溶于水
D.不导电
8.下列有关一氧化碳和二氧化碳的说法,正确的是
A.它们的分子构成相同
B.它们都溶于水
C.它们之间可以相互转化
D.闻气味可将它们区别
9.下列物质的用途体现其物理性质的是
A.小苏打用作发酵粉
B.干冰用于人工降雨
C.氧气用于医疗急救
D.氮气用作保护气
10.下列说法中错误的是
A.现代科学技术的进步与化学科学密切相关
B.煤、石油和天然气等都属于不可再生的化石燃料
C.酸雨的形成与P2.5有直接关系
D.废旧金属、化肥和农药很可能会造成水污染和土壤污染
11.下列有关碳和碳的氧化物的说法正确的是( )
A.干冰可用于人工降雨
B.金刚石和石墨都可用作电极
C.在常温下,碳的化学性质活泼
D.CO和CO2都具有还原性
12.80gFe2O3和CuO的固体混合物,在高温条件下与足量的CO充分反应后,得到金属的质量可能是(
)
A.50g
B.60g
C.70g
D.80g
13.下列化学方程式,表示正确的是(
)
A.紫色石蕊试液中,通入CO2时,溶液变红色
H2CO3═H2O+CO2↑
B.澄清石灰水中,通入CO2时,溶液变浑浊
CaCO3CaO+CO2↑
C.实验室用稀盐酸和大理石反应制CO2CaCO3+2HCl═CaCl2+H2CO3
D.一氧化碳在空气中燃烧生成CO22CO+O22CO2
二、实验题
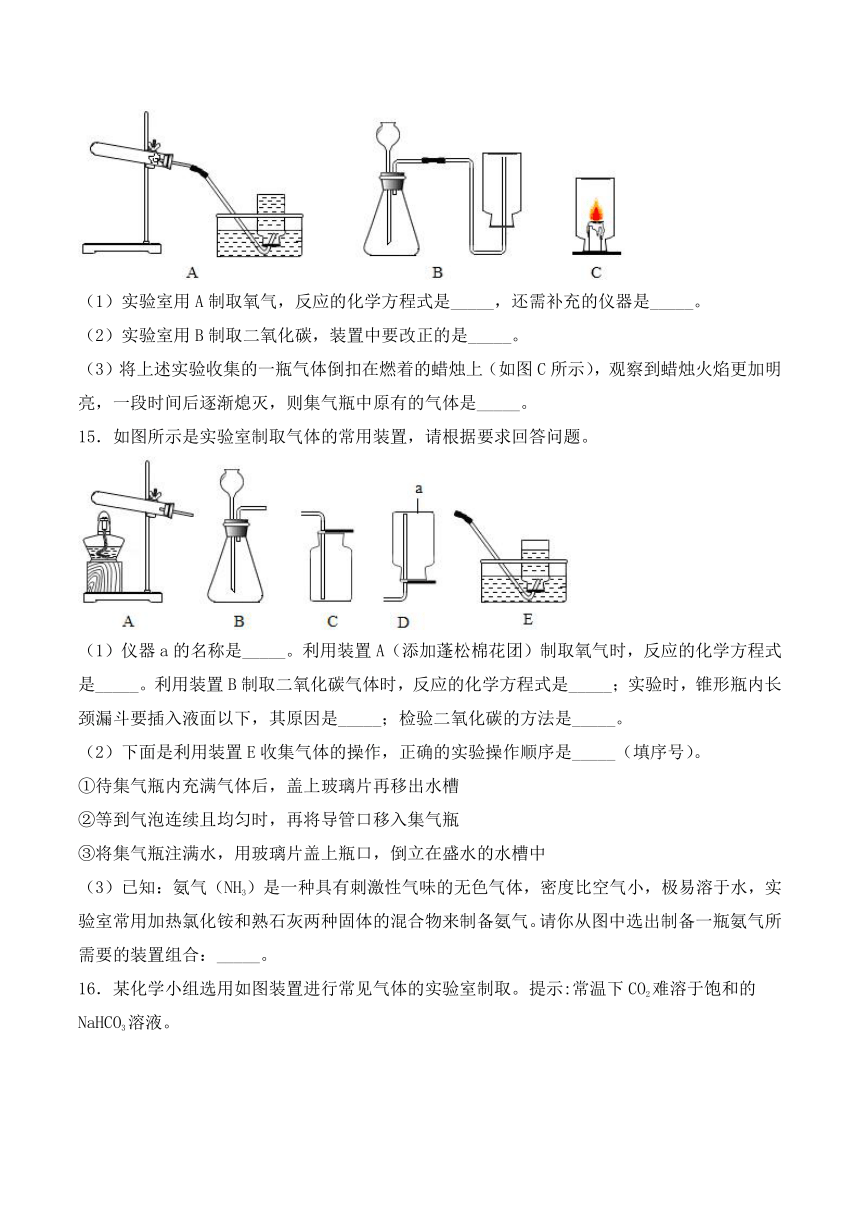
14.根据下图回答问题。
(1)实验室用A制取氧气,反应的化学方程式是_____,还需补充的仪器是_____。
(2)实验室用B制取二氧化碳,装置中要改正的是_____。
(3)将上述实验收集的一瓶气体倒扣在燃着的蜡烛上(如图C所示),观察到蜡烛火焰更加明亮,一段时间后逐渐熄灭,则集气瓶中原有的气体是_____。
15.如图所示是实验室制取气体的常用装置,请根据要求回答问题。
(1)仪器a的名称是_____。利用装置A(添加蓬松棉花团)制取氧气时,反应的化学方程式是_____。利用装置B制取二氧化碳气体时,反应的化学方程式是_____;实验时,锥形瓶内长颈漏斗要插入液面以下,其原因是_____;检验二氧化碳的方法是_____。
(2)下面是利用装置E收集气体的操作,正确的实验操作顺序是_____(填序号)。
①待集气瓶内充满气体后,盖上玻璃片再移出水槽
②等到气泡连续且均匀时,再将导管口移入集气瓶
③将集气瓶注满水,用玻璃片盖上瓶口,倒立在盛水的水槽中
(3)已知:氨气(NH3)是一种具有刺激性气味的无色气体,密度比空气小,极易溶于水,实验室常用加热氯化铵和熟石灰两种固体的混合物来制备氨气。请你从图中选出制备一瓶氨气所需要的装置组合:_____。
16.某化学小组选用如图装置进行常见气体的实验室制取。提示:常温下CO2难溶于饱和的NaHCO3溶液。
回答下列问题:
(1)仪器①的名称为_____________。
(2)若实验室要加热KMnO4制取较纯净的氧气,选择的装置组合是____________和___________,反应的化学方程式为_____________。
(3)实验室常用大理石和稀盐酸,选取B、D装置制取CO2,制得的CO2中混有HC1。为了除去CO2中混有的HCl,可在B、D装置之间连接F装置,导管口a应连接______
(填
“b”或“c”),F装置中盛装的试剂为__________。
三、推断题
17.甲、乙、丙、丁是常见的化合物,它们有如下图所示转化关系(部分物质已略去)。甲是相对分子质量为16的气体;乙是最常见的液体;丁是白色难溶固体,其中金属元素的质量分数为40%。
(1)则甲的化学式为_____。(2)写出①②反应的化学方程式_____,_____
18.A~E是初中化学常见的物质,E是大理石的主要成分,D是能供给呼吸的气
体单质。它们的相互转化关系如图甲所示。“-”表示相互间能反应,“→”表示能转
化。部分反应条件、反应物、生成物已略去。图乙表示的是A、C的相关信息。
请回答下列问题。
(1)D、E的化学式分别为_______、_______,
(2)C的用途之一为_______,写出其相应的化学方程式:_______。
(3)①②③三个反应的基本反应类型都可能为_______,写出③反应的化学方程
式为_______。
(4)A→E反应的化学方程式为_______。
19.甲、乙、丙、丁、M是初中化学常见的化合物,其中甲、乙、丙、丁分属酸、碱、盐、氧化物中不同类别的化合物,M与甲属于同种类别的化合物。甲是石灰石的主要成分,它们之间的部分转化关系如图所示(部分反应物、生成物、反应条件已略去,“一”表示物质之间能发生反应,“→”表示物质之间的转化关系)。
(1)甲的化学式为_____,M的化学式为_____;
(2)乙→丙的反应方程式为_____;
(3)甲→M的反应类型为_____。
四、计算题
20.为了测定某石灰石中碳酸钙的质量分数,进行了如下实验:①在三个烧杯中都加入了10g样品;②向三个烧杯中加入质量不等、相同浓度的稀盐酸;③记录产生气体的质量。实验数据如下:
实验
加入稀盐酸的质量/g
W/g
烧杯Ⅰ
36.5
2.2
烧杯Ⅱ
73
3.52
烧杯Ⅲ
100
3.52
回答下列问题:
(1)样品中碳酸钙完全反应时,得到气体的质量为
g。
(2)样品中碳酸钙的质量分数是多少?
21.火山爆发时,大量水蒸气和二氧化硫混杂在火山灰中,随空气流动,大面积蔓延。
(1)二氧化硫()中硫和氧两种元素的质量比为______________。
(2)据专家估算,全球火山每年释放出数百亿千克的二氧化硫,二氧化硫在空气中经过一系列变化生成硫酸,加剧了酸雨污染。二氧化硫形成硫酸的化学方程式可表示为,试计算二氧化硫完全反应生成硫酸的质量______________。
(3)除火山等自然因素外,人类活动也会加剧酸雨的形成。写出一种有利于减少酸雨的措施:________________。
参考答案
1.C
2.A
3.A
4.C
5.C
6.D
7.C
8.C
9.B
10.C
11.A
12.B
13.D
14.2KMnO4K2MnO4+MnO2+O2↑
酒精灯
将集气瓶口向上
O2
15.集气瓶;
2KMnO4K2MnO4+MnO2+O2↑,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
防止生成的气体从长颈漏斗逸出
将生成的气体通入澄清石灰水,若澄清石灰水变浑浊,证明气体是二氧化碳;
③②①;
AD。
16.长颈漏斗
A
C
b
饱和的碳酸氢钠溶液
17.CH4
CH4
+
2O2
CO2
+
2H2O
Ca(OH)2+CO2═CaCO3↓+H2O
18.O2
CaCO3
做燃料(或冶炼金属)
2CO+O22CO2(或CuO+COCu+CO2)
化合反应
CO2+C2CO
CO2+Ca(OH)2=CaCO3↓+H2O
19.CaCO3
CaCl2
CaO+H2O=Ca(OH)2
复分解反应
20.(1)3.52
(2)80%
21.
植树造林(答案合理即可)
一、单选题
1.下列实验方案及操作中,合理的是( )
A.除去CO2中少量CO:将混合气体点燃
B.实验室制取CO2:利用稀硫酸和大理石反应
C.鉴别甲烷、一氧化碳、氢气三种气体:分别燃烧,检验燃烧产物
D.比较空气和人体呼出气体中CO2含量:向分别装有两种气体集气瓶中伸入燃着小木条
2.有关金刚石、石墨和C60的说法正确的是
A.都属于单质
B.元素组成不同
C.硬度相同
D.碳原子排列方式相同
3.化学与生活密切相关。生活中的下列做法不合理的是(
)
A.煤炉火上放一盆水,就能防止一氧化碳中毒
B.冰箱中的异味,可用活性炭除去
C.电器着火,应先切断电源再灭火
D.为防止煤气泄漏引发危险,可在煤气中添加有刺激性气味的乙硫醇
4.某合作学习小组讨论辨析以下说法:①CO2和KClO3中都含有氧元素,都是氧化物;②生活中常用煮沸法来降低水的硬度③有的元素有变价,在同种化合物里也可能显不同的化合价;④推广使用无氟冰箱防止“臭氧空洞”;⑤加高工厂烟囱可减少废气对大气的污染;⑥在食品袋中填充氮气可延长食品的保质期。其中正确的一组是( )
A.①②③④⑤⑥
B.②③④⑤⑥
C.②③④⑥
D.②④⑤⑥
5.水是生命之源,下列有关水的说法正确的是
A.水是常用的溶质
B.水汽化时分子大小发生了变化
C.正常雨水呈酸性
D.电解水得到氢气与氧气的质量比为2:1
6.燃烧柴禾时,通常把柴禾架空一些,才能燃烧得更旺,这是因为
A.散热的速度加快
B.聚集的热量增加
C.柴禾的着火点降低
D.柴禾与空气的接触面积增大
7.二氧化碳常用来对电器灭火,与之无关的性质是( )
A.本身不能燃烧
B.不支持燃烧
C.能溶于水
D.不导电
8.下列有关一氧化碳和二氧化碳的说法,正确的是
A.它们的分子构成相同
B.它们都溶于水
C.它们之间可以相互转化
D.闻气味可将它们区别
9.下列物质的用途体现其物理性质的是
A.小苏打用作发酵粉
B.干冰用于人工降雨
C.氧气用于医疗急救
D.氮气用作保护气
10.下列说法中错误的是
A.现代科学技术的进步与化学科学密切相关
B.煤、石油和天然气等都属于不可再生的化石燃料
C.酸雨的形成与P2.5有直接关系
D.废旧金属、化肥和农药很可能会造成水污染和土壤污染
11.下列有关碳和碳的氧化物的说法正确的是( )
A.干冰可用于人工降雨
B.金刚石和石墨都可用作电极
C.在常温下,碳的化学性质活泼
D.CO和CO2都具有还原性
12.80gFe2O3和CuO的固体混合物,在高温条件下与足量的CO充分反应后,得到金属的质量可能是(
)
A.50g
B.60g
C.70g
D.80g
13.下列化学方程式,表示正确的是(
)
A.紫色石蕊试液中,通入CO2时,溶液变红色
H2CO3═H2O+CO2↑
B.澄清石灰水中,通入CO2时,溶液变浑浊
CaCO3CaO+CO2↑
C.实验室用稀盐酸和大理石反应制CO2CaCO3+2HCl═CaCl2+H2CO3
D.一氧化碳在空气中燃烧生成CO22CO+O22CO2
二、实验题
14.根据下图回答问题。
(1)实验室用A制取氧气,反应的化学方程式是_____,还需补充的仪器是_____。
(2)实验室用B制取二氧化碳,装置中要改正的是_____。
(3)将上述实验收集的一瓶气体倒扣在燃着的蜡烛上(如图C所示),观察到蜡烛火焰更加明亮,一段时间后逐渐熄灭,则集气瓶中原有的气体是_____。
15.如图所示是实验室制取气体的常用装置,请根据要求回答问题。
(1)仪器a的名称是_____。利用装置A(添加蓬松棉花团)制取氧气时,反应的化学方程式是_____。利用装置B制取二氧化碳气体时,反应的化学方程式是_____;实验时,锥形瓶内长颈漏斗要插入液面以下,其原因是_____;检验二氧化碳的方法是_____。
(2)下面是利用装置E收集气体的操作,正确的实验操作顺序是_____(填序号)。
①待集气瓶内充满气体后,盖上玻璃片再移出水槽
②等到气泡连续且均匀时,再将导管口移入集气瓶
③将集气瓶注满水,用玻璃片盖上瓶口,倒立在盛水的水槽中
(3)已知:氨气(NH3)是一种具有刺激性气味的无色气体,密度比空气小,极易溶于水,实验室常用加热氯化铵和熟石灰两种固体的混合物来制备氨气。请你从图中选出制备一瓶氨气所需要的装置组合:_____。
16.某化学小组选用如图装置进行常见气体的实验室制取。提示:常温下CO2难溶于饱和的NaHCO3溶液。
回答下列问题:
(1)仪器①的名称为_____________。
(2)若实验室要加热KMnO4制取较纯净的氧气,选择的装置组合是____________和___________,反应的化学方程式为_____________。
(3)实验室常用大理石和稀盐酸,选取B、D装置制取CO2,制得的CO2中混有HC1。为了除去CO2中混有的HCl,可在B、D装置之间连接F装置,导管口a应连接______
(填
“b”或“c”),F装置中盛装的试剂为__________。
三、推断题
17.甲、乙、丙、丁是常见的化合物,它们有如下图所示转化关系(部分物质已略去)。甲是相对分子质量为16的气体;乙是最常见的液体;丁是白色难溶固体,其中金属元素的质量分数为40%。
(1)则甲的化学式为_____。(2)写出①②反应的化学方程式_____,_____
18.A~E是初中化学常见的物质,E是大理石的主要成分,D是能供给呼吸的气
体单质。它们的相互转化关系如图甲所示。“-”表示相互间能反应,“→”表示能转
化。部分反应条件、反应物、生成物已略去。图乙表示的是A、C的相关信息。
请回答下列问题。
(1)D、E的化学式分别为_______、_______,
(2)C的用途之一为_______,写出其相应的化学方程式:_______。
(3)①②③三个反应的基本反应类型都可能为_______,写出③反应的化学方程
式为_______。
(4)A→E反应的化学方程式为_______。
19.甲、乙、丙、丁、M是初中化学常见的化合物,其中甲、乙、丙、丁分属酸、碱、盐、氧化物中不同类别的化合物,M与甲属于同种类别的化合物。甲是石灰石的主要成分,它们之间的部分转化关系如图所示(部分反应物、生成物、反应条件已略去,“一”表示物质之间能发生反应,“→”表示物质之间的转化关系)。
(1)甲的化学式为_____,M的化学式为_____;
(2)乙→丙的反应方程式为_____;
(3)甲→M的反应类型为_____。
四、计算题
20.为了测定某石灰石中碳酸钙的质量分数,进行了如下实验:①在三个烧杯中都加入了10g样品;②向三个烧杯中加入质量不等、相同浓度的稀盐酸;③记录产生气体的质量。实验数据如下:
实验
加入稀盐酸的质量/g
W/g
烧杯Ⅰ
36.5
2.2
烧杯Ⅱ
73
3.52
烧杯Ⅲ
100
3.52
回答下列问题:
(1)样品中碳酸钙完全反应时,得到气体的质量为
g。
(2)样品中碳酸钙的质量分数是多少?
21.火山爆发时,大量水蒸气和二氧化硫混杂在火山灰中,随空气流动,大面积蔓延。
(1)二氧化硫()中硫和氧两种元素的质量比为______________。
(2)据专家估算,全球火山每年释放出数百亿千克的二氧化硫,二氧化硫在空气中经过一系列变化生成硫酸,加剧了酸雨污染。二氧化硫形成硫酸的化学方程式可表示为,试计算二氧化硫完全反应生成硫酸的质量______________。
(3)除火山等自然因素外,人类活动也会加剧酸雨的形成。写出一种有利于减少酸雨的措施:________________。
参考答案
1.C
2.A
3.A
4.C
5.C
6.D
7.C
8.C
9.B
10.C
11.A
12.B
13.D
14.2KMnO4K2MnO4+MnO2+O2↑
酒精灯
将集气瓶口向上
O2
15.集气瓶;
2KMnO4K2MnO4+MnO2+O2↑,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
防止生成的气体从长颈漏斗逸出
将生成的气体通入澄清石灰水,若澄清石灰水变浑浊,证明气体是二氧化碳;
③②①;
AD。
16.长颈漏斗
A
C
b
饱和的碳酸氢钠溶液
17.CH4
CH4
+
2O2
CO2
+
2H2O
Ca(OH)2+CO2═CaCO3↓+H2O
18.O2
CaCO3
做燃料(或冶炼金属)
2CO+O22CO2(或CuO+COCu+CO2)
化合反应
CO2+C2CO
CO2+Ca(OH)2=CaCO3↓+H2O
19.CaCO3
CaCl2
CaO+H2O=Ca(OH)2
复分解反应
20.(1)3.52
(2)80%
21.
植树造林(答案合理即可)
