人教版高中选修四化学4.1-原电池-课件(29张PPT)
文档属性
| 名称 | 人教版高中选修四化学4.1-原电池-课件(29张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-10-15 00:00:00 | ||
图片预览






文档简介
(共29张PPT)
第四章
电化学基础
第一节
原
电
池
1.
本节要点
构成原电池的条件?
3.
原电池的工作原理?
什么是原电池?
4.
原电池的正负极和电子流向如何判断?
2.
阅读材料
1780年意大利著名生物学家伽伐尼。解剖青蛙时,已死去的青蛙竟然发生了抽搐。伽伐尼做了如下实验:
实验1:
用一枝铜钩插入死青蛙的脊髓中,再挂在铁栏杆上,当青蛙腿碰到铁栏杆时,就发生颤抖。
实验2:将青蛙放到铜制的解剖盘里,当解剖刀接触蛙腿时,蛙腿发生抽搐.
他根据实验得出:青蛙自身肌肉和神经里的“生物电”是导致抽搐的原因。1791年,伽伐尼发表了《论肌肉中的生物电》论文,引起广泛关注。
善于质疑的意大利物理学家伏打,提出了疑问:为什么只有青蛙腿和铜器或铁器接触时才发生抽搐?他做了如下实验:
实验1:将青蛙腿放在铜盘里,用解剖刀去接触,蛙腿抽搐.
实验2:将青蛙腿放在木盘里,用解剖刀去接触,蛙腿不动.
伏打用实验推翻了伽伐尼的结论,认为要有两种活泼性不同的金属同时接触蛙腿,蛙腿才会抽搐。
由此,伏打加以研究,于1799年发明了世界上
第一个电池—伏打电池即原电池
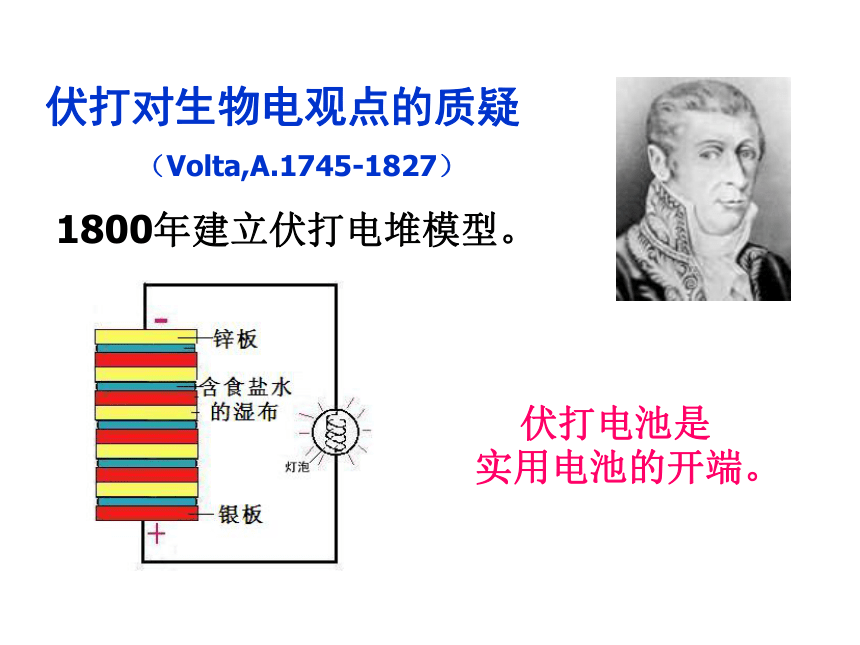
伏打对生物电观点的质疑
(Volta,A.1745-1827)
1800年建立伏打电堆模型。
伏打电池是
实用电池的开端。
回顾旧知
1、原电池
的装置。
原电池反应的本质是发生_____
________反应。
2、原电池的构成条件:
3、原电池正、负极规律
①负极——电子
的极。通常是活泼性
的金属,发生
反应
②正极——电子
的极。通常是活泼性
的金属或非金属导体,发生
反应
流出
较强
氧化
流入
较弱
还原
①有两种活泼性不同的金属(或其中一种为非金属导体)
②电解质溶液
③构成闭合回路
④能自发地发生氧化还原反应
将化学能转变为电能
氧化还原
实验探究
请根据反应:
Zn
+
CuSO4
=
ZnSO4
+
Cu
设计一个原电池,并进行实验。
CuSO4
溶液
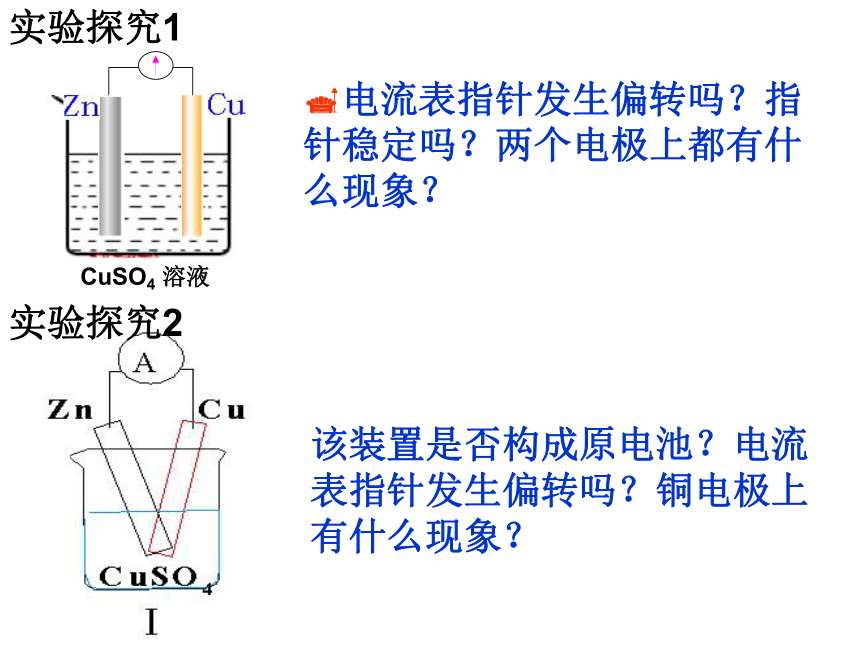
电流表指针发生偏转吗?指针稳定吗?两个电极上都有什么现象?
该装置是否构成原电池?电流表指针发生偏转吗?铜电极上有什么现象?
实验探究1
实验探究2
CuSO4
溶液
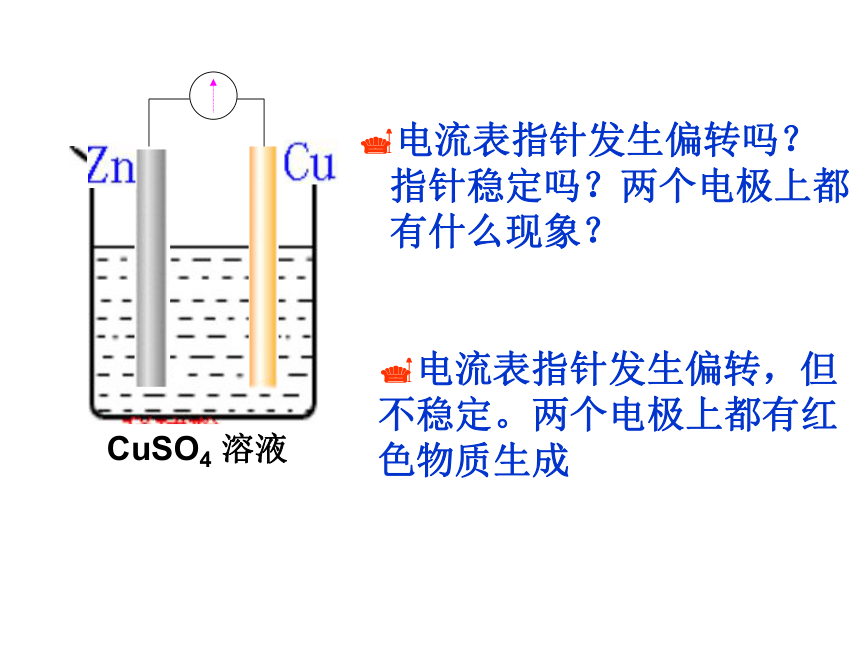
电流表指针发生偏转吗?指针稳定吗?两个电极上都有什么现象?
电流表指针发生偏转,但不稳定。两个电极上都有红色物质生成
补充实验1
现象:铜片表面明显有铜析出,锌片逐渐溶解,电流表指示无电流通过。
判断、假设:有原电池中电极反应的特点;电流表指针不动的原因可能与锌片与铜片直接接触有关。
问题:该装置是否构成原电池?电流表指针发生偏转吗?铜电极上有什么现象?
CuSO4
溶液
思考:如何才能得到持续稳定的电流?
分析:
由于锌片与硫酸铜溶液直接接触,铜在锌片表面析出,锌表面也构成了原电池,进一步加速铜在锌表面析出,致使向外输出的电流强度减弱。当锌片表面完全被铜覆盖后,不再构成原电池,也就没有电流产生。
在原有实验基础上进行改进,设计成一个能产生持续稳定电流的原电池。
实验探究
铜锌原电池
将化学能转变为电能的装置
1.组成——两个半电池、盐桥
②使两个烧杯中的溶液连成一个通路
盐桥的作用
①让溶液始终保持电中性使电极反应得以继续进行
盐桥:饱和
KCl
溶液(以琼
胶制作成冻胶)
一、原电池
2、工作原理
外电路:Zn失去电子沿导线通过电流表进入
铜片
内电路:
Zn原子失去电子成为Zn2+进入溶液,使ZnSO4溶液因Zn2+增加而带正电,盐桥中的Cl—会移向ZnSO4溶液;同时Cu2+获得电子成为金属沉淀在铜片上,使CuSO4溶液因SO42—相对增加而带负电,盐桥中的K+移向CuSO4溶液,从而形成闭合回路。
Zn——负极
3、电极反应
Cu——正极
一、原电池
Zn
-
2e-
=
Zn2+
总反应方程式:Zn+Cu2+=Zn2++Cu
已知反应AsO43-+2I-+2H+
AsO33-+I2+H2O
是可逆反应.设计如图装置,进行下述操作:
(Ⅰ)向(B)烧杯中逐滴加入浓盐酸,发现微安培表
指针偏转;(Ⅱ)若改往(B)烧杯中滴加40%NaOH
溶液,发现微安培表指针向前述相反方向偏转.
试回答:
(1)两次操作过程中指针为什么会发生偏转?
答:
。
(2)两次操作过程中指针偏转方向为什么会相反?试用平衡移动原理解释此现象.
答:____________________________________________________。
(3)(Ⅰ)操作过程中C1棒上发生的反应为
。
(4)(Ⅱ)操作过程中C2棒上发生的反应为
。
这是原电池,指针偏转是由于电子流过电流表
B中加盐酸,AsO43—发生得电子反应为正极;而当加入NaOH后,AsO33—发生失电子反应,为负极;
2I——2e—
=I2
AsO33——2e—+2OH-
=
AsO43—+H2O
拓展训练
练习
1.锌铜原电池产生电流时,阳离子(
)
A、移向Zn
极,阴离子移向Cu
极
B、移向Cu
极,阴离子移向Zn
极
C、和阴离子都移向Zn极
D、和阴离子都移向Cu
极
B
2.某金属能跟稀盐酸作用发出氢气,该金属与锌组成原电池时,锌为负极,此金属是(
)
A.Mg
B.Fe
C.Al
D.Cu
B
3.由铜锌和稀硫酸组成的原电池工作时,电解质溶液的
pH(
)
A.不变
B先变大后变小
C逐渐变大
D.逐渐变小
C
4.如图所示,在铁圈和银圈的焊接处,用一根棉线将其悬在盛水的烧杯中,使之平衡;小心的向烧杯中央滴入CuSO4溶液,片刻后可观察到的现象是(
)
铁圈和银圈左右摇摆不定
保持平衡状态
铁圈向下倾斜,银圈向上倾斜
D.
银圈向下倾斜,铁圈向上倾斜
5、利用原电池的反应原理:Cu+2AgNO3=2Ag+Cu(NO3)2设计一个能持续产生电流的原电池装置。
D
5、把a、b、c、d四块金属片浸入稀硫酸中,用导线两两相连组成原电池。若a、b相连时,a为负极;c、d相连时,电流由d到c;a、c相连时,c极上产生大量气泡,b、d相连时,b上有大量气泡产生,则四种金属的活动性顺序由强到弱的为
(
)
A.a
>
b
>
c
>
d
B.a
>
c
>
d
>
b
C.c
>
a
>
b
.>
d
D.b
>
d
>
c
>
a
6.下列哪几个装置能形成原电池?
A
B
C
D
E
F
A
B
E
H
Zn
Cu
H2SO4
G
H
拓展练习
(1)若烧杯中溶液为稀硫酸,则观察到的
现象。
两极反应式为:正极
;
负极
。
该装置将
能转化为
能。
(2)若烧杯中溶液为氢氧化钠溶液,
则负极为
,
总反应方程为
。
镁逐渐溶解,铝极上有气泡冒出,电流表指针发生偏转;
2H++2e—=H2↑
Mg-2e—=Mg2+
化学能
电能
Al
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
(1)比较金属活动性强弱。
例1:
下列叙述中,可以说明金属甲比乙活泼性强的是
C.将甲乙作电极组成原电池时甲是负极;
A.甲和乙用导线连接插入稀盐酸溶液中,乙溶解,甲
上有H2气放出;
B.在氧化–还原反应中,甲比乙失去的电子多;
D.同价态的阳离子,甲比乙的氧化性强;
(C)
原电池原理应用:
(2)比较反应速率
例2
:
下列制氢气的反应速率最快的是
粗锌和
1mol/L
盐酸;
B.
A.
纯锌和1mol/L
硫酸;
纯锌和18
mol/L
硫酸;
C.
粗锌和1mol/L
硫酸的反应中加入几滴CuSO4溶液。
D.
(
D
)
原电池原理应用:
(3)比较金属腐蚀的快慢
例3:
下列各情况,在其中Fe片腐蚀由快到慢的顺序是
(5)
(2)
(1)
(3)
(4)
原电池原理应用:
例4:
下列装置中四块相同的Zn片,放置一段时间后腐蚀速
率由慢到快的顺序是
(4)
(2)
(1)
(3)
(4)判断溶液pH值变化
例5:
在Cu-Zn原电池中,200mLH2SO4
溶液的浓度为0.125mol/L
,
若工作一段时间后,从装置中共收集到
0.168L升气体,则流过导线的电子为————
mol,溶液的pH值变_________?(溶液体积变化忽略不计)
0.2
解得:
y
=0.015
(mol)
x
=0.015
(mol)
=
=3.75×
10﹣
4(mol/L
)
∴pH
=-lg3.75
×10-4
=4
-lg3.75
答:……
-0.015
根据电极反应:
正极:
负极:
Zn-2e-=Zn2+
2H++2e-
=H2↑
得:
2
2
22.4
x
y
0.168
解:
0.2×0.125×2
c(H+)余
∴
2H+
——
2e——H2↑
大
0.015
原电池原理应用:
(5)原电池原理的综合应用
例6:市场上出售的“热敷袋”的主要成分为铁屑、炭粉、木屑、少量氯化钠和水等。
“热敷袋”启用之前用塑料袋使其与空气隔绝,启用时,打开塑料袋轻轻揉搓就会放出热量。使用完后,会发现有大量铁锈存在。
“热敷袋”是利用
放出热量。
2)炭粉的主要作用是
。
3)加入氯化钠的主要作用是
。
4)木屑的作用是
。
铁被氧化
与铁屑、氯化钠溶液构成原电池,加速铁屑的氧化
氯化钠溶于水、形成电解质溶液
使用“热敷袋”时受热均匀
原电池原理应用:
第四章
电化学基础
第一节
原
电
池
1.
本节要点
构成原电池的条件?
3.
原电池的工作原理?
什么是原电池?
4.
原电池的正负极和电子流向如何判断?
2.
阅读材料
1780年意大利著名生物学家伽伐尼。解剖青蛙时,已死去的青蛙竟然发生了抽搐。伽伐尼做了如下实验:
实验1:
用一枝铜钩插入死青蛙的脊髓中,再挂在铁栏杆上,当青蛙腿碰到铁栏杆时,就发生颤抖。
实验2:将青蛙放到铜制的解剖盘里,当解剖刀接触蛙腿时,蛙腿发生抽搐.
他根据实验得出:青蛙自身肌肉和神经里的“生物电”是导致抽搐的原因。1791年,伽伐尼发表了《论肌肉中的生物电》论文,引起广泛关注。
善于质疑的意大利物理学家伏打,提出了疑问:为什么只有青蛙腿和铜器或铁器接触时才发生抽搐?他做了如下实验:
实验1:将青蛙腿放在铜盘里,用解剖刀去接触,蛙腿抽搐.
实验2:将青蛙腿放在木盘里,用解剖刀去接触,蛙腿不动.
伏打用实验推翻了伽伐尼的结论,认为要有两种活泼性不同的金属同时接触蛙腿,蛙腿才会抽搐。
由此,伏打加以研究,于1799年发明了世界上
第一个电池—伏打电池即原电池
伏打对生物电观点的质疑
(Volta,A.1745-1827)
1800年建立伏打电堆模型。
伏打电池是
实用电池的开端。
回顾旧知
1、原电池
的装置。
原电池反应的本质是发生_____
________反应。
2、原电池的构成条件:
3、原电池正、负极规律
①负极——电子
的极。通常是活泼性
的金属,发生
反应
②正极——电子
的极。通常是活泼性
的金属或非金属导体,发生
反应
流出
较强
氧化
流入
较弱
还原
①有两种活泼性不同的金属(或其中一种为非金属导体)
②电解质溶液
③构成闭合回路
④能自发地发生氧化还原反应
将化学能转变为电能
氧化还原
实验探究
请根据反应:
Zn
+
CuSO4
=
ZnSO4
+
Cu
设计一个原电池,并进行实验。
CuSO4
溶液
电流表指针发生偏转吗?指针稳定吗?两个电极上都有什么现象?
该装置是否构成原电池?电流表指针发生偏转吗?铜电极上有什么现象?
实验探究1
实验探究2
CuSO4
溶液
电流表指针发生偏转吗?指针稳定吗?两个电极上都有什么现象?
电流表指针发生偏转,但不稳定。两个电极上都有红色物质生成
补充实验1
现象:铜片表面明显有铜析出,锌片逐渐溶解,电流表指示无电流通过。
判断、假设:有原电池中电极反应的特点;电流表指针不动的原因可能与锌片与铜片直接接触有关。
问题:该装置是否构成原电池?电流表指针发生偏转吗?铜电极上有什么现象?
CuSO4
溶液
思考:如何才能得到持续稳定的电流?
分析:
由于锌片与硫酸铜溶液直接接触,铜在锌片表面析出,锌表面也构成了原电池,进一步加速铜在锌表面析出,致使向外输出的电流强度减弱。当锌片表面完全被铜覆盖后,不再构成原电池,也就没有电流产生。
在原有实验基础上进行改进,设计成一个能产生持续稳定电流的原电池。
实验探究
铜锌原电池
将化学能转变为电能的装置
1.组成——两个半电池、盐桥
②使两个烧杯中的溶液连成一个通路
盐桥的作用
①让溶液始终保持电中性使电极反应得以继续进行
盐桥:饱和
KCl
溶液(以琼
胶制作成冻胶)
一、原电池
2、工作原理
外电路:Zn失去电子沿导线通过电流表进入
铜片
内电路:
Zn原子失去电子成为Zn2+进入溶液,使ZnSO4溶液因Zn2+增加而带正电,盐桥中的Cl—会移向ZnSO4溶液;同时Cu2+获得电子成为金属沉淀在铜片上,使CuSO4溶液因SO42—相对增加而带负电,盐桥中的K+移向CuSO4溶液,从而形成闭合回路。
Zn——负极
3、电极反应
Cu——正极
一、原电池
Zn
-
2e-
=
Zn2+
总反应方程式:Zn+Cu2+=Zn2++Cu
已知反应AsO43-+2I-+2H+
AsO33-+I2+H2O
是可逆反应.设计如图装置,进行下述操作:
(Ⅰ)向(B)烧杯中逐滴加入浓盐酸,发现微安培表
指针偏转;(Ⅱ)若改往(B)烧杯中滴加40%NaOH
溶液,发现微安培表指针向前述相反方向偏转.
试回答:
(1)两次操作过程中指针为什么会发生偏转?
答:
。
(2)两次操作过程中指针偏转方向为什么会相反?试用平衡移动原理解释此现象.
答:____________________________________________________。
(3)(Ⅰ)操作过程中C1棒上发生的反应为
。
(4)(Ⅱ)操作过程中C2棒上发生的反应为
。
这是原电池,指针偏转是由于电子流过电流表
B中加盐酸,AsO43—发生得电子反应为正极;而当加入NaOH后,AsO33—发生失电子反应,为负极;
2I——2e—
=I2
AsO33——2e—+2OH-
=
AsO43—+H2O
拓展训练
练习
1.锌铜原电池产生电流时,阳离子(
)
A、移向Zn
极,阴离子移向Cu
极
B、移向Cu
极,阴离子移向Zn
极
C、和阴离子都移向Zn极
D、和阴离子都移向Cu
极
B
2.某金属能跟稀盐酸作用发出氢气,该金属与锌组成原电池时,锌为负极,此金属是(
)
A.Mg
B.Fe
C.Al
D.Cu
B
3.由铜锌和稀硫酸组成的原电池工作时,电解质溶液的
pH(
)
A.不变
B先变大后变小
C逐渐变大
D.逐渐变小
C
4.如图所示,在铁圈和银圈的焊接处,用一根棉线将其悬在盛水的烧杯中,使之平衡;小心的向烧杯中央滴入CuSO4溶液,片刻后可观察到的现象是(
)
铁圈和银圈左右摇摆不定
保持平衡状态
铁圈向下倾斜,银圈向上倾斜
D.
银圈向下倾斜,铁圈向上倾斜
5、利用原电池的反应原理:Cu+2AgNO3=2Ag+Cu(NO3)2设计一个能持续产生电流的原电池装置。
D
5、把a、b、c、d四块金属片浸入稀硫酸中,用导线两两相连组成原电池。若a、b相连时,a为负极;c、d相连时,电流由d到c;a、c相连时,c极上产生大量气泡,b、d相连时,b上有大量气泡产生,则四种金属的活动性顺序由强到弱的为
(
)
A.a
>
b
>
c
>
d
B.a
>
c
>
d
>
b
C.c
>
a
>
b
.>
d
D.b
>
d
>
c
>
a
6.下列哪几个装置能形成原电池?
A
B
C
D
E
F
A
B
E
H
Zn
Cu
H2SO4
G
H
拓展练习
(1)若烧杯中溶液为稀硫酸,则观察到的
现象。
两极反应式为:正极
;
负极
。
该装置将
能转化为
能。
(2)若烧杯中溶液为氢氧化钠溶液,
则负极为
,
总反应方程为
。
镁逐渐溶解,铝极上有气泡冒出,电流表指针发生偏转;
2H++2e—=H2↑
Mg-2e—=Mg2+
化学能
电能
Al
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
(1)比较金属活动性强弱。
例1:
下列叙述中,可以说明金属甲比乙活泼性强的是
C.将甲乙作电极组成原电池时甲是负极;
A.甲和乙用导线连接插入稀盐酸溶液中,乙溶解,甲
上有H2气放出;
B.在氧化–还原反应中,甲比乙失去的电子多;
D.同价态的阳离子,甲比乙的氧化性强;
(C)
原电池原理应用:
(2)比较反应速率
例2
:
下列制氢气的反应速率最快的是
粗锌和
1mol/L
盐酸;
B.
A.
纯锌和1mol/L
硫酸;
纯锌和18
mol/L
硫酸;
C.
粗锌和1mol/L
硫酸的反应中加入几滴CuSO4溶液。
D.
(
D
)
原电池原理应用:
(3)比较金属腐蚀的快慢
例3:
下列各情况,在其中Fe片腐蚀由快到慢的顺序是
(5)
(2)
(1)
(3)
(4)
原电池原理应用:
例4:
下列装置中四块相同的Zn片,放置一段时间后腐蚀速
率由慢到快的顺序是
(4)
(2)
(1)
(3)
(4)判断溶液pH值变化
例5:
在Cu-Zn原电池中,200mLH2SO4
溶液的浓度为0.125mol/L
,
若工作一段时间后,从装置中共收集到
0.168L升气体,则流过导线的电子为————
mol,溶液的pH值变_________?(溶液体积变化忽略不计)
0.2
解得:
y
=0.015
(mol)
x
=0.015
(mol)
=
=3.75×
10﹣
4(mol/L
)
∴pH
=-lg3.75
×10-4
=4
-lg3.75
答:……
-0.015
根据电极反应:
正极:
负极:
Zn-2e-=Zn2+
2H++2e-
=H2↑
得:
2
2
22.4
x
y
0.168
解:
0.2×0.125×2
c(H+)余
∴
2H+
——
2e——H2↑
大
0.015
原电池原理应用:
(5)原电池原理的综合应用
例6:市场上出售的“热敷袋”的主要成分为铁屑、炭粉、木屑、少量氯化钠和水等。
“热敷袋”启用之前用塑料袋使其与空气隔绝,启用时,打开塑料袋轻轻揉搓就会放出热量。使用完后,会发现有大量铁锈存在。
“热敷袋”是利用
放出热量。
2)炭粉的主要作用是
。
3)加入氯化钠的主要作用是
。
4)木屑的作用是
。
铁被氧化
与铁屑、氯化钠溶液构成原电池,加速铁屑的氧化
氯化钠溶于水、形成电解质溶液
使用“热敷袋”时受热均匀
原电池原理应用:
