人教版选修五高二化学3.3《羧酸 酯》课件(30张PPT)
文档属性
| 名称 | 人教版选修五高二化学3.3《羧酸 酯》课件(30张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-10-17 00:00:00 | ||
图片预览









文档简介
(共34张PPT)
第三章
烃的含氧衍生物
醋酸
CH3COOH
第三节
羧酸
酯
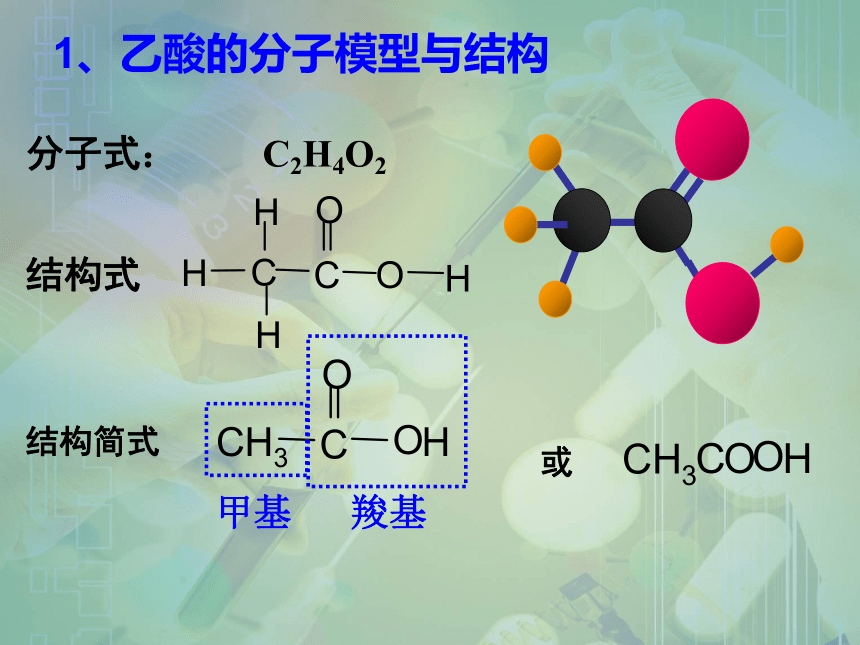
1、乙酸的分子模型与结构
甲基
羧基
分子式:
结构式
结构简式
或
C2H4O2
2、乙酸的物理性质
颜色、状态:
气味:
沸点:
熔点:
溶解性:
无色液体
有强烈刺激性气味
117.9℃
(易挥发)
16.6℃
易溶于水、乙醇等溶剂
(无水乙酸又称为:冰醋酸)
E、与某些盐反应:
A、使紫色石蕊试液变色:
B、与活泼金属反应:
D、与碱反应:
C、与碱性氧化物反应:
3、乙酸的化学性质
(1)
酸性:
CH3COOH
CH3COO-+H+
【思考与交流】
必修Ⅰ已介绍过乙酸是一种有机弱酸。请同学们根据
现有的化学药品设计实验方案:
(1)证明乙酸确有酸性;(2)比较乙酸与碳酸的酸性的强弱。
方案1:
方案2:
方案3:
方案4:
方案5:
往镁粉中加入乙酸
Mg
+
2CH3COOH
=
(CH3COO)2
Mg+
H2↑
乙酸和NaOH溶液混合(滴加酚酞)。
NaOH
+
CH3COOH
=
CH3COONa
+
H2O
乙酸和MgO悬浊液混合。
2CH3COOH
+
MgO
=
(CH3COO)2Mg
+
H2O
往Na2CO3粉末中加入乙酸。
2CH3COOH
+
Na2CO3
=
2
CH3COONa
+
CO2
↑
+
H2O
乙酸使石蕊变色
科
学
探
究
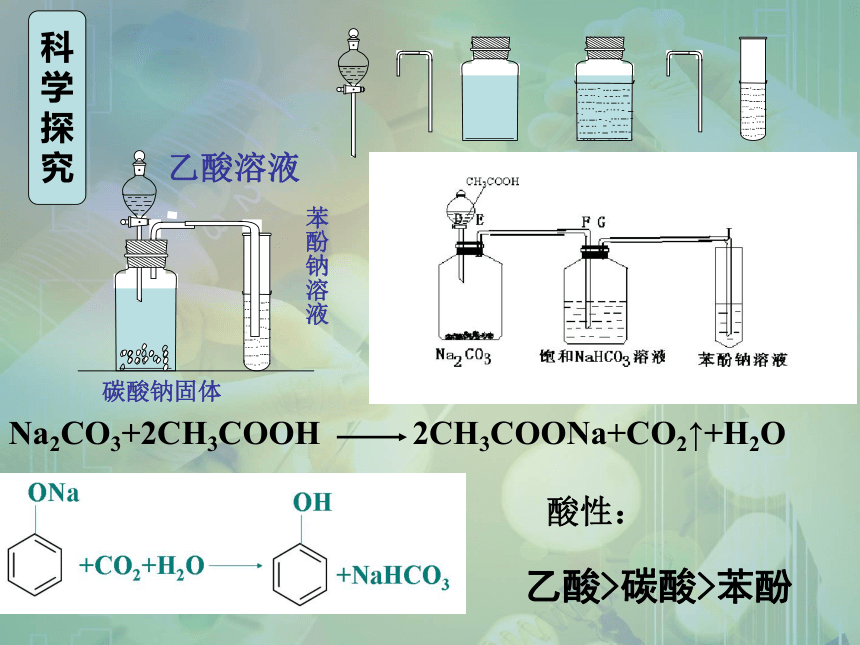
碳酸钠固体
乙酸溶液
苯酚钠溶液
酸性:
Na2CO3+2CH3COOH
2CH3COONa+CO2↑+H2O
乙酸>碳酸>苯酚
【思考
交流】
证明乙酸是弱酸的方法:
1
2
3
4
5
CH3COOH
CH3COO-+H+
思考1:可以用几种方法证明乙酸是弱酸?
厨师烧鱼时常加醋并加点酒,这样鱼的味道就变得无腥、香醇,特别鲜美。
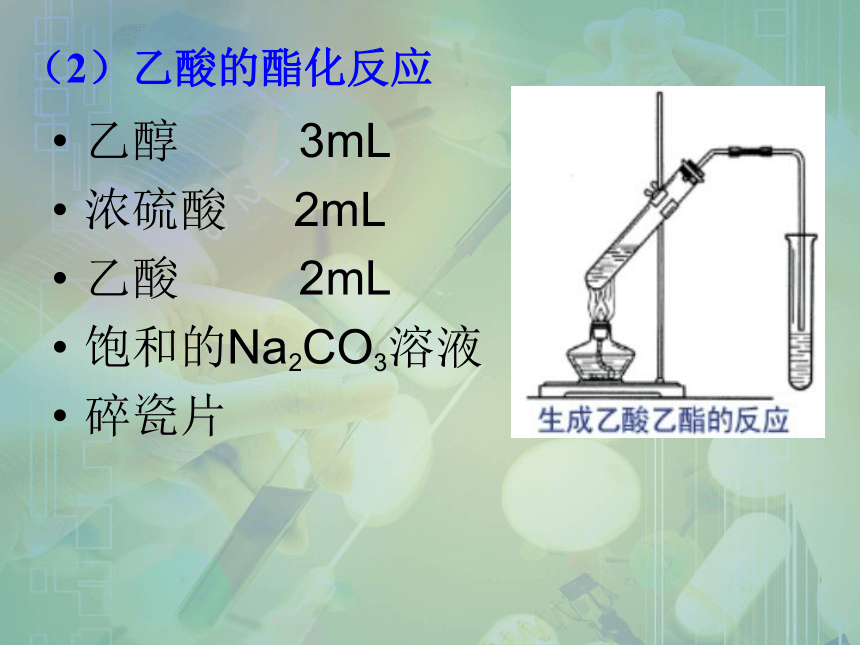
乙醇
3mL
浓硫酸
2mL
乙酸
2mL
饱和的Na2CO3溶液
碎瓷片
(2)乙酸的酯化反应
酯类广泛存在于自然界中
酯是有芳香气味的液体,存在于各种水果和花草中。如梨里含有乙酸异戊酯,苹果和香蕉里含有异戊酸异戊酯等。酯的密度一般小于水,并难溶于水,易溶于乙醇和乙醚等有机溶剂。酯可用作溶剂,也可用作制备饮料和糖果的香料。
【知识回顾】
1.浓硫酸的作用是什么?
2.得到的反应产物是否纯净?主要杂质有哪些?
3.饱和Na2CO3溶液有什么作用?
4.
为什么导管不插入饱和Na2CO3溶液中?有无其它防倒吸的方法?
催化剂,吸水剂
不纯净;乙酸、乙醇
①
中和乙酸,消除乙酸气味对酯气味的影响,以便闻到乙酸乙酯的气味.
②
溶解乙醇。
③
冷凝酯蒸气、降低酯在水中的溶解度,以便使酯分层析出。
防止受热不匀发生倒吸
【探究】乙酸乙酯的酯化过程
——酯化反应的脱水方式
可能一
可能二
同位素示踪法
酯化反应的本质:酸脱羟基、醇脱羟基氢。
CH3COOH
+
H18OCH2
CH3
浓硫酸
△
+
H2O
CH3COO18CH2
CH3
实验验证
是一种重要的化工原料
在日常生活中也有广泛的用途
3)乙酸的用途
O
CH3—C—O—H
小结:
酸性
酯化
自然界和日常生活中的有机酸
资料卡片
蚁酸(甲酸)
HCOOH
柠檬酸
HO—C—COOH
CH2—COOH
CH2—COOH
未成熟的梅子、李子、杏子等水果中,含有草酸、安息香酸等成分
草酸
(乙二酸)
COOH
COOH
安息香酸
(苯甲酸)
COOH
CH2COOH
CH(OH)COOH
苹果酸
CH3COOH
醋酸(乙酸)
CH3CHCOOH
OH
乳酸
二、羧酸
1、定义:
由烃基(或氢)与羧基相连构成的有机化合物。
2、分类:
烃基不同
羧基数目
芳香酸
脂肪酸
一元羧酸
二元羧酸
多元羧酸
CH3COOH
C17H35COOH
硬脂酸
CH2=CHCOOH
C17H33COOH
油酸
C6H5COOH
HOOC-COOH
HO—C—COOH
CH2—COOH
CH2—COOH
CH3COOH
3、结构
①一元羧酸通式:R—COOH
②饱和一元羧酸的通式:
CnH2n+1COOH
或CnH2nO2
③多元羧酸中含有多个羧基。
4、化学性质
(1)酸性
(2)酯化反应
1、
酯化反应属于(
).
A.中和反应
B.不可逆反应
C.离子反应
D.取代反应
D
课堂练习
2.胆固醇是人体必须的生物活性物质,分子式为C27H46O。一种胆固醇酯是液晶材料,分子式为C34H50O2,生成这种胆固醇酯的羧酸是(
)
C6H13COOH
B.C6H5COOH
C.C7H15COOH
D.C6H5CH2COOH
B
R’COOH
+
R’’-OH
R’COOR’’
+
H2O
浓硫酸
△
3.确定乙酸是弱酸的依据是(
)
A.乙酸可以和乙醇发生酯化反应
B.乙酸钠的水溶液显碱性
C.乙酸能使石蕊试液变红
D.Na2CO3中加入乙酸产生CO2
B
4、请用一种试剂鉴别下面三种有机物?
乙醇、乙醛、乙酸
新制Cu(OH)2悬浊液
三、两种重要的羧酸
1、甲酸
——俗称蚁酸
结构特点:既有羧基又有醛基
化学性质
醛基
羧基
氧化反应(如银镜反应)
酸性,酯化反应
O
H—C—O—H
2、乙二酸
——俗称草酸
+
2H2O
【知识迁移】写出下列酸和醇的酯化反应
CH3COOCH3
+
H2O
CH3COOH
+
HOCH3
乙酸甲酯
足量
浓H2SO4
二乙酸乙二酯
浓H2SO4
代表物
结构简式
羟基氢的活泼性
酸性
与钠反应
与NaOH的反应
与Na2CO3的反应
乙醇
苯酚
乙酸
CH3CH2OH
C6H5OH
CH3COOH
增强
中性
比碳酸弱
比碳酸强
能
能
能
能
能
不能
不能
能
能,不产
生CO2
醇、酚、羧酸中羟基的比较
【知识归纳】
辨
析
配制一定浓度的乙酸测定PH值
配制一定浓度的乙酸钠溶液测定PH值
在相同条件下与同浓度的盐酸
比较与金属反应的速率
取少量乙酸溶液,加入石蕊试液,
加热后再次观察颜色变化
取少量乙酸,用PH试纸检测其PH值,
再加入一定量乙酸钠晶体,再次检测PH值。
第三章
烃的含氧衍生物
醋酸
CH3COOH
第三节
羧酸
酯
1、乙酸的分子模型与结构
甲基
羧基
分子式:
结构式
结构简式
或
C2H4O2
2、乙酸的物理性质
颜色、状态:
气味:
沸点:
熔点:
溶解性:
无色液体
有强烈刺激性气味
117.9℃
(易挥发)
16.6℃
易溶于水、乙醇等溶剂
(无水乙酸又称为:冰醋酸)
E、与某些盐反应:
A、使紫色石蕊试液变色:
B、与活泼金属反应:
D、与碱反应:
C、与碱性氧化物反应:
3、乙酸的化学性质
(1)
酸性:
CH3COOH
CH3COO-+H+
【思考与交流】
必修Ⅰ已介绍过乙酸是一种有机弱酸。请同学们根据
现有的化学药品设计实验方案:
(1)证明乙酸确有酸性;(2)比较乙酸与碳酸的酸性的强弱。
方案1:
方案2:
方案3:
方案4:
方案5:
往镁粉中加入乙酸
Mg
+
2CH3COOH
=
(CH3COO)2
Mg+
H2↑
乙酸和NaOH溶液混合(滴加酚酞)。
NaOH
+
CH3COOH
=
CH3COONa
+
H2O
乙酸和MgO悬浊液混合。
2CH3COOH
+
MgO
=
(CH3COO)2Mg
+
H2O
往Na2CO3粉末中加入乙酸。
2CH3COOH
+
Na2CO3
=
2
CH3COONa
+
CO2
↑
+
H2O
乙酸使石蕊变色
科
学
探
究
碳酸钠固体
乙酸溶液
苯酚钠溶液
酸性:
Na2CO3+2CH3COOH
2CH3COONa+CO2↑+H2O
乙酸>碳酸>苯酚
【思考
交流】
证明乙酸是弱酸的方法:
1
2
3
4
5
CH3COOH
CH3COO-+H+
思考1:可以用几种方法证明乙酸是弱酸?
厨师烧鱼时常加醋并加点酒,这样鱼的味道就变得无腥、香醇,特别鲜美。
乙醇
3mL
浓硫酸
2mL
乙酸
2mL
饱和的Na2CO3溶液
碎瓷片
(2)乙酸的酯化反应
酯类广泛存在于自然界中
酯是有芳香气味的液体,存在于各种水果和花草中。如梨里含有乙酸异戊酯,苹果和香蕉里含有异戊酸异戊酯等。酯的密度一般小于水,并难溶于水,易溶于乙醇和乙醚等有机溶剂。酯可用作溶剂,也可用作制备饮料和糖果的香料。
【知识回顾】
1.浓硫酸的作用是什么?
2.得到的反应产物是否纯净?主要杂质有哪些?
3.饱和Na2CO3溶液有什么作用?
4.
为什么导管不插入饱和Na2CO3溶液中?有无其它防倒吸的方法?
催化剂,吸水剂
不纯净;乙酸、乙醇
①
中和乙酸,消除乙酸气味对酯气味的影响,以便闻到乙酸乙酯的气味.
②
溶解乙醇。
③
冷凝酯蒸气、降低酯在水中的溶解度,以便使酯分层析出。
防止受热不匀发生倒吸
【探究】乙酸乙酯的酯化过程
——酯化反应的脱水方式
可能一
可能二
同位素示踪法
酯化反应的本质:酸脱羟基、醇脱羟基氢。
CH3COOH
+
H18OCH2
CH3
浓硫酸
△
+
H2O
CH3COO18CH2
CH3
实验验证
是一种重要的化工原料
在日常生活中也有广泛的用途
3)乙酸的用途
O
CH3—C—O—H
小结:
酸性
酯化
自然界和日常生活中的有机酸
资料卡片
蚁酸(甲酸)
HCOOH
柠檬酸
HO—C—COOH
CH2—COOH
CH2—COOH
未成熟的梅子、李子、杏子等水果中,含有草酸、安息香酸等成分
草酸
(乙二酸)
COOH
COOH
安息香酸
(苯甲酸)
COOH
CH2COOH
CH(OH)COOH
苹果酸
CH3COOH
醋酸(乙酸)
CH3CHCOOH
OH
乳酸
二、羧酸
1、定义:
由烃基(或氢)与羧基相连构成的有机化合物。
2、分类:
烃基不同
羧基数目
芳香酸
脂肪酸
一元羧酸
二元羧酸
多元羧酸
CH3COOH
C17H35COOH
硬脂酸
CH2=CHCOOH
C17H33COOH
油酸
C6H5COOH
HOOC-COOH
HO—C—COOH
CH2—COOH
CH2—COOH
CH3COOH
3、结构
①一元羧酸通式:R—COOH
②饱和一元羧酸的通式:
CnH2n+1COOH
或CnH2nO2
③多元羧酸中含有多个羧基。
4、化学性质
(1)酸性
(2)酯化反应
1、
酯化反应属于(
).
A.中和反应
B.不可逆反应
C.离子反应
D.取代反应
D
课堂练习
2.胆固醇是人体必须的生物活性物质,分子式为C27H46O。一种胆固醇酯是液晶材料,分子式为C34H50O2,生成这种胆固醇酯的羧酸是(
)
C6H13COOH
B.C6H5COOH
C.C7H15COOH
D.C6H5CH2COOH
B
R’COOH
+
R’’-OH
R’COOR’’
+
H2O
浓硫酸
△
3.确定乙酸是弱酸的依据是(
)
A.乙酸可以和乙醇发生酯化反应
B.乙酸钠的水溶液显碱性
C.乙酸能使石蕊试液变红
D.Na2CO3中加入乙酸产生CO2
B
4、请用一种试剂鉴别下面三种有机物?
乙醇、乙醛、乙酸
新制Cu(OH)2悬浊液
三、两种重要的羧酸
1、甲酸
——俗称蚁酸
结构特点:既有羧基又有醛基
化学性质
醛基
羧基
氧化反应(如银镜反应)
酸性,酯化反应
O
H—C—O—H
2、乙二酸
——俗称草酸
+
2H2O
【知识迁移】写出下列酸和醇的酯化反应
CH3COOCH3
+
H2O
CH3COOH
+
HOCH3
乙酸甲酯
足量
浓H2SO4
二乙酸乙二酯
浓H2SO4
代表物
结构简式
羟基氢的活泼性
酸性
与钠反应
与NaOH的反应
与Na2CO3的反应
乙醇
苯酚
乙酸
CH3CH2OH
C6H5OH
CH3COOH
增强
中性
比碳酸弱
比碳酸强
能
能
能
能
能
不能
不能
能
能,不产
生CO2
醇、酚、羧酸中羟基的比较
【知识归纳】
辨
析
配制一定浓度的乙酸测定PH值
配制一定浓度的乙酸钠溶液测定PH值
在相同条件下与同浓度的盐酸
比较与金属反应的速率
取少量乙酸溶液,加入石蕊试液,
加热后再次观察颜色变化
取少量乙酸,用PH试纸检测其PH值,
再加入一定量乙酸钠晶体,再次检测PH值。
