新人教版必修2高中化学3.3:生活中两种常见的有机物(68张PPT)
文档属性
| 名称 | 新人教版必修2高中化学3.3:生活中两种常见的有机物(68张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 3.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-10-19 00:00:00 | ||
图片预览









文档简介
(共69张PPT)
清明时节雨纷纷,
路上行人欲断魂。
借问酒家何处有?
牧童遥指杏花村。
明月几时有?
把酒问青天!
酒之于药主要有四个方面的作用:
1.行药势,古人谓“酒为诸药之长”;?
2.有助于药物有效成分的析出;
3.防腐作用;
4.现代医学认为,适量饮酒能增加唾液和胃液的分泌,促进胃肠的消化和吸收;促进血液循环;精神兴奋,强心提神,消除疲劳,促进睡眠等。在一定程度上可减少心脏病和脑中风的发作危险。
溶剂
饮料
消毒剂(75%的乙醇溶液)
燃料
让我
看一看?
想一想?
颜
色
:
气
味
:
状
态:
挥发性:
密
度:
溶解性:
无色透明
特殊香味
液体
比水小
跟水以任意比互溶
能够溶解多种无机物和有机物
易挥发
一、乙醇
1、乙醇的物理性质
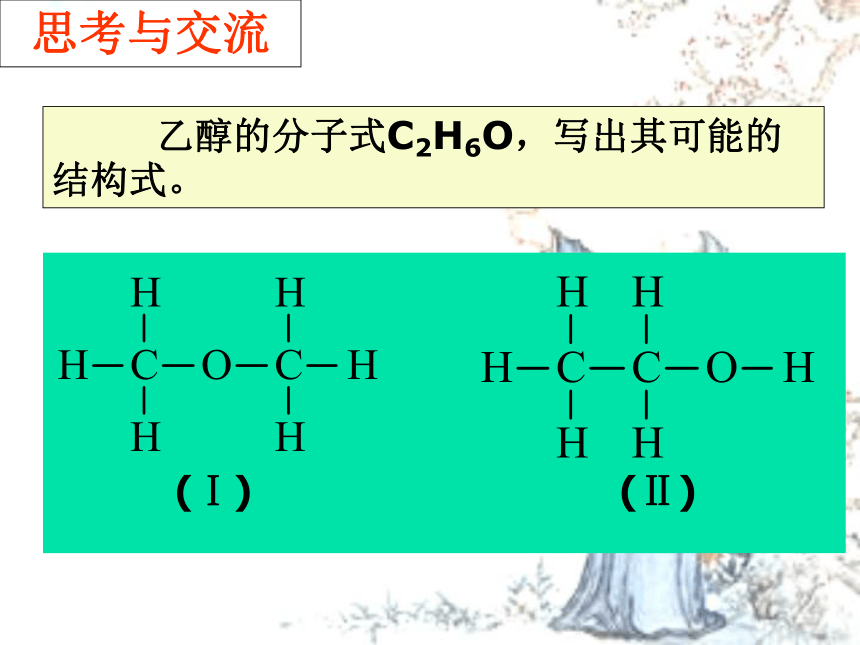
思考与交流
乙醇的分子式C2H6O,写出其可能的结构式。
(Ⅰ)
(Ⅱ)
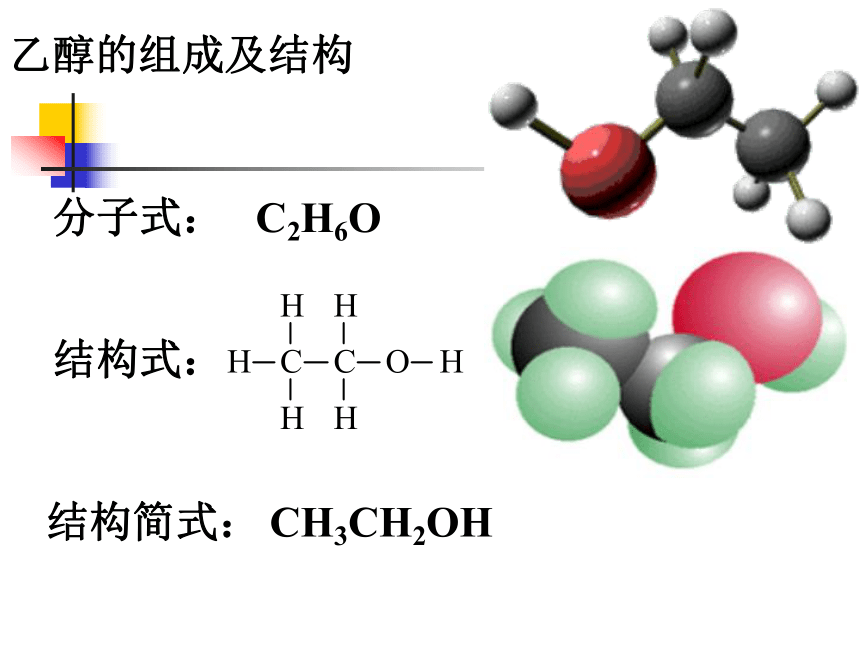
乙醇的组成及结构
C2H6O
分子式:
结构式:
结构简式:
CH3CH2OH
羟基与氢氧根离子的比较
羟基
氢氧根离子
电子式
电荷数
存在形式
相同点
不显电性
带一个单位负电荷
组成元素相同
能独立存在于离子晶体或溶液中
不能独立存在
.
..
..
H
O
..
O
..
..
..
H
..
注意:
1、几个概念
①羟基:
有机化合物分子中含有_____的基团,称为羟基
②烃的衍生物:从结构上看,烃分子中的氢原子被其他_________________所取代而生成的一系列化合物成为烃的衍生物。
③官能团:使烃的衍生物具有不同于烃的特殊性质的__________,称为官能团。
-OH
原子或原子团
基团
注意:
H—O—H
H+
+
OH-
C2H5—O—H
?
现象:试管中有气体生成,可以燃烧,烧杯内壁出现水滴,石灰水不变浑浊.
结论:气体是氢气
演示:钠与无水酒精的反应
[学生实验]将两块金属钠分别投入盛有冷水和乙醇的小烧杯中,观察钠与水、与乙醇反应的现象有何异、同?哪一个更剧烈?填写下表:
钠与水
钠与乙醇
钠是否浮在液面上
钠的形状是否变化
有无声音
有无气泡
剧烈程度
反应方程式
剧烈
缓慢
2Na+2H2O=
2
NaOH
+H2↑
沉在底部
形状不变
响声很小
放出气泡
浮在水面
熔成球形
发出嘶声
放出气体
金属钠的变化
气体燃烧现象
检验产物
水
乙醇
“浮、熔、
游、响”
“沉、不熔、
不响”
发出淡蓝
色火焰。
安静燃烧,发出
淡蓝色火焰,
烧杯内壁有水珠
加酚酞后溶液变红,
说明有碱性物质
(NaOH)生成。
加酚酞后溶液变红,
说明有碱性物质生成;
烧杯中石灰水无明显现
象,说明无CO2生成。
比较水、乙醇与钠反应
思考:乙醇分子里的氢跟烃分子里的氢有不同吗?乙醇分子可
能是哪一种结构呢?
思考与交流
1、写出水、乙醇分别跟金属钠反应的化学方程式。
2、比较乙醇与水中H的活泼性强弱。
2H2O+
2Na
=
2NaOH
+
H2↑
2
2
2
CH3CH2OH
+
Na
→
CH3CH2ONa
+
H2↑
乙醇钠
思考与交流
根据所学知识判断:乙醇还能被氧化成什么,写出化学方程式。
CH3CH2OH+3O2
2CO2+3H2O
点燃
科学探究
把一根光亮的铜丝,在酒精灯外焰上加热至黑色,立即伸入盛有无水乙醇的试管中,反复几次,观察铜丝的颜色变化,并闻取味道。
铜丝
Δ
变黑
有刺激性气味
插入乙醇溶液中
又变红
②催化氧化
由此可见,实际起氧化作用的是O2,Cu是催化剂
总式
2CH3CH2OH
+
O2
2CH3CHO+2H2O
Cu
△
现象:Cu丝黑色又变为红色,液体产生特殊气味
2Cu
+
O2
2CuO
红色变为黑色
△
CH3CH2OH
+
CuO
CH3CHO+Cu+H2O
△
乙
醛
乙
醇
醇氧化机理:
2CH3CH2OH
+
O2
2CH3CHO
+
2H2O
催化剂
两个氢脱去与O结合成水
C—C—H
H
H
H
H
O—H
C—C
H
H
H
H
O
(CH3CHO)
练习写出下列醇催化氧化的反应方程式:
CH3CH2CH2OH
CH3CH(OH)CH3
拓展
叔醇(—OH所在碳有三个烃基),
则不能去氢氧化。
C
OH
R2
R1
R3
(3).
(2).
2
CH—OH
+
O2
R2
R1
Cu
△
(1).
2R—CH2—OH
+
O2
Cu
△
连接-OH的碳原子上必须有H,
才发生去氢氧化(催化氧化)
伯醇(—OH所在碳只有一个烃基或没有烃基),去氢氧化为醛
O
=
2R—C—H
+
2H2O
仲醇(—OH所在碳有两个烃基),去氢氧化为酮
O
=
2R1—C—R2
+
2H2O
③与强氧化剂反应
乙醇还可以与_________
溶液或________溶液反应,被直接氧化成__________________。
酸性高锰酸钾
酸性重铬酸钾
乙酸
K2Cr2O7
+
C2H5OH
+H2SO4
━
(橙红色)
Cr2(SO4)3
+CH3COOH
+K2SO4+H2O
(绿色)
乙醇的主要性质
CH3CH2OH
CH3COOH
Cu/Ag
O2
△
CH3CHO
催化剂
O2
△
O2
点燃
CO2+H2O
Na
CH3CH2ONa+H2
与钠等活泼金属的反应;
被氧化
乙醇的工业制法、用途
(2)乙烯水化法:
CaO,
△
蒸溜
酒精溶液
无水酒精
(1)
发酵法:
含糖类丰富的各种农产品经发酵,
分馏可得到95%的乙醇。
H2SO4
△、P
CH2=CH2
+
H—OH
CH3CH2OH
用途:重要的化工原料,可用作车用燃料,是一类新的可再生能源。
资料卡片
世界卫生组织的事故调查显示,大约50%-60%的交通事故与酒后驾驶有关。
K2Cr2O7
+
C2H5OH
+H2SO4
→
(橙红色)
Cr2(SO4)3
+CH3COOH
+K2SO4+H2O
(绿色)
K2Cr2O7
Cr2(SO4)3
(橙红色)
(绿色)
交警判断驾驶员是否酒后驾车的方法
K2Cr2O7
Cr2(SO4)3
(橙红色)
(绿色)
练习
1.向装有乙醇的烧杯中投入一小块金属钠,下列对该实验现象的描述中正确的是(
)
A.钠块沉在乙醇液面以下
B.钠块熔化成小球
C.钠块在乙醇的液面上游动
D.钠块表面有气体放出
AD
2.关于乙醇的说法中不正确的是
(
)
A.检验乙醇是否含水可加入金属钠
B.0.1mol乙醇与足量金属钠反应生成0.05
mol
H2说明乙醇分子中含有1个-OH
C.由于乙醇容易挥发,所以才有俗语“酒香不怕巷子深”的说法
D.乙醇与钠反应非常平缓,所以乙醇羟基上的氢原子不如水中的氢原子活泼
A
3.将铜丝放在酒精灯火焰上加热后,分别再将其放入下列物质中,取出洗涤、干燥后质量没有变化的是
(
)
A.水
B.乙醇
C.盐酸
D.CO
BD
4.科学家正在研究开发新的能源。“绿色能源”目前是研究的新能源之一,高粱、玉米等绿色植物的种子经发酵、蒸馏就可以得到一种“绿色能源”。这种物质是
(
)
A.氢气
B.甲烷
C.酒精
D.木炭
C
5.将等质量的铜片在酒精灯上加热后,分别插入下列溶液中,放置片刻,铜片质量增加的是
(
)
A.硝酸
B.无水乙醇
C.石灰水
D.盐酸
C
二、乙酸
乙酸又名醋酸,它是食醋的主要成分,是日常生活中经常接触的一种有机酸。
传说古代山西省有个酿酒高手叫杜康。他儿子黑塔跟父亲也学会了酿酒技术。后来,从山西迁到镇江。黑塔觉得酿酒后把酒糟扔掉可惜,把酒糟浸泡在水缸里。到了第二十一日的酉时,一开缸,一股浓郁的香气扑鼻而来。黑塔忍不住尝了一口,酸酸的,味道很美。烧菜时放了一些,味道特别鲜美,便贮藏着作为“调味酱”。故醋在古代又叫“苦酒”
醋的来历?
乙酸的物理性质:
颜色、状态:
无色液体
气味:
有强烈刺激性气味
沸点:
117.9℃
(易挥发)
熔点:
16.6℃
(无水乙酸又称为:冰醋酸)
溶解性:
易溶于水、乙醇等溶剂
[思维延伸]在室温较低时,无水乙酸就会凝结成像冰一样的晶体。请简单说明在实验中若遇到这种情况时,你将如何从试剂瓶中取出无水乙酸。
分子组成与结构
C2H4O2
CH3COOH
结构简式:
分子式:
结构式:
官能团:
羟基
羰基
(或—COOH)
O
—C—OH
羧基
C
H
H
H
H
O
C
O
乙酸分子比例模型
羧基球棍模型
乙酸的结构与分子模型
甲基
羧基
分子式:
结构式
结构简式
或
C2H4O2
推测:
羧基的性质
想一想?
羰基
羟基
上的反应
结构分析
发生在
羧基
受C=O的影响:
断碳氧单键
氢氧健更易断
上的反应
发生在
受-O-H的影响:
碳氧双键不易断
酸的通性:
A、使酸碱指示剂变色:
B、与活泼金属反应:
D、与碱反应:
E、与盐反应:
C、与碱性氧化物反应:
2CH3COOH
+
CaCO3
=
Ca(CH3COO)2
+H2O+CO2↑
CH3COOH
CH3COO-
+H+
2CH3COOH
+
Zn
=
Zn(CH3COO)2+H2↑
2CH3COOH
+
Cu(OH)2
=
Cu(CH3COO)2+
H2O
2
CH3COOH
+
CuO
=
Cu(CH3COO)2
+
H2O
化学性质
设计一个实验,比较醋酸和碳酸的酸性强弱.
科学探究
酸性:
CH3COOH>H2CO3
可以看到试管里有气泡产生,是二氧化碳气体。这说明乙酸的酸性强于碳酸。尽管如此,但它在水溶液里还是只能发生部分电离,仍是一种弱酸。
厨师烧鱼时常加醋并加点酒,这样鱼的味道就变得无腥、香醇,特别鲜美。
碎瓷片
乙醇
3mL
浓硫酸
2mL
乙酸
2mL
饱和的Na2CO3溶液
乙酸的酯化反应
(防止暴沸)
CH3COOH
+
HOC2H5
CH3COOC2H5+H2O
乙酸乙酯的实验室
制备的注意事项
1.装药品的顺序如何?试管倾斜加热的目的是什么?
2.浓硫酸的作用是什么?
3.如何提高乙酸乙酯的产率?
4.得到的反应产物是否纯净?主要杂质有哪些?
5.饱和Na2CO3溶液有什么作用?能否用氢氧化钠溶液代替饱和碳酸钠溶液?
6.为什么导管不插入饱和Na2CO3溶液中?有无其它防倒吸的方法?
催化剂,吸水剂。酯化反应在常温下反应极慢,一般15年才能达到平衡。
防止受热不匀发生倒吸
乙酸乙酯制取注意事项
2.
浓硫酸的作用:
6.
导管位置高于液面的目的:
①
中和乙酸,消除乙酸气味对酯气味的影响,以便闻到乙酸乙酯的气味.
②
溶解乙醇,吸收乙醇。
③
冷凝酯蒸气、降低酯在水中的溶解度,以便使酯分层析出。
5.
饱和碳酸钠溶液的作用:
4.杂质有:
乙酸;乙醇
酯化反应
CH3COOH
+
HOC2H5
CH3COOC2H5+H2O
定义:酸和醇起作用,生成酯和水的反应叫做酯化反应。
浓硫酸作用:催化剂、吸水剂
乙酸乙酯
探究酯化反应可能的脱水方式
浓H2SO4
b、
O
O
CH3—C—O—H+HO—C2H5
CH3—C—O—C2H5
+
H2O
a、
CH3—C—OH+H—O—C2H5
CH3—C—O—C2H5
+
H2O
浓H2SO4
=
=
O
O
实验:示踪原子法
酯化反应实质:
酸脱羟基
,
醇脱羟基氢。
CH3
C
OH
+
H
18O
C2H5
浓H2SO4
=
O
CH3
C
18O
C2H5
+
H2O
=
O
有机羧酸和无机含氧酸(如
H2SO4、HNO3等)
酸和醇的酯化反应
C2H5O—NO2
+
H2O
CH3COOCH3
+
H2O
CH3COOH
+
HOCH3
浓H2SO4
C2H5OH
+
HO—NO2
浓H2SO4
硝酸乙酯
乙酸甲酯
O
CH3—C—O—H
酸性
酯化反应
小结:
是一种重要的化工原料
在日常生活中也有广泛的用途
乙酸的用途
水垢主要成份:
Mg(OH)2和CaCO3
酯类广泛存在于自然界中
低级酯是有芳香气味的液体,存在于各种水果和花草中。如梨里含有乙酸异戊酯,苹果和香蕉里含有异戊酸异戊酯等。酯的密度一般小于水,并难溶于水,易溶于乙醇和乙醚等有机溶剂。酯可用作溶剂,也可用作制备饮料和糖果的香料。
练习
1.为使95%的乙醇变为无水乙醇,工业上常常加入一种物质,然后蒸馏,这种物质可以是(
)
A.冰醋酸
B.熟石灰
C.生石灰
D.浓硫酸
A
2.除去乙酸乙酯中含有的乙酸,最好的处理和操作是(
)
A.蒸馏
B.水洗后分液
C.用过量饱和碳酸钠溶液洗涤后分液
D.用过量氢氧化钠溶液洗涤后分液
3.下列物质中,不能与乙醇发生酯化反应的是(
)
A.乙醛
B.硝酸 C.苯甲酸
D.硫酸
C
A
4.
关于乙酸的下列说法中不正确的是
(
)
A.乙酸易溶于水和乙醇
B.无水乙酸又称冰醋酸,它是纯净物
C.乙酸是一种重要的有机酸,是有刺激
性气味的液体
D.乙酸分子里有四个氢原子,所以不是一元酸
D
5.
酯化反应属于(
).
A.中和反应
B.不可逆反应
C.离子反应
D.取代反应
D
5.下列有关乙醇的物理性质的应用中不正确的是
(
)
A.由于乙醇的密度比水小,所以乙醇中的水可以通过分液的方法除去
B.由于乙醇能够溶解很多有机物和无机物,所以可用乙醇提取中草药的有效成分
C.由于乙醇能够以任意比溶解于水,所以酒厂可以勾兑各种浓度的酒
D.由于乙醇容易挥发,所以才有俗语“酒好不怕巷子深”的说法
A
6.关于冰醋酸的说法中正确的是
(
)
A.冰醋酸是冰和醋酸的混合物
B.冰醋酸是纯净的乙酸
C.冰醋酸是无色无味的液体
D.冰醋酸易溶解于水和乙醇
7.关于乙醇结构方面的说法中正确的是
(
)
A.乙醇结构中有-OH,所以乙醇溶解于水,可以电离出OH
-而显碱性
B.乙醇与乙酸反应生成乙酸乙酯,所以乙醇显碱性
C.乙醇与钠反应可以产生氢气,所以乙醇显酸性
D.乙醇与钠反应非常平缓,所以乙醇羟基上的氢原子不如水中的氢原子活泼
B
D
D
8.下列是有关生活中对醋酸的应用,其中主要利用了醋酸酸性的是
(
)
A.醋酸溶液可一定程度上治疗手足癣
B.熏醋可一定程度上防止流行性感冒
C.醋可以除去水壶上的水垢
D.用醋烹饪鱼,除去鱼的腥味
9.下列物质能够使紫色石蕊试液变色的是
(
)
A.甲烷
B.乙醇
C.乙酸
D.苯
C
C
10.下列物质中不能用来从碘水中提取碘单质的是
(
)
A.乙醇
B.苯
C.四氯化碳
D.乙酸
11.酯化反应是有机化学中的一类重要反应,下列对酯化反应理解不正确的是
(
)
A.酯化反应的反应物之一般是醇
B.酯化反应生成物不一定有酯
C.酯化反应是有限度的
D.酯化反应一般需要催化剂
A
D
B
12.为使95%的乙醇变为无水乙醇,工业上常常加入一种物质,然后蒸馏,这种物质可以是
(
)
A.冰醋酸
B.熟石灰
C.生石灰
D.浓硫酸
13.将铜丝放在酒精灯火焰上加热后,分别再将其放入下列溶液中,取出洗涤、干燥后质量没有变化的是
(
)
A.水
B.乙醇
C.醋酸
D.硫酸
C
B
14.能够用来检验酒精中是否含有水的试剂是
(
)
A.金属钠
B.无水硫酸铜
C.无水氯化钙
D.浓硫酸
15.钠与下列物质反应都能够产生氢气:
①H2O;②CH3COOH;③CH3CH2OH。试推断这三种物质电离出H+的难易程度(从难到易的顺序)
(
)
A.①②③
B.②③①
C.③①②
D.②①③
B
D
16.下列涉及有关乙酸的物理性质知识的叙述中不正确的是
(
)
A.食醋的颜色(红褐色)就是乙酸的颜色
B.乙酸的熔点比水高,很容易变成固体
C.醋酸是一种具有强烈刺激性气味的液体
D.乙酸和乙醇可以互溶故不能用分液法分离
17.
下列说法正确的是(
)
A.
检测乙醇中是否含有水可加入少量无水硫酸铜,如变蓝则含水
B.
除去乙醇中的微量水可加入金属钠,使其完全反应
C.
获得无水乙醇的方法通常采用先用浓H2SO4吸水,然后再加热蒸馏的方法
D.
获得无水乙醇的方法通常采用先用生石灰吸水,然后再加热蒸馏的方法
A
A
D
18.制取乙酸乙酯的装置正确的是(其中B和D的玻璃导管是插入到小试管内液面以下的(
)
A
19.等质量的Cu片,在酒精灯上加热后,分别插入下列溶液中,放置片刻,铜片质量增加的是(
)
A.
硝酸
B.
无水乙醇
C.
石灰水
D.
盐酸
20.制备CH3COOC2H5所需要的试剂是(
)
A.
C2H5OH
CH3COOH
B.
C2H5OH
CH3COOH
浓硫酸
C.
C2H5OH
3%的乙酸溶液
浓硫酸
D.
C2H5OH
冰醋酸
3mol/L
H2SO4
C
B
21.分别将下列各组物质等体积混合,在室温下剧烈振荡,静置后能够形成均匀溶液的是(
)
A.乙酸乙酯、水
B.苯、水
C.甲醇、水
D.四氯化碳、碘水
22.下列含有羟基的化合物的水溶液显中性的是(
)
A.HONO2
B.HOCH3
C.KOH
D.CH3COOH
C
B
23.下列选项中能说明乙醇(酒精)作为燃料的优点是(
)
①燃烧时发生氧化反应
②充分燃烧的产物不污染环境
③乙醇是一种再生能源
④燃烧时放出大量热能
A.
①②③
B.
①②④
C.
①③④
D.
②③④
24.下列物质中,能与醋酸发生反应的是(
)
①石蕊
②乙醇
③乙醛
④金属铝
⑤氧化镁
⑥碳酸钙
⑦氢氧化铜
A.①③④⑤⑥⑦
B.②③④⑤
C.
①②④⑤⑥⑦
D.全部
D
C
25.在脂化反应的实验中制得的乙酸乙酯中混有少量的CH3COOH,应选用下列哪种试剂洗涤除去:(
)
A.乙醇
B.饱和Na2CO3溶液
C.水
D.NaOH溶液
26.下列操作错误的是(
)
A.除去CO2中少量的SO2:通过盛有饱和NaHCO3溶液的洗气瓶
B.除去苯中的少量苯酚:加入NaOH溶液,振荡、静置分层后,除去水层
C.提取碘水中的碘:用四氯化碳萃取
D.除去乙酸乙酯中的少量乙酸:加入乙醇和浓硫酸,使乙酸全部转化为乙酸乙酯
B
D
清明时节雨纷纷,
路上行人欲断魂。
借问酒家何处有?
牧童遥指杏花村。
明月几时有?
把酒问青天!
酒之于药主要有四个方面的作用:
1.行药势,古人谓“酒为诸药之长”;?
2.有助于药物有效成分的析出;
3.防腐作用;
4.现代医学认为,适量饮酒能增加唾液和胃液的分泌,促进胃肠的消化和吸收;促进血液循环;精神兴奋,强心提神,消除疲劳,促进睡眠等。在一定程度上可减少心脏病和脑中风的发作危险。
溶剂
饮料
消毒剂(75%的乙醇溶液)
燃料
让我
看一看?
想一想?
颜
色
:
气
味
:
状
态:
挥发性:
密
度:
溶解性:
无色透明
特殊香味
液体
比水小
跟水以任意比互溶
能够溶解多种无机物和有机物
易挥发
一、乙醇
1、乙醇的物理性质
思考与交流
乙醇的分子式C2H6O,写出其可能的结构式。
(Ⅰ)
(Ⅱ)
乙醇的组成及结构
C2H6O
分子式:
结构式:
结构简式:
CH3CH2OH
羟基与氢氧根离子的比较
羟基
氢氧根离子
电子式
电荷数
存在形式
相同点
不显电性
带一个单位负电荷
组成元素相同
能独立存在于离子晶体或溶液中
不能独立存在
.
..
..
H
O
..
O
..
..
..
H
..
注意:
1、几个概念
①羟基:
有机化合物分子中含有_____的基团,称为羟基
②烃的衍生物:从结构上看,烃分子中的氢原子被其他_________________所取代而生成的一系列化合物成为烃的衍生物。
③官能团:使烃的衍生物具有不同于烃的特殊性质的__________,称为官能团。
-OH
原子或原子团
基团
注意:
H—O—H
H+
+
OH-
C2H5—O—H
?
现象:试管中有气体生成,可以燃烧,烧杯内壁出现水滴,石灰水不变浑浊.
结论:气体是氢气
演示:钠与无水酒精的反应
[学生实验]将两块金属钠分别投入盛有冷水和乙醇的小烧杯中,观察钠与水、与乙醇反应的现象有何异、同?哪一个更剧烈?填写下表:
钠与水
钠与乙醇
钠是否浮在液面上
钠的形状是否变化
有无声音
有无气泡
剧烈程度
反应方程式
剧烈
缓慢
2Na+2H2O=
2
NaOH
+H2↑
沉在底部
形状不变
响声很小
放出气泡
浮在水面
熔成球形
发出嘶声
放出气体
金属钠的变化
气体燃烧现象
检验产物
水
乙醇
“浮、熔、
游、响”
“沉、不熔、
不响”
发出淡蓝
色火焰。
安静燃烧,发出
淡蓝色火焰,
烧杯内壁有水珠
加酚酞后溶液变红,
说明有碱性物质
(NaOH)生成。
加酚酞后溶液变红,
说明有碱性物质生成;
烧杯中石灰水无明显现
象,说明无CO2生成。
比较水、乙醇与钠反应
思考:乙醇分子里的氢跟烃分子里的氢有不同吗?乙醇分子可
能是哪一种结构呢?
思考与交流
1、写出水、乙醇分别跟金属钠反应的化学方程式。
2、比较乙醇与水中H的活泼性强弱。
2H2O+
2Na
=
2NaOH
+
H2↑
2
2
2
CH3CH2OH
+
Na
→
CH3CH2ONa
+
H2↑
乙醇钠
思考与交流
根据所学知识判断:乙醇还能被氧化成什么,写出化学方程式。
CH3CH2OH+3O2
2CO2+3H2O
点燃
科学探究
把一根光亮的铜丝,在酒精灯外焰上加热至黑色,立即伸入盛有无水乙醇的试管中,反复几次,观察铜丝的颜色变化,并闻取味道。
铜丝
Δ
变黑
有刺激性气味
插入乙醇溶液中
又变红
②催化氧化
由此可见,实际起氧化作用的是O2,Cu是催化剂
总式
2CH3CH2OH
+
O2
2CH3CHO+2H2O
Cu
△
现象:Cu丝黑色又变为红色,液体产生特殊气味
2Cu
+
O2
2CuO
红色变为黑色
△
CH3CH2OH
+
CuO
CH3CHO+Cu+H2O
△
乙
醛
乙
醇
醇氧化机理:
2CH3CH2OH
+
O2
2CH3CHO
+
2H2O
催化剂
两个氢脱去与O结合成水
C—C—H
H
H
H
H
O—H
C—C
H
H
H
H
O
(CH3CHO)
练习写出下列醇催化氧化的反应方程式:
CH3CH2CH2OH
CH3CH(OH)CH3
拓展
叔醇(—OH所在碳有三个烃基),
则不能去氢氧化。
C
OH
R2
R1
R3
(3).
(2).
2
CH—OH
+
O2
R2
R1
Cu
△
(1).
2R—CH2—OH
+
O2
Cu
△
连接-OH的碳原子上必须有H,
才发生去氢氧化(催化氧化)
伯醇(—OH所在碳只有一个烃基或没有烃基),去氢氧化为醛
O
=
2R—C—H
+
2H2O
仲醇(—OH所在碳有两个烃基),去氢氧化为酮
O
=
2R1—C—R2
+
2H2O
③与强氧化剂反应
乙醇还可以与_________
溶液或________溶液反应,被直接氧化成__________________。
酸性高锰酸钾
酸性重铬酸钾
乙酸
K2Cr2O7
+
C2H5OH
+H2SO4
━
(橙红色)
Cr2(SO4)3
+CH3COOH
+K2SO4+H2O
(绿色)
乙醇的主要性质
CH3CH2OH
CH3COOH
Cu/Ag
O2
△
CH3CHO
催化剂
O2
△
O2
点燃
CO2+H2O
Na
CH3CH2ONa+H2
与钠等活泼金属的反应;
被氧化
乙醇的工业制法、用途
(2)乙烯水化法:
CaO,
△
蒸溜
酒精溶液
无水酒精
(1)
发酵法:
含糖类丰富的各种农产品经发酵,
分馏可得到95%的乙醇。
H2SO4
△、P
CH2=CH2
+
H—OH
CH3CH2OH
用途:重要的化工原料,可用作车用燃料,是一类新的可再生能源。
资料卡片
世界卫生组织的事故调查显示,大约50%-60%的交通事故与酒后驾驶有关。
K2Cr2O7
+
C2H5OH
+H2SO4
→
(橙红色)
Cr2(SO4)3
+CH3COOH
+K2SO4+H2O
(绿色)
K2Cr2O7
Cr2(SO4)3
(橙红色)
(绿色)
交警判断驾驶员是否酒后驾车的方法
K2Cr2O7
Cr2(SO4)3
(橙红色)
(绿色)
练习
1.向装有乙醇的烧杯中投入一小块金属钠,下列对该实验现象的描述中正确的是(
)
A.钠块沉在乙醇液面以下
B.钠块熔化成小球
C.钠块在乙醇的液面上游动
D.钠块表面有气体放出
AD
2.关于乙醇的说法中不正确的是
(
)
A.检验乙醇是否含水可加入金属钠
B.0.1mol乙醇与足量金属钠反应生成0.05
mol
H2说明乙醇分子中含有1个-OH
C.由于乙醇容易挥发,所以才有俗语“酒香不怕巷子深”的说法
D.乙醇与钠反应非常平缓,所以乙醇羟基上的氢原子不如水中的氢原子活泼
A
3.将铜丝放在酒精灯火焰上加热后,分别再将其放入下列物质中,取出洗涤、干燥后质量没有变化的是
(
)
A.水
B.乙醇
C.盐酸
D.CO
BD
4.科学家正在研究开发新的能源。“绿色能源”目前是研究的新能源之一,高粱、玉米等绿色植物的种子经发酵、蒸馏就可以得到一种“绿色能源”。这种物质是
(
)
A.氢气
B.甲烷
C.酒精
D.木炭
C
5.将等质量的铜片在酒精灯上加热后,分别插入下列溶液中,放置片刻,铜片质量增加的是
(
)
A.硝酸
B.无水乙醇
C.石灰水
D.盐酸
C
二、乙酸
乙酸又名醋酸,它是食醋的主要成分,是日常生活中经常接触的一种有机酸。
传说古代山西省有个酿酒高手叫杜康。他儿子黑塔跟父亲也学会了酿酒技术。后来,从山西迁到镇江。黑塔觉得酿酒后把酒糟扔掉可惜,把酒糟浸泡在水缸里。到了第二十一日的酉时,一开缸,一股浓郁的香气扑鼻而来。黑塔忍不住尝了一口,酸酸的,味道很美。烧菜时放了一些,味道特别鲜美,便贮藏着作为“调味酱”。故醋在古代又叫“苦酒”
醋的来历?
乙酸的物理性质:
颜色、状态:
无色液体
气味:
有强烈刺激性气味
沸点:
117.9℃
(易挥发)
熔点:
16.6℃
(无水乙酸又称为:冰醋酸)
溶解性:
易溶于水、乙醇等溶剂
[思维延伸]在室温较低时,无水乙酸就会凝结成像冰一样的晶体。请简单说明在实验中若遇到这种情况时,你将如何从试剂瓶中取出无水乙酸。
分子组成与结构
C2H4O2
CH3COOH
结构简式:
分子式:
结构式:
官能团:
羟基
羰基
(或—COOH)
O
—C—OH
羧基
C
H
H
H
H
O
C
O
乙酸分子比例模型
羧基球棍模型
乙酸的结构与分子模型
甲基
羧基
分子式:
结构式
结构简式
或
C2H4O2
推测:
羧基的性质
想一想?
羰基
羟基
上的反应
结构分析
发生在
羧基
受C=O的影响:
断碳氧单键
氢氧健更易断
上的反应
发生在
受-O-H的影响:
碳氧双键不易断
酸的通性:
A、使酸碱指示剂变色:
B、与活泼金属反应:
D、与碱反应:
E、与盐反应:
C、与碱性氧化物反应:
2CH3COOH
+
CaCO3
=
Ca(CH3COO)2
+H2O+CO2↑
CH3COOH
CH3COO-
+H+
2CH3COOH
+
Zn
=
Zn(CH3COO)2+H2↑
2CH3COOH
+
Cu(OH)2
=
Cu(CH3COO)2+
H2O
2
CH3COOH
+
CuO
=
Cu(CH3COO)2
+
H2O
化学性质
设计一个实验,比较醋酸和碳酸的酸性强弱.
科学探究
酸性:
CH3COOH>H2CO3
可以看到试管里有气泡产生,是二氧化碳气体。这说明乙酸的酸性强于碳酸。尽管如此,但它在水溶液里还是只能发生部分电离,仍是一种弱酸。
厨师烧鱼时常加醋并加点酒,这样鱼的味道就变得无腥、香醇,特别鲜美。
碎瓷片
乙醇
3mL
浓硫酸
2mL
乙酸
2mL
饱和的Na2CO3溶液
乙酸的酯化反应
(防止暴沸)
CH3COOH
+
HOC2H5
CH3COOC2H5+H2O
乙酸乙酯的实验室
制备的注意事项
1.装药品的顺序如何?试管倾斜加热的目的是什么?
2.浓硫酸的作用是什么?
3.如何提高乙酸乙酯的产率?
4.得到的反应产物是否纯净?主要杂质有哪些?
5.饱和Na2CO3溶液有什么作用?能否用氢氧化钠溶液代替饱和碳酸钠溶液?
6.为什么导管不插入饱和Na2CO3溶液中?有无其它防倒吸的方法?
催化剂,吸水剂。酯化反应在常温下反应极慢,一般15年才能达到平衡。
防止受热不匀发生倒吸
乙酸乙酯制取注意事项
2.
浓硫酸的作用:
6.
导管位置高于液面的目的:
①
中和乙酸,消除乙酸气味对酯气味的影响,以便闻到乙酸乙酯的气味.
②
溶解乙醇,吸收乙醇。
③
冷凝酯蒸气、降低酯在水中的溶解度,以便使酯分层析出。
5.
饱和碳酸钠溶液的作用:
4.杂质有:
乙酸;乙醇
酯化反应
CH3COOH
+
HOC2H5
CH3COOC2H5+H2O
定义:酸和醇起作用,生成酯和水的反应叫做酯化反应。
浓硫酸作用:催化剂、吸水剂
乙酸乙酯
探究酯化反应可能的脱水方式
浓H2SO4
b、
O
O
CH3—C—O—H+HO—C2H5
CH3—C—O—C2H5
+
H2O
a、
CH3—C—OH+H—O—C2H5
CH3—C—O—C2H5
+
H2O
浓H2SO4
=
=
O
O
实验:示踪原子法
酯化反应实质:
酸脱羟基
,
醇脱羟基氢。
CH3
C
OH
+
H
18O
C2H5
浓H2SO4
=
O
CH3
C
18O
C2H5
+
H2O
=
O
有机羧酸和无机含氧酸(如
H2SO4、HNO3等)
酸和醇的酯化反应
C2H5O—NO2
+
H2O
CH3COOCH3
+
H2O
CH3COOH
+
HOCH3
浓H2SO4
C2H5OH
+
HO—NO2
浓H2SO4
硝酸乙酯
乙酸甲酯
O
CH3—C—O—H
酸性
酯化反应
小结:
是一种重要的化工原料
在日常生活中也有广泛的用途
乙酸的用途
水垢主要成份:
Mg(OH)2和CaCO3
酯类广泛存在于自然界中
低级酯是有芳香气味的液体,存在于各种水果和花草中。如梨里含有乙酸异戊酯,苹果和香蕉里含有异戊酸异戊酯等。酯的密度一般小于水,并难溶于水,易溶于乙醇和乙醚等有机溶剂。酯可用作溶剂,也可用作制备饮料和糖果的香料。
练习
1.为使95%的乙醇变为无水乙醇,工业上常常加入一种物质,然后蒸馏,这种物质可以是(
)
A.冰醋酸
B.熟石灰
C.生石灰
D.浓硫酸
A
2.除去乙酸乙酯中含有的乙酸,最好的处理和操作是(
)
A.蒸馏
B.水洗后分液
C.用过量饱和碳酸钠溶液洗涤后分液
D.用过量氢氧化钠溶液洗涤后分液
3.下列物质中,不能与乙醇发生酯化反应的是(
)
A.乙醛
B.硝酸 C.苯甲酸
D.硫酸
C
A
4.
关于乙酸的下列说法中不正确的是
(
)
A.乙酸易溶于水和乙醇
B.无水乙酸又称冰醋酸,它是纯净物
C.乙酸是一种重要的有机酸,是有刺激
性气味的液体
D.乙酸分子里有四个氢原子,所以不是一元酸
D
5.
酯化反应属于(
).
A.中和反应
B.不可逆反应
C.离子反应
D.取代反应
D
5.下列有关乙醇的物理性质的应用中不正确的是
(
)
A.由于乙醇的密度比水小,所以乙醇中的水可以通过分液的方法除去
B.由于乙醇能够溶解很多有机物和无机物,所以可用乙醇提取中草药的有效成分
C.由于乙醇能够以任意比溶解于水,所以酒厂可以勾兑各种浓度的酒
D.由于乙醇容易挥发,所以才有俗语“酒好不怕巷子深”的说法
A
6.关于冰醋酸的说法中正确的是
(
)
A.冰醋酸是冰和醋酸的混合物
B.冰醋酸是纯净的乙酸
C.冰醋酸是无色无味的液体
D.冰醋酸易溶解于水和乙醇
7.关于乙醇结构方面的说法中正确的是
(
)
A.乙醇结构中有-OH,所以乙醇溶解于水,可以电离出OH
-而显碱性
B.乙醇与乙酸反应生成乙酸乙酯,所以乙醇显碱性
C.乙醇与钠反应可以产生氢气,所以乙醇显酸性
D.乙醇与钠反应非常平缓,所以乙醇羟基上的氢原子不如水中的氢原子活泼
B
D
D
8.下列是有关生活中对醋酸的应用,其中主要利用了醋酸酸性的是
(
)
A.醋酸溶液可一定程度上治疗手足癣
B.熏醋可一定程度上防止流行性感冒
C.醋可以除去水壶上的水垢
D.用醋烹饪鱼,除去鱼的腥味
9.下列物质能够使紫色石蕊试液变色的是
(
)
A.甲烷
B.乙醇
C.乙酸
D.苯
C
C
10.下列物质中不能用来从碘水中提取碘单质的是
(
)
A.乙醇
B.苯
C.四氯化碳
D.乙酸
11.酯化反应是有机化学中的一类重要反应,下列对酯化反应理解不正确的是
(
)
A.酯化反应的反应物之一般是醇
B.酯化反应生成物不一定有酯
C.酯化反应是有限度的
D.酯化反应一般需要催化剂
A
D
B
12.为使95%的乙醇变为无水乙醇,工业上常常加入一种物质,然后蒸馏,这种物质可以是
(
)
A.冰醋酸
B.熟石灰
C.生石灰
D.浓硫酸
13.将铜丝放在酒精灯火焰上加热后,分别再将其放入下列溶液中,取出洗涤、干燥后质量没有变化的是
(
)
A.水
B.乙醇
C.醋酸
D.硫酸
C
B
14.能够用来检验酒精中是否含有水的试剂是
(
)
A.金属钠
B.无水硫酸铜
C.无水氯化钙
D.浓硫酸
15.钠与下列物质反应都能够产生氢气:
①H2O;②CH3COOH;③CH3CH2OH。试推断这三种物质电离出H+的难易程度(从难到易的顺序)
(
)
A.①②③
B.②③①
C.③①②
D.②①③
B
D
16.下列涉及有关乙酸的物理性质知识的叙述中不正确的是
(
)
A.食醋的颜色(红褐色)就是乙酸的颜色
B.乙酸的熔点比水高,很容易变成固体
C.醋酸是一种具有强烈刺激性气味的液体
D.乙酸和乙醇可以互溶故不能用分液法分离
17.
下列说法正确的是(
)
A.
检测乙醇中是否含有水可加入少量无水硫酸铜,如变蓝则含水
B.
除去乙醇中的微量水可加入金属钠,使其完全反应
C.
获得无水乙醇的方法通常采用先用浓H2SO4吸水,然后再加热蒸馏的方法
D.
获得无水乙醇的方法通常采用先用生石灰吸水,然后再加热蒸馏的方法
A
A
D
18.制取乙酸乙酯的装置正确的是(其中B和D的玻璃导管是插入到小试管内液面以下的(
)
A
19.等质量的Cu片,在酒精灯上加热后,分别插入下列溶液中,放置片刻,铜片质量增加的是(
)
A.
硝酸
B.
无水乙醇
C.
石灰水
D.
盐酸
20.制备CH3COOC2H5所需要的试剂是(
)
A.
C2H5OH
CH3COOH
B.
C2H5OH
CH3COOH
浓硫酸
C.
C2H5OH
3%的乙酸溶液
浓硫酸
D.
C2H5OH
冰醋酸
3mol/L
H2SO4
C
B
21.分别将下列各组物质等体积混合,在室温下剧烈振荡,静置后能够形成均匀溶液的是(
)
A.乙酸乙酯、水
B.苯、水
C.甲醇、水
D.四氯化碳、碘水
22.下列含有羟基的化合物的水溶液显中性的是(
)
A.HONO2
B.HOCH3
C.KOH
D.CH3COOH
C
B
23.下列选项中能说明乙醇(酒精)作为燃料的优点是(
)
①燃烧时发生氧化反应
②充分燃烧的产物不污染环境
③乙醇是一种再生能源
④燃烧时放出大量热能
A.
①②③
B.
①②④
C.
①③④
D.
②③④
24.下列物质中,能与醋酸发生反应的是(
)
①石蕊
②乙醇
③乙醛
④金属铝
⑤氧化镁
⑥碳酸钙
⑦氢氧化铜
A.①③④⑤⑥⑦
B.②③④⑤
C.
①②④⑤⑥⑦
D.全部
D
C
25.在脂化反应的实验中制得的乙酸乙酯中混有少量的CH3COOH,应选用下列哪种试剂洗涤除去:(
)
A.乙醇
B.饱和Na2CO3溶液
C.水
D.NaOH溶液
26.下列操作错误的是(
)
A.除去CO2中少量的SO2:通过盛有饱和NaHCO3溶液的洗气瓶
B.除去苯中的少量苯酚:加入NaOH溶液,振荡、静置分层后,除去水层
C.提取碘水中的碘:用四氯化碳萃取
D.除去乙酸乙酯中的少量乙酸:加入乙醇和浓硫酸,使乙酸全部转化为乙酸乙酯
B
D
