氧气制法专题复习
图片预览







文档简介
(共32张PPT)
氧气的实验室制法 专题
烟台华侨学校 于梅
反应原理
装
置
图
装置要点
操作要点
收集方法
氧气实验室制法比较
反应原理
过氧化氢 氧气+水
装
置
图
装置要点
操作要点
收集方法
氧气实验室制法比较
二氧化锰
反应原理 高锰酸钾 锰酸钾+二氧化锰+氧气
氯酸钾 氯化钾+氧气
过氧化氢 氧气+水
装
置
图
装置要点
操作要点
收集方法
氧气实验室制法比较
加热
二氧化锰
加热
二氧化锰
加热
加热
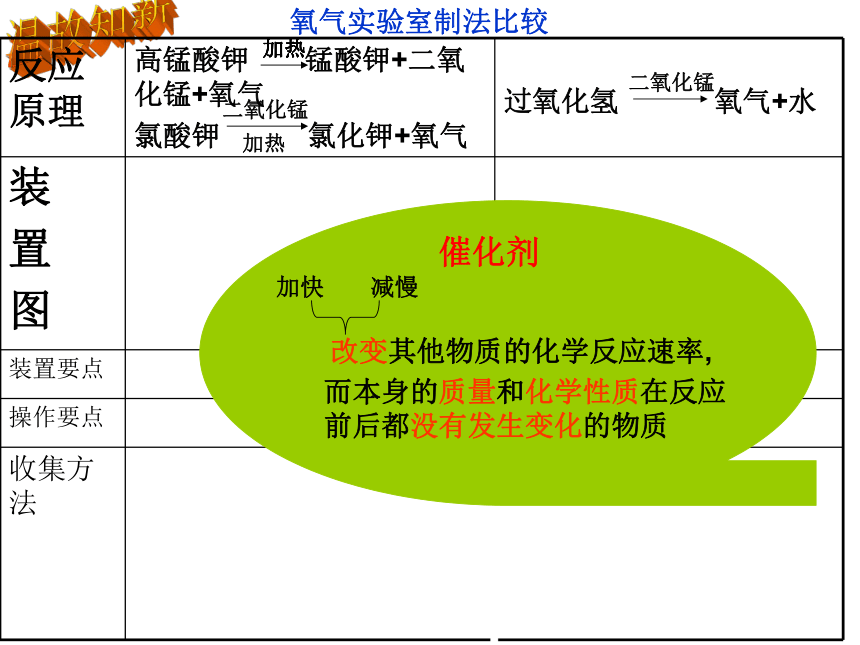
催化剂
加快 减慢
而本身的质量和化学性质在反应前后都没有发生变化的物质
改变其他物质的化学反应速率,
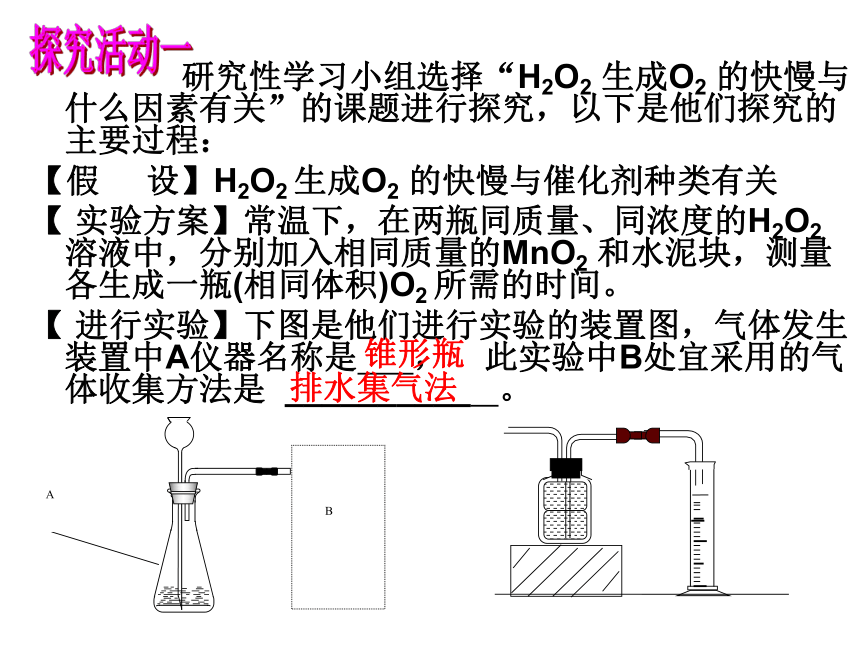
研究性学习小组选择“H2O2 生成O2 的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:
【假 设】H2O2 生成O2 的快慢与催化剂种类有关
【 实验方案】常温下,在两瓶同质量、同浓度的H2O2 溶液中,分别加入相同质量的MnO2 和水泥块,测量各生成一瓶(相同体积)O2 所需的时间。
【 进行实验】下图是他们进行实验的装置图,气体发生装置中A仪器名称是 , 此实验中B处宜采用的气体收集方法是 __________ 。
A
B
锥形瓶
排水集气法
【 结 论】该探究过程得出的结论是__________________
【 反 思】H2O2在常温下分解缓慢,加入MnO2 或水泥块后反应明显加快,则证明MnO2 和水泥块是该反应的催化剂,你认为此结论正确吗?
【 实验记录】
实验编号 1 2
反应物 5%H2O2 5%H2O2
催化剂 1g水泥块 1gMnO2
时间 165秒 46秒
还需要增加实验来验证它们在化学反应前后的质量和
化学性质,是否改变。
在相同条件下,H2O2 生成O2 的快慢与催化剂种类有关
不对,若要证明MnO2 和水泥块是该反应的催化剂,
H2O2 生成O2 的快慢与哪些因素有关?请你帮助他们继续探究。(只要求提出一种影响H2O2 生成O2 的快慢的因素以及相关假设和实验方案)
【假 设】____________________。
【实验方案】
浓度或温度等
取两份质量相等,浓度相等的过氧化氢溶液,
一份加热,一份在常温下进行,测量各收集
一瓶气体所需的时间
剂,测量各收集一瓶气体所需的时间。
在同温下,取二份质量相等的不同浓度的
H2O2 溶液,分别加入质量相等的同种催化
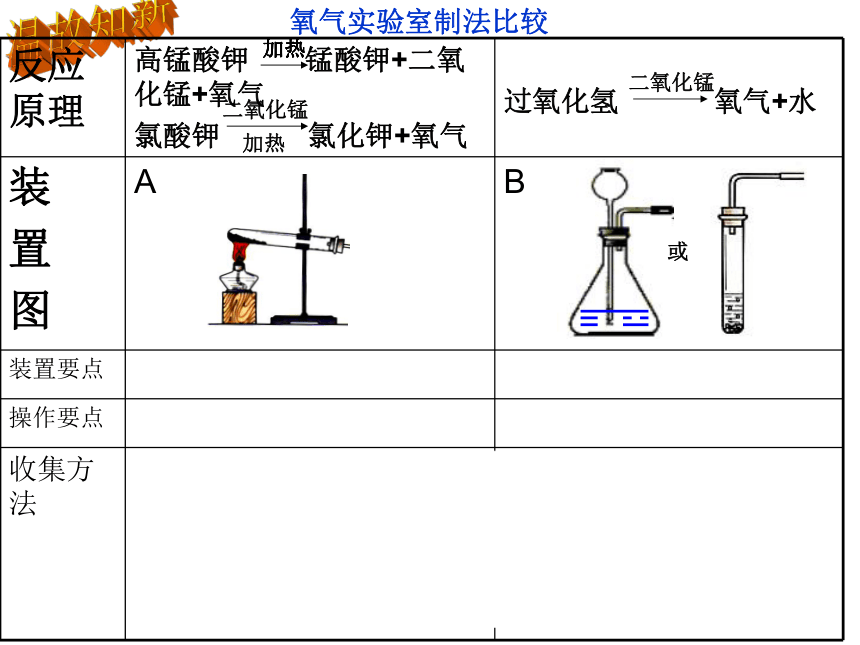
反应原理 高锰酸钾 锰酸钾+二氧化锰+氧气
氯酸钾 氯化钾+氧气
过氧化氢 氧气+水
装
置
图 A B
装置要点
操作要点
收集方法
氧气实验室制法比较
加热
二氧化锰
加热
二氧化锰
加热
加热
反应原理 高锰酸钾 锰酸钾+二氧化锰+氧气
氯酸钾 氯化钾+氧气
过氧化氢 氧气+水
装
置
图 A
B
装置要点
操作要点
收集方法
氧气实验室制法比较
加热
二氧化锰
加热
二氧化锰
加热
加热
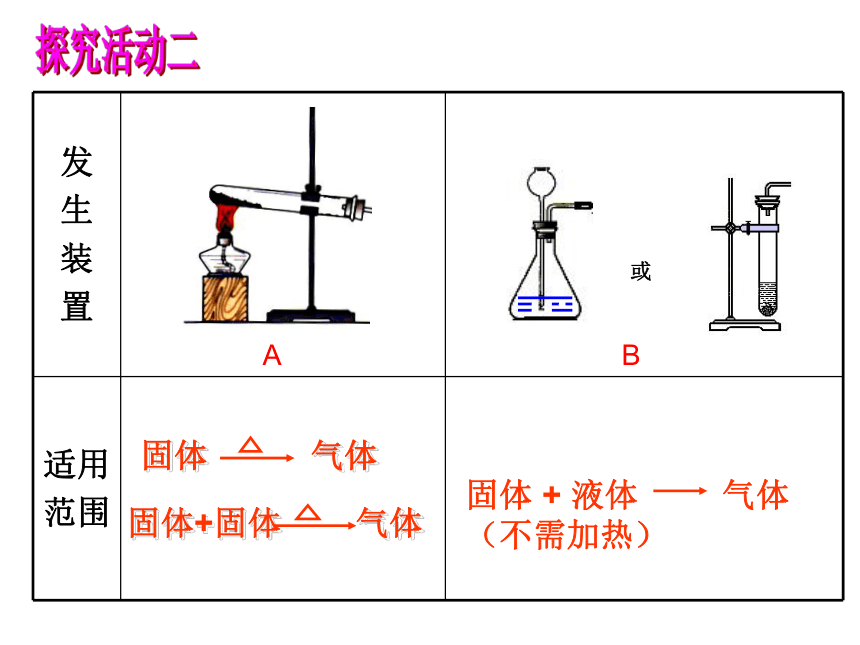
或
发
生
装
置
适用
范围
或
A
B
固体 气体
固体 + 液体 气体
(不需加热)
固体+固体 气体
一、发生装置的选择
选择气体发生装置的依据:
反应物状态
反应条件
将实验盘中的仪器组装成三套制氧气的发生装置,并说明所用的反应原理,这三种装置的适用范围
A
B
1、实验室常用下列方法制取一些气体,请从下图中选择合适的发生装置填空:
①块状的硫酸亚铁与稀硫酸反应制取硫化氢气体,
应选用 装置制取;
②用醋酸钠固体与碱石灰共热制甲烷,应选用
装置制取;
③用固体过氧化钠常温下与水反应制取氧气,
应选用 装置制取。
A
B
B
反应原理 高锰酸钾 锰酸钾+二氧化锰+氧气
氯酸钾 氯化钾+氧气
过氧化氢 氧气+水
装
置
图 A B
装置要点
操作要点
收集方法
氧气实验室制法比较
加热
二氧化锰
加热
二氧化锰
加热
加热
或
B
装置要点
操作要点
长颈漏斗末端必须伸入液面下
锥形瓶内的导管不能太长,应与橡皮塞平齐
先检查装置的气密性,再装药品
待导管口有气泡连续冒出时,才能收集
待集气瓶口有气泡冒出时,才能在水下盖上玻璃片。
收集满氧气的集气瓶要正放在桌上
反应原理 高锰酸钾 锰酸钾+二氧化锰+氧气
氯酸钾 氯化钾+氧气
过氧化氢 氧气+水
装
置
图 A B
装置要点 长颈漏斗末端必须伸入液面下
操作要点
收集方法
氧气实验室制法比较
加热
二氧化锰
加热
二氧化锰
加热
加热
或
A
装置要点
操作要点
试管口略向下倾斜
试管内的导管不能太长,应与橡皮塞平齐
铁夹应夹在离试管口的 处
3
1
加热应用酒精灯的外焰
药品应平铺在试管底部
加热高锰酸钾时,试管口要塞一团棉花
先检查装置的气密性,再加药品
先预热在集中加热
排水法收集时,待导管口有气泡连续冒出时,才能收集
待集气瓶口有气泡冒出时,才能在水下盖上玻璃片。
反应完毕,先把导管移出水面,再熄灭酒精灯
反应原理 高锰酸钾 锰酸钾+二氧化锰+氧气
氯酸钾 氯化钾+氧气
过氧化氢 氧气+水
装
置
图 A B
装置要点 试管口略向下倾斜 长颈漏斗末端必须伸入液面下
操作要点
收集方法
氧气实验室制法比较
加热
二氧化锰
加热
二氧化锰
加热
加热
或
反应原理 高锰酸钾 锰酸钾+二氧化锰+氧气
氯酸钾 氯化钾+氧气
过氧化氢 氧气+水
装
置
图 A B
装置要点 试管口略向下倾斜 长颈漏斗末端必须伸入液面下
操作要点 反应完毕,先撤导管再撤酒精灯
收集方法
氧气实验室制法比较
加热
二氧化锰
加热
二氧化锰
加热
加热
或
.甲图所示的是实验室用过氧化氢溶液与二氧化锰混合制取氧气的装置。请你回答1 :
(1)长颈漏斗的下端管口如果没有伸到液面以下造成的后果是______________。
(2)乙图所示装置也可以用来制取氧气,甲图中的发生装置与之相比较具有的优点是____________________
产生的气体会从长颈漏斗中逸出
可以随时添加液体药品 。
丙
(3)如用丙图所示制取氧气,则与乙图相比有什么 优点________________、______________、 ____________________________
可以随时添加液体药品,
甲 乙
可以控制反应速率。
友情提示
分液漏斗颈有活塞,可根据需要,打开或关上,也可控制水流
可以随时控制反应的发生和停止,
反应原理 高锰酸钾 锰酸钾+二氧化锰+氧气
氯酸钾 氯化钾+氧气
过氧化氢 氧气+水
装
置
图 A B
装置要点 试管口略向下倾斜 长颈漏斗末端必须伸入液面下
操作要点 反应完毕,先撤导管再撤酒精灯
收集方法
氧气实验室制法比较
加热
二氧化锰
加热
二氧化锰
加热
加热
(1)向上排空气法 (2)排水法
或
验满方法?
二、收集装置的选择
选择气体收集装置的依据:
气体的溶解性等
气体的密度
2、几种常见的气体和空气的性质见下表,根据气体的性质回答:
空气 甲烷 一氧化碳 一氧化氮 氨气
标准状况下,气体的密度(g/L) 1.29 0.72 1.25 1.34 0.77
通常状况下,在1体积水中溶解气体的体积
0.033 0.02 0.018 680
①收集甲烷的方法是
②只能用向下排空气法收集的气体是
向下排空气法 排水法
氨气
③只能用排水法收集的气体是
一氧化氮
一氧化碳
(3)若用排水法收集氧气,现将瓶内装满水,然后氧气从 ________端通入;若要测定收集的氧气体积,应怎样操作?
2、如下图所示,该装置有洗气、检验及储气等多种用途。
(1)若用排空气法收集二氧化碳,则CO2气体应从______端进入
(2)若用排空气法收集氢气,则氢气应从_______端进入
a
b
b
作业
作业
激情闯关二
小明参观某养鱼池时,好奇的发现农民向养鱼池中撒一种 叫过氧化钙的固体,用来增加鱼池中的含氧量。小明刚学完
氧气的实验室制法,于是他想可否用过氧化钙来制取氧气。
[猜想与验证]
(1)小明依据_______________________________________ ___________,提出猜想Ⅰ。
猜想Ⅰ:加热过氧化钙可制取氧气。
过氧化钙(CaO2)室温下稳定,在300℃时分解生成氧气
实验装置 实验主要过程
①检查装置气密性。操作如下:先将导管伸入液面下,用手紧握试管,观察到__________ ,松开手后,有液体进入导管。②加入过氧化钙,加热,导管口有大量气泡昌出。③收集满一瓶气体。④停止加热。熄灭酒精灯前,应先 。⑤检验气体,方法是将______________________
实验结论:加热过氧化钙可制取氧气。
导管口有气泡冒出
将导管移出水面
带火星的木条伸入集气瓶中
分析与反思:
①虽然没有快速收集到大量氧气,由此实验现象,小明认为农民用过氧化钙作增氧剂的主要原因是_____________________ ___________②小明希望对此实验进行改进,使该反应加快,你能帮他提出建议吗?
你的合理建议是_________________________ 。
过氧化钙在水中持续缓慢放出氧气 。
加热过氧化钙和水的混合物
巩固性作业
实践性作业
在你的家中,有制氧设备吗 如”氧立得”等.请同学们选取一种,研究一下其中的制取氧气的原理,并写一篇调查报告.
完成导学提纲上的内容
拓展性作业
提纲上的“知识提升”和”课后延伸”
作业
药品选择依据:
必须含有相关成分(科学性),
无毒无害没有污染(安全性),
条件许可 (可行性),
节约能源,价格便宜,
装置简便,易于操作(简约性)
(1)你发现的规律__________________________________________________________________________________________________
(2)实验室制取氨气(其相对分子质量是17,并且易溶于水),用___________法收集。
气体 相对分子质量 标准状况下的密度(g·L-1) 收集方法
空气 29 1.293
氧气 32 1.429 向上排空气法
二氧化碳 44 1.964 向上排空气法
氢气 2 0.089 向下排空气法
在学习中要不断总结、归纳,发现规律,解题就会简约化。例如,在标准状况下,部分气体的相对分子质量、密度、实验室收集方法如下表所示,通过比较找出规律回答下列问题:
在相同条件下,气体的相对分子质量越大,它密度就越大。所以相对分子质量小于29的气体,可以用向下排空气法收集;相对分子质量大于29的气体,可以用向上排空气法收集
向下排空气法
反应原理 高锰酸钾 锰酸钾+二氧化锰+氧气
氯酸钾 氯化钾+氧气
过氧化氢 氧气+水
装
置
图 A B
装置要点
操作要点
收集方法
氧气实验室制法比较
加热
二氧化锰
加热
二氧化锰
加热
加热
或
氧气的实验室制法 专题
烟台华侨学校 于梅
反应原理
装
置
图
装置要点
操作要点
收集方法
氧气实验室制法比较
反应原理
过氧化氢 氧气+水
装
置
图
装置要点
操作要点
收集方法
氧气实验室制法比较
二氧化锰
反应原理 高锰酸钾 锰酸钾+二氧化锰+氧气
氯酸钾 氯化钾+氧气
过氧化氢 氧气+水
装
置
图
装置要点
操作要点
收集方法
氧气实验室制法比较
加热
二氧化锰
加热
二氧化锰
加热
加热
催化剂
加快 减慢
而本身的质量和化学性质在反应前后都没有发生变化的物质
改变其他物质的化学反应速率,
研究性学习小组选择“H2O2 生成O2 的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:
【假 设】H2O2 生成O2 的快慢与催化剂种类有关
【 实验方案】常温下,在两瓶同质量、同浓度的H2O2 溶液中,分别加入相同质量的MnO2 和水泥块,测量各生成一瓶(相同体积)O2 所需的时间。
【 进行实验】下图是他们进行实验的装置图,气体发生装置中A仪器名称是 , 此实验中B处宜采用的气体收集方法是 __________ 。
A
B
锥形瓶
排水集气法
【 结 论】该探究过程得出的结论是__________________
【 反 思】H2O2在常温下分解缓慢,加入MnO2 或水泥块后反应明显加快,则证明MnO2 和水泥块是该反应的催化剂,你认为此结论正确吗?
【 实验记录】
实验编号 1 2
反应物 5%H2O2 5%H2O2
催化剂 1g水泥块 1gMnO2
时间 165秒 46秒
还需要增加实验来验证它们在化学反应前后的质量和
化学性质,是否改变。
在相同条件下,H2O2 生成O2 的快慢与催化剂种类有关
不对,若要证明MnO2 和水泥块是该反应的催化剂,
H2O2 生成O2 的快慢与哪些因素有关?请你帮助他们继续探究。(只要求提出一种影响H2O2 生成O2 的快慢的因素以及相关假设和实验方案)
【假 设】____________________。
【实验方案】
浓度或温度等
取两份质量相等,浓度相等的过氧化氢溶液,
一份加热,一份在常温下进行,测量各收集
一瓶气体所需的时间
剂,测量各收集一瓶气体所需的时间。
在同温下,取二份质量相等的不同浓度的
H2O2 溶液,分别加入质量相等的同种催化
反应原理 高锰酸钾 锰酸钾+二氧化锰+氧气
氯酸钾 氯化钾+氧气
过氧化氢 氧气+水
装
置
图 A B
装置要点
操作要点
收集方法
氧气实验室制法比较
加热
二氧化锰
加热
二氧化锰
加热
加热
反应原理 高锰酸钾 锰酸钾+二氧化锰+氧气
氯酸钾 氯化钾+氧气
过氧化氢 氧气+水
装
置
图 A
B
装置要点
操作要点
收集方法
氧气实验室制法比较
加热
二氧化锰
加热
二氧化锰
加热
加热
或
发
生
装
置
适用
范围
或
A
B
固体 气体
固体 + 液体 气体
(不需加热)
固体+固体 气体
一、发生装置的选择
选择气体发生装置的依据:
反应物状态
反应条件
将实验盘中的仪器组装成三套制氧气的发生装置,并说明所用的反应原理,这三种装置的适用范围
A
B
1、实验室常用下列方法制取一些气体,请从下图中选择合适的发生装置填空:
①块状的硫酸亚铁与稀硫酸反应制取硫化氢气体,
应选用 装置制取;
②用醋酸钠固体与碱石灰共热制甲烷,应选用
装置制取;
③用固体过氧化钠常温下与水反应制取氧气,
应选用 装置制取。
A
B
B
反应原理 高锰酸钾 锰酸钾+二氧化锰+氧气
氯酸钾 氯化钾+氧气
过氧化氢 氧气+水
装
置
图 A B
装置要点
操作要点
收集方法
氧气实验室制法比较
加热
二氧化锰
加热
二氧化锰
加热
加热
或
B
装置要点
操作要点
长颈漏斗末端必须伸入液面下
锥形瓶内的导管不能太长,应与橡皮塞平齐
先检查装置的气密性,再装药品
待导管口有气泡连续冒出时,才能收集
待集气瓶口有气泡冒出时,才能在水下盖上玻璃片。
收集满氧气的集气瓶要正放在桌上
反应原理 高锰酸钾 锰酸钾+二氧化锰+氧气
氯酸钾 氯化钾+氧气
过氧化氢 氧气+水
装
置
图 A B
装置要点 长颈漏斗末端必须伸入液面下
操作要点
收集方法
氧气实验室制法比较
加热
二氧化锰
加热
二氧化锰
加热
加热
或
A
装置要点
操作要点
试管口略向下倾斜
试管内的导管不能太长,应与橡皮塞平齐
铁夹应夹在离试管口的 处
3
1
加热应用酒精灯的外焰
药品应平铺在试管底部
加热高锰酸钾时,试管口要塞一团棉花
先检查装置的气密性,再加药品
先预热在集中加热
排水法收集时,待导管口有气泡连续冒出时,才能收集
待集气瓶口有气泡冒出时,才能在水下盖上玻璃片。
反应完毕,先把导管移出水面,再熄灭酒精灯
反应原理 高锰酸钾 锰酸钾+二氧化锰+氧气
氯酸钾 氯化钾+氧气
过氧化氢 氧气+水
装
置
图 A B
装置要点 试管口略向下倾斜 长颈漏斗末端必须伸入液面下
操作要点
收集方法
氧气实验室制法比较
加热
二氧化锰
加热
二氧化锰
加热
加热
或
反应原理 高锰酸钾 锰酸钾+二氧化锰+氧气
氯酸钾 氯化钾+氧气
过氧化氢 氧气+水
装
置
图 A B
装置要点 试管口略向下倾斜 长颈漏斗末端必须伸入液面下
操作要点 反应完毕,先撤导管再撤酒精灯
收集方法
氧气实验室制法比较
加热
二氧化锰
加热
二氧化锰
加热
加热
或
.甲图所示的是实验室用过氧化氢溶液与二氧化锰混合制取氧气的装置。请你回答1 :
(1)长颈漏斗的下端管口如果没有伸到液面以下造成的后果是______________。
(2)乙图所示装置也可以用来制取氧气,甲图中的发生装置与之相比较具有的优点是____________________
产生的气体会从长颈漏斗中逸出
可以随时添加液体药品 。
丙
(3)如用丙图所示制取氧气,则与乙图相比有什么 优点________________、______________、 ____________________________
可以随时添加液体药品,
甲 乙
可以控制反应速率。
友情提示
分液漏斗颈有活塞,可根据需要,打开或关上,也可控制水流
可以随时控制反应的发生和停止,
反应原理 高锰酸钾 锰酸钾+二氧化锰+氧气
氯酸钾 氯化钾+氧气
过氧化氢 氧气+水
装
置
图 A B
装置要点 试管口略向下倾斜 长颈漏斗末端必须伸入液面下
操作要点 反应完毕,先撤导管再撤酒精灯
收集方法
氧气实验室制法比较
加热
二氧化锰
加热
二氧化锰
加热
加热
(1)向上排空气法 (2)排水法
或
验满方法?
二、收集装置的选择
选择气体收集装置的依据:
气体的溶解性等
气体的密度
2、几种常见的气体和空气的性质见下表,根据气体的性质回答:
空气 甲烷 一氧化碳 一氧化氮 氨气
标准状况下,气体的密度(g/L) 1.29 0.72 1.25 1.34 0.77
通常状况下,在1体积水中溶解气体的体积
0.033 0.02 0.018 680
①收集甲烷的方法是
②只能用向下排空气法收集的气体是
向下排空气法 排水法
氨气
③只能用排水法收集的气体是
一氧化氮
一氧化碳
(3)若用排水法收集氧气,现将瓶内装满水,然后氧气从 ________端通入;若要测定收集的氧气体积,应怎样操作?
2、如下图所示,该装置有洗气、检验及储气等多种用途。
(1)若用排空气法收集二氧化碳,则CO2气体应从______端进入
(2)若用排空气法收集氢气,则氢气应从_______端进入
a
b
b
作业
作业
激情闯关二
小明参观某养鱼池时,好奇的发现农民向养鱼池中撒一种 叫过氧化钙的固体,用来增加鱼池中的含氧量。小明刚学完
氧气的实验室制法,于是他想可否用过氧化钙来制取氧气。
[猜想与验证]
(1)小明依据_______________________________________ ___________,提出猜想Ⅰ。
猜想Ⅰ:加热过氧化钙可制取氧气。
过氧化钙(CaO2)室温下稳定,在300℃时分解生成氧气
实验装置 实验主要过程
①检查装置气密性。操作如下:先将导管伸入液面下,用手紧握试管,观察到__________ ,松开手后,有液体进入导管。②加入过氧化钙,加热,导管口有大量气泡昌出。③收集满一瓶气体。④停止加热。熄灭酒精灯前,应先 。⑤检验气体,方法是将______________________
实验结论:加热过氧化钙可制取氧气。
导管口有气泡冒出
将导管移出水面
带火星的木条伸入集气瓶中
分析与反思:
①虽然没有快速收集到大量氧气,由此实验现象,小明认为农民用过氧化钙作增氧剂的主要原因是_____________________ ___________②小明希望对此实验进行改进,使该反应加快,你能帮他提出建议吗?
你的合理建议是_________________________ 。
过氧化钙在水中持续缓慢放出氧气 。
加热过氧化钙和水的混合物
巩固性作业
实践性作业
在你的家中,有制氧设备吗 如”氧立得”等.请同学们选取一种,研究一下其中的制取氧气的原理,并写一篇调查报告.
完成导学提纲上的内容
拓展性作业
提纲上的“知识提升”和”课后延伸”
作业
药品选择依据:
必须含有相关成分(科学性),
无毒无害没有污染(安全性),
条件许可 (可行性),
节约能源,价格便宜,
装置简便,易于操作(简约性)
(1)你发现的规律__________________________________________________________________________________________________
(2)实验室制取氨气(其相对分子质量是17,并且易溶于水),用___________法收集。
气体 相对分子质量 标准状况下的密度(g·L-1) 收集方法
空气 29 1.293
氧气 32 1.429 向上排空气法
二氧化碳 44 1.964 向上排空气法
氢气 2 0.089 向下排空气法
在学习中要不断总结、归纳,发现规律,解题就会简约化。例如,在标准状况下,部分气体的相对分子质量、密度、实验室收集方法如下表所示,通过比较找出规律回答下列问题:
在相同条件下,气体的相对分子质量越大,它密度就越大。所以相对分子质量小于29的气体,可以用向下排空气法收集;相对分子质量大于29的气体,可以用向上排空气法收集
向下排空气法
反应原理 高锰酸钾 锰酸钾+二氧化锰+氧气
氯酸钾 氯化钾+氧气
过氧化氢 氧气+水
装
置
图 A B
装置要点
操作要点
收集方法
氧气实验室制法比较
加热
二氧化锰
加热
二氧化锰
加热
加热
或
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 自然界中的水
- 第三节 水分子的变化
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 物质构成的奥秘
- 第一节 原子的构成
- 第二节 元素
- 第三节 物质组成的表示
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去 二氧化碳的实验室制取与性质
