新人教版化学高中选修5第二节:芳香烃(37张PPT)
文档属性
| 名称 | 新人教版化学高中选修5第二节:芳香烃(37张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-10-24 00:00:00 | ||
图片预览





文档简介
(共37张PPT)
第二节
芳香烃
第1课时
1.了解苯的结构。
2.掌握苯的结构与性质的关系。
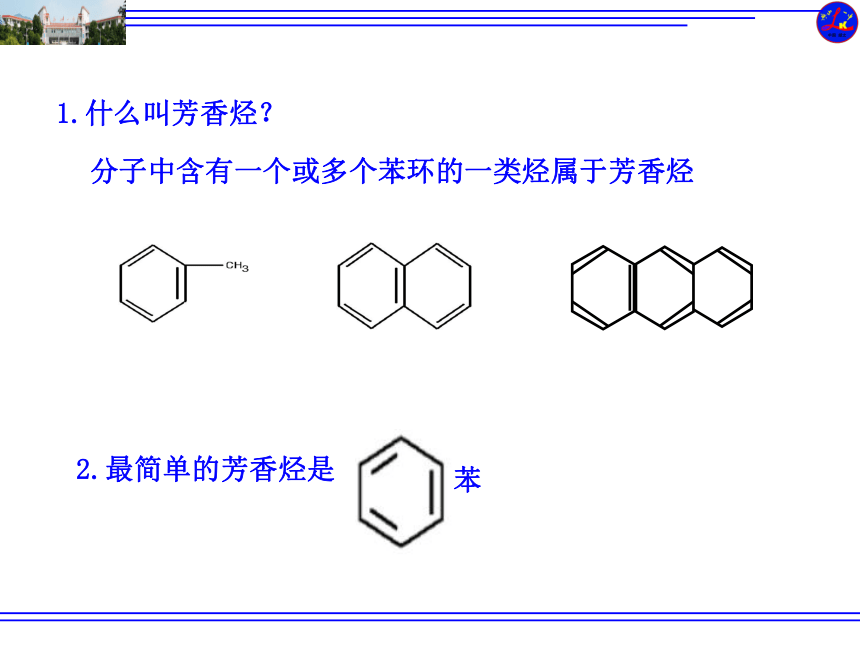
1.什么叫芳香烃?
分子中含有一个或多个苯环的一类烃属于芳香烃
2.最简单的芳香烃是
苯
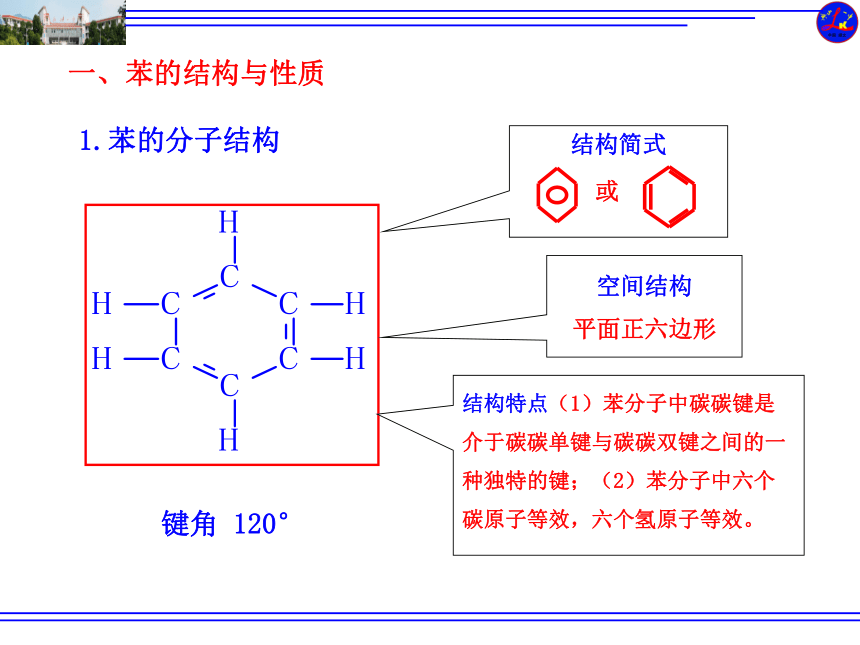
结构简式
或
空间结构
平面正六边形
结构特点(1)苯分子中碳碳键是介于碳碳单键与碳碳双键之间的一种独特的键;(2)苯分子中六个碳原子等效,六个氢原子等效。
一、苯的结构与性质
1.苯的分子结构
键角
120°
颜色
状态
气味
密度
溶解性
挥发性
毒性
无色
芳香气味
液态
比水小
难溶于水,易溶于有机溶剂
易挥发
有毒
2.苯的物理性质
点燃
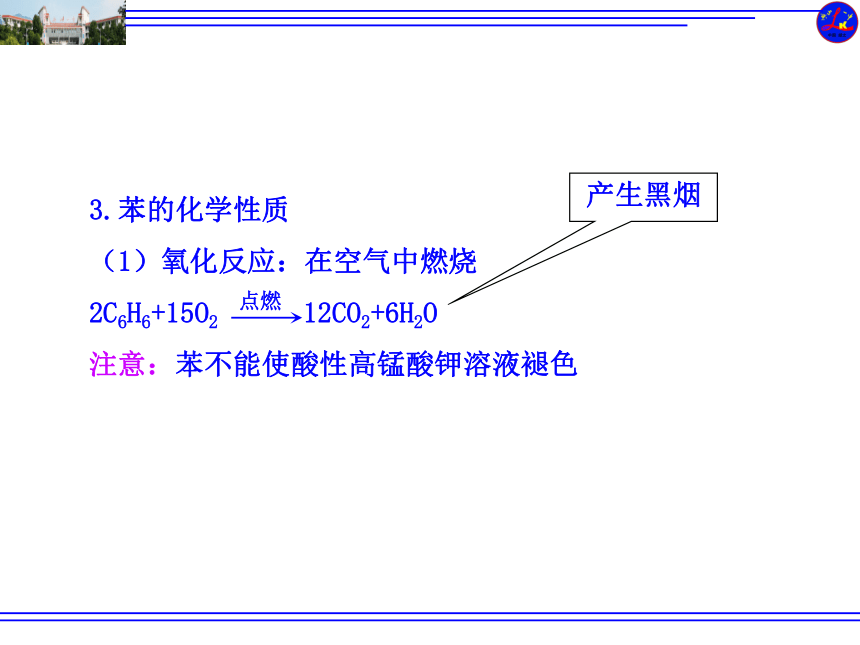
产生黑烟
3.苯的化学性质
(1)氧化反应:在空气中燃烧
2C6H6+15O2
12CO2+6H2O
注意:苯不能使酸性高锰酸钾溶液褪色
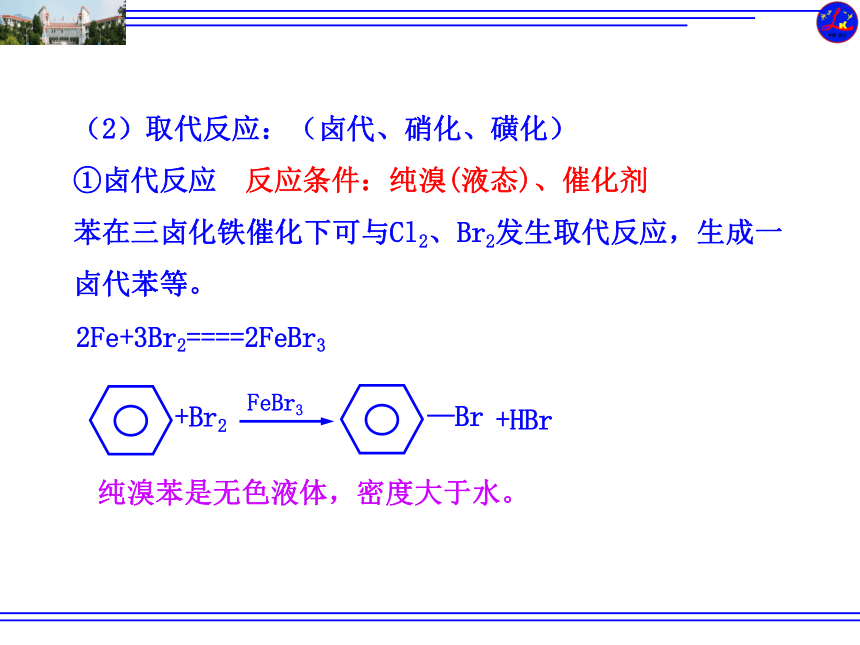
(2)取代反应:(卤代、硝化、磺化)
①卤代反应
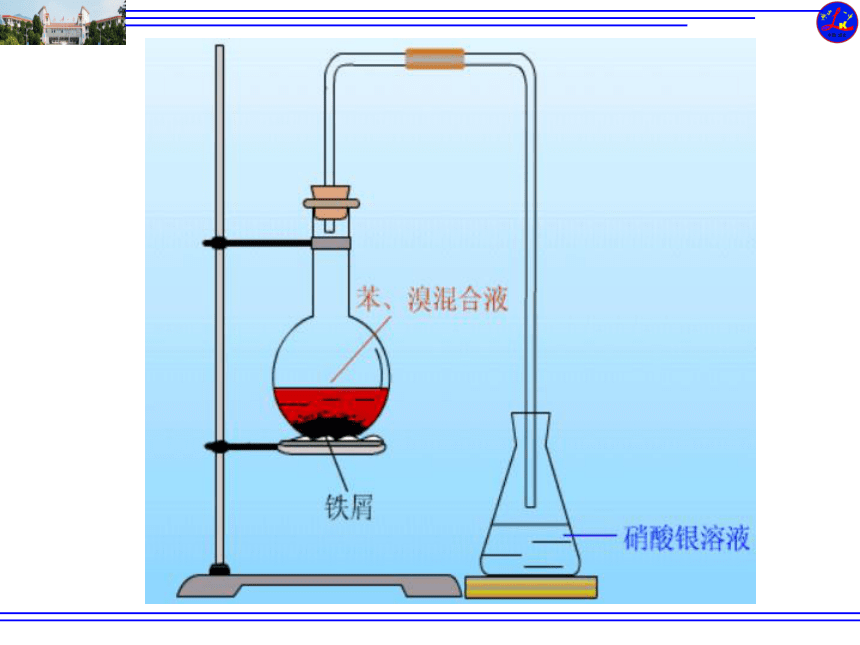
苯在三卤化铁催化下可与Cl2、Br2发生取代反应,生成一卤代苯等。
2Fe+3Br2====2FeBr3
+Br2
—Br
+HBr
FeBr3
纯溴苯是无色液体,密度大于水。
反应条件:纯溴(液态)、催化剂
实验思考题
1.苯、溴、Fe屑等试剂加入烧瓶的顺序是怎样的?
2.Fe屑的作用是什么?
3.将Fe屑加入烧瓶后,烧瓶内有什么现象?这说明什么?
4.长导管的作用是什么?
5.为什么导管末端不插入液面下?
6.哪些现象说明发生了取代反应而不是加成反应?
7.纯净的溴苯应是无色的,为什么所得溴苯为褐色?怎样使之恢复本来的面目?
苯
液溴
Fe屑
用作催化剂(起催化作用的是FeBr3)
剧烈反应,轻微翻腾,有气体逸出。反应放热。
用于导气和冷凝回流(或冷凝器)
溴化氢易溶于水,防止倒吸。
苯与溴反应生成溴苯的同时有溴化氢生成,说明它们发生了取代反应而非加成反应。因加成反应不会生成溴化氢。
因为未发生反应的溴溶解在生成的溴苯中。用水和碱溶液反复洗涤可以使褐色褪去,还溴苯本来的面目。
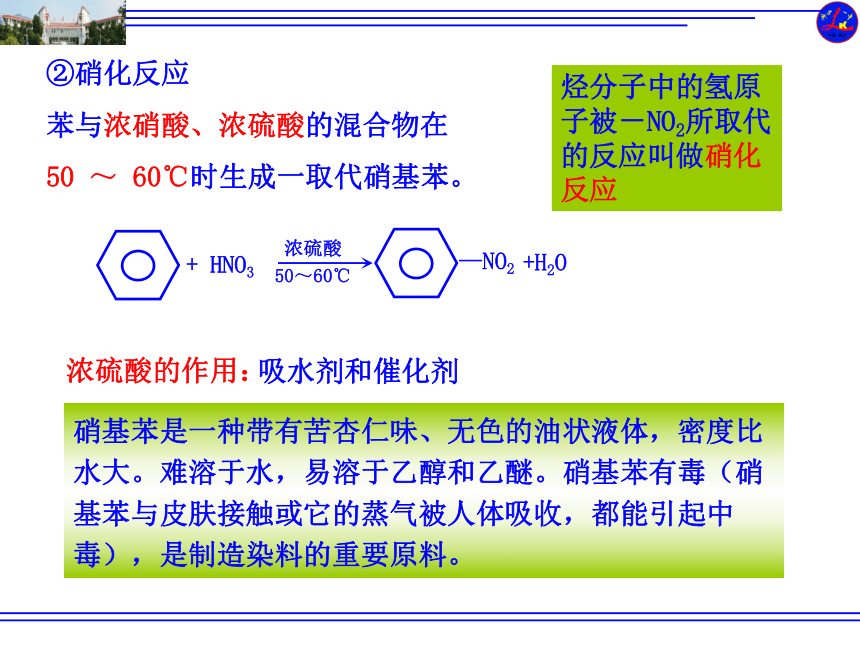
②硝化反应
苯与浓硝酸、浓硫酸的混合物在50
~
60℃时生成一取代硝基苯。
+
HNO3
—NO2
+H2O
浓硫酸
50~60℃
硝基苯是一种带有苦杏仁味、无色的油状液体,密度比水大。难溶于水,易溶于乙醇和乙醚。硝基苯有毒(硝基苯与皮肤接触或它的蒸气被人体吸收,都能引起中毒),是制造染料的重要原料。
烃分子中的氢原子被-NO2所取代的反应叫做硝化反应
吸水剂和催化剂
浓硫酸的作用:
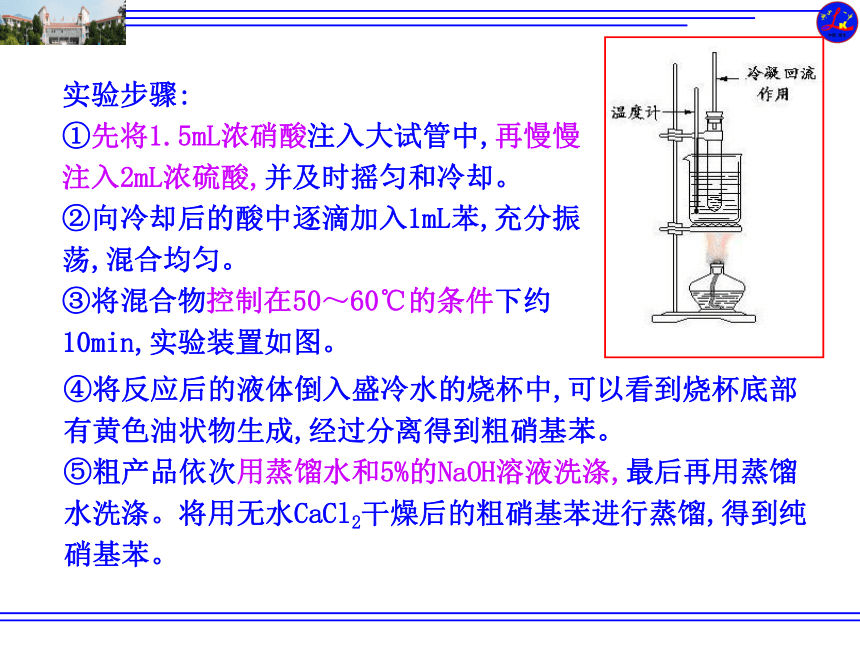
实验步骤:
①先将1.5mL浓硝酸注入大试管中,再慢慢注入2mL浓硫酸,并及时摇匀和冷却。
②向冷却后的酸中逐滴加入1mL苯,充分振荡,混合均匀。
③将混合物控制在50~60℃的条件下约10min,实验装置如图。
④将反应后的液体倒入盛冷水的烧杯中,可以看到烧杯底部有黄色油状物生成,经过分离得到粗硝基苯。
⑤粗产品依次用蒸馏水和5%的NaOH溶液洗涤,最后再用蒸馏水洗涤。将用无水CaCl2干燥后的粗硝基苯进行蒸馏,得到纯硝基苯。
注意:
①浓硝酸和浓硫酸的混合酸要冷却到50-60℃以下,再慢慢滴入苯,边加边振荡,因为反应放热,温度过高,苯易挥发,且硝酸也会分解,同时苯和浓硫酸在75-80℃时会发生反应。
②什么时候采用水浴加热:需要加热,而且一定要控制在100℃以下,均可采用水浴加热。如果超过100
℃,还可采用油浴(0~300
℃)、沙浴温度更高。
⑤为提纯硝基苯,一般将粗产品依次用蒸馏水和NaOH溶液洗涤。
③温度计必须悬挂在水浴中。
④不纯的硝基苯显黄色
(因为溶有NO2)而纯净硝基苯是无色,有苦杏仁味,比水重,油状液体。
——工业制取环己烷的主要方法
+3Cl2
催化剂
Cl
Cl
Cl
Cl
Cl
Cl
H
H
H
H
H
H
+H2
Ni
环己烷
苯的化学性质小结:苯环结构比较稳定,易发生取代反应,而破坏结构的加成反应和氧化反应比较困难。
(3)加成反应
AB
1.下列可用来鉴别乙烯、四氯化碳、苯的是(
)A.酸性高锰酸钾溶液
B.溴水
C.液溴
D.硝化反应
2.下列说法正确的是(
)
A.苯和液溴发生加成反应
B.苯和液溴发生反应时,常用的长直玻璃导管主要起
平衡内外气压和冷凝的作用
C.苯的硝化反应是吸热反应,可用酒精灯直接加热
D.制硝基苯过程中浓硫酸的作用是脱水剂
B
苯
苯的同系物
取代反应
氧化反应
加成反应
被酸性高锰酸钾溶液氧化
苯环上的氢原子被烷基取代
特性
共性
1.能够说明苯中不是单双键交递的事实是(
)
A.邻二甲苯只有一种
B.对二甲苯只有一种
C.苯为平面正六边形结构
D.苯能和液溴反应
AC
2.(1)1866年凯库勒提出了苯的单双键交替的正六边形平面结构(如图所示),解释了苯的部分性质,但还有一些问题尚未解决,它不能解释的事实是
。
A.苯不能使溴水褪色
B.苯能与H2发生加成反应
C.溴苯没有同分异构体
D.邻二溴苯只有一种
(2)现代化学认为苯分子碳碳之间的键是
_____________________________________
A、D
介于单键和双键之间的一种独特的键
第二节
芳香烃
第2课时
1、了解苯的同系物的性质。
2、了解芳香烃分子中基团间存在的相互影响。
3、简单了解芳香烃的来源及其应用。
1.定义
苯环上的氢原子被烷基取代的产物
2.通式
CnH2n-6(n≥6)
3.特点
只含有一个苯环,苯环上连接烷基
4.实例
一
CH3
一
一
CH3
CH3
二、苯的同系物
只含有一个苯环,且侧链为C-C单键的芳香烃。
物理性质:类似于苯,均为难溶于水、密度小于水的、有特殊气味的液体(或固体)
取苯、甲苯各2mL分别注入2支试管中,各加入3滴酸性KMnO4溶液,充分振荡,观察现象。
结论:甲苯能被酸性KMnO4溶液氧化
C
H
H
H
KMnO4
H+
COOH
(1)取代反应(可与卤素、硝酸、硫酸等反应)
浓硫酸
△
+
3HNO3
+
3H2O
淡黄色针状晶体,不溶于水。不稳定,易爆炸,俗称TNT。
—CH3对苯环的影响使取代反应更易进行
5.化学性质
卤代反应
产物以邻、对位取代为主
Fe
Fe
条件一:光照
条件二:FeCl3
(2)氧化反应
①可燃性
②可使酸性高锰酸钾溶液褪色(可鉴别苯和甲苯等苯的同系物)
苯环对甲基的影响使甲基可以被酸性高锰酸钾溶液氧化
2CnH2n-6
+
3
(n-1)O2
点燃
2nCO2+
2(n-3)H2O
现象:火焰明亮并带有浓烟
CH3
KMnO4、H+
COOH
(苯甲酸)
反应机理:
|
—C—H
|
O
||
C—OH
|
酸性高锰酸钾溶液
烷基上与苯环直接相连的碳原子直接连氢原子
H
|
—C—H
|
H
H
|
|
—C—C—
|
|
H
C
|
—C—C
|
C
×
苯的同系物的氧化反应
CH3
|
—C—CH3
|
CH3
CH3
|
|
CH2—R
CH3
|
CH3—CH—
CH3
|
—C—CH3
|
CH3
HOOC
|
|
COOH
HOOC—
KMnO4/H+
思考:产物是什么?
可用KMnO4酸性溶液作试剂鉴别苯的同系物和苯、苯的同系物和烷烃。
苯的同系物的性质:
可以使酸性高锰酸钾褪色,但不能因反应而使溴水褪色;在苯的同系物中,由于烃基与苯环的相互影响。使苯环上的氢原子更易被取代,而烃基则易被氧化。
学与问:P39
(3)加成反应
催化剂
△
+3H2
多苯代脂烃:苯环通过脂肪烃连在一起
联苯或多联苯:苯环之间通过碳碳单键直接相连
稠环芳烃:苯环之间通过共用苯环的若干环边而形成
—CH2—
—
二苯甲烷(C13H12)
联苯(C12H10)
萘(C10H8)
蒽(C14H10)
四、多环芳烃
萘
蒽
苯环间共用两个或两个以上碳原子形成的一类芳香烃
菲
苯并芘
稠环芳香烃
(P.39
资料卡片)
五、芳香烃的来源及其应用
1、来源:a、煤的干馏
b、石油的催化重整
2、应用:简单的芳香烃是基本的有机化工原料。
苯
稠环
芳烃
是黏合剂、油性涂料、油墨等的常用有机溶剂
操作车间空气中苯的浓度≤40mg·m-3
居室内空气中苯含量平均每小时≤0.09mg·m-3
制鞋、皮革、箱包、家具、喷漆、油漆等工作
引起急性中毒或慢性中毒,诱发白血病
致癌物质
萘——过去卫生球的主要成分
秸秆、树叶等不完全燃烧形成的烟雾中
香烟的烟雾中
芳香烃对健康的危害
(2)苯的同系物含有侧链,性质与苯又有不同
①侧链影响苯环,使苯环上的氢原子比苯更易被取代
②苯环影响侧链,使侧链能被强氧化剂氧化
(1)苯的同系物和苯都含有苯环,性质相似
①氧化反应
②取代反应
③加成反应
有机物
烷烃
烯烃
炔烃
芳香烃
代表物
CH4
C2H4
C2H2
C6H6
结构特点
全部单键
饱和烃
含碳碳双键不饱和
含碳碳叁键不饱和
特殊的键不饱和
空间结构
物理性质
燃烧
与溴水
KMnO4
主要反应类型
正四面体型
平面型
直线型
平面正六边形
无色气体,难溶于水
无色液体
易燃,完全燃烧时生成CO2和H2O
不反应
不反应
取代
加成反应
氧化反应
加成、聚合
加成反应
氧化反应
加成、聚合
不反应
不反应
取代、加成
1.能使酸性高锰酸钾溶液褪色但不能使溴水褪色的是(
)
A.乙烯
B.乙炔
C.苯
D.乙苯
2.下列关于硝化反应说法正确的是( )
A.硝化反应是酯化反应,属于取代反应类型
B.硝化反应中混合酸的配制是先加浓硫酸再加浓硝酸
C.甲苯硝化反应的产物只有一种
D.硝基苯的密度大于水
D
D
A
3.下列化合物属于苯的同系物的是(
)
A.
B.
C.
D.
4.(1)1866年凯库勒提出了苯的单双键交替的正六边形平面结构(如图所示),解释了苯的部分性质,但还有一些问题尚未解决,它不能解释的事实是
。
A.苯不能使溴水褪色
B.苯能与H2发生加成反应
C.溴苯没有同分异构体
D.邻二溴苯只有一种
(2)现代化学认为苯分子碳碳之间的键是
_____________________________________
A、D
介于单键和双键之间的一种独特的键
第二节
芳香烃
第1课时
1.了解苯的结构。
2.掌握苯的结构与性质的关系。
1.什么叫芳香烃?
分子中含有一个或多个苯环的一类烃属于芳香烃
2.最简单的芳香烃是
苯
结构简式
或
空间结构
平面正六边形
结构特点(1)苯分子中碳碳键是介于碳碳单键与碳碳双键之间的一种独特的键;(2)苯分子中六个碳原子等效,六个氢原子等效。
一、苯的结构与性质
1.苯的分子结构
键角
120°
颜色
状态
气味
密度
溶解性
挥发性
毒性
无色
芳香气味
液态
比水小
难溶于水,易溶于有机溶剂
易挥发
有毒
2.苯的物理性质
点燃
产生黑烟
3.苯的化学性质
(1)氧化反应:在空气中燃烧
2C6H6+15O2
12CO2+6H2O
注意:苯不能使酸性高锰酸钾溶液褪色
(2)取代反应:(卤代、硝化、磺化)
①卤代反应
苯在三卤化铁催化下可与Cl2、Br2发生取代反应,生成一卤代苯等。
2Fe+3Br2====2FeBr3
+Br2
—Br
+HBr
FeBr3
纯溴苯是无色液体,密度大于水。
反应条件:纯溴(液态)、催化剂
实验思考题
1.苯、溴、Fe屑等试剂加入烧瓶的顺序是怎样的?
2.Fe屑的作用是什么?
3.将Fe屑加入烧瓶后,烧瓶内有什么现象?这说明什么?
4.长导管的作用是什么?
5.为什么导管末端不插入液面下?
6.哪些现象说明发生了取代反应而不是加成反应?
7.纯净的溴苯应是无色的,为什么所得溴苯为褐色?怎样使之恢复本来的面目?
苯
液溴
Fe屑
用作催化剂(起催化作用的是FeBr3)
剧烈反应,轻微翻腾,有气体逸出。反应放热。
用于导气和冷凝回流(或冷凝器)
溴化氢易溶于水,防止倒吸。
苯与溴反应生成溴苯的同时有溴化氢生成,说明它们发生了取代反应而非加成反应。因加成反应不会生成溴化氢。
因为未发生反应的溴溶解在生成的溴苯中。用水和碱溶液反复洗涤可以使褐色褪去,还溴苯本来的面目。
②硝化反应
苯与浓硝酸、浓硫酸的混合物在50
~
60℃时生成一取代硝基苯。
+
HNO3
—NO2
+H2O
浓硫酸
50~60℃
硝基苯是一种带有苦杏仁味、无色的油状液体,密度比水大。难溶于水,易溶于乙醇和乙醚。硝基苯有毒(硝基苯与皮肤接触或它的蒸气被人体吸收,都能引起中毒),是制造染料的重要原料。
烃分子中的氢原子被-NO2所取代的反应叫做硝化反应
吸水剂和催化剂
浓硫酸的作用:
实验步骤:
①先将1.5mL浓硝酸注入大试管中,再慢慢注入2mL浓硫酸,并及时摇匀和冷却。
②向冷却后的酸中逐滴加入1mL苯,充分振荡,混合均匀。
③将混合物控制在50~60℃的条件下约10min,实验装置如图。
④将反应后的液体倒入盛冷水的烧杯中,可以看到烧杯底部有黄色油状物生成,经过分离得到粗硝基苯。
⑤粗产品依次用蒸馏水和5%的NaOH溶液洗涤,最后再用蒸馏水洗涤。将用无水CaCl2干燥后的粗硝基苯进行蒸馏,得到纯硝基苯。
注意:
①浓硝酸和浓硫酸的混合酸要冷却到50-60℃以下,再慢慢滴入苯,边加边振荡,因为反应放热,温度过高,苯易挥发,且硝酸也会分解,同时苯和浓硫酸在75-80℃时会发生反应。
②什么时候采用水浴加热:需要加热,而且一定要控制在100℃以下,均可采用水浴加热。如果超过100
℃,还可采用油浴(0~300
℃)、沙浴温度更高。
⑤为提纯硝基苯,一般将粗产品依次用蒸馏水和NaOH溶液洗涤。
③温度计必须悬挂在水浴中。
④不纯的硝基苯显黄色
(因为溶有NO2)而纯净硝基苯是无色,有苦杏仁味,比水重,油状液体。
——工业制取环己烷的主要方法
+3Cl2
催化剂
Cl
Cl
Cl
Cl
Cl
Cl
H
H
H
H
H
H
+H2
Ni
环己烷
苯的化学性质小结:苯环结构比较稳定,易发生取代反应,而破坏结构的加成反应和氧化反应比较困难。
(3)加成反应
AB
1.下列可用来鉴别乙烯、四氯化碳、苯的是(
)A.酸性高锰酸钾溶液
B.溴水
C.液溴
D.硝化反应
2.下列说法正确的是(
)
A.苯和液溴发生加成反应
B.苯和液溴发生反应时,常用的长直玻璃导管主要起
平衡内外气压和冷凝的作用
C.苯的硝化反应是吸热反应,可用酒精灯直接加热
D.制硝基苯过程中浓硫酸的作用是脱水剂
B
苯
苯的同系物
取代反应
氧化反应
加成反应
被酸性高锰酸钾溶液氧化
苯环上的氢原子被烷基取代
特性
共性
1.能够说明苯中不是单双键交递的事实是(
)
A.邻二甲苯只有一种
B.对二甲苯只有一种
C.苯为平面正六边形结构
D.苯能和液溴反应
AC
2.(1)1866年凯库勒提出了苯的单双键交替的正六边形平面结构(如图所示),解释了苯的部分性质,但还有一些问题尚未解决,它不能解释的事实是
。
A.苯不能使溴水褪色
B.苯能与H2发生加成反应
C.溴苯没有同分异构体
D.邻二溴苯只有一种
(2)现代化学认为苯分子碳碳之间的键是
_____________________________________
A、D
介于单键和双键之间的一种独特的键
第二节
芳香烃
第2课时
1、了解苯的同系物的性质。
2、了解芳香烃分子中基团间存在的相互影响。
3、简单了解芳香烃的来源及其应用。
1.定义
苯环上的氢原子被烷基取代的产物
2.通式
CnH2n-6(n≥6)
3.特点
只含有一个苯环,苯环上连接烷基
4.实例
一
CH3
一
一
CH3
CH3
二、苯的同系物
只含有一个苯环,且侧链为C-C单键的芳香烃。
物理性质:类似于苯,均为难溶于水、密度小于水的、有特殊气味的液体(或固体)
取苯、甲苯各2mL分别注入2支试管中,各加入3滴酸性KMnO4溶液,充分振荡,观察现象。
结论:甲苯能被酸性KMnO4溶液氧化
C
H
H
H
KMnO4
H+
COOH
(1)取代反应(可与卤素、硝酸、硫酸等反应)
浓硫酸
△
+
3HNO3
+
3H2O
淡黄色针状晶体,不溶于水。不稳定,易爆炸,俗称TNT。
—CH3对苯环的影响使取代反应更易进行
5.化学性质
卤代反应
产物以邻、对位取代为主
Fe
Fe
条件一:光照
条件二:FeCl3
(2)氧化反应
①可燃性
②可使酸性高锰酸钾溶液褪色(可鉴别苯和甲苯等苯的同系物)
苯环对甲基的影响使甲基可以被酸性高锰酸钾溶液氧化
2CnH2n-6
+
3
(n-1)O2
点燃
2nCO2+
2(n-3)H2O
现象:火焰明亮并带有浓烟
CH3
KMnO4、H+
COOH
(苯甲酸)
反应机理:
|
—C—H
|
O
||
C—OH
|
酸性高锰酸钾溶液
烷基上与苯环直接相连的碳原子直接连氢原子
H
|
—C—H
|
H
H
|
|
—C—C—
|
|
H
C
|
—C—C
|
C
×
苯的同系物的氧化反应
CH3
|
—C—CH3
|
CH3
CH3
|
|
CH2—R
CH3
|
CH3—CH—
CH3
|
—C—CH3
|
CH3
HOOC
|
|
COOH
HOOC—
KMnO4/H+
思考:产物是什么?
可用KMnO4酸性溶液作试剂鉴别苯的同系物和苯、苯的同系物和烷烃。
苯的同系物的性质:
可以使酸性高锰酸钾褪色,但不能因反应而使溴水褪色;在苯的同系物中,由于烃基与苯环的相互影响。使苯环上的氢原子更易被取代,而烃基则易被氧化。
学与问:P39
(3)加成反应
催化剂
△
+3H2
多苯代脂烃:苯环通过脂肪烃连在一起
联苯或多联苯:苯环之间通过碳碳单键直接相连
稠环芳烃:苯环之间通过共用苯环的若干环边而形成
—CH2—
—
二苯甲烷(C13H12)
联苯(C12H10)
萘(C10H8)
蒽(C14H10)
四、多环芳烃
萘
蒽
苯环间共用两个或两个以上碳原子形成的一类芳香烃
菲
苯并芘
稠环芳香烃
(P.39
资料卡片)
五、芳香烃的来源及其应用
1、来源:a、煤的干馏
b、石油的催化重整
2、应用:简单的芳香烃是基本的有机化工原料。
苯
稠环
芳烃
是黏合剂、油性涂料、油墨等的常用有机溶剂
操作车间空气中苯的浓度≤40mg·m-3
居室内空气中苯含量平均每小时≤0.09mg·m-3
制鞋、皮革、箱包、家具、喷漆、油漆等工作
引起急性中毒或慢性中毒,诱发白血病
致癌物质
萘——过去卫生球的主要成分
秸秆、树叶等不完全燃烧形成的烟雾中
香烟的烟雾中
芳香烃对健康的危害
(2)苯的同系物含有侧链,性质与苯又有不同
①侧链影响苯环,使苯环上的氢原子比苯更易被取代
②苯环影响侧链,使侧链能被强氧化剂氧化
(1)苯的同系物和苯都含有苯环,性质相似
①氧化反应
②取代反应
③加成反应
有机物
烷烃
烯烃
炔烃
芳香烃
代表物
CH4
C2H4
C2H2
C6H6
结构特点
全部单键
饱和烃
含碳碳双键不饱和
含碳碳叁键不饱和
特殊的键不饱和
空间结构
物理性质
燃烧
与溴水
KMnO4
主要反应类型
正四面体型
平面型
直线型
平面正六边形
无色气体,难溶于水
无色液体
易燃,完全燃烧时生成CO2和H2O
不反应
不反应
取代
加成反应
氧化反应
加成、聚合
加成反应
氧化反应
加成、聚合
不反应
不反应
取代、加成
1.能使酸性高锰酸钾溶液褪色但不能使溴水褪色的是(
)
A.乙烯
B.乙炔
C.苯
D.乙苯
2.下列关于硝化反应说法正确的是( )
A.硝化反应是酯化反应,属于取代反应类型
B.硝化反应中混合酸的配制是先加浓硫酸再加浓硝酸
C.甲苯硝化反应的产物只有一种
D.硝基苯的密度大于水
D
D
A
3.下列化合物属于苯的同系物的是(
)
A.
B.
C.
D.
4.(1)1866年凯库勒提出了苯的单双键交替的正六边形平面结构(如图所示),解释了苯的部分性质,但还有一些问题尚未解决,它不能解释的事实是
。
A.苯不能使溴水褪色
B.苯能与H2发生加成反应
C.溴苯没有同分异构体
D.邻二溴苯只有一种
(2)现代化学认为苯分子碳碳之间的键是
_____________________________________
A、D
介于单键和双键之间的一种独特的键
