高中化学新人教版选修五3-2《醛》课件-(37张PPT)
文档属性
| 名称 | 高中化学新人教版选修五3-2《醛》课件-(37张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-10-25 00:00:00 | ||
图片预览









文档简介
(共37张PPT)
第二节《醛》
教学目标:
1.掌握乙醛的主要化学性质
2.了解乙醛的物理性质和用途
3.了解醛的分类和命名
4.理解饱和一元醛的一般通性和同分异构现象
5.了解丙酮的物理性质和用途
6.掌握醛基的检验方法
重点:
乙醛的化学性质
醛基的检验
为求延长保质期
不良奸商竟然给冰鲜鱼浸甲醛保鲜
甲醛有毒,如果用它来浸泡水产,可以固定海鲜、河鲜形态,保持鱼类色泽水发鱿鱼全部含甲醛
食用过量会休克和致癌
花20多万元买辆轿车
开了一周后嗓子发炎、人发烧
经检测车内甲醛含量高
林某买了一盒包装精美的月饼,全家人吃过后,都出现了呕吐、咳嗽等现状,经查是食用了过量的甲醛。林某带着月饼相关单位检测时得知,原来是木质包装盒甲醛超标惹的祸。经市工商局多次调节,月饼生产厂家给林某一家赔了医药费1080元,及退了月饼款198元。
儿童房甲醛超标易诱发儿童白血病
给孩子买衣服既要注意款式也要注意安全
去甲醛十大植物高手
吊兰
龙舌兰
第二节醛
1、醛的定义:
从结构上看,由烃基(或氢原子)跟醛基(-CHO)相连而成的化合物叫醛。
一、醛的概念和通式
R
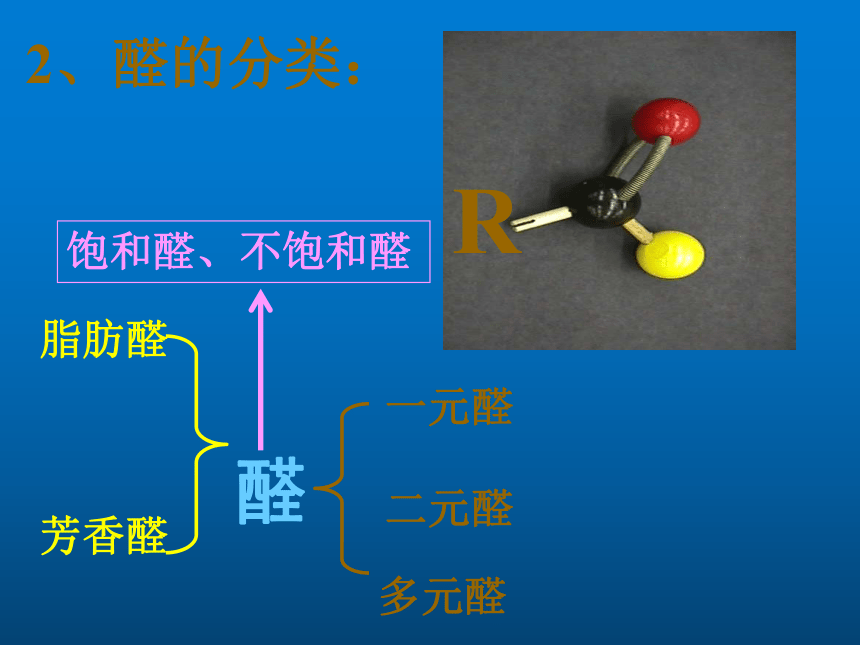
2、醛的分类:
醛
脂肪醛
芳香醛
一元醛
二元醛
多元醛
饱和醛、不饱和醛
R
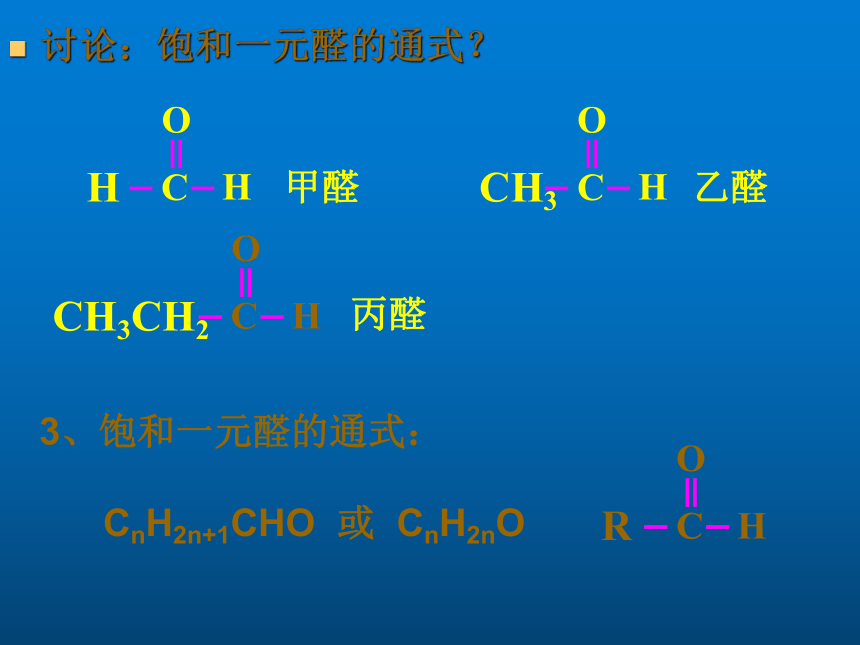
讨论:饱和一元醛的通式?
C
O
H
H
甲醛
C
O
H
CH3
乙醛
丙醛
C
O
H
CH3CH2
C
O
H
R
3、饱和一元醛的通式:
CnH2n+1CHO
或
CnH2nO
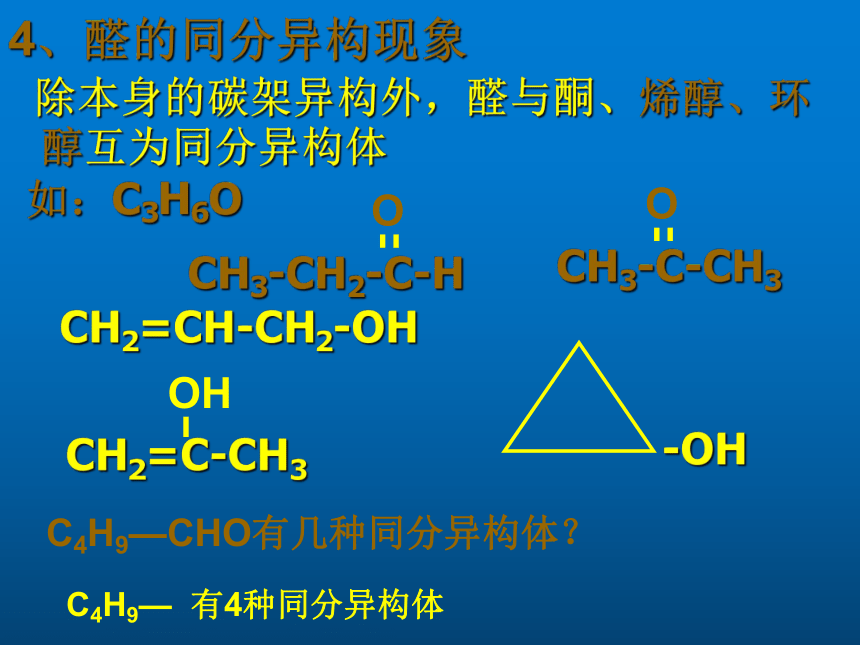
4、醛的同分异构现象
除本身的碳架异构外,醛与酮、烯醇、环醇互为同分异构体
如:C3H6O
CH3-CH2-C-H
O
CH3-C-CH3
O
CH2=CH-CH2-OH
-OH
CH2=C-CH3
OH
C4H9—CHO有几种同分异构体?
C4H9—
有4种同分异构体
1、乙醛
(1)分子结构
分子式:C2H4O
结构式:
结构简式:CH3CHO
官能团:醛基—CHO
H
H
H
H
C
C
O
醛基的写法,不要写成—COH
友情提示
二、醛的性质
吸收强度
10
8
6
4
2
0
P56
图3-12
核磁共振氢谱
乙醛分子结构中含有两类不同位置的氢原子,因此在核磁共振氢谱中有两组峰,峰的面积与氢原子数成正比。因此峰面积较大或峰高较高的是甲基氢原子,反之,是醛基上的氢原子。
(2)乙醛的物理性质
常温下为无色有刺激性气味的液体,
密度比水小,
沸点:20.8℃,
易挥发,易燃烧,
能与水、乙醇、乙醚、氯仿等互溶。
思考:
根据醛基的结构,判断醛基有哪些化学性质?
醛基中碳氧双键发生加成反应,被H2还原为醇
醛基中碳氢键较活泼,能被氧化成相应羧酸
1、氧化性
2、还原性
H—C—C—H
O
H
H
注:醛基不能与卤素单质加成,
这点与C=C双键不同,
能跟烯烃起加成反应的试剂一般不跟醛起加成反应。
Ni
CH3CHO+H2
CH3CH2OH
根据加成反应的概念,写出CH3CHO
和H2加成反应的方程式。
这个反应属于氧化反应还是还原反应?
还原反应
(3)乙醇的化学性质
①加成反应
2CH3CHO+5O2
4CO2+4H2O
点燃
a、
燃烧
乙醛可以被还原为乙醇,能否被氧化?
②氧化反应
b
催化氧化
2CH3CHO+O2
2CH3COOH
催化剂
△
还原
氧化
氧化
乙醇
乙醛
乙酸
c.
被弱氧化剂氧化
①配制银氨溶液
取一洁净试管,加入2ml2%的AgNO3溶液,再逐滴滴入2%的稀氨水,至生成的沉淀恰好溶解
银镜反应
与新制的氢氧化铜反应
Ⅰ、银镜反应
AgNO3+NH3·H2O
→
AgOH↓+NH4NO3
AgOH+NH3·H2O
→[Ag(NH3)2]OH
+2H2O
(氢氧化二氨合银)
注意:
1、碱性环境下,乙醛被氧化成乙酸后又与NH3反应生成乙酸铵。
2、1mol
–CHO被氧化,就应有2molAg被还原。
3、可用稀HNO3清洗试管内壁的银镜。
4、银氨溶液必须随配随用,不可久置,否则会产生易爆炸的物质。
水浴
CH3CHO+2Ag(NH3)2OH
CH3COONH4+2Ag↓+3NH3↑+H2O
氧化剂
还原剂
②水浴加热生成银镜
在配好的上述银氨溶液中滴入三滴乙醛溶液,然后把试管放在热水浴中静置。
银镜反应有什么应用,有什么工业价值?
应用:
(1)检验醛基的存在
(2)测定醛基的数目
(3)工业上用来制瓶胆和镜子
Ⅱ、与新制的氢氧化铜反应
1、配制新制的Cu(OH)2悬浊液:
在2ml
10%
NaOH溶液中滴入2%CuSO4溶液
4~8滴,振荡。
碱必须过量
Cu2++2OH-=
Cu(OH)2
CH3CHO
+
2Cu(OH)2
CH3COOH+
+2H2O
Cu2O↓
砖红色
2、乙醛的氧化:在上述蓝色浊液中加入0.5ml乙
醛溶液,加热至沸腾。
注意:
氢氧化铜溶液一定要新制,
且碱一定要过量。
应用:
(1)检验醛基的存在
(2)医学上检验病人是否患糖尿病
乙醛能否被强氧化剂氧化呢??
d.
被酸性KMnO4溶液、酸性K2Cr2O7溶液溴水等强氧化剂氧化
常用的氧化剂:
银氨溶液、新制的Cu(OH)2、
O2、
酸性KMnO4溶液、酸性K2Cr2O7溶液
溴水等。
2、甲醛(蚁醛)
结构式:
甲醛中有2个活泼氢可被氧化。
分子式:CH2O
结构简式:H—CHO
物理性质:无色、有强烈刺激性气味、
气体,易溶于水
应用:重要的有机合成原料
其水溶液(福尔马林)有杀菌和防腐能力。工业上
主要用于制造酚醛树脂以及多种有机化合物等。
H
H
C
O
化学性质:
(1)加成反应(还原反应)
HCHO+H2
→
CH3OH
Ni
(2)氧化反应
HCHO+O2
→
CO2+H2O
点燃
2HCHO+O2
→
2HCOOH
催化剂
或:HCHO+O2
→
H—O—C—O—
H
O
催化剂
(H2CO3)
注:甲醛在空气中完全燃烧,反应前后物质的量相等,
若水为气态,反应前后气体的体积不变。
H—
C—H
O
H—O—C—O—
H
O
?1mol甲醛最多可以还原得到多少m
o
l
Ag?
即:H2CO3
CO2↑+
2Cu2O↓+5H2O
HCHO+4Cu(OH)2
△
写出甲醛发生银镜反应,以及与新制的氢氧化铜反应的化学方程式。
HCHO+4Ag(NH3)2OH
水浴
(NH4)2CO3+4Ag↓+6NH3+2H2O
注:由于甲醛分子相当于含有2个醛基,所以1mol甲醛发
生银镜反应时最多可生成4molAg
1mol甲醛与新制的氢氧化铜反应最多可生成2molCu2O
化学性质
(1)和H2加成被还原成醇
(2)氧化反应
a.
燃烧
b.
催化氧化成羧酸
c.
被弱氧化剂氧化
Ⅰ、银镜反应
Ⅱ、与新制的氢氧化铜反应
d.
使酸性KMnO4溶液和溴水褪色
小结:醛类的化学性质
C
O
H
R
还原反应:加氢或失氧
氧化反应:加氧或失氢
有机的氧化还原反应
学与问
1、写出甲醛发生银镜反应,以及与新制
氢氧化铜反应
的化学方程式
2、乙醛与氢气的加成反应,也可说乙醛发生了还原反
应,为什么?
3、结合乙醛的结构,说明乙醛的氧化反应和还原反应有
什么特点?
HCHO+4Ag(NH3)2OH
→(NH4)2CO3+4Ag↓+6NH3+2H2O
△
HCHO+4Cu(OH)2
→
CO2↑+2Cu2O↓+5H2O
△
在有机化学反应里,通常还可以从加氢或去氢来分析氧化还原反应,即加氢就是还原反应去氢就是氧化反应。
乙醛能发生氧化反应是由于醛基上的H原子受C=O的影响,活性增强,能被氧化剂所氧化;能发生还原反应是由于醛基上的C=O与C=C类似,可以与H2发生加成反应。
1、某学生做乙醛的还原实验,取1mol/L的CuSO4溶液2mL和0.4mol/L的NaOH溶液5mL,在一个试管中混合加入40%的乙醛溶液加热至沸腾,无红色沉淀,实验失败的原因是(
)
A、乙醛溶液太少
B、氢氧化钠不够用
C、硫酸铜不够用
D、加热时间不够.
2、甲醛、乙醛、丙醛组成的混合物里,氢元素的质量分数是9%,则氧元素的质量分数是(
)
A、16%
B、37%
C、48%
D、无法计算
B
例:
B
1、哪些有机物中含有—CHO?
2、下列哪些不能使酸性KMnO4溶液褪色?
乙烯、甲烷、苯、
乙酸、甲苯、乙醛、
葡萄糖、SO2、H2S、苯酚、裂化汽油
巩固练习
甲烷、苯、
乙酸
醛、HCOOH、HCOOR、
葡萄糖、麦芽糖
3、已知柠檬醛的结构简式为:
若要检验出其中的碳碳双键,其方法是什么?
CH3
O
CH3C=CHCH2CH2CH=CHCH
1、足量的银氨溶液(或新制的Cu(OH)2)使醛基氧化;
2、再用酸性KMnO4溶液(或溴水)检验碳碳双键,碳碳
双键能使酸性KMnO4溶液(或溴水)褪色。
4、某醛的结构简式为(CH3)2C=CHCH2CH2CHO。
(1)检验分子中醛基的方法是
化学方程式为
(2)检验分子中碳碳双键的方法是
化学方程式为
(3)实验操作中,哪一个官能团应先检验?
水浴加热有银镜生成,可证明有醛基
(CH3)2C=CHCH2CH2CHO
+2Ag(NH3)2OH→
(CH3)2C=CHCH2CH2COONH4
+2Ag↓+3NH3+H2O
—CHO后,调pH至酸性再加入溴水,看是否褪色。
(CH3)2C=CHCH2CH2COOH+Br2→(CH3)2CBrCHBrCH2CH2COOH
在加银氨溶液氧化
加入银氨溶液后,
由于Br2也能氧化—CHO,所以必须先用银氨溶液氧化醛基,又因为氧化后溶液为碱性,所以应先酸化后在加溴水检验碳碳双键。
CD
5、一定量的某饱和一元醛发生银镜反应,析出21.6g银,等量的此醛完全燃烧时生成CO2
0.89L,则此醛是(
)
A、乙醛
B、丙醛
C、丁醛
D、2-甲基丙醛
6、一定量某一元醛发生银镜反应得到银21.6g,
等量的
此醛完全燃烧时生成5.4g水,通过计算求该醛可能的化
学式。
CnH2nO
~
2Ag
n(Ag)=0.2mol
1
2
0.1
0.2
n(H2O)=0.3mol
n(
H)=0.6mol
该醛若饱和则化学式为:C3H6O
该醛若不饱和则化学式为:C4H6O
7、在实验室里不宜长期放置,应在使用前配置的溶液
是(
)
①酚酞试剂
②银氨溶液
③Na2CO3溶液
④Cu(OH)2悬浊液
⑤酸化的FeCl3溶液
⑥硫化氢水溶液
A、只有②和④
B、除①之外
C、只有②③⑥
D、全部
C
9、写出丙醛与下列物质反应的化学方程式:
与银氨溶液反应
与新制的氢氧化铜反应
与氢气反应
8、下列物质中不能与金属钠反应的是(
)
A、甲醇
B、丙醛
C、福尔马林
D、苯酚
B
>C=O称羰基,是酮的官能团,丙酮是最简单的酮。
科学视野
酮:羰基碳原子与两个烃基相连的化合物。
丙酮
丙酮不能被银氨溶液、新制的氢氧化铜等弱氧化剂氧化,但可催化加氢生成醇。
作业
P.59
1、2、3、4
第二节《醛》
教学目标:
1.掌握乙醛的主要化学性质
2.了解乙醛的物理性质和用途
3.了解醛的分类和命名
4.理解饱和一元醛的一般通性和同分异构现象
5.了解丙酮的物理性质和用途
6.掌握醛基的检验方法
重点:
乙醛的化学性质
醛基的检验
为求延长保质期
不良奸商竟然给冰鲜鱼浸甲醛保鲜
甲醛有毒,如果用它来浸泡水产,可以固定海鲜、河鲜形态,保持鱼类色泽水发鱿鱼全部含甲醛
食用过量会休克和致癌
花20多万元买辆轿车
开了一周后嗓子发炎、人发烧
经检测车内甲醛含量高
林某买了一盒包装精美的月饼,全家人吃过后,都出现了呕吐、咳嗽等现状,经查是食用了过量的甲醛。林某带着月饼相关单位检测时得知,原来是木质包装盒甲醛超标惹的祸。经市工商局多次调节,月饼生产厂家给林某一家赔了医药费1080元,及退了月饼款198元。
儿童房甲醛超标易诱发儿童白血病
给孩子买衣服既要注意款式也要注意安全
去甲醛十大植物高手
吊兰
龙舌兰
第二节醛
1、醛的定义:
从结构上看,由烃基(或氢原子)跟醛基(-CHO)相连而成的化合物叫醛。
一、醛的概念和通式
R
2、醛的分类:
醛
脂肪醛
芳香醛
一元醛
二元醛
多元醛
饱和醛、不饱和醛
R
讨论:饱和一元醛的通式?
C
O
H
H
甲醛
C
O
H
CH3
乙醛
丙醛
C
O
H
CH3CH2
C
O
H
R
3、饱和一元醛的通式:
CnH2n+1CHO
或
CnH2nO
4、醛的同分异构现象
除本身的碳架异构外,醛与酮、烯醇、环醇互为同分异构体
如:C3H6O
CH3-CH2-C-H
O
CH3-C-CH3
O
CH2=CH-CH2-OH
-OH
CH2=C-CH3
OH
C4H9—CHO有几种同分异构体?
C4H9—
有4种同分异构体
1、乙醛
(1)分子结构
分子式:C2H4O
结构式:
结构简式:CH3CHO
官能团:醛基—CHO
H
H
H
H
C
C
O
醛基的写法,不要写成—COH
友情提示
二、醛的性质
吸收强度
10
8
6
4
2
0
P56
图3-12
核磁共振氢谱
乙醛分子结构中含有两类不同位置的氢原子,因此在核磁共振氢谱中有两组峰,峰的面积与氢原子数成正比。因此峰面积较大或峰高较高的是甲基氢原子,反之,是醛基上的氢原子。
(2)乙醛的物理性质
常温下为无色有刺激性气味的液体,
密度比水小,
沸点:20.8℃,
易挥发,易燃烧,
能与水、乙醇、乙醚、氯仿等互溶。
思考:
根据醛基的结构,判断醛基有哪些化学性质?
醛基中碳氧双键发生加成反应,被H2还原为醇
醛基中碳氢键较活泼,能被氧化成相应羧酸
1、氧化性
2、还原性
H—C—C—H
O
H
H
注:醛基不能与卤素单质加成,
这点与C=C双键不同,
能跟烯烃起加成反应的试剂一般不跟醛起加成反应。
Ni
CH3CHO+H2
CH3CH2OH
根据加成反应的概念,写出CH3CHO
和H2加成反应的方程式。
这个反应属于氧化反应还是还原反应?
还原反应
(3)乙醇的化学性质
①加成反应
2CH3CHO+5O2
4CO2+4H2O
点燃
a、
燃烧
乙醛可以被还原为乙醇,能否被氧化?
②氧化反应
b
催化氧化
2CH3CHO+O2
2CH3COOH
催化剂
△
还原
氧化
氧化
乙醇
乙醛
乙酸
c.
被弱氧化剂氧化
①配制银氨溶液
取一洁净试管,加入2ml2%的AgNO3溶液,再逐滴滴入2%的稀氨水,至生成的沉淀恰好溶解
银镜反应
与新制的氢氧化铜反应
Ⅰ、银镜反应
AgNO3+NH3·H2O
→
AgOH↓+NH4NO3
AgOH+NH3·H2O
→[Ag(NH3)2]OH
+2H2O
(氢氧化二氨合银)
注意:
1、碱性环境下,乙醛被氧化成乙酸后又与NH3反应生成乙酸铵。
2、1mol
–CHO被氧化,就应有2molAg被还原。
3、可用稀HNO3清洗试管内壁的银镜。
4、银氨溶液必须随配随用,不可久置,否则会产生易爆炸的物质。
水浴
CH3CHO+2Ag(NH3)2OH
CH3COONH4+2Ag↓+3NH3↑+H2O
氧化剂
还原剂
②水浴加热生成银镜
在配好的上述银氨溶液中滴入三滴乙醛溶液,然后把试管放在热水浴中静置。
银镜反应有什么应用,有什么工业价值?
应用:
(1)检验醛基的存在
(2)测定醛基的数目
(3)工业上用来制瓶胆和镜子
Ⅱ、与新制的氢氧化铜反应
1、配制新制的Cu(OH)2悬浊液:
在2ml
10%
NaOH溶液中滴入2%CuSO4溶液
4~8滴,振荡。
碱必须过量
Cu2++2OH-=
Cu(OH)2
CH3CHO
+
2Cu(OH)2
CH3COOH+
+2H2O
Cu2O↓
砖红色
2、乙醛的氧化:在上述蓝色浊液中加入0.5ml乙
醛溶液,加热至沸腾。
注意:
氢氧化铜溶液一定要新制,
且碱一定要过量。
应用:
(1)检验醛基的存在
(2)医学上检验病人是否患糖尿病
乙醛能否被强氧化剂氧化呢??
d.
被酸性KMnO4溶液、酸性K2Cr2O7溶液溴水等强氧化剂氧化
常用的氧化剂:
银氨溶液、新制的Cu(OH)2、
O2、
酸性KMnO4溶液、酸性K2Cr2O7溶液
溴水等。
2、甲醛(蚁醛)
结构式:
甲醛中有2个活泼氢可被氧化。
分子式:CH2O
结构简式:H—CHO
物理性质:无色、有强烈刺激性气味、
气体,易溶于水
应用:重要的有机合成原料
其水溶液(福尔马林)有杀菌和防腐能力。工业上
主要用于制造酚醛树脂以及多种有机化合物等。
H
H
C
O
化学性质:
(1)加成反应(还原反应)
HCHO+H2
→
CH3OH
Ni
(2)氧化反应
HCHO+O2
→
CO2+H2O
点燃
2HCHO+O2
→
2HCOOH
催化剂
或:HCHO+O2
→
H—O—C—O—
H
O
催化剂
(H2CO3)
注:甲醛在空气中完全燃烧,反应前后物质的量相等,
若水为气态,反应前后气体的体积不变。
H—
C—H
O
H—O—C—O—
H
O
?1mol甲醛最多可以还原得到多少m
o
l
Ag?
即:H2CO3
CO2↑+
2Cu2O↓+5H2O
HCHO+4Cu(OH)2
△
写出甲醛发生银镜反应,以及与新制的氢氧化铜反应的化学方程式。
HCHO+4Ag(NH3)2OH
水浴
(NH4)2CO3+4Ag↓+6NH3+2H2O
注:由于甲醛分子相当于含有2个醛基,所以1mol甲醛发
生银镜反应时最多可生成4molAg
1mol甲醛与新制的氢氧化铜反应最多可生成2molCu2O
化学性质
(1)和H2加成被还原成醇
(2)氧化反应
a.
燃烧
b.
催化氧化成羧酸
c.
被弱氧化剂氧化
Ⅰ、银镜反应
Ⅱ、与新制的氢氧化铜反应
d.
使酸性KMnO4溶液和溴水褪色
小结:醛类的化学性质
C
O
H
R
还原反应:加氢或失氧
氧化反应:加氧或失氢
有机的氧化还原反应
学与问
1、写出甲醛发生银镜反应,以及与新制
氢氧化铜反应
的化学方程式
2、乙醛与氢气的加成反应,也可说乙醛发生了还原反
应,为什么?
3、结合乙醛的结构,说明乙醛的氧化反应和还原反应有
什么特点?
HCHO+4Ag(NH3)2OH
→(NH4)2CO3+4Ag↓+6NH3+2H2O
△
HCHO+4Cu(OH)2
→
CO2↑+2Cu2O↓+5H2O
△
在有机化学反应里,通常还可以从加氢或去氢来分析氧化还原反应,即加氢就是还原反应去氢就是氧化反应。
乙醛能发生氧化反应是由于醛基上的H原子受C=O的影响,活性增强,能被氧化剂所氧化;能发生还原反应是由于醛基上的C=O与C=C类似,可以与H2发生加成反应。
1、某学生做乙醛的还原实验,取1mol/L的CuSO4溶液2mL和0.4mol/L的NaOH溶液5mL,在一个试管中混合加入40%的乙醛溶液加热至沸腾,无红色沉淀,实验失败的原因是(
)
A、乙醛溶液太少
B、氢氧化钠不够用
C、硫酸铜不够用
D、加热时间不够.
2、甲醛、乙醛、丙醛组成的混合物里,氢元素的质量分数是9%,则氧元素的质量分数是(
)
A、16%
B、37%
C、48%
D、无法计算
B
例:
B
1、哪些有机物中含有—CHO?
2、下列哪些不能使酸性KMnO4溶液褪色?
乙烯、甲烷、苯、
乙酸、甲苯、乙醛、
葡萄糖、SO2、H2S、苯酚、裂化汽油
巩固练习
甲烷、苯、
乙酸
醛、HCOOH、HCOOR、
葡萄糖、麦芽糖
3、已知柠檬醛的结构简式为:
若要检验出其中的碳碳双键,其方法是什么?
CH3
O
CH3C=CHCH2CH2CH=CHCH
1、足量的银氨溶液(或新制的Cu(OH)2)使醛基氧化;
2、再用酸性KMnO4溶液(或溴水)检验碳碳双键,碳碳
双键能使酸性KMnO4溶液(或溴水)褪色。
4、某醛的结构简式为(CH3)2C=CHCH2CH2CHO。
(1)检验分子中醛基的方法是
化学方程式为
(2)检验分子中碳碳双键的方法是
化学方程式为
(3)实验操作中,哪一个官能团应先检验?
水浴加热有银镜生成,可证明有醛基
(CH3)2C=CHCH2CH2CHO
+2Ag(NH3)2OH→
(CH3)2C=CHCH2CH2COONH4
+2Ag↓+3NH3+H2O
—CHO后,调pH至酸性再加入溴水,看是否褪色。
(CH3)2C=CHCH2CH2COOH+Br2→(CH3)2CBrCHBrCH2CH2COOH
在加银氨溶液氧化
加入银氨溶液后,
由于Br2也能氧化—CHO,所以必须先用银氨溶液氧化醛基,又因为氧化后溶液为碱性,所以应先酸化后在加溴水检验碳碳双键。
CD
5、一定量的某饱和一元醛发生银镜反应,析出21.6g银,等量的此醛完全燃烧时生成CO2
0.89L,则此醛是(
)
A、乙醛
B、丙醛
C、丁醛
D、2-甲基丙醛
6、一定量某一元醛发生银镜反应得到银21.6g,
等量的
此醛完全燃烧时生成5.4g水,通过计算求该醛可能的化
学式。
CnH2nO
~
2Ag
n(Ag)=0.2mol
1
2
0.1
0.2
n(H2O)=0.3mol
n(
H)=0.6mol
该醛若饱和则化学式为:C3H6O
该醛若不饱和则化学式为:C4H6O
7、在实验室里不宜长期放置,应在使用前配置的溶液
是(
)
①酚酞试剂
②银氨溶液
③Na2CO3溶液
④Cu(OH)2悬浊液
⑤酸化的FeCl3溶液
⑥硫化氢水溶液
A、只有②和④
B、除①之外
C、只有②③⑥
D、全部
C
9、写出丙醛与下列物质反应的化学方程式:
与银氨溶液反应
与新制的氢氧化铜反应
与氢气反应
8、下列物质中不能与金属钠反应的是(
)
A、甲醇
B、丙醛
C、福尔马林
D、苯酚
B
>C=O称羰基,是酮的官能团,丙酮是最简单的酮。
科学视野
酮:羰基碳原子与两个烃基相连的化合物。
丙酮
丙酮不能被银氨溶液、新制的氢氧化铜等弱氧化剂氧化,但可催化加氢生成醇。
作业
P.59
1、2、3、4
