铝及铝合金-邓杨
图片预览



文档简介
化学1
专题3
从矿物到基础材料
第一单元
从铝土矿到铝合金
第一节
铝及铝合金
一、设计思路
本节课重点内容为铝的化学性质。我对教材进行解读与整理后,把化学性质分为三个部分:一是铝热反应、二是氧化膜、三是铝与酸碱的反应。
以下为本课的设计思路和每个环节的衔接:
二、教材分析
本课时位于苏教版必修1专题3《从矿物到基础材料》中第一单元《从铝土矿到铝合金》的第一课时。是浙江省学科教学指导意见中的发展要求,为选考内容。让学生通过学习能够体验和感受化学家研究和认识物质的科学方法,了解化学学科研究的主要内容和基本方法;从专题2海水中提取化学物质转向从地壳矿物资源中获取基础材料,学习铝的性质,不仅使学生了解了金属钠、镁、铝的金属活动性的差异,还为后来学习从铝土矿中提取铝、铝的氧化物与氢氧化物的知识建立基础,因此本节起到了承上启下的作用。
三、学情分析
1.已有知识:
学习过氯、溴、钠、镁、铁、铜的性质,对元素、化合物知识的学习有一点的心得和知识积累
2.已具备的能力:
学生已初步具备观察能力、实验简单操作能力、分析能力、质疑能力
3.不足之处:
实验操作的规范性不足,思维的严谨性、逻辑性和整理归纳能力不足
四、教学目标
(一)、知识与技能
1.通过观察铝片的外观,知道铝是一种在空气中易被氧化的金属
2.知道铝在浓硫酸、浓硝酸中发生钝化,以及铝的应用。
3.通过铝与盐酸和氢氧化钠的反应,掌握铝与酸和碱的反应规律
(二)、过程与方法
1.学习以实验为基础的实验探究方法;
2.通过铝与浓硫酸、浓硝酸反应以及铝与稀盐酸、稀硫酸反应的现象的探讨,了解对比这一重要科学方法在科学学习过程中的应用
(三)、情感态度与价值观
1.引导学生关注身边的化学物质,让他们认识到化学是一门有用的学科。
2.通过实验或观察或找出金属在生产、生活中的应用,提高学习化学的兴趣,增强学好化学、服务社会的责任感和使命感。
五、重点难点
教学重点:铝的化学性质。
教学难点:铝的化学性质
六、教学策略与手段
借助多媒体辅助教学,以情境激发学生的学习积极性。以实验探究法为主线,通过设疑引导学生积极猜想,同时用实验观察、实验操作、交流讨论等方法完成本课的教学。
七、课前准备
仪器药品:铝箔,铝粉,已打磨过的铝片,未打磨过的铝片,生锈的铁片,稀氢氧化钠溶液,稀盐酸,稀硫酸,浓硫酸,洁净的试管,砂纸,生活中常见铝制品
相关资料:了解铝在生产生活中对人类产生的利弊。
八、教学过程
【问题引入】【板书】【关于铝的两个趣事】【设问】【过渡】【板书】【分析铝的结构】【实物展示】【设疑】【学生设计实验,教师点评】【观察实验】【板书】【学生板书】【讲解】【板书】【学生读课本】【过渡】【实物展示】【板书】【学生板书】【讲解和阅读】【过渡】【板书】【演示实验】【学生观察现象并汇报结果】【疑问】【教师解释现象及讲解】【板书】【总结】【过渡】【学生设计实验并教师点评】【板书】【学生1板书】【学生2板书】【学生3板书】【学生4板书】【过渡】【学生实验】【学生观察并汇报实验现象】【板书】【学生板书】【讲解】【板书】【过渡】【学生阅读课本并回答问题】【板书】【小结】【作业】
问题:你在日常生活中见到过哪些铝制品?
(铝锅、铝制餐具、易拉罐、烧烤用铝箔纸、装药的铝箔纸、铝制导线等。)观察桌面上的金属铝,你能说出铝的物理性质吗?(物理性质一般从哪几个角度说明?)物理性质具有银白色金属光泽的固体,密度较小,有导热性、导电性、延展性。(口述补充:熔点约660℃,其熔点比钠高,比铁、铜低。)趣事一:在19世纪以前,铝是一种非常稀有的贵金属,价格比黄金还要贵。拿破仑三世时,拿破仑使用一套珍藏的铝制餐具,而大臣们使用的是银制餐具。趣事二:门捷列夫创建了元素周期表,受到英国皇家学会的表彰,奖品非常非常贵重,是一只铝制奖杯。问题:地壳中含量最多的金属元素是什么?(铝)追问:既然铝在自然界的含量这么大,为什么它在当时如此珍贵?(讲解:其实,这不足为奇,因为铝的价值贵贱,完全取决于炼铝工业的水平。那时,炼铝的工业水平比较低,铝比较稀少,所以很珍贵。)问题:铝在地壳中以什么形式存在?游离态还是化合态?为什么?(化合态,分析铝的原子结构,对铝的化学性质进行猜想。)
结构
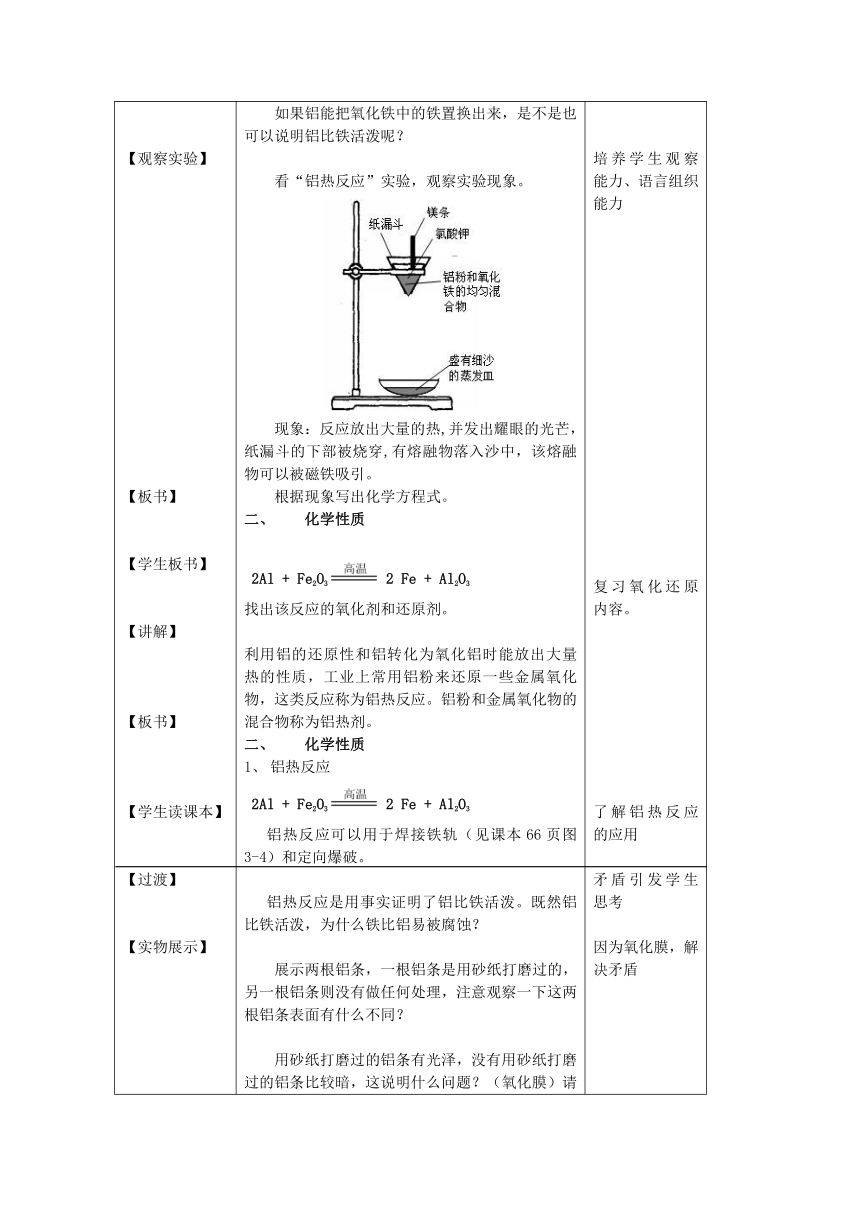
性质铝的最外层有三个电子,化学反应中,容易失去这三个电子,是性质比较活泼的金属,在反应中常表现出较强的还原性。所以在自然界以化合态形式存在,如氧化铝。请大家看久置在潮湿空气中的一个铝片和一个铁片。我们很清楚看到铁发生了严重的腐蚀,而铝却完好无损。(改成:铁也是我们日常生活中常见的金属,比较铁和铝的活泼性)这能否说明:铁比铝活泼?(金属活动性顺序表,铝排在铁之前,铝活泼)请同学们用实验的方法,证明铝比铁活泼。(铝能把氯化亚铁中的铁置换出来;过量的铝能把氯化铁中的铁置换出来;大小相同的铝片和铁片,放入相同稀盐酸中,比较反应快慢……)如果铝能把氧化铁中的铁置换出来,是不是也可以说明铝比铁活泼呢?看“铝热反应”实验,观察实验现象。现象:反应放出大量的热,并发出耀眼的光芒,纸漏斗的下部被烧穿,有熔融物落入沙中,该熔融物可以被磁铁吸引。根据现象写出化学方程式。化学性质2Al
+
Fe2O3
2
Fe
+
Al2O3
找出该反应的氧化剂和还原剂。利用铝的还原性和铝转化为氧化铝时能放出大量热的性质,工业上常用铝粉来还原一些金属氧化物,这类反应称为铝热反应。铝粉和金属氧化物的混合物称为铝热剂。化学性质铝热反应2Al
+
Fe2O3
2
Fe
+
Al2O3
铝热反应可以用于焊接铁轨(见课本66页图3-4)和定向爆破。铝热反应是用事实证明了铝比铁活泼。既然铝比铁活泼,为什么铁比铝易被腐蚀?展示两根铝条,一根铝条是用砂纸打磨过的,另一根铝条则没有做任何处理,注意观察一下这两根铝条表面有什么不同?用砂纸打磨过的铝条有光泽,没有用砂纸打磨过的铝条比较暗,这说明什么问题?(氧化膜)请同学们写出铝条在空气中表面变暗的化学方程式。2、与氧气反应4Al
+
3O2
===
2Al2O3铝表面的这层致密的氧化膜牢固的覆盖在铝的表面,阻止了内部的铝和空气接触,从而防止铝进一步被氧化,因而铝在空气中表现出良好的抗腐蚀性。而铁之所以会严重腐蚀是因为表面没有这层致密氧化膜。根据铝的这一性质,在实际生活中人们常通过一定的方法来增加氧化膜的厚度,使铝更加耐用。还可以对铝进行着色以加强对铝的保护。
阅读课本第64页,“观察与思考”的下面一段。另外,铝粉也能在空气中燃烧生成氧化铝除了氧气以外,还有哪些物质能使铝表面出现氧化膜呢?应该是具有什么性质的物质?(应该是强氧化性的物质,如浓硫酸、浓硝酸)3、与酸反应(1)强氧化性酸(浓硫酸、浓硝酸)接下来探究一下铝和浓硫酸的反应。实验:展示一根已经打磨过的铝条,把它放入一只洁净的试管中,再加入约3ml的浓硫酸。观察实验现象。请一个同学来回答一下他所观察到的实验现象。(无明显现象)
无明显现象就说明没有发生反应吗?
如何证明已经发生了反应?(把铝片放入硫酸铜溶液中,如无法置换出金属铜,说明已经形成氧化膜)
除了浓硫酸以外,浓硝酸也可以发生类似反应。在常温下,铝遇浓硫酸,浓硝酸会在表面生成一层致密的氧化膜,阻止内部的铝进一步氧化,我们把这种现象叫做钝化。常温下,铝在浓硫酸,浓硝酸中钝化。利用铝这个特殊的性质,我们可以用铝槽车来运输浓硫酸和浓硝酸。氧气,浓硫酸,浓硝酸都可以使铝表面出现氧化膜。还有没有其他实验的方法证明,铝表面出现了一层氧化膜?请设计实验。(把铝放入稀盐酸或稀硫酸中,刚开始没有明显现象,后产生气泡;把铝放入氯化铜溶液中,无明显现象……)
铝能与稀盐酸或稀硫酸反应放出气体,写出这两个化学方程式。(2)弱氧化性酸(如盐酸、稀硫酸)2Al
+
6HCl
===
2AlCl3
+
3H2↑2Al
+
3H2SO4
===
Al2(SO4)3
+
3H2↑把上述两个反应改成离子方程式。2Al
+
6H+
===
2Al3+
+
3H2↑2Al
+
6H+
===
2Al3+
+
3H2↑铝除了与酸反应以外,能否与碱发生反应?(从铝在元素周期表中的位置说明,并用实验验证)学生实验:把打磨过的铝片放入试管中,再向其中加入稀氢氧化钠溶液,观察实验现象。现象:铝表面有气泡产生,点燃产生的气体有爆鸣声。通过现象及氧化还原反应规律写出化学方程式。4、与碱反应2Al
+
2NaOH+
2H2O
===
2NaAlO2
+
3H2↑试写出该反应的离子方程式。2Al
+
2OH-+
2H2O
===
2AlO2-
+
3H2↑从上述反应可知道铝既可以和酸反应又可以和碱反应,像这样既能和酸反应,也能和碱反应的金属,称为两性金属。两性金属铝这种金属虽然很活泼,由于表面有氧化膜,所以抗腐蚀能力强,密度比较小(质量轻),铝的优点很多,但它质地比较软,强度和韧性都较差,所以常常把铝制成铝合金来应用。一般地,金属制成合金之后,会有更加优良的性能,比如说铝与其他金属或非金属熔合成合金后,强度高、可塑性好、抗腐蚀能力强,在生产生活中应用广泛。阅读课本66页一段,说说铝合金有哪些优点?铝合金有哪些应用?总结铝的用途与性质之间的关系,得出结论:性质
用途学习了本节课之后,学生总结这样两个问题:根据本节课所学,总结铝能与哪些物质发生反应?根据钠和镁的性质,猜测铝还能与哪些物质发生反应?铝有什么用途?铝和铝合金制品的用处很大,在生产生活中的各领域都有涉及,但是经研究发现,铝元素能损害人的脑细胞,因此在日常生活中要防止铝的吸收,减少铝制品的使用。比如少吃炸油条、由铝包装的糖果等食品,少喝易拉罐装的饮料。虽然铝离子有毒,但危害和其贡献是无法相提并论的,我们要学会扬长避短,让它对人类社会将发挥出更为重要的作用。完成学案中的练习
提问学生,并教师板书。学生阅读,提高进一步学习的兴趣矛盾引发学生思考让学生了解结构、性质之间的关系。复习了氧化还原反应相关知识点培养学生设计实验的能力,和严谨的科学态度培养学生观察能力、语言组织能力复习氧化还原内容。了解铝热反应的应用矛盾引发学生思考因为氧化膜,解决矛盾让学生养成利用教材的习惯涉及氧化还原内容培养学生观察能力提高学生设计实验能力及语言表达能力,和严谨的科学态度学生根据金属与酸反应规律直接写出化学方程式复习离子方程式培养学生实验操作能力,实验观察能力,及书写化学方程式的能力(可以通过实验判断氢气的产生,也可以根据化合价升降判断产物氢气。)复习离子方程式让学生了解结构、性质、用途之间的关系培养学生总结归纳能力教师补充
【板书设计】
铝及铝合金
一、物理性质
具有银白色金属光泽的固体,密度较小,有导热性、导电性、延展性。
结构
性质
用途
2、
化学性质
1、铝热反应
2Al
+
Fe2O3
2
Fe
+
Al2O3
1、
与氧气反应
4Al
+
3O2
===
2Al2O3
4Al
+
3O2
2Al2O3
3、与酸反应
(1)强氧化性酸(浓硫酸、浓硝酸)
常温下,铝在浓硫酸,浓硝酸中钝化。
(2)弱氧化性酸(如盐酸、稀硫酸)
2Al
+
6HCl
===
2AlCl3
+
3H2↑
2Al
+
3H2SO4
===
Al2(SO4)3
+
3H2↑
2Al
+
6H+
===
2Al3+
+
3H2↑
4、与碱反应
2Al
+
2NaOH+
2H2O
===
2NaAlO2+3H2↑
2Al
+
2OH-+
2H2O
===
2AlO2-
+
3H2
决定
决定
决定
决定
专题3
从矿物到基础材料
第一单元
从铝土矿到铝合金
第一节
铝及铝合金
一、设计思路
本节课重点内容为铝的化学性质。我对教材进行解读与整理后,把化学性质分为三个部分:一是铝热反应、二是氧化膜、三是铝与酸碱的反应。
以下为本课的设计思路和每个环节的衔接:
二、教材分析
本课时位于苏教版必修1专题3《从矿物到基础材料》中第一单元《从铝土矿到铝合金》的第一课时。是浙江省学科教学指导意见中的发展要求,为选考内容。让学生通过学习能够体验和感受化学家研究和认识物质的科学方法,了解化学学科研究的主要内容和基本方法;从专题2海水中提取化学物质转向从地壳矿物资源中获取基础材料,学习铝的性质,不仅使学生了解了金属钠、镁、铝的金属活动性的差异,还为后来学习从铝土矿中提取铝、铝的氧化物与氢氧化物的知识建立基础,因此本节起到了承上启下的作用。
三、学情分析
1.已有知识:
学习过氯、溴、钠、镁、铁、铜的性质,对元素、化合物知识的学习有一点的心得和知识积累
2.已具备的能力:
学生已初步具备观察能力、实验简单操作能力、分析能力、质疑能力
3.不足之处:
实验操作的规范性不足,思维的严谨性、逻辑性和整理归纳能力不足
四、教学目标
(一)、知识与技能
1.通过观察铝片的外观,知道铝是一种在空气中易被氧化的金属
2.知道铝在浓硫酸、浓硝酸中发生钝化,以及铝的应用。
3.通过铝与盐酸和氢氧化钠的反应,掌握铝与酸和碱的反应规律
(二)、过程与方法
1.学习以实验为基础的实验探究方法;
2.通过铝与浓硫酸、浓硝酸反应以及铝与稀盐酸、稀硫酸反应的现象的探讨,了解对比这一重要科学方法在科学学习过程中的应用
(三)、情感态度与价值观
1.引导学生关注身边的化学物质,让他们认识到化学是一门有用的学科。
2.通过实验或观察或找出金属在生产、生活中的应用,提高学习化学的兴趣,增强学好化学、服务社会的责任感和使命感。
五、重点难点
教学重点:铝的化学性质。
教学难点:铝的化学性质
六、教学策略与手段
借助多媒体辅助教学,以情境激发学生的学习积极性。以实验探究法为主线,通过设疑引导学生积极猜想,同时用实验观察、实验操作、交流讨论等方法完成本课的教学。
七、课前准备
仪器药品:铝箔,铝粉,已打磨过的铝片,未打磨过的铝片,生锈的铁片,稀氢氧化钠溶液,稀盐酸,稀硫酸,浓硫酸,洁净的试管,砂纸,生活中常见铝制品
相关资料:了解铝在生产生活中对人类产生的利弊。
八、教学过程
【问题引入】【板书】【关于铝的两个趣事】【设问】【过渡】【板书】【分析铝的结构】【实物展示】【设疑】【学生设计实验,教师点评】【观察实验】【板书】【学生板书】【讲解】【板书】【学生读课本】【过渡】【实物展示】【板书】【学生板书】【讲解和阅读】【过渡】【板书】【演示实验】【学生观察现象并汇报结果】【疑问】【教师解释现象及讲解】【板书】【总结】【过渡】【学生设计实验并教师点评】【板书】【学生1板书】【学生2板书】【学生3板书】【学生4板书】【过渡】【学生实验】【学生观察并汇报实验现象】【板书】【学生板书】【讲解】【板书】【过渡】【学生阅读课本并回答问题】【板书】【小结】【作业】
问题:你在日常生活中见到过哪些铝制品?
(铝锅、铝制餐具、易拉罐、烧烤用铝箔纸、装药的铝箔纸、铝制导线等。)观察桌面上的金属铝,你能说出铝的物理性质吗?(物理性质一般从哪几个角度说明?)物理性质具有银白色金属光泽的固体,密度较小,有导热性、导电性、延展性。(口述补充:熔点约660℃,其熔点比钠高,比铁、铜低。)趣事一:在19世纪以前,铝是一种非常稀有的贵金属,价格比黄金还要贵。拿破仑三世时,拿破仑使用一套珍藏的铝制餐具,而大臣们使用的是银制餐具。趣事二:门捷列夫创建了元素周期表,受到英国皇家学会的表彰,奖品非常非常贵重,是一只铝制奖杯。问题:地壳中含量最多的金属元素是什么?(铝)追问:既然铝在自然界的含量这么大,为什么它在当时如此珍贵?(讲解:其实,这不足为奇,因为铝的价值贵贱,完全取决于炼铝工业的水平。那时,炼铝的工业水平比较低,铝比较稀少,所以很珍贵。)问题:铝在地壳中以什么形式存在?游离态还是化合态?为什么?(化合态,分析铝的原子结构,对铝的化学性质进行猜想。)
结构
性质铝的最外层有三个电子,化学反应中,容易失去这三个电子,是性质比较活泼的金属,在反应中常表现出较强的还原性。所以在自然界以化合态形式存在,如氧化铝。请大家看久置在潮湿空气中的一个铝片和一个铁片。我们很清楚看到铁发生了严重的腐蚀,而铝却完好无损。(改成:铁也是我们日常生活中常见的金属,比较铁和铝的活泼性)这能否说明:铁比铝活泼?(金属活动性顺序表,铝排在铁之前,铝活泼)请同学们用实验的方法,证明铝比铁活泼。(铝能把氯化亚铁中的铁置换出来;过量的铝能把氯化铁中的铁置换出来;大小相同的铝片和铁片,放入相同稀盐酸中,比较反应快慢……)如果铝能把氧化铁中的铁置换出来,是不是也可以说明铝比铁活泼呢?看“铝热反应”实验,观察实验现象。现象:反应放出大量的热,并发出耀眼的光芒,纸漏斗的下部被烧穿,有熔融物落入沙中,该熔融物可以被磁铁吸引。根据现象写出化学方程式。化学性质2Al
+
Fe2O3
2
Fe
+
Al2O3
找出该反应的氧化剂和还原剂。利用铝的还原性和铝转化为氧化铝时能放出大量热的性质,工业上常用铝粉来还原一些金属氧化物,这类反应称为铝热反应。铝粉和金属氧化物的混合物称为铝热剂。化学性质铝热反应2Al
+
Fe2O3
2
Fe
+
Al2O3
铝热反应可以用于焊接铁轨(见课本66页图3-4)和定向爆破。铝热反应是用事实证明了铝比铁活泼。既然铝比铁活泼,为什么铁比铝易被腐蚀?展示两根铝条,一根铝条是用砂纸打磨过的,另一根铝条则没有做任何处理,注意观察一下这两根铝条表面有什么不同?用砂纸打磨过的铝条有光泽,没有用砂纸打磨过的铝条比较暗,这说明什么问题?(氧化膜)请同学们写出铝条在空气中表面变暗的化学方程式。2、与氧气反应4Al
+
3O2
===
2Al2O3铝表面的这层致密的氧化膜牢固的覆盖在铝的表面,阻止了内部的铝和空气接触,从而防止铝进一步被氧化,因而铝在空气中表现出良好的抗腐蚀性。而铁之所以会严重腐蚀是因为表面没有这层致密氧化膜。根据铝的这一性质,在实际生活中人们常通过一定的方法来增加氧化膜的厚度,使铝更加耐用。还可以对铝进行着色以加强对铝的保护。
阅读课本第64页,“观察与思考”的下面一段。另外,铝粉也能在空气中燃烧生成氧化铝除了氧气以外,还有哪些物质能使铝表面出现氧化膜呢?应该是具有什么性质的物质?(应该是强氧化性的物质,如浓硫酸、浓硝酸)3、与酸反应(1)强氧化性酸(浓硫酸、浓硝酸)接下来探究一下铝和浓硫酸的反应。实验:展示一根已经打磨过的铝条,把它放入一只洁净的试管中,再加入约3ml的浓硫酸。观察实验现象。请一个同学来回答一下他所观察到的实验现象。(无明显现象)
无明显现象就说明没有发生反应吗?
如何证明已经发生了反应?(把铝片放入硫酸铜溶液中,如无法置换出金属铜,说明已经形成氧化膜)
除了浓硫酸以外,浓硝酸也可以发生类似反应。在常温下,铝遇浓硫酸,浓硝酸会在表面生成一层致密的氧化膜,阻止内部的铝进一步氧化,我们把这种现象叫做钝化。常温下,铝在浓硫酸,浓硝酸中钝化。利用铝这个特殊的性质,我们可以用铝槽车来运输浓硫酸和浓硝酸。氧气,浓硫酸,浓硝酸都可以使铝表面出现氧化膜。还有没有其他实验的方法证明,铝表面出现了一层氧化膜?请设计实验。(把铝放入稀盐酸或稀硫酸中,刚开始没有明显现象,后产生气泡;把铝放入氯化铜溶液中,无明显现象……)
铝能与稀盐酸或稀硫酸反应放出气体,写出这两个化学方程式。(2)弱氧化性酸(如盐酸、稀硫酸)2Al
+
6HCl
===
2AlCl3
+
3H2↑2Al
+
3H2SO4
===
Al2(SO4)3
+
3H2↑把上述两个反应改成离子方程式。2Al
+
6H+
===
2Al3+
+
3H2↑2Al
+
6H+
===
2Al3+
+
3H2↑铝除了与酸反应以外,能否与碱发生反应?(从铝在元素周期表中的位置说明,并用实验验证)学生实验:把打磨过的铝片放入试管中,再向其中加入稀氢氧化钠溶液,观察实验现象。现象:铝表面有气泡产生,点燃产生的气体有爆鸣声。通过现象及氧化还原反应规律写出化学方程式。4、与碱反应2Al
+
2NaOH+
2H2O
===
2NaAlO2
+
3H2↑试写出该反应的离子方程式。2Al
+
2OH-+
2H2O
===
2AlO2-
+
3H2↑从上述反应可知道铝既可以和酸反应又可以和碱反应,像这样既能和酸反应,也能和碱反应的金属,称为两性金属。两性金属铝这种金属虽然很活泼,由于表面有氧化膜,所以抗腐蚀能力强,密度比较小(质量轻),铝的优点很多,但它质地比较软,强度和韧性都较差,所以常常把铝制成铝合金来应用。一般地,金属制成合金之后,会有更加优良的性能,比如说铝与其他金属或非金属熔合成合金后,强度高、可塑性好、抗腐蚀能力强,在生产生活中应用广泛。阅读课本66页一段,说说铝合金有哪些优点?铝合金有哪些应用?总结铝的用途与性质之间的关系,得出结论:性质
用途学习了本节课之后,学生总结这样两个问题:根据本节课所学,总结铝能与哪些物质发生反应?根据钠和镁的性质,猜测铝还能与哪些物质发生反应?铝有什么用途?铝和铝合金制品的用处很大,在生产生活中的各领域都有涉及,但是经研究发现,铝元素能损害人的脑细胞,因此在日常生活中要防止铝的吸收,减少铝制品的使用。比如少吃炸油条、由铝包装的糖果等食品,少喝易拉罐装的饮料。虽然铝离子有毒,但危害和其贡献是无法相提并论的,我们要学会扬长避短,让它对人类社会将发挥出更为重要的作用。完成学案中的练习
提问学生,并教师板书。学生阅读,提高进一步学习的兴趣矛盾引发学生思考让学生了解结构、性质之间的关系。复习了氧化还原反应相关知识点培养学生设计实验的能力,和严谨的科学态度培养学生观察能力、语言组织能力复习氧化还原内容。了解铝热反应的应用矛盾引发学生思考因为氧化膜,解决矛盾让学生养成利用教材的习惯涉及氧化还原内容培养学生观察能力提高学生设计实验能力及语言表达能力,和严谨的科学态度学生根据金属与酸反应规律直接写出化学方程式复习离子方程式培养学生实验操作能力,实验观察能力,及书写化学方程式的能力(可以通过实验判断氢气的产生,也可以根据化合价升降判断产物氢气。)复习离子方程式让学生了解结构、性质、用途之间的关系培养学生总结归纳能力教师补充
【板书设计】
铝及铝合金
一、物理性质
具有银白色金属光泽的固体,密度较小,有导热性、导电性、延展性。
结构
性质
用途
2、
化学性质
1、铝热反应
2Al
+
Fe2O3
2
Fe
+
Al2O3
1、
与氧气反应
4Al
+
3O2
===
2Al2O3
4Al
+
3O2
2Al2O3
3、与酸反应
(1)强氧化性酸(浓硫酸、浓硝酸)
常温下,铝在浓硫酸,浓硝酸中钝化。
(2)弱氧化性酸(如盐酸、稀硫酸)
2Al
+
6HCl
===
2AlCl3
+
3H2↑
2Al
+
3H2SO4
===
Al2(SO4)3
+
3H2↑
2Al
+
6H+
===
2Al3+
+
3H2↑
4、与碱反应
2Al
+
2NaOH+
2H2O
===
2NaAlO2+3H2↑
2Al
+
2OH-+
2H2O
===
2AlO2-
+
3H2
决定
决定
决定
决定
