人教版初中化学 2.4 辨别物质的元素组成(课件40页)
文档属性
| 名称 | 人教版初中化学 2.4 辨别物质的元素组成(课件40页) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.6MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-11-02 00:00:00 | ||
图片预览








文档简介
九年级 上册
化学(科粤版)
第二章 空气、物质的构成
专题2.4 辨别物质的元素组成
(课件)
2.【云南?中考】如图为氯原子的原子结构示意图。下列说法不正确的是( )
A.氯原子的质子数为17 B.氯原子在化学变化中易失电子 C.氯原子的第二层电子数为8 D.氯原子核外有3个电子层
B
1.下列有关原子结构的说法正确的是( )
A.原子中的中子带负电荷 B.决定原子种类的是质子数
C.原子中质子与中子的数目一定相同
D.原子的质量主要集中在质子和电子上
B
知识回顾
4.下列是几种粒子的结构示意图,属于阳离子的是( )
D
3.【聊城?中考】分子、原子和离子都是构成物质的基本粒子。下列说法正确的是( )
A.分子由原子构成,分子比原子大 B.水遇冷凝结成冰,水分子停止了运动 C.原子是最小的粒子,不可再分 D.氯化钠是由
钠离子和氯离子构成的
D
知识回顾
你知道标签中的钙、镁、钾、钠指的是什么?
某矿泉水瓶上的标签
元素
那么什么是元素呢?
趣味导学
物质
构成该物质的分子
构成该分子的原子
氧气
水
二氧化碳
五氧化二磷
氧化汞
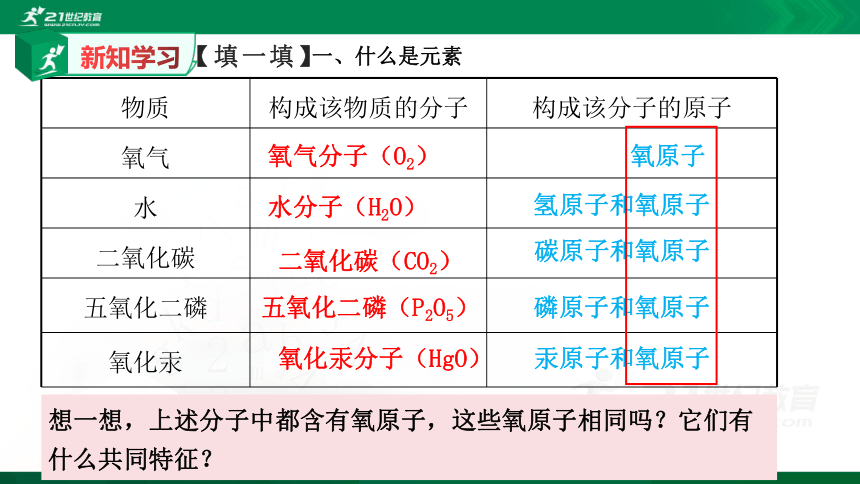
【填一填】
氧原子
碳原子和氧原子
氢原子和氧原子
磷原子和氧原子
汞原子和氧原子
氧气分子(O2)
水分子(H2O)
二氧化碳(CO2)
五氧化二磷(P2O5)
氧化汞分子(HgO)
想一想,上述分子中都含有氧原子,这些氧原子相同吗?它们有什么共同特征?
一、什么是元素
新知学习
上述分子中的氧原子中都含有8个质子,即核电荷数为8.
在化学上,把具有相同核电荷数(即质子数)的一类原子总称为元素。
如:我们将质子数为8的氧原子统称为氧元素;
将质子数为1的氢原子统称为氢元素;
将质子数为12的碳原子统称为碳元素
氢元素和氧元素最根本的区别是什么?
思考:
区别:质子数(或核电荷数)不同。
总称
一、什么是元素
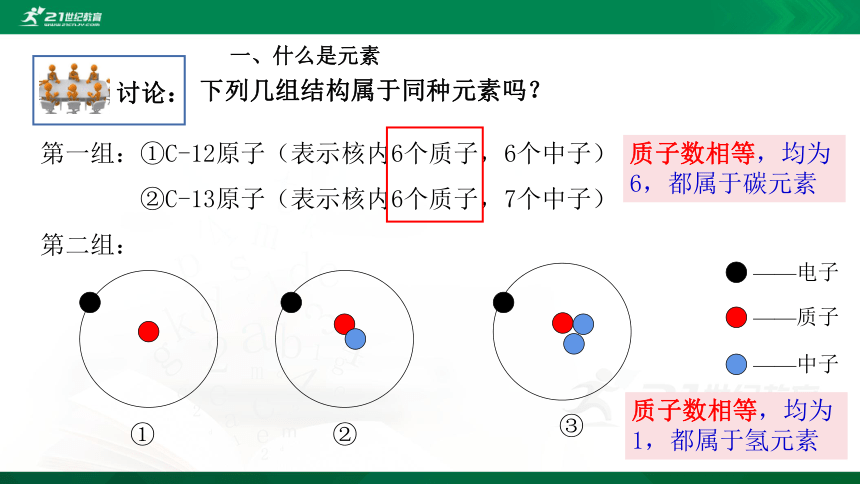
讨论:
下列几组结构属于同种元素吗?
第一组:①C-12原子(表示核内6个质子,6个中子)
②C-13原子(表示核内6个质子,7个中子)
质子数相等,均为6,都属于碳元素
——电子
——质子
——中子
第二组:
①
②
③
质子数相等,均为1,都属于氢元素
一、什么是元素
一、什么是元素
如:P2O5是由磷、氧两种元素组成,不能说成P2O5是由2个磷元素和5个氧元素组成。
【练一练】a、b、c三种原子的原子核中质子数相同,但中子数不同,它们是( )A.同一种原子 B.同一种分子 C.同一种元素 D.不同种元素
C
②元素是宏观概念,不能用“个”等单位形容,只区分元素种类。
【注意】
①元素的种类由原子的质子数决定,质子数不同,元素种类就不同;
【练一练】决定元素种类的依据是( ) A.质子数 B.中子数 C.核外电子数 D.原子的相对原子质量
A
【练一练】
1.二氧化碳是由 和 组成的,共有 种元素;
2.1个二氧化碳分子是由 和 构成的,共有 个原子。
3.酒精(C2H6O)是由 种元素组成的,1个酒精分子中含有2个 、6个 和2个 。
碳元素
氧元素
两
1个碳原子
3
2个氧原子
氢原子
碳原子
3
氧原子
一、什么是元素
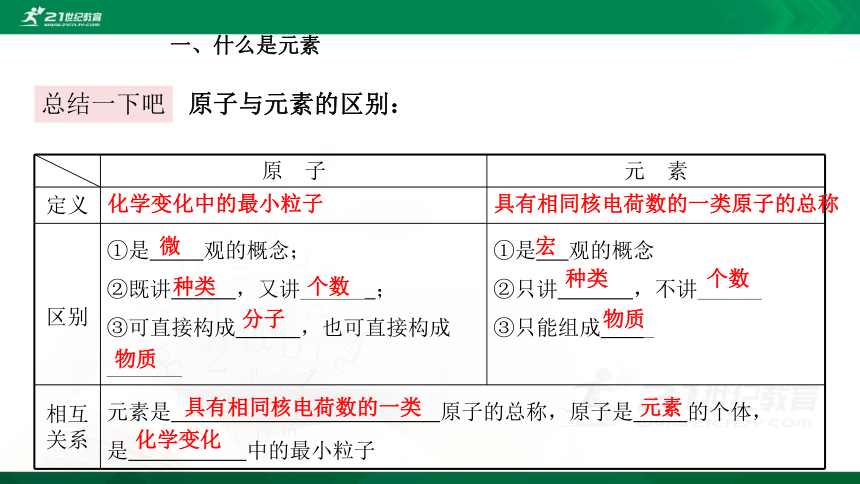
原子与元素的区别:
原 子
元 素
定义
区别
①是 观的概念;
②既讲 ,又讲______ ;
③可直接构成 ,也可直接构成_______
①是 观的概念
②只讲 ,不讲______
③只能组成 _
相互
关系
元素是 原子的总称,原子是 的个体,
是 中的最小粒子
具有相同核电荷数的一类原子的总称
化学变化中的最小粒子
种类
微
物质
分子
个数
种类
宏
物质
个数
具有相同核电荷数的一类
化学变化
元素
总结一下吧
一、什么是元素
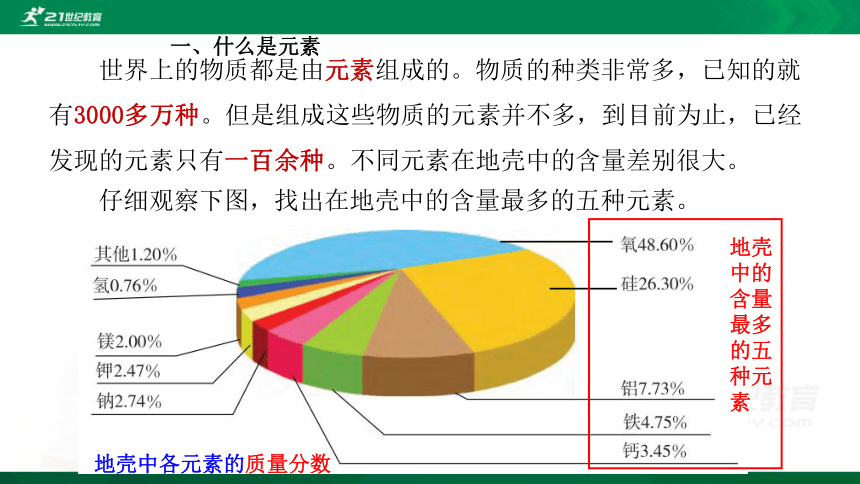
世界上的物质都是由元素组成的。物质的种类非常多,已知的就有3000多万种。但是组成这些物质的元素并不多,到目前为止,已经发现的元素只有一百余种。不同元素在地壳中的含量差别很大。
仔细观察下图,找出在地壳中的含量最多的五种元素。
地壳中各元素的质量分数
地壳中的含量最多的五种元素
一、什么是元素
知识视窗
动植物细胞中各元素所占的质量分数
下表是动植物细胞中各元素所占的质量分数,其中所占质量分数最大的元素是 。
氧元素
这部分元素所占的质量分数很小,但是对机体却有非常重要的作用
一、什么是元素
【练一练】如图为地壳中的元素含量示意图(质量分数)。其中Z表示的元素为( )
A.氧 B.硅 C.铝 D.铁
C
【练一练】我国早期的化学著作《化学鉴原》(1871年)中把一种元素翻译为“矽(xi)”.该元素在地壳里的含量占第二位,现在这种“矽”元素的名称为( )A.硅 B.硒 C.锡 D.氧
A
一、什么是元素
观察下列用汉字表示的元素名称,你能观察到什么规律?
观察:
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}金属元素
非金属元素
银
铜
铁
钠
氢
氧
氮
溴
碘
碳
硫
都有“钅”旁
都有“气”旁,常呈气态
都有“氵”,常呈液态
都有“石”旁,常呈固态
我们用不同部首偏旁的汉字来表示元素,为元素的中文名称。
这种元素的命名方法有何优缺点?
思考:
优点:
缺点:
非常形象化。
书写不太方便,在国际学术交流时也非常困难。
二、怎样表示元素的名称和符号
为了书写和学术交流的方便,国际上采用统一的符号来表示各种元素,这就是元素符号。
·我们用元素拉丁文名称的第一个大写字母来表示元素,如氢元素的符号为H,氧元素的符号为O;
·如果几种元素拉丁文名称的第一个字母相同时,就附加一个小写字母来区别,如用Cu表示 ,用Ca表示 ,用Cl表示 。
元素符号的书写规律:
铜元素
钙元素
氯元素
二、怎样表示元素的名称和符号
中文名称
拉丁文
元素符号
氢
Hydrongenium
氧
Oxygenium
碳
Carbonium
铁
Ferrum
铜
Cuprum
【注意】
①由一个字母表示的元素符号要大写;
②由两个字母表示的元素符号,第一个字母大写,第二个字母小写。
H
Ca
Fe
Mg
Ag
H
O
C
Fe
Cu
【填一填】
二、怎样表示元素的名称和符号
【练一练】写出下列元素的符号。
铁_______;钙_______;碘_______;硫_______;
钡_______;氖_______;氟_______;镁_______。
【练一练】钙元素符号是( )A.C B.Cu C.CA D.Ca
D
想一想:
【练一练】元素符号“ CO”的写法对吗?如果不对的话应该如何改正?
不对,元素符号的第二个字母要小写。应写为Co。
元素符号“ Co”能表示哪些意义呢?
Fe
Ca
I
S
Ba
Ne
F
Mg
二、怎样表示元素的名称和符号
微观上,元素符号表示 ;
宏观上,元素符号表示 。
一种元素
该元素的一个原子
【注意】由原子构成的物质,其元素符号还能表示该种物质,如C、S、Cu、Fe、He等
所以,微观上,Co表示 。
宏观上,Co表示 ,还表示 ;
钴元素
一个钴原子
钴这种物质
想一想:
元素符号“2O”能表示2个氧元素吗?为什么?
不能,元素是宏观概念,只讲种类不讲个数。“2O”只能表示2个氧原子。
二、怎样表示元素的名称和符号
【练一练】下列元素符号分别表示什么意义?
(1)3H: ;5C: ;10S: ;
3个氢原子
5个碳原子
10个硫原子
【练一练】下列既能表示一种元素又能表示一个原子,还能表示一种物质的是( )A.H B.O2 C.2N D.Cu
D
【练一练】元素符号“H”表示什么意义?
微观上,表示 ;
宏观上,表示 。
氢元素
一个氢原子
注意:若元素符号前面加上阿拉伯数字,就只表示原子个数,没有宏观意义。
二、怎样表示元素的名称和符号
迄今为止,自然界的元素种类有100多种,这些元素彼此之间有无联系?有无规律可循?
科学家们早在很多年前就开始进行探索。
1869年,俄国化学家门捷列夫根据元素的原子结构和性质,把它们科学有序地排列起来,这样就得到了元素周期表。
门捷列夫
观察:
1.仔细观察元素周期表,数一数元素周期表有几个横行?有几个纵行?
三、元素周期表
三、元素周期表
元素周期表中:
·共有 个横行,每一横行叫一周期,共 个周期。
·共有 个纵行,它们分成了 个族(其中8、9、10三个纵行共同组成
一个族)
7
7
18
16
2.仔细观察元素周期表上的颜色有几种?分别代表什么意思?
·元素周期表的浅色区(左侧)为 ,该类元素原子的最外层电子数一般 4,在化学反应中容易 电子变成稳定结构。
·元素周期表的深色区(右侧)为 ,该类元素原子的最外层电子数一般 4(氢元素只有1个电子)。其中:
金属元素
非金属元素
小于
失去
大于
三、元素周期表
元素周期表最右侧一列为 ,该元素原子最外层为 个电子(氦元素原子最外层为2),不易得失电子,均为 结构。
稀有气体元素
8
稳定
其它非金属元素原子的最外层电子数(氢元素除外)一般 4,在化学反应中容易 电子变成稳定结构。
大于
得到
除第一周期外,每个周期均是 开头,过渡到 ,最后以 结尾。
金属元素
非金属元素
稀有气体
三、元素周期表
观察:
观察元素周期表前三周元素的原子结构示意图,同周期的元素有何异同点?同族呢?
同周期: 相同,最外层电子数从左到右依次 。
同族: 相同,电子层数从上到下依次 。
最外层电子数相同的原子化学性质相似。
电子层数
增大
最外层电子数
增大
三、元素周期表
你知道吗?
在元素周期表中,每种元素周围的数字或字母分别代表什么意思?
硫
原子序数
相对原子质量
元素符号
元素名称
S
16
32.07
【注意】
1.原子序数=核电荷数= = ;
2.相对原子质量≈ + ,单位为1,通常不写。
质子数
中子数
核外电子数
质子数
三、元素周期表
【练一练】在元周期表中,应用于计算机的硅元素如图所示,下列
有关硅的说法正确的是( )
A.原子序数是14 B.原子个数是14
C.相对原子质量是14 D.质子数是28.1
14 Si
硅
28.1
C
【练一练】如图为碘元素在元素周期表的部分信息及其原子结构示意图。下列说法锆误的是( )
A.碘属于非金属元素
B.碘原子的核内质子数为53
C.碘的相对原子质量为126.9 D.碘属于第7周期元素
D
三、元素周期表
【练一练】1869年,俄国化学家门捷列夫编制了元素周期表。(1)为纪念门捷列夫,科学家将一种由人工核反应获得的新元素命名为钔(元素符号是Md),已知钔原子核电荷数为101,相对原子质量为256,则其中子数为 ,钔原子失去三个电子后形成离子,该离子符号为 。(2)如图为镁元素在元素周期表中的部分信息及部分原子的结构示意图。
①镁元素的相对原子质量为 。②A、B、C、D原子结构示意图中,与镁原子的化学性质最相似的是 (填字母序号)。③已知原子的核外电子层数与元素所在周期表中周期的序数相同,则B在元素周期表中排在第 周期。
Md3+
155
24.31
D
二
三、元素周期表
想一想:
以下两组纯净物在元素组成上有什么不同之处?
第一组:氧气(O2)、氩气(Ar)、碳(C)、铁(Fe)、汞(Hg)
第二组:二氧化碳(CO2)、氨气(NH3)、水(H2O)、硫酸(H2SO4)
只有一种元素构成
有两种或两种以上的元素构成
像氧气、氩气等由一种元素组成的纯净物叫做单质。
O
O
C
H
H
氧气(O2)
氢气(H2)
碳(C)
四、单质和化合物有何不同
像水、二氧化碳等由两种或两种以上元素组成的纯净物叫做化合物。
O
O
C
O
H
H
O
C
水(H2O)
二氧化碳(CO2)
一氧化碳(CO)
C
H
H
H
H
甲烷(NH4)
由两种元素组成且其中一种是氧元素的化合物叫做氧化物。
由同种元素组成的物质一定是纯净物吗?
想一想:
不一定,如氧气(O2)和臭氧(O2)的混合物。
四、单质和化合物有何不同
物质的简单分类:
物质
混合物
纯净物
化合物
单质
金属单质 (如铁、镁等)
非金属单质(如碳、氧气等)
氧化物
其它化合物(酸、碱、盐等)
由两种或多种物质混合而成的物质(如:空气、溶液等)
根据物质的组成是否单一
由一种物质组成的物质。(例如氧气、二氧化碳、高锰酸钾等)
根据元素的组成是否单一
同种元素组成的纯净物
不同种元素组成的纯净物
由两种元素组成,其中
一种是氧元素的化合物
四、单质和化合物有何不同
【练一练】下列各组物质,按混合物、化合物、单质顺序排列的是( )A.洁净的空气、干冰、液态氧 B.二氧化锰、酒精、水银 C.冰水共存物、过氧化氢、氮气 D.食盐、铁钉、石灰石
A
【练一练】下列物质中,属于氧化物的是( )A.Na2SO4 B.O2 C.H2O D.KOH
C
B
C
D
A
【练一练】下列各图中〇和●分别表示不同元素的原子,则其中表示化合物的是( )
A
四、单质和化合物有何不同
1.什么是元素:
2.元素的分布:①地壳中含量前五位的元素: ;②细胞中含量最高的元素: ;
具有相同质子数(或核电荷数)的一类原子的总称。
O、Si、Al、Fe、Ca
O
3.元素的简单分类:
元素分为金属元素、非金属元素和稀有气体元素。
4.元素符号(1)书写原则:
(2)元素符号表示的意义:
①表示某种元素②表示某种元素的一个原子。
有些元素符号还可表示一种单质,如Fe、He 、C 、Si(由原子直接构成的物质)
第一个字母大写,第二个字母小写,若该元素符号中只有一个字母,则大写。
课堂小结
5.元素周期表
(1)发现者:
(2)结构:
(3)排列规律: 同周期: 同族:
俄国科学家门捷列夫
7个周期16个族(7个横行18个纵行)
原子电子层数相同,最外层电子数逐渐增加
原子最电外层电子数相同(He例外),电子层数逐渐增加(化学性质相似)
(4)元素周期表中每一方格提供的信息:
硫
原子序数
相对原子质量
元素符号
元素名称
S
16
32.07
6.单质、化合物、氧化物
(1)单质:
由同种元素组成的纯净物,如氢气(H2)、 氮气(N2)、 氧气(O2)等
(2)化合物:
由不同种元素组成的纯净物,如二氧化碳(CO2)、 氧化铁(Fe2O3)等
(3)氧化物:
由两种元素组成,其中一种元素是氧元素的化合物,如CO2、Fe2O3等
物质
纯净物
混合物
单质
化合物
氧化物
其它化合物
1.“高钙牛奶”中的“钙”指的是( )A.元素 B.单质 C.分子 D.电子
A
2.人体中含量(质量分数)最多的化学元素是( )A.氧 B.碳 C.氢 D.钙
A
3.镍元素在元素周期表的相关信息如图所示。下列有关镍元素的说法正确的是( )
A.镍属于非金属元素 B.镍原子核外电子数为28 C.原子核内中子数为28 D.相对原子质量为58.69g
B
课堂检测
4.下列各组物质中,前者是化合物,后者是单质的是( )
A.氮气 二氧化锰 B.二氧化碳 氧气
C.空气 硫 D.冰 水
B
5.下列属于氧化物的是( )A.双氧水 B.干冰 C.铁锈 D.氯酸钾
B
6.右图表示的是地壳中所含各种元素的质量分数。请据图回答下列问题。
(1)含量最多的非金属元素是________,
最多的金属元素为________。
(2)图中表示出的金属元素有_____
_____________________。
(3)地壳中铝元素的含量为________。
氧
铝
铝、铁、钙、钠、钾、镁
7.73%
7.元素周期表是学习和研究化学的重要工具。如图是元素周期表的一部分。
(2)氮元素和磷元素的化学性质相似,是因为氮原子和磷原子的 相同。(3)x2+与O2﹣的核外电子排布相同,则x的元素符号是 。(4)表中不同种元素最本质的区别是 (填序号)。 A.质子数不同 B.中子数不同 C.相对原子质量不同 D.最外层电子数不同
(1)地壳中含量最多的元素是 ,该元素位于元素周期表中的第 周期。在化学反应中,原子序数为17的元素的原子容易 (填“得到”或“失去”)电子。
最外层电子数
Mg
A
氧元素
二
得到
谢谢聆听
化学(科粤版)
第二章 空气、物质的构成
专题2.4 辨别物质的元素组成
(课件)
2.【云南?中考】如图为氯原子的原子结构示意图。下列说法不正确的是( )
A.氯原子的质子数为17 B.氯原子在化学变化中易失电子 C.氯原子的第二层电子数为8 D.氯原子核外有3个电子层
B
1.下列有关原子结构的说法正确的是( )
A.原子中的中子带负电荷 B.决定原子种类的是质子数
C.原子中质子与中子的数目一定相同
D.原子的质量主要集中在质子和电子上
B
知识回顾
4.下列是几种粒子的结构示意图,属于阳离子的是( )
D
3.【聊城?中考】分子、原子和离子都是构成物质的基本粒子。下列说法正确的是( )
A.分子由原子构成,分子比原子大 B.水遇冷凝结成冰,水分子停止了运动 C.原子是最小的粒子,不可再分 D.氯化钠是由
钠离子和氯离子构成的
D
知识回顾
你知道标签中的钙、镁、钾、钠指的是什么?
某矿泉水瓶上的标签
元素
那么什么是元素呢?
趣味导学
物质
构成该物质的分子
构成该分子的原子
氧气
水
二氧化碳
五氧化二磷
氧化汞
【填一填】
氧原子
碳原子和氧原子
氢原子和氧原子
磷原子和氧原子
汞原子和氧原子
氧气分子(O2)
水分子(H2O)
二氧化碳(CO2)
五氧化二磷(P2O5)
氧化汞分子(HgO)
想一想,上述分子中都含有氧原子,这些氧原子相同吗?它们有什么共同特征?
一、什么是元素
新知学习
上述分子中的氧原子中都含有8个质子,即核电荷数为8.
在化学上,把具有相同核电荷数(即质子数)的一类原子总称为元素。
如:我们将质子数为8的氧原子统称为氧元素;
将质子数为1的氢原子统称为氢元素;
将质子数为12的碳原子统称为碳元素
氢元素和氧元素最根本的区别是什么?
思考:
区别:质子数(或核电荷数)不同。
总称
一、什么是元素
讨论:
下列几组结构属于同种元素吗?
第一组:①C-12原子(表示核内6个质子,6个中子)
②C-13原子(表示核内6个质子,7个中子)
质子数相等,均为6,都属于碳元素
——电子
——质子
——中子
第二组:
①
②
③
质子数相等,均为1,都属于氢元素
一、什么是元素
一、什么是元素
如:P2O5是由磷、氧两种元素组成,不能说成P2O5是由2个磷元素和5个氧元素组成。
【练一练】a、b、c三种原子的原子核中质子数相同,但中子数不同,它们是( )A.同一种原子 B.同一种分子 C.同一种元素 D.不同种元素
C
②元素是宏观概念,不能用“个”等单位形容,只区分元素种类。
【注意】
①元素的种类由原子的质子数决定,质子数不同,元素种类就不同;
【练一练】决定元素种类的依据是( ) A.质子数 B.中子数 C.核外电子数 D.原子的相对原子质量
A
【练一练】
1.二氧化碳是由 和 组成的,共有 种元素;
2.1个二氧化碳分子是由 和 构成的,共有 个原子。
3.酒精(C2H6O)是由 种元素组成的,1个酒精分子中含有2个 、6个 和2个 。
碳元素
氧元素
两
1个碳原子
3
2个氧原子
氢原子
碳原子
3
氧原子
一、什么是元素
原子与元素的区别:
原 子
元 素
定义
区别
①是 观的概念;
②既讲 ,又讲______ ;
③可直接构成 ,也可直接构成_______
①是 观的概念
②只讲 ,不讲______
③只能组成 _
相互
关系
元素是 原子的总称,原子是 的个体,
是 中的最小粒子
具有相同核电荷数的一类原子的总称
化学变化中的最小粒子
种类
微
物质
分子
个数
种类
宏
物质
个数
具有相同核电荷数的一类
化学变化
元素
总结一下吧
一、什么是元素
世界上的物质都是由元素组成的。物质的种类非常多,已知的就有3000多万种。但是组成这些物质的元素并不多,到目前为止,已经发现的元素只有一百余种。不同元素在地壳中的含量差别很大。
仔细观察下图,找出在地壳中的含量最多的五种元素。
地壳中各元素的质量分数
地壳中的含量最多的五种元素
一、什么是元素
知识视窗
动植物细胞中各元素所占的质量分数
下表是动植物细胞中各元素所占的质量分数,其中所占质量分数最大的元素是 。
氧元素
这部分元素所占的质量分数很小,但是对机体却有非常重要的作用
一、什么是元素
【练一练】如图为地壳中的元素含量示意图(质量分数)。其中Z表示的元素为( )
A.氧 B.硅 C.铝 D.铁
C
【练一练】我国早期的化学著作《化学鉴原》(1871年)中把一种元素翻译为“矽(xi)”.该元素在地壳里的含量占第二位,现在这种“矽”元素的名称为( )A.硅 B.硒 C.锡 D.氧
A
一、什么是元素
观察下列用汉字表示的元素名称,你能观察到什么规律?
观察:
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}金属元素
非金属元素
银
铜
铁
钠
氢
氧
氮
溴
碘
碳
硫
都有“钅”旁
都有“气”旁,常呈气态
都有“氵”,常呈液态
都有“石”旁,常呈固态
我们用不同部首偏旁的汉字来表示元素,为元素的中文名称。
这种元素的命名方法有何优缺点?
思考:
优点:
缺点:
非常形象化。
书写不太方便,在国际学术交流时也非常困难。
二、怎样表示元素的名称和符号
为了书写和学术交流的方便,国际上采用统一的符号来表示各种元素,这就是元素符号。
·我们用元素拉丁文名称的第一个大写字母来表示元素,如氢元素的符号为H,氧元素的符号为O;
·如果几种元素拉丁文名称的第一个字母相同时,就附加一个小写字母来区别,如用Cu表示 ,用Ca表示 ,用Cl表示 。
元素符号的书写规律:
铜元素
钙元素
氯元素
二、怎样表示元素的名称和符号
中文名称
拉丁文
元素符号
氢
Hydrongenium
氧
Oxygenium
碳
Carbonium
铁
Ferrum
铜
Cuprum
【注意】
①由一个字母表示的元素符号要大写;
②由两个字母表示的元素符号,第一个字母大写,第二个字母小写。
H
Ca
Fe
Mg
Ag
H
O
C
Fe
Cu
【填一填】
二、怎样表示元素的名称和符号
【练一练】写出下列元素的符号。
铁_______;钙_______;碘_______;硫_______;
钡_______;氖_______;氟_______;镁_______。
【练一练】钙元素符号是( )A.C B.Cu C.CA D.Ca
D
想一想:
【练一练】元素符号“ CO”的写法对吗?如果不对的话应该如何改正?
不对,元素符号的第二个字母要小写。应写为Co。
元素符号“ Co”能表示哪些意义呢?
Fe
Ca
I
S
Ba
Ne
F
Mg
二、怎样表示元素的名称和符号
微观上,元素符号表示 ;
宏观上,元素符号表示 。
一种元素
该元素的一个原子
【注意】由原子构成的物质,其元素符号还能表示该种物质,如C、S、Cu、Fe、He等
所以,微观上,Co表示 。
宏观上,Co表示 ,还表示 ;
钴元素
一个钴原子
钴这种物质
想一想:
元素符号“2O”能表示2个氧元素吗?为什么?
不能,元素是宏观概念,只讲种类不讲个数。“2O”只能表示2个氧原子。
二、怎样表示元素的名称和符号
【练一练】下列元素符号分别表示什么意义?
(1)3H: ;5C: ;10S: ;
3个氢原子
5个碳原子
10个硫原子
【练一练】下列既能表示一种元素又能表示一个原子,还能表示一种物质的是( )A.H B.O2 C.2N D.Cu
D
【练一练】元素符号“H”表示什么意义?
微观上,表示 ;
宏观上,表示 。
氢元素
一个氢原子
注意:若元素符号前面加上阿拉伯数字,就只表示原子个数,没有宏观意义。
二、怎样表示元素的名称和符号
迄今为止,自然界的元素种类有100多种,这些元素彼此之间有无联系?有无规律可循?
科学家们早在很多年前就开始进行探索。
1869年,俄国化学家门捷列夫根据元素的原子结构和性质,把它们科学有序地排列起来,这样就得到了元素周期表。
门捷列夫
观察:
1.仔细观察元素周期表,数一数元素周期表有几个横行?有几个纵行?
三、元素周期表
三、元素周期表
元素周期表中:
·共有 个横行,每一横行叫一周期,共 个周期。
·共有 个纵行,它们分成了 个族(其中8、9、10三个纵行共同组成
一个族)
7
7
18
16
2.仔细观察元素周期表上的颜色有几种?分别代表什么意思?
·元素周期表的浅色区(左侧)为 ,该类元素原子的最外层电子数一般 4,在化学反应中容易 电子变成稳定结构。
·元素周期表的深色区(右侧)为 ,该类元素原子的最外层电子数一般 4(氢元素只有1个电子)。其中:
金属元素
非金属元素
小于
失去
大于
三、元素周期表
元素周期表最右侧一列为 ,该元素原子最外层为 个电子(氦元素原子最外层为2),不易得失电子,均为 结构。
稀有气体元素
8
稳定
其它非金属元素原子的最外层电子数(氢元素除外)一般 4,在化学反应中容易 电子变成稳定结构。
大于
得到
除第一周期外,每个周期均是 开头,过渡到 ,最后以 结尾。
金属元素
非金属元素
稀有气体
三、元素周期表
观察:
观察元素周期表前三周元素的原子结构示意图,同周期的元素有何异同点?同族呢?
同周期: 相同,最外层电子数从左到右依次 。
同族: 相同,电子层数从上到下依次 。
最外层电子数相同的原子化学性质相似。
电子层数
增大
最外层电子数
增大
三、元素周期表
你知道吗?
在元素周期表中,每种元素周围的数字或字母分别代表什么意思?
硫
原子序数
相对原子质量
元素符号
元素名称
S
16
32.07
【注意】
1.原子序数=核电荷数= = ;
2.相对原子质量≈ + ,单位为1,通常不写。
质子数
中子数
核外电子数
质子数
三、元素周期表
【练一练】在元周期表中,应用于计算机的硅元素如图所示,下列
有关硅的说法正确的是( )
A.原子序数是14 B.原子个数是14
C.相对原子质量是14 D.质子数是28.1
14 Si
硅
28.1
C
【练一练】如图为碘元素在元素周期表的部分信息及其原子结构示意图。下列说法锆误的是( )
A.碘属于非金属元素
B.碘原子的核内质子数为53
C.碘的相对原子质量为126.9 D.碘属于第7周期元素
D
三、元素周期表
【练一练】1869年,俄国化学家门捷列夫编制了元素周期表。(1)为纪念门捷列夫,科学家将一种由人工核反应获得的新元素命名为钔(元素符号是Md),已知钔原子核电荷数为101,相对原子质量为256,则其中子数为 ,钔原子失去三个电子后形成离子,该离子符号为 。(2)如图为镁元素在元素周期表中的部分信息及部分原子的结构示意图。
①镁元素的相对原子质量为 。②A、B、C、D原子结构示意图中,与镁原子的化学性质最相似的是 (填字母序号)。③已知原子的核外电子层数与元素所在周期表中周期的序数相同,则B在元素周期表中排在第 周期。
Md3+
155
24.31
D
二
三、元素周期表
想一想:
以下两组纯净物在元素组成上有什么不同之处?
第一组:氧气(O2)、氩气(Ar)、碳(C)、铁(Fe)、汞(Hg)
第二组:二氧化碳(CO2)、氨气(NH3)、水(H2O)、硫酸(H2SO4)
只有一种元素构成
有两种或两种以上的元素构成
像氧气、氩气等由一种元素组成的纯净物叫做单质。
O
O
C
H
H
氧气(O2)
氢气(H2)
碳(C)
四、单质和化合物有何不同
像水、二氧化碳等由两种或两种以上元素组成的纯净物叫做化合物。
O
O
C
O
H
H
O
C
水(H2O)
二氧化碳(CO2)
一氧化碳(CO)
C
H
H
H
H
甲烷(NH4)
由两种元素组成且其中一种是氧元素的化合物叫做氧化物。
由同种元素组成的物质一定是纯净物吗?
想一想:
不一定,如氧气(O2)和臭氧(O2)的混合物。
四、单质和化合物有何不同
物质的简单分类:
物质
混合物
纯净物
化合物
单质
金属单质 (如铁、镁等)
非金属单质(如碳、氧气等)
氧化物
其它化合物(酸、碱、盐等)
由两种或多种物质混合而成的物质(如:空气、溶液等)
根据物质的组成是否单一
由一种物质组成的物质。(例如氧气、二氧化碳、高锰酸钾等)
根据元素的组成是否单一
同种元素组成的纯净物
不同种元素组成的纯净物
由两种元素组成,其中
一种是氧元素的化合物
四、单质和化合物有何不同
【练一练】下列各组物质,按混合物、化合物、单质顺序排列的是( )A.洁净的空气、干冰、液态氧 B.二氧化锰、酒精、水银 C.冰水共存物、过氧化氢、氮气 D.食盐、铁钉、石灰石
A
【练一练】下列物质中,属于氧化物的是( )A.Na2SO4 B.O2 C.H2O D.KOH
C
B
C
D
A
【练一练】下列各图中〇和●分别表示不同元素的原子,则其中表示化合物的是( )
A
四、单质和化合物有何不同
1.什么是元素:
2.元素的分布:①地壳中含量前五位的元素: ;②细胞中含量最高的元素: ;
具有相同质子数(或核电荷数)的一类原子的总称。
O、Si、Al、Fe、Ca
O
3.元素的简单分类:
元素分为金属元素、非金属元素和稀有气体元素。
4.元素符号(1)书写原则:
(2)元素符号表示的意义:
①表示某种元素②表示某种元素的一个原子。
有些元素符号还可表示一种单质,如Fe、He 、C 、Si(由原子直接构成的物质)
第一个字母大写,第二个字母小写,若该元素符号中只有一个字母,则大写。
课堂小结
5.元素周期表
(1)发现者:
(2)结构:
(3)排列规律: 同周期: 同族:
俄国科学家门捷列夫
7个周期16个族(7个横行18个纵行)
原子电子层数相同,最外层电子数逐渐增加
原子最电外层电子数相同(He例外),电子层数逐渐增加(化学性质相似)
(4)元素周期表中每一方格提供的信息:
硫
原子序数
相对原子质量
元素符号
元素名称
S
16
32.07
6.单质、化合物、氧化物
(1)单质:
由同种元素组成的纯净物,如氢气(H2)、 氮气(N2)、 氧气(O2)等
(2)化合物:
由不同种元素组成的纯净物,如二氧化碳(CO2)、 氧化铁(Fe2O3)等
(3)氧化物:
由两种元素组成,其中一种元素是氧元素的化合物,如CO2、Fe2O3等
物质
纯净物
混合物
单质
化合物
氧化物
其它化合物
1.“高钙牛奶”中的“钙”指的是( )A.元素 B.单质 C.分子 D.电子
A
2.人体中含量(质量分数)最多的化学元素是( )A.氧 B.碳 C.氢 D.钙
A
3.镍元素在元素周期表的相关信息如图所示。下列有关镍元素的说法正确的是( )
A.镍属于非金属元素 B.镍原子核外电子数为28 C.原子核内中子数为28 D.相对原子质量为58.69g
B
课堂检测
4.下列各组物质中,前者是化合物,后者是单质的是( )
A.氮气 二氧化锰 B.二氧化碳 氧气
C.空气 硫 D.冰 水
B
5.下列属于氧化物的是( )A.双氧水 B.干冰 C.铁锈 D.氯酸钾
B
6.右图表示的是地壳中所含各种元素的质量分数。请据图回答下列问题。
(1)含量最多的非金属元素是________,
最多的金属元素为________。
(2)图中表示出的金属元素有_____
_____________________。
(3)地壳中铝元素的含量为________。
氧
铝
铝、铁、钙、钠、钾、镁
7.73%
7.元素周期表是学习和研究化学的重要工具。如图是元素周期表的一部分。
(2)氮元素和磷元素的化学性质相似,是因为氮原子和磷原子的 相同。(3)x2+与O2﹣的核外电子排布相同,则x的元素符号是 。(4)表中不同种元素最本质的区别是 (填序号)。 A.质子数不同 B.中子数不同 C.相对原子质量不同 D.最外层电子数不同
(1)地壳中含量最多的元素是 ,该元素位于元素周期表中的第 周期。在化学反应中,原子序数为17的元素的原子容易 (填“得到”或“失去”)电子。
最外层电子数
Mg
A
氧元素
二
得到
谢谢聆听
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
