2021届鲁教版中考化学大一轮单元总复习:第八单元 海水中的化学第一节 海水中的化学(共48张PPT)
文档属性
| 名称 | 2021届鲁教版中考化学大一轮单元总复习:第八单元 海水中的化学第一节 海水中的化学(共48张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 2.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-11-02 00:00:00 | ||
图片预览









文档简介
第八单元 海水中的化学
第一节 海水中的化学
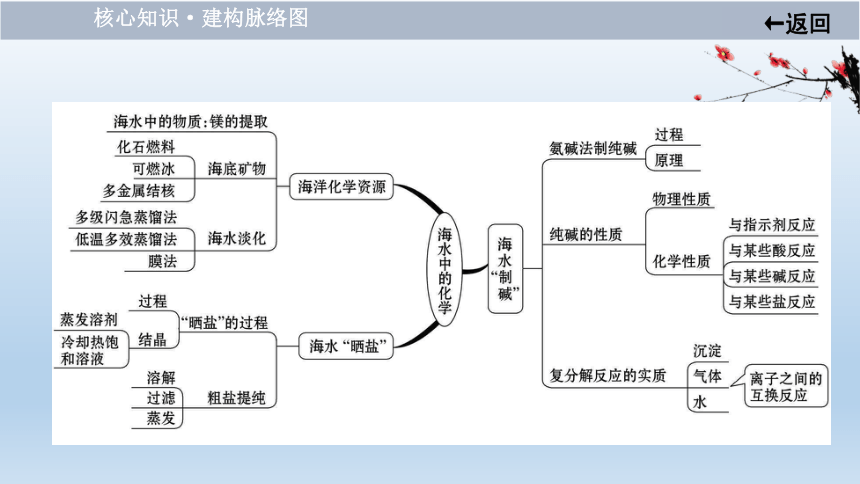
核心知识·建构脉络图
【主干回顾】
一、海洋化学资源
1.海水中最多的物质是 ___ ,最多的盐是 _______ 。?
2.海底矿物
3.海水淡化的方法:蒸馏法、结晶法、 _____ 和热法。热法中较为常用的
有 _______________ 和 _______________ 。
主干回顾·厚积知识力
水
氯化钠
膜法
低温多效蒸馏法
多级闪急蒸馏法
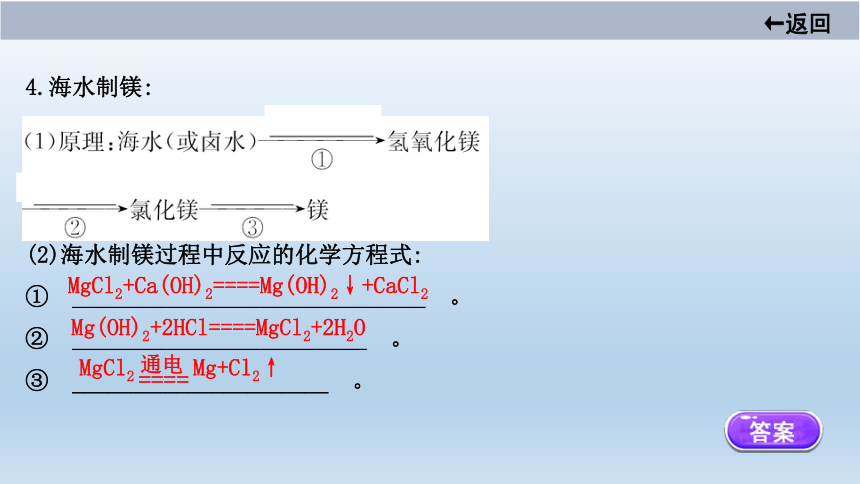
4.海水制镁:
(2)海水制镁过程中反应的化学方程式:
① ______________________________ 。?
② _________________________ 。?
③ ______________________ 。?
MgCl2+Ca(OH)2====Mg(OH)2↓+CaCl2
Mg(OH)2+2HCl====MgCl2+2H2O
MgCl2 Mg+Cl2↑
通电
====
【微思考】 海水中含有MgCl2,为什么还需经过加石灰乳、加盐酸等步骤重新得到MgCl2?
提示:海水中MgCl2的含量很低,经过反应可得到纯度高的MgCl2。 ?
二、海水“晒盐”
1.海水“晒盐”的过程:
海水→蒸发池→结晶池→
2.结晶:
(1)定义:固体物质从它的 _________ 中以 _____ 的形式析出的过程。?
(2)方法:
结晶方法
适用范围
降温结晶
溶解度随温度变化 _______ 的固体物质?
蒸发结晶
溶解度随温度变化 _______ 的固体物质?
饱和溶液
晶体
比较大
比较小
3.粗盐的提纯:
(1)粗盐中难溶性杂质的去除。(详见P86“实验突破 强化探究力”)
(2)除去食盐中可溶性杂质。
①原理:用化学方法除去可溶性杂质。
②方法。
a.流程图
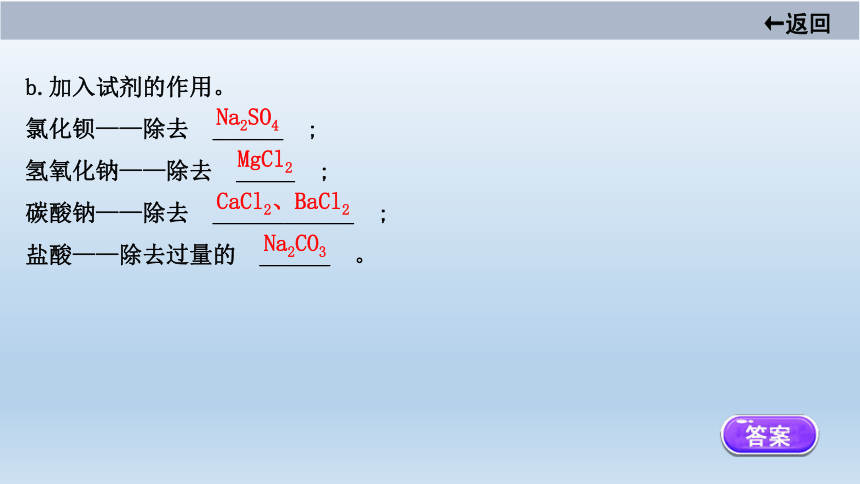
b.加入试剂的作用。
氯化钡——除去 ______ ;?
氢氧化钠——除去 _____ ;?
碳酸钠——除去 ____________ ;?
盐酸——除去过量的 ______ 。?
Na2SO4
MgCl2
CaCl2、BaCl2
Na2CO3
特别提醒除杂的原则
①不增→不能引入新的杂质;
②不减→非杂质的成分不能减少;
③易分→分离简便易行,杂质应转化为气体、沉淀等易分离的物质或水。
【微点拨】 (1)操作中加入过量药品的目的是将杂质除净。
(2)过量的碳酸钠溶液既除去粗盐中的钙离子,也除去过量的钡离子,因此,加入药品时,碳酸钠溶液必须加在氯化钡溶液之后。
(3)过滤操作必须在加入盐酸之前。
(4)加入盐酸的作用是除去食盐溶液中过量的碳酸根离子和氢氧根离子,将溶液的pH调整为7。
三、氨碱法制纯碱
1.工业流程:
_________? _______ 。?
2.化学反应原理(用化学方程式表示):
______________________________ ,?
________________________________。?
碳酸氢钠
纯碱
NaCl+NH3+CO2+H2O=====NaHCO3+NH4Cl
2NaHCO3 Na2CO3+H2O+CO2↑
△
====
【微思考】 氨盐水吸收二氧化碳后生成碳酸氢钠和氯化铵,为什么碳酸氢钠首先结晶析出?
提示:查看溶解度曲线图,可以看出相同条件下,氯化铵比碳酸氢钠更易溶于水,并且在反应NaCl+NH3+CO2+H2O====NaHCO3+NH4Cl中,生成碳酸氢钠和氯化铵的质量比为168∶107,所以碳酸氢钠首先析出。 ?
四、纯碱的化学性质
1.能与指示剂作用:碳酸钠溶液呈 _____ ,能使酚酞试液 _____ ,使紫色
石蕊试液 _____ 。?
2.能与酸反应:如与硫酸反应,化学方程式为
_____________________________ 。?
3.能与某些碱溶液反应:如与氢氧化钙反应,化学方程式为
_____________________________ 。?
4.能与某些盐溶液反应:如与氯化钡溶液反应,化学方程式为
___________________________ 。?
碱性
变红
变蓝
Na2CO3+H2SO4====Na2SO4+H2O+CO2↑
Ca(OH)2+Na2CO3====CaCO3↓+2NaOH
Na2CO3+BaCl2====BaCO3↓+2NaCl
【微点拨】 1.与碱和盐反应时,碱和盐须为可溶的。
2.常见盐的溶解性记忆口诀:
钾钠铵硝皆可溶,盐酸盐中银不溶,硫酸盐中钡不溶,其他碳酸盐都不溶。
五、复分解反应
1.概念:由两种化合物互相 _________ ,生成另外 ___________ 的反
应。?
2.反应表示:AB+CD====CB+AD。
3.实质:酸、碱、盐的离子相互结合,生成 _______ 的碱或盐、不稳定的酸
(分解放出 _____ )或 ___ 。
交换成分
两种化合物
难溶性
气体
水
【微点拨】
(1)复分解反应的特点:双交换、价不变。
(2)两种化合物反应生成另外两种化合物的反应不一定是复分解反应,如碱+
非金属氧化物 盐+水的反应就不属于复分解反应,
如2NaOH+CO2====Na2CO3+H2O。
【核心反应】一、含钠化合物之间的转化
①________________________________________________________________
②________________________________________________________
③ ____________________________
④_____________________________________
Na2CO3+H2SO4====Na2SO4+H2O+CO2↑、Na2CO3 +2HCl====2NaCl +H2O+ CO2↑
HCl+ NaOH====NaCl+ H2O、H2SO4 +2NaOH====Na2SO4 +2H2O ?
2NaOH +CO2====Na2CO3 + H2O ?
Ca(OH)2 +Na2CO3====CaCO3↓ +2NaOH ?
⑤__________________________________________________________________
⑥__________________________________________________________________
⑦___________________________________
⑧_________________________________
⑨____________________________________
Na2CO3+ BaCl2====BaCO3↓+ 2NaCl、Na2CO3+ CaCl2====CaCO3↓+ 2NaCl ?
2NaHCO3 +H2SO4====Na2SO4+2H2O +2CO2↑、NaHCO3 + HCl====NaCl +H2O +CO2↑ ?
2NaHCO3 Na2CO3 +H2O +CO2↑ ?
NaCl +AgNO3====AgCl↓+ NaNO3 ?
Na2SO4 + BaCl2====BaSO4↓+ 2NaCl ?
△
====
二、含钙化合物之间的转化
①______________________
②__________________________
③__________________________________
④____________________________________
⑤____________________________________
⑥_________________________________
CaCO3 CaO+CO2↑ ?
CaO+H2O====Ca(OH)2 ?
Ca(OH)2+2HCl====CaCl2+2H2O ?
CaCO3+2HCl====CaCl2+H2O+CO2↑ ?
CaCl2+Na2CO3====CaCO3↓+2NaCl ?
Ca(OH)2+CO2====CaCO3↓+H2O ?
【自我测评】
1.(2020·泰安泰山区期末)下列关于海洋资源的叙述中,不正确的是 ( )
A.海洋资源包括化学资源、矿产资源、动力资源和生物资源等
B.海底蕴藏着无以计数的能源,所以我们不用担心未来的能源问题
C.在合理开发海洋资源的同时,应重视保护海洋环境
D.从海洋中获得淡水是解决淡水危机的重要途径
B
2.下列方法可用来淡化海水的是 ( )
①蒸馏 ②过滤 ③多级闪急蒸馏法 ④使海水结冰脱盐 ⑤膜法 ⑥加入
明矾
A.①②③④⑤ B.①②③④⑤⑥
C.③④⑤ D.①③④⑤
3.(2020·威海文登区质检)下列不属于氨碱法制纯碱所需的原料是 ( )
A.石灰石 B.氯化钠 C.氢氧化钠 D.水
D
C
4.(2020·重庆中考A卷)某同学将一定量的Na2CO3与Ba(OH)2溶液混合,要想检验
反应后Ba(OH)2是否过量,应选用的试剂是 ( )
A.酚酞 B.CuCl2溶液
C.Na2CO3溶液 D.NaCl溶液
5.下列化学反应属于复分解反应的是 ( )
A.3Fe+2O2 Fe3O4
B.H2CO3===H2O+CO2↑
C.Mg(OH)2+2HNO3====Mg(NO3)2+2H2O
D.2C2H2+5O2 2H2O+4CO2
C
C
6.(2020·淄博质检)有三瓶无标签的无色溶液,只知道它们分别是稀盐酸、
BaCl2溶液和KNO3溶液中的一种。下列四种溶液中,能将三种无色溶液一次鉴别
出来的是 ( )
A.NaCl B.稀硫酸
C.K2CO3溶液 D.AgNO3溶液
C
7.(2020·淄博博山区模拟)氨碱法制纯碱的工业流程如图:
(1)在步骤②中通入氨气的作用是__________________________________________,
由步骤③所得的碳酸氢钠在生产和生活中有许多重要用途,在医疗上,它是治疗
_____过多的药剂之一;?
(2)请写出步骤④中发生反应的化学方程式:
_____________________________。?
氨气极易溶于水,溶液显碱性,更易吸收二氧化碳
胃酸
2NaHCO3 Na2CO3+H2O+CO2↑
△
====
8.如图为“蒸馏法淡化海水”的实验,请回答下列问题:
(1)实验开始应该先 _______________ 。?
(2)向试管中加入5~10 ml海水,塞好塞子加热然后往小试管冷凝的水中加入硝
酸银溶液,观察到的现象为 _______________ 。?
检查装置气密性
无白色沉淀产生
(3)下列哪种方法冷凝效果最好______(填字母序号)。?
A.玻璃管加长
B.在烧杯内加冰块
C.使用冷凝器
(4)实验结束时应该先 _______ (填“撤导管”或“熄灭酒精灯”),这样做
的目的是 ___________ 。?
(5)某同学向海水里加入硝酸银溶液做对比实验,发现有白色沉淀产生,该反应
的化学方程式为 _________________________ 。
撤导管
防止水倒吸
AgNO3+NaCl====AgCl↓+NaNO3
C
9.(2020·淄博质检)如图是海水制镁的流程,请回答下列问题: 世纪金榜导学号
(1)上述一系列转化过程中,属于中和反应的是 _________________________
(用化学方程式表示),①步骤中加入石灰乳的量应 _____ ,要得到氢氧化镁
固体,①步骤中需进行的操作是 _____ 。?
Mg(OH)2+2HCl===MgCl2+2H2O
过量
过滤
(2)海水制镁过程中对于如何富集镁离子,甲、乙、丙三位同学各自提出自己的
设想:
甲:直接往海水中加入石灰乳;
乙:高温加热蒸发海水后,加入石灰乳;
丙:向晒盐后的卤水中,加入石灰乳。
通过分析比较,你认为 ___ 的设想最经济合理(选填“甲”“乙”或“丙”)?
丙
10.(2020·德阳中考)有一包固体粉末可能含有NaOH、NaCl、CuCl2、Mg(OH)2、
CaCO3中的一种或多种,为探究其成分,某同学取样进行了如下图所示实验: 世纪金榜导学号
(1)操作Ⅰ和操作Ⅱ相同,其名称是_____。?
(2)无色气体的化学式为___。?
(3)反应生成白色沉淀Ⅱ的化学方程式为 _________________________ 。?
(4)原固体粉末中不能确定是否含有的物质是 _____________ 。?
过滤
CO2
NaCl+AgNO3====AgCl↓+NaNO3
NaCl、Mg(OH)2
全解全析P238
命题点一 海洋化学资源
【典例1】(2020·岳阳中考)海洋中蕴藏着丰富的化学资源,从海水中提取金属镁的主要步骤如下:
资料:海滩贝壳的主要成分是CaCO3
考点研磨·提升审题力
(1)为节约资源,试剂A常用海滩贝壳为原料制得,则试剂A为 _______ (填化
学式)。?
(2)操作Y的名称为 _____ 。?
(3)在熔融状态下的MgCl2,通电后会生成镁与一种气体单质,该反应的化学方程
式为 ________________ 。?
Ca(OH)2
过滤
MgCl2 Mg+Cl2↑
【题组过关】
1.(2020·眉山中考)海水资源丰富,工业以海水为原料提取镁的过程如下:
回答下列问题:
(1)操作①的名称是 _____ 。?
(2)反应③的化学方程式为 _________________________ 。?
(3)上述反应①②③未涉及的基本反应类型为 _________ 。?
过滤
Mg(OH)2+2HCl====MgCl2+2H2O
置换反应
2.(2020·济南历城区模拟)从海水中可制备纯碱和金属镁,其流程如图所示。
世纪金榜导学号
(1)粗盐提纯时,每步操作都会用到的一种玻璃仪器是 _______ 。(填仪器名
称)?
(2)粗盐水中主要含有CaCl2、MgSO4等可溶性杂质,可加入下列物质:
a.适量的盐酸 b.稍过量的Na2CO3溶液 c.稍过量的Ba(OH)2溶液
利用过滤等操作进行除杂,则加入这三种物质的先后顺序为____。
(填字母序号)?
玻璃棒
cba
(3)向饱和的氯化钠溶液中通入氨气和二氧化碳,经过一系列变化,最终可制得
纯碱。请写出第Ⅲ步反应的化学方程式___________________________________。
(4)第Ⅴ步Mg(OH)2与盐酸的反应 ___ (选填“是”或“不是”)中和反应。?
2NaHCO3 Na2CO3+CO2↑+H2O
是
△
====
命题点二 盐的化学性质
【典例2】(2020·济宁中考)为鉴别氯化钠、氢氧化钠、碳酸钠和硫酸钠四种
物质的溶液,设计如下实验:
下面对试剂①、试剂②和试剂③的选择,合理的是 ( )
A.①酚酞②稀盐酸③氯化钡
B.①酚酞②稀盐酸③稀盐酸
C.①石蕊②氯化钡③稀盐酸
D.①石蕊②氯化钡③碳酸钠
A
【题组过关】
1.(2020·临沂中考)将下列各组物质放入足量的水中,充分搅拌后,得到无色溶
液的是 ( )
A.硝酸钾和氯化铁 B.氢氧化钾和盐酸
C.硫酸铜和氢氧化钠 D.硫酸钠和氯化钡
B
2.(2020·烟台龙口模拟)向K2CO3溶液中滴入Ba(OH)2溶液至恰好完全反应。
(1)可以观察到的实验现象是 _______________ 。?
(2)如图表示该反应前后溶液中存在的主要离子,写出每种图形代表的离子。
(填离子符号)
(3)下列物质能与K2CO3溶液反应产生类似上述实验现象的是_________。(双项
选择)?
A.Ca(OH)2 B.HCl C.BaCl2 D.(NH4)2SO4
有白色沉淀生成
A、C
命题三复分解反应及其应用
【典例3】(2020·苏州中考)下列各组离子在溶液中能大量共存的是( )
A. 、 、 B.H+、Ba2+、OH-
C.Fe2+、Na+、OH- D. Ca2+、Cl-、
A
【方法点拨】不能共存的离子对
(1)强酸性溶液(H+)中不能大量存在OH-、 、 等。
(2)强碱性溶液(OH-)不能和 、Mg2+、Al3+、Fe3+、Cu2+等大量共存。
(3)能相互结合生成难溶性物质的离子不能大量共存:Ba2+与 、Ag+与Cl-、
Ca2+与 、Ba2+与 等。
【题组过关】 1.(2020·龙东中考)下列各物质在同一溶液中可以大量共存的
是 ( )
A.NaOH、FeCl3、K2SO4
B.NaCl、HNO3、AgNO3
C.NaCl、K2CO3、Ca(OH)2
D.KNO3、NaCl、Ba(OH)2
2.(2020·淄博张店质检)下列各组离子在水中一定能大量共存,并形成无色溶
液的是 ( )
A.Cu2+、H+、 、Cl- B.Ba2+、Na+、Cl-、
C.K+、Ca2+、OH-、 D.Na+、H+、 、
D
B
实验突破·强化探究力
实验 粗盐中难溶性杂质的去除
1.实验原理
依据物质的溶解性不同,利用 _____ 的方法除去食盐中的泥沙等不溶性杂
质,然后 _____ 水得到较纯的精盐。?
2.实验装置
过滤
蒸发
3.实验步骤
实验
步骤
操作方法
玻璃棒的作用
溶解
①称量粗盐;
②加水溶解并用 _______ 搅拌,直到粗盐不再溶解为止?
搅拌、加速溶解
过滤
①做好过滤器,装配好仪器;②将粗盐水用 _______ 引流到过滤器;?
③若滤液浑浊应再过滤
引流
玻璃棒
玻璃棒
3.实验步骤
实验
步骤
操作方法
玻璃棒的作用
蒸发
①装配好仪器;②将过滤后的澄清液倒入蒸发皿中,边加热边用玻璃棒搅拌,当 _______________ 时停止加热,利用余热使滤液蒸干?
均匀受热、防止液滴飞溅
计算
产率
①用 _______ 将固体转移到纸上,称量后回收到指定容器中;②将提纯后的精盐与溶解的粗盐作比较?
转移固体
出现较多量固体
玻璃棒
4.误差分析
(1)造成产率偏低的原因可能有
①溶解过程中食盐未完全溶解;
②过滤时液体溅出或倾倒不彻底或过滤不彻底;
③蒸发时造成液体或固体飞溅;
④器皿上沾有的精盐没全部转移到称量纸上。
(2)造成产率偏高的原因可能有
①称量时多称了;
②蒸发时未充分蒸干。
【典例1】(2020·自贡中考)“粗盐中难溶性杂质的去除”实验操作的主要步
骤如图。
(1)操作A的名称为 _____ 。?
(2)操作C中玻璃棒的作用是 ___________________________________ 。?
(3)正确的操作顺序为 ____ (填字母)。?
过滤
搅拌,防止局部温度过高,造成液体飞溅
BAC
【拓展延伸】除去粗盐中可溶性杂质的方法
(1)操作中加入过量药品的目的是将杂质除净。
(2)过量的碳酸钠溶液既除去粗盐中的钙离子,也除去过量的钡离子,因此,加入药品时,碳酸钠溶液必须加在氯化钡溶液之后。
(3)过滤操作必须在加入盐酸之前。
(4)加入盐酸的作用是除去食盐溶液中过量的碳酸根离子和氢氧根离子,将溶液的pH调为7。
【典例2】( 2019·河南中考)为除去氯化钠中的泥沙和CaCl2、MgCl2、Na2SO4
杂质,某化学兴趣小组的同学先将粗盐样品溶解、过滤,除去泥沙后,取粗盐水
按以下流程进行实验探究。 世纪金榜导学号
(1)溶解、过滤、蒸发操作中都要用到的一种玻璃仪器是___________。?
(2)写出一个加入Na2CO3溶液时所发生反应的化学方程式____________________________________________________________ 。?
(3)上述流程中,若将过滤和加盐酸的操作顺序颠倒,所得精盐产品中含哪些杂
质?(BaSO4不溶于水,也不溶于酸) _______________________ ?
玻璃棒
Na2CO3+CaCl2====CaCO3↓+2NaCl(或BaCl2+Na2CO3====BaCO3↓+2NaCl)
氯化钙、氯化镁、氯化钡
本课结束
第一节 海水中的化学
核心知识·建构脉络图
【主干回顾】
一、海洋化学资源
1.海水中最多的物质是 ___ ,最多的盐是 _______ 。?
2.海底矿物
3.海水淡化的方法:蒸馏法、结晶法、 _____ 和热法。热法中较为常用的
有 _______________ 和 _______________ 。
主干回顾·厚积知识力
水
氯化钠
膜法
低温多效蒸馏法
多级闪急蒸馏法
4.海水制镁:
(2)海水制镁过程中反应的化学方程式:
① ______________________________ 。?
② _________________________ 。?
③ ______________________ 。?
MgCl2+Ca(OH)2====Mg(OH)2↓+CaCl2
Mg(OH)2+2HCl====MgCl2+2H2O
MgCl2 Mg+Cl2↑
通电
====
【微思考】 海水中含有MgCl2,为什么还需经过加石灰乳、加盐酸等步骤重新得到MgCl2?
提示:海水中MgCl2的含量很低,经过反应可得到纯度高的MgCl2。 ?
二、海水“晒盐”
1.海水“晒盐”的过程:
海水→蒸发池→结晶池→
2.结晶:
(1)定义:固体物质从它的 _________ 中以 _____ 的形式析出的过程。?
(2)方法:
结晶方法
适用范围
降温结晶
溶解度随温度变化 _______ 的固体物质?
蒸发结晶
溶解度随温度变化 _______ 的固体物质?
饱和溶液
晶体
比较大
比较小
3.粗盐的提纯:
(1)粗盐中难溶性杂质的去除。(详见P86“实验突破 强化探究力”)
(2)除去食盐中可溶性杂质。
①原理:用化学方法除去可溶性杂质。
②方法。
a.流程图
b.加入试剂的作用。
氯化钡——除去 ______ ;?
氢氧化钠——除去 _____ ;?
碳酸钠——除去 ____________ ;?
盐酸——除去过量的 ______ 。?
Na2SO4
MgCl2
CaCl2、BaCl2
Na2CO3
特别提醒除杂的原则
①不增→不能引入新的杂质;
②不减→非杂质的成分不能减少;
③易分→分离简便易行,杂质应转化为气体、沉淀等易分离的物质或水。
【微点拨】 (1)操作中加入过量药品的目的是将杂质除净。
(2)过量的碳酸钠溶液既除去粗盐中的钙离子,也除去过量的钡离子,因此,加入药品时,碳酸钠溶液必须加在氯化钡溶液之后。
(3)过滤操作必须在加入盐酸之前。
(4)加入盐酸的作用是除去食盐溶液中过量的碳酸根离子和氢氧根离子,将溶液的pH调整为7。
三、氨碱法制纯碱
1.工业流程:
_________? _______ 。?
2.化学反应原理(用化学方程式表示):
______________________________ ,?
________________________________。?
碳酸氢钠
纯碱
NaCl+NH3+CO2+H2O=====NaHCO3+NH4Cl
2NaHCO3 Na2CO3+H2O+CO2↑
△
====
【微思考】 氨盐水吸收二氧化碳后生成碳酸氢钠和氯化铵,为什么碳酸氢钠首先结晶析出?
提示:查看溶解度曲线图,可以看出相同条件下,氯化铵比碳酸氢钠更易溶于水,并且在反应NaCl+NH3+CO2+H2O====NaHCO3+NH4Cl中,生成碳酸氢钠和氯化铵的质量比为168∶107,所以碳酸氢钠首先析出。 ?
四、纯碱的化学性质
1.能与指示剂作用:碳酸钠溶液呈 _____ ,能使酚酞试液 _____ ,使紫色
石蕊试液 _____ 。?
2.能与酸反应:如与硫酸反应,化学方程式为
_____________________________ 。?
3.能与某些碱溶液反应:如与氢氧化钙反应,化学方程式为
_____________________________ 。?
4.能与某些盐溶液反应:如与氯化钡溶液反应,化学方程式为
___________________________ 。?
碱性
变红
变蓝
Na2CO3+H2SO4====Na2SO4+H2O+CO2↑
Ca(OH)2+Na2CO3====CaCO3↓+2NaOH
Na2CO3+BaCl2====BaCO3↓+2NaCl
【微点拨】 1.与碱和盐反应时,碱和盐须为可溶的。
2.常见盐的溶解性记忆口诀:
钾钠铵硝皆可溶,盐酸盐中银不溶,硫酸盐中钡不溶,其他碳酸盐都不溶。
五、复分解反应
1.概念:由两种化合物互相 _________ ,生成另外 ___________ 的反
应。?
2.反应表示:AB+CD====CB+AD。
3.实质:酸、碱、盐的离子相互结合,生成 _______ 的碱或盐、不稳定的酸
(分解放出 _____ )或 ___ 。
交换成分
两种化合物
难溶性
气体
水
【微点拨】
(1)复分解反应的特点:双交换、价不变。
(2)两种化合物反应生成另外两种化合物的反应不一定是复分解反应,如碱+
非金属氧化物 盐+水的反应就不属于复分解反应,
如2NaOH+CO2====Na2CO3+H2O。
【核心反应】一、含钠化合物之间的转化
①________________________________________________________________
②________________________________________________________
③ ____________________________
④_____________________________________
Na2CO3+H2SO4====Na2SO4+H2O+CO2↑、Na2CO3 +2HCl====2NaCl +H2O+ CO2↑
HCl+ NaOH====NaCl+ H2O、H2SO4 +2NaOH====Na2SO4 +2H2O ?
2NaOH +CO2====Na2CO3 + H2O ?
Ca(OH)2 +Na2CO3====CaCO3↓ +2NaOH ?
⑤__________________________________________________________________
⑥__________________________________________________________________
⑦___________________________________
⑧_________________________________
⑨____________________________________
Na2CO3+ BaCl2====BaCO3↓+ 2NaCl、Na2CO3+ CaCl2====CaCO3↓+ 2NaCl ?
2NaHCO3 +H2SO4====Na2SO4+2H2O +2CO2↑、NaHCO3 + HCl====NaCl +H2O +CO2↑ ?
2NaHCO3 Na2CO3 +H2O +CO2↑ ?
NaCl +AgNO3====AgCl↓+ NaNO3 ?
Na2SO4 + BaCl2====BaSO4↓+ 2NaCl ?
△
====
二、含钙化合物之间的转化
①______________________
②__________________________
③__________________________________
④____________________________________
⑤____________________________________
⑥_________________________________
CaCO3 CaO+CO2↑ ?
CaO+H2O====Ca(OH)2 ?
Ca(OH)2+2HCl====CaCl2+2H2O ?
CaCO3+2HCl====CaCl2+H2O+CO2↑ ?
CaCl2+Na2CO3====CaCO3↓+2NaCl ?
Ca(OH)2+CO2====CaCO3↓+H2O ?
【自我测评】
1.(2020·泰安泰山区期末)下列关于海洋资源的叙述中,不正确的是 ( )
A.海洋资源包括化学资源、矿产资源、动力资源和生物资源等
B.海底蕴藏着无以计数的能源,所以我们不用担心未来的能源问题
C.在合理开发海洋资源的同时,应重视保护海洋环境
D.从海洋中获得淡水是解决淡水危机的重要途径
B
2.下列方法可用来淡化海水的是 ( )
①蒸馏 ②过滤 ③多级闪急蒸馏法 ④使海水结冰脱盐 ⑤膜法 ⑥加入
明矾
A.①②③④⑤ B.①②③④⑤⑥
C.③④⑤ D.①③④⑤
3.(2020·威海文登区质检)下列不属于氨碱法制纯碱所需的原料是 ( )
A.石灰石 B.氯化钠 C.氢氧化钠 D.水
D
C
4.(2020·重庆中考A卷)某同学将一定量的Na2CO3与Ba(OH)2溶液混合,要想检验
反应后Ba(OH)2是否过量,应选用的试剂是 ( )
A.酚酞 B.CuCl2溶液
C.Na2CO3溶液 D.NaCl溶液
5.下列化学反应属于复分解反应的是 ( )
A.3Fe+2O2 Fe3O4
B.H2CO3===H2O+CO2↑
C.Mg(OH)2+2HNO3====Mg(NO3)2+2H2O
D.2C2H2+5O2 2H2O+4CO2
C
C
6.(2020·淄博质检)有三瓶无标签的无色溶液,只知道它们分别是稀盐酸、
BaCl2溶液和KNO3溶液中的一种。下列四种溶液中,能将三种无色溶液一次鉴别
出来的是 ( )
A.NaCl B.稀硫酸
C.K2CO3溶液 D.AgNO3溶液
C
7.(2020·淄博博山区模拟)氨碱法制纯碱的工业流程如图:
(1)在步骤②中通入氨气的作用是__________________________________________,
由步骤③所得的碳酸氢钠在生产和生活中有许多重要用途,在医疗上,它是治疗
_____过多的药剂之一;?
(2)请写出步骤④中发生反应的化学方程式:
_____________________________。?
氨气极易溶于水,溶液显碱性,更易吸收二氧化碳
胃酸
2NaHCO3 Na2CO3+H2O+CO2↑
△
====
8.如图为“蒸馏法淡化海水”的实验,请回答下列问题:
(1)实验开始应该先 _______________ 。?
(2)向试管中加入5~10 ml海水,塞好塞子加热然后往小试管冷凝的水中加入硝
酸银溶液,观察到的现象为 _______________ 。?
检查装置气密性
无白色沉淀产生
(3)下列哪种方法冷凝效果最好______(填字母序号)。?
A.玻璃管加长
B.在烧杯内加冰块
C.使用冷凝器
(4)实验结束时应该先 _______ (填“撤导管”或“熄灭酒精灯”),这样做
的目的是 ___________ 。?
(5)某同学向海水里加入硝酸银溶液做对比实验,发现有白色沉淀产生,该反应
的化学方程式为 _________________________ 。
撤导管
防止水倒吸
AgNO3+NaCl====AgCl↓+NaNO3
C
9.(2020·淄博质检)如图是海水制镁的流程,请回答下列问题: 世纪金榜导学号
(1)上述一系列转化过程中,属于中和反应的是 _________________________
(用化学方程式表示),①步骤中加入石灰乳的量应 _____ ,要得到氢氧化镁
固体,①步骤中需进行的操作是 _____ 。?
Mg(OH)2+2HCl===MgCl2+2H2O
过量
过滤
(2)海水制镁过程中对于如何富集镁离子,甲、乙、丙三位同学各自提出自己的
设想:
甲:直接往海水中加入石灰乳;
乙:高温加热蒸发海水后,加入石灰乳;
丙:向晒盐后的卤水中,加入石灰乳。
通过分析比较,你认为 ___ 的设想最经济合理(选填“甲”“乙”或“丙”)?
丙
10.(2020·德阳中考)有一包固体粉末可能含有NaOH、NaCl、CuCl2、Mg(OH)2、
CaCO3中的一种或多种,为探究其成分,某同学取样进行了如下图所示实验: 世纪金榜导学号
(1)操作Ⅰ和操作Ⅱ相同,其名称是_____。?
(2)无色气体的化学式为___。?
(3)反应生成白色沉淀Ⅱ的化学方程式为 _________________________ 。?
(4)原固体粉末中不能确定是否含有的物质是 _____________ 。?
过滤
CO2
NaCl+AgNO3====AgCl↓+NaNO3
NaCl、Mg(OH)2
全解全析P238
命题点一 海洋化学资源
【典例1】(2020·岳阳中考)海洋中蕴藏着丰富的化学资源,从海水中提取金属镁的主要步骤如下:
资料:海滩贝壳的主要成分是CaCO3
考点研磨·提升审题力
(1)为节约资源,试剂A常用海滩贝壳为原料制得,则试剂A为 _______ (填化
学式)。?
(2)操作Y的名称为 _____ 。?
(3)在熔融状态下的MgCl2,通电后会生成镁与一种气体单质,该反应的化学方程
式为 ________________ 。?
Ca(OH)2
过滤
MgCl2 Mg+Cl2↑
【题组过关】
1.(2020·眉山中考)海水资源丰富,工业以海水为原料提取镁的过程如下:
回答下列问题:
(1)操作①的名称是 _____ 。?
(2)反应③的化学方程式为 _________________________ 。?
(3)上述反应①②③未涉及的基本反应类型为 _________ 。?
过滤
Mg(OH)2+2HCl====MgCl2+2H2O
置换反应
2.(2020·济南历城区模拟)从海水中可制备纯碱和金属镁,其流程如图所示。
世纪金榜导学号
(1)粗盐提纯时,每步操作都会用到的一种玻璃仪器是 _______ 。(填仪器名
称)?
(2)粗盐水中主要含有CaCl2、MgSO4等可溶性杂质,可加入下列物质:
a.适量的盐酸 b.稍过量的Na2CO3溶液 c.稍过量的Ba(OH)2溶液
利用过滤等操作进行除杂,则加入这三种物质的先后顺序为____。
(填字母序号)?
玻璃棒
cba
(3)向饱和的氯化钠溶液中通入氨气和二氧化碳,经过一系列变化,最终可制得
纯碱。请写出第Ⅲ步反应的化学方程式___________________________________。
(4)第Ⅴ步Mg(OH)2与盐酸的反应 ___ (选填“是”或“不是”)中和反应。?
2NaHCO3 Na2CO3+CO2↑+H2O
是
△
====
命题点二 盐的化学性质
【典例2】(2020·济宁中考)为鉴别氯化钠、氢氧化钠、碳酸钠和硫酸钠四种
物质的溶液,设计如下实验:
下面对试剂①、试剂②和试剂③的选择,合理的是 ( )
A.①酚酞②稀盐酸③氯化钡
B.①酚酞②稀盐酸③稀盐酸
C.①石蕊②氯化钡③稀盐酸
D.①石蕊②氯化钡③碳酸钠
A
【题组过关】
1.(2020·临沂中考)将下列各组物质放入足量的水中,充分搅拌后,得到无色溶
液的是 ( )
A.硝酸钾和氯化铁 B.氢氧化钾和盐酸
C.硫酸铜和氢氧化钠 D.硫酸钠和氯化钡
B
2.(2020·烟台龙口模拟)向K2CO3溶液中滴入Ba(OH)2溶液至恰好完全反应。
(1)可以观察到的实验现象是 _______________ 。?
(2)如图表示该反应前后溶液中存在的主要离子,写出每种图形代表的离子。
(填离子符号)
(3)下列物质能与K2CO3溶液反应产生类似上述实验现象的是_________。(双项
选择)?
A.Ca(OH)2 B.HCl C.BaCl2 D.(NH4)2SO4
有白色沉淀生成
A、C
命题三复分解反应及其应用
【典例3】(2020·苏州中考)下列各组离子在溶液中能大量共存的是( )
A. 、 、 B.H+、Ba2+、OH-
C.Fe2+、Na+、OH- D. Ca2+、Cl-、
A
【方法点拨】不能共存的离子对
(1)强酸性溶液(H+)中不能大量存在OH-、 、 等。
(2)强碱性溶液(OH-)不能和 、Mg2+、Al3+、Fe3+、Cu2+等大量共存。
(3)能相互结合生成难溶性物质的离子不能大量共存:Ba2+与 、Ag+与Cl-、
Ca2+与 、Ba2+与 等。
【题组过关】 1.(2020·龙东中考)下列各物质在同一溶液中可以大量共存的
是 ( )
A.NaOH、FeCl3、K2SO4
B.NaCl、HNO3、AgNO3
C.NaCl、K2CO3、Ca(OH)2
D.KNO3、NaCl、Ba(OH)2
2.(2020·淄博张店质检)下列各组离子在水中一定能大量共存,并形成无色溶
液的是 ( )
A.Cu2+、H+、 、Cl- B.Ba2+、Na+、Cl-、
C.K+、Ca2+、OH-、 D.Na+、H+、 、
D
B
实验突破·强化探究力
实验 粗盐中难溶性杂质的去除
1.实验原理
依据物质的溶解性不同,利用 _____ 的方法除去食盐中的泥沙等不溶性杂
质,然后 _____ 水得到较纯的精盐。?
2.实验装置
过滤
蒸发
3.实验步骤
实验
步骤
操作方法
玻璃棒的作用
溶解
①称量粗盐;
②加水溶解并用 _______ 搅拌,直到粗盐不再溶解为止?
搅拌、加速溶解
过滤
①做好过滤器,装配好仪器;②将粗盐水用 _______ 引流到过滤器;?
③若滤液浑浊应再过滤
引流
玻璃棒
玻璃棒
3.实验步骤
实验
步骤
操作方法
玻璃棒的作用
蒸发
①装配好仪器;②将过滤后的澄清液倒入蒸发皿中,边加热边用玻璃棒搅拌,当 _______________ 时停止加热,利用余热使滤液蒸干?
均匀受热、防止液滴飞溅
计算
产率
①用 _______ 将固体转移到纸上,称量后回收到指定容器中;②将提纯后的精盐与溶解的粗盐作比较?
转移固体
出现较多量固体
玻璃棒
4.误差分析
(1)造成产率偏低的原因可能有
①溶解过程中食盐未完全溶解;
②过滤时液体溅出或倾倒不彻底或过滤不彻底;
③蒸发时造成液体或固体飞溅;
④器皿上沾有的精盐没全部转移到称量纸上。
(2)造成产率偏高的原因可能有
①称量时多称了;
②蒸发时未充分蒸干。
【典例1】(2020·自贡中考)“粗盐中难溶性杂质的去除”实验操作的主要步
骤如图。
(1)操作A的名称为 _____ 。?
(2)操作C中玻璃棒的作用是 ___________________________________ 。?
(3)正确的操作顺序为 ____ (填字母)。?
过滤
搅拌,防止局部温度过高,造成液体飞溅
BAC
【拓展延伸】除去粗盐中可溶性杂质的方法
(1)操作中加入过量药品的目的是将杂质除净。
(2)过量的碳酸钠溶液既除去粗盐中的钙离子,也除去过量的钡离子,因此,加入药品时,碳酸钠溶液必须加在氯化钡溶液之后。
(3)过滤操作必须在加入盐酸之前。
(4)加入盐酸的作用是除去食盐溶液中过量的碳酸根离子和氢氧根离子,将溶液的pH调为7。
【典例2】( 2019·河南中考)为除去氯化钠中的泥沙和CaCl2、MgCl2、Na2SO4
杂质,某化学兴趣小组的同学先将粗盐样品溶解、过滤,除去泥沙后,取粗盐水
按以下流程进行实验探究。 世纪金榜导学号
(1)溶解、过滤、蒸发操作中都要用到的一种玻璃仪器是___________。?
(2)写出一个加入Na2CO3溶液时所发生反应的化学方程式____________________________________________________________ 。?
(3)上述流程中,若将过滤和加盐酸的操作顺序颠倒,所得精盐产品中含哪些杂
质?(BaSO4不溶于水,也不溶于酸) _______________________ ?
玻璃棒
Na2CO3+CaCl2====CaCO3↓+2NaCl(或BaCl2+Na2CO3====BaCO3↓+2NaCl)
氯化钙、氯化镁、氯化钡
本课结束
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
