1.6 常见的盐 同步练习(含答案)
图片预览




文档简介
1.6常见的盐
一.选择题
1.Na2CO3的水溶液呈碱性,下列说法错误的是( )
A.碳酸钠在水中会电离出OH﹣ B.往碳酸钠溶液中加稀硫酸后溶液的pH降低
C.碳酸钠溶液中存在OH﹣ D.往碳酸钠溶液中滴加紫色石蕊试液后溶液显蓝色
2.张大伯为了庄稼生长茂盛,茎杆粗壮,增强抗病虫害能力,需要施肥,下列物质属于钾肥的是( )
A.NH4HCO3 B.Ca(H2PO4)2 C.K2CO3 D.CO(NH2)2
3.有关物质用途正确的是( )
A.氢氧化钠改良酸性土壤 B.用BaCl2处理大量泄漏的浓硫酸
C.氢氧化铜治疗胃酸过多 D.熟石灰配制农药波尔多液
4.下列各组物质不能发生化学反应的是( )
A.NaOH溶液和稀HNO3 B.AgCl和KNO3
C.CaCO3和稀HCl D.BaCl2溶液和稀H2SO4
5.某一无色溶液具有下列性质:①使无色酚酞试液变红;②与CuSO4溶液反应可产生蓝色沉淀;③与纯碱溶液反应产生白色沉淀。此溶液是( )
A.氢氧化钠溶液 B.澄清石灰水
C.氯化钙溶液 D.盐酸
6.下列两种物质的溶液混合后,能发生反应,且溶液的总质量不会发生改变的是( )
A.氢氧化钠溶液和稀盐酸 B.碳酸钠溶液和稀盐酸
C.氯化钠溶液和稀硫酸 D.碳酸钠溶液和氯化钙溶液
7.下列各组物质的溶液,不能发生复分解反应的是( )
A.HCl和Ca(OH)2 B.H2SO4和Na2CO3
C.AgNO3 和 BaCl2 D.KCl和CuSO4
8.向含有稀盐酸和氯化铜的混合溶液中滴加NaOH溶液,如图曲线中描述正确的是( )
A.B.
C.D.
9.现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量的某物质X,溶液的pH随滴入X的量的变化关系如图所示,则X可能是( )
A.水 B.纯碱溶液 C.澄清石灰水 D.稀盐酸
10.某粗盐固体样品中含有少量CaCl2、MgCl2、Na2SO4、MgSO4和泥沙,进行以下操作可得到纯净的NaCl晶体:①加过量的NaOH溶液;②加H2O溶解;③加过量的BaCl2溶液;④过滤;⑤蒸发;⑥加过量的Na2CO3溶液;⑦加适量的稀盐酸,则正确的操作顺序是( )
A.②①⑥③④⑦⑤B.②①③⑥⑦④⑤
C.⑥②①③④⑤⑦ D.②③①⑥④⑦⑤
11.甲、乙两化工分布在某排污渠两岸(如图所示),箭头代表水流方向.若甲厂附近a处水样经检测含有的阴离子是OH﹣、SO42﹣,c处水样经检测pH=7且只含有少量的NaCl.则乙厂排放到b处水中的物质可能是( )
A.BaCl2、HCl B.H2SO4、Ba(NO3)2
C.MgSO4、NaCl D.H2SO4、MgCl2
12.从HCl、CuSO4、NaOH、Na2CO3、Na2SO4、Ca(NO3)2六种溶液中,任意取出两种溶液(分别编号为a和b)混合,得到无色澄清溶液,无其他明显现象,测得混合后溶液pH=1.仅根据上述实验现象和数据,对a、b作出的推断中,不正确的是( )
A.肯定有一种是HCl,另一种可能是NaOH溶液
B.符合上述实验现象的a、b组合可能不止一种
C.b都不可能是CuSO4溶液、Na2CO3溶液
D.b都不可能是CuSO4溶液、Na2CO3溶液、NaOH溶液
13.下列各组物质加入水中充分搅拌后,同组反应物恰好完全反应,过滤后,在滤纸上留下两种不溶物质的是( )
A.Ca(NO3)2、BaCl2、AgNO3
B.MgCl2、KOH、NaCl
C.CuSO4、Ba(OH)2、Cu(NO3)2
D.K2CO3、CuSO4、KCl
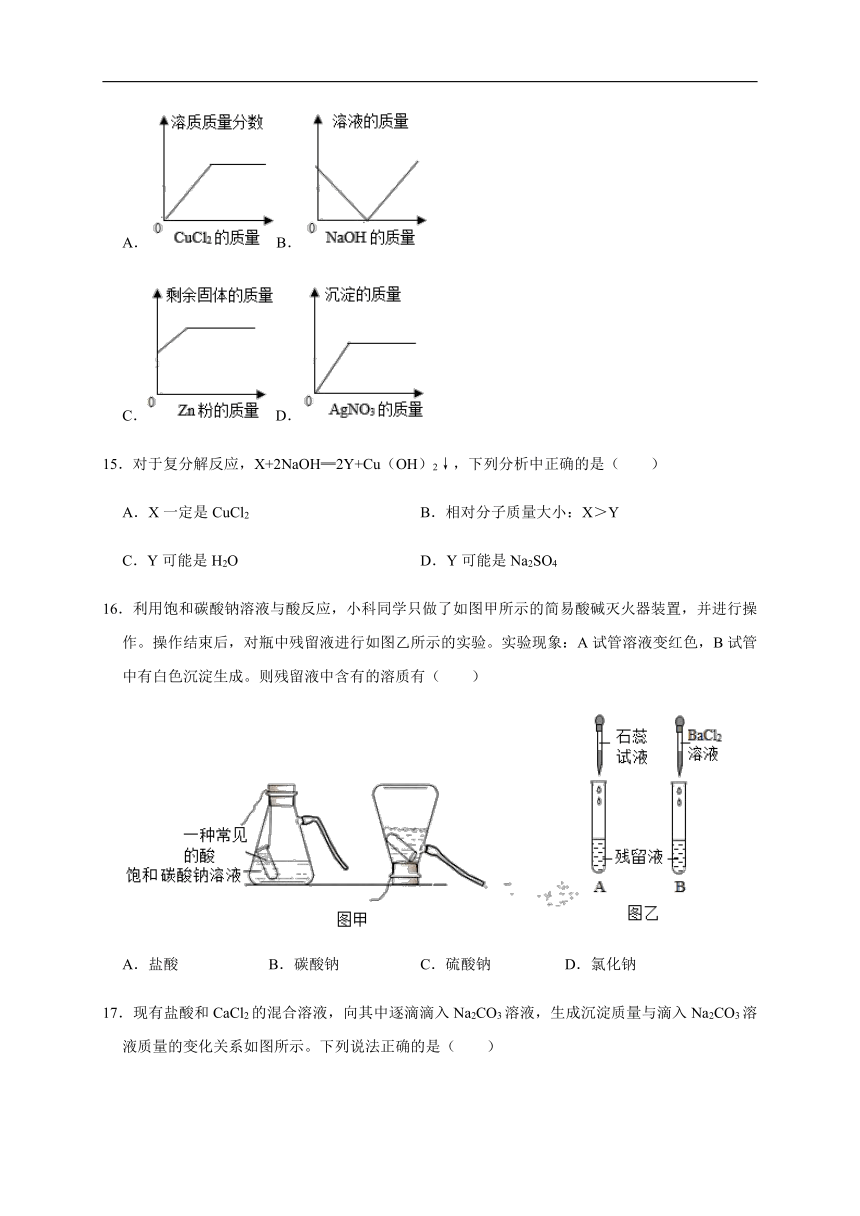
14.一定温度下,向不饱和的氯化铜溶液中加入足量的下列固体,其对应关系正确的是( )
A.B.
C.D.
15.对于复分解反应,X+2NaOH═2Y+Cu(OH)2↓,下列分析中正确的是( )
A.X一定是CuCl2 B.相对分子质量大小:X>Y
C.Y可能是H2O D.Y可能是Na2SO4
16.利用饱和碳酸钠溶液与酸反应,小科同学只做了如图甲所示的简易酸碱灭火器装置,并进行操作。操作结束后,对瓶中残留液进行如图乙所示的实验。实验现象:A试管溶液变红色,B试管中有白色沉淀生成。则残留液中含有的溶质有( )
A.盐酸 B.碳酸钠 C.硫酸钠 D.氯化钠
17.现有盐酸和CaCl2的混合溶液,向其中逐滴滴入Na2CO3溶液,生成沉淀质量与滴入Na2CO3溶液质量的变化关系如图所示。下列说法正确的是( )
A.滴加碳酸钠溶液质量为0~a g时,溶液中有三种离子
B.滴加碳酸钠溶液质量至b g时,溶液中含两种溶质
C.滴加碳酸钠溶液质量至a g时,溶液中溶质质量比原混合溶液中溶质质量小
D.滴加碳酸钠溶液质量为a~c g时,溶液呈酸性
18.小乐完成了图示甲、乙实验后,依次将反应后的溶液缓慢倒入同一洁净的废液缸中,观察到废液缸中先有气泡产生,然后又出现白色沉淀,则下列说法中,正确的是( )
A.甲实验结束后,试管中的废液含稀盐酸和CaCl2
B.乙实验结束后,试管中的废液只含NaCl溶质
C.最终,废液缸中一定含NaCl、CaCl2两种溶质
D.最终,废液缸中一定含NaCl、Na2CO3两种溶质
19.推理是化学学习中常见的思维方法,下列推理正确的是( )
A.碱性溶液能使酚酞试液变红,滴入酚酞试液后变红的溶液一定呈碱性
B.Na2CO3溶液能够使酚酞变红,所以它属于碱
C.酸能使石蕊试液变红,CO2也能使紫色的石蕊试液变红,所以CO2是酸
D.酸和碳酸盐反应产生气体,所以与酸反应能产生气体的物质里一定含有碳酸根离子
20.按如图所示装置进行实验(图中铁架台等仪器均已略去)。先在试管Ⅱ中加入试剂乙,然后在试管Ⅰ中加入试剂甲,立即塞紧橡皮塞,一段时间后,观察到试管Ⅱ中有白色沉淀生成。符合以上实验现象的一组试剂是( )
A.甲:Na2CO3、稀HCl乙:NaOH
B.甲:Zn、稀H2SO4乙:Ba(NO3)2溶液
C.甲:MgO、稀盐酸乙:AgNO3
D.甲:CuO、稀H2SO4乙:BaCl2溶液
二.填空题
21.盐中含有金属离子(或NH4+)和酸根离子,组成相似的盐具有一些相似的化学性质。
(1)硫酸铜、硝酸铜两种物质的溶液均显 色,因为它们都具有相同的阳离子;向这两种物质的溶液中分别加入NaOH溶液,有相同的实验现象发生,写出其中一个反应的化学方程式 。
(2)向硫酸铜、硝酸铜两种物质的溶液中分别加入BaCl2溶液,能发生反应的物质是 (填化学式),另外一种物质不反应。
(3)向硫酸铜溶液中,加入某纯净物的溶液,能同时将铜离子和硫酸根离子转变成沉淀,该纯净物的化学式为 。
22.酸、碱、盐的在日常生活、生产中用途广泛,请回答以下问题.
(1)碳酸钠可用于洗涤剂是因为它的水溶液呈 性(填“酸、碱、中”).碳酸钾的水溶液中能导电的粒子符号是 ;
(2)氢氧化钠是一种常见的碱,根据题意写出下列反应的化学方程式:
①用氢氧化钠溶液吸收二氧化碳气体 ;
②除去氯化钠中的氯化镁杂质 ;
在与二氧化碳反应中,下列物质代替氢氧化钠溶液也能出现同样现象的试剂是 (填编号).
A、KOH B、Ca(OH)2 C、Ba(OH)2 D、Cu(OH)2
(3)硫酸的下列用途中,不能用盐酸代替硫酸的是 (填编号)
①制氢气 ②金属除锈 ③制化肥硫酸铵.
23. 如图,几种物质是常见的盐,请回答下列问题。
(1)在碳酸钠溶液中滴入氯化钙溶液,现象是 。
(2)碳酸钙、碳酸钠均能与稀盐酸反应生成CO2,是因为碳酸钙、碳酸钠中均含有 (写离子符号)。
(3)硫酸铜溶液与氢氧化钠溶液能发生反应,该反应的化学方程式为 ;硫酸铜溶液与氯化钠溶液不能反应,其理由是 。
24.判断下列物质组合能发生复分解反应的有 (填序号)
①K2CO3+CaCl2②H2SO4+KCl ③CuO+HCl ④Fe+CuSO4⑤CO2+NaOH
⑥K2SO4+BaCl2⑦Mg(OH)2+CuSO4⑧BaCO3+NaOH.
三.实验探究题
25.实验室现有一瓶含少量水的碳酸氢铵样品,为测定其中碳酸氢铵的质量分数,某化学兴趣小组利用如图所示装置进行实验(该装置气密性良好,装置B、C中所装药品均足量,碱石灰是氧化钙和氢氧化钠的混合物)。已知:碳酸氢铵受热易分解,反应的化学方程式为:NH4HCO3NH3↑+H2O↑+CO2↑,NH3能被酸溶液吸收
部分实验步骤如下
Ⅰ.打开弹簧夹,通入一段时间的氮气;
Ⅱ.关闭弹簧夹,给碳酸氢铵样品加热
Ⅲ.当样品反应完全,…,再停止加热,直到玻璃管冷却;
N.实验完毕,测得装置B、C中药品的质量分别增加了m1、m2
请回答下列问题:
(1)NH4HCO3属于 (选填“氮肥”“磷肥”“钾肥”或“复合肥”),装置B中盛放的液体是
。
(2)装置C中发生反应的化学方程式为 。
(3)步骤Ⅲ中,停止加热前应进行的操作是 。
(4)该样品中碳酸氢铵的质量分数的表达式为 (用m1、m2的代数式表示)。
26.通常,粗盐中含有不溶性杂质(泥沙等)和可溶性杂质(氯化钙、氯化镁等)。
(1)为了除去粗盐中泥沙等不溶性杂质,可利用 的方法除去。下面提供的几组物质中,也能用该方法除去杂质的是 (选填字母序号)。
A.氯化钾中混有少量的二氧化锰
B.木炭粉末中混有少量的氧化钙
C.氯化钡中混有少量的氢氧化钡
(2)对于如何除去粗盐中可溶性的氯化镁和氯化钙、硫酸钠等杂质,同学们提出以下方案:
请回答:
a.操作中②的物质X为 ;
b.操作①②顺序能否相反? 原因是 。
27.侯氏制碱法所得的纯碱中常含有少量氯化钠,现用如图所示装置来测定纯碱样品中碳酸钠的质量分数(铁架台、铁夹等固定用装置已略去)
实验步骤如下:
①按图连接装置,并检查气密性;②准确称得盛有碱石灰(固体氢氧化钠和生石灰的混合物)的干燥管D的质量ag;③准确称得m g纯碱样品放入装置B的广口瓶中;④打开装置B的分液漏斗旋塞,缓缓滴入稀硫酸,至不再产生气泡为止;⑤打开弹簧夹,往试管A中缓缓鼓入空气数分钟,然后称得干燥管D的总质量为b g。
试回答:
(1)鼓入空气的目的是 ,装置A中试剂X最适宜选用 。
(2)实验中,是否可以去除C装置?理由是什么? 。
(3)碳酸钠的质量分数表达式 。
四.计算题
28.某溶液可能含CuSO4、HCl、MgCl2、Na2CO3中的几种,向其中加入一定溶质质量分数的Ba(OH)2溶液,反应中加入的Ba(OH)2溶液质量与产生沉淀的质量关系如图,回答下列问题。
(1)ab段生成的沉淀是: (填写物质的化学式)。
(2)某同学说该溶液中一定没有CuSO4,他的理由是 。
(3)a中溶液含有 种溶质。
(4)原溶液中含有的溶质是 。(填写物质的化学式)
29.某学校在进行植物园建设时设置了一个无土栽培区。无土栽培是利用磷酸钙、碳酸钾和氯化铵等盐类配置营养液栽培植物的一种方法。很多学生对此很感兴趣,并进行了研究和实践。
(1)营养液中的碳酸钾(K2CO3)为植物生长提供了 肥(填“氮”或“磷”或“钾”);
(2)无土栽培时,营养液浓度不宜过高,其原因是 。
(3)氯化铵(NH4Cl)中氮元素和氢元素的质量比为 ;
(4)小明在某次配制营养液时需要加入14克氮元素,如果这些氮元素都由氯化铵提供,则需要加入多少克氯化铵?(写出计算步骤)
参考答案
选择题
1.A; 2.C; 3.D; 4.B; 5.B; 6.A; 7.D; 8.D; 9.B; 10.D; 11.A; 12.D; 13.C; 14.D; 15.B; 16.C; 17.B; 18.A; 19.A; 20.B;
二.填空题
21.蓝;CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;CuSO4;Ba(OH)2; 22.碱;K+、CO32﹣;CO2+2NaOH═Na2CO3+H2O;MgCl2+2NaOH═2NaCl+Mg(OH)2↓;A;③; 23.产生白色沉淀;CO32﹣;CuSO4+2NaOH═Na2SO4+Cu(OH)2↓;没有沉淀生成; 24.①③⑥;
三.实验探究题
25.氮肥;浓硫酸;2NaOH+CO2═Na2CO3+H2O;打开弹簧夹,通入一段时间的氮气;×100%; 26.溶解、过滤、蒸发;A;碳酸钠溶液;否;.如果先加入碳酸钠,后加入的过量的氯化钡就无法除去。; 27.使B中产生的二氧化碳全部进入D中;氢氧化钠溶液;不可以,没有C装置,则会导致测定结果偏大;×100%;
四.计算题
28.Mg(OH)2;硫酸铜能与氢氧化钡反应生成了硫酸钡,图象中开始没有沉淀生成;2;HCl、MgCl2;
29.钾;防止植物细胞渗透失水;7:2;53.5g
一.选择题
1.Na2CO3的水溶液呈碱性,下列说法错误的是( )
A.碳酸钠在水中会电离出OH﹣ B.往碳酸钠溶液中加稀硫酸后溶液的pH降低
C.碳酸钠溶液中存在OH﹣ D.往碳酸钠溶液中滴加紫色石蕊试液后溶液显蓝色
2.张大伯为了庄稼生长茂盛,茎杆粗壮,增强抗病虫害能力,需要施肥,下列物质属于钾肥的是( )
A.NH4HCO3 B.Ca(H2PO4)2 C.K2CO3 D.CO(NH2)2
3.有关物质用途正确的是( )
A.氢氧化钠改良酸性土壤 B.用BaCl2处理大量泄漏的浓硫酸
C.氢氧化铜治疗胃酸过多 D.熟石灰配制农药波尔多液
4.下列各组物质不能发生化学反应的是( )
A.NaOH溶液和稀HNO3 B.AgCl和KNO3
C.CaCO3和稀HCl D.BaCl2溶液和稀H2SO4
5.某一无色溶液具有下列性质:①使无色酚酞试液变红;②与CuSO4溶液反应可产生蓝色沉淀;③与纯碱溶液反应产生白色沉淀。此溶液是( )
A.氢氧化钠溶液 B.澄清石灰水
C.氯化钙溶液 D.盐酸
6.下列两种物质的溶液混合后,能发生反应,且溶液的总质量不会发生改变的是( )
A.氢氧化钠溶液和稀盐酸 B.碳酸钠溶液和稀盐酸
C.氯化钠溶液和稀硫酸 D.碳酸钠溶液和氯化钙溶液
7.下列各组物质的溶液,不能发生复分解反应的是( )
A.HCl和Ca(OH)2 B.H2SO4和Na2CO3
C.AgNO3 和 BaCl2 D.KCl和CuSO4
8.向含有稀盐酸和氯化铜的混合溶液中滴加NaOH溶液,如图曲线中描述正确的是( )
A.B.
C.D.
9.现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量的某物质X,溶液的pH随滴入X的量的变化关系如图所示,则X可能是( )
A.水 B.纯碱溶液 C.澄清石灰水 D.稀盐酸
10.某粗盐固体样品中含有少量CaCl2、MgCl2、Na2SO4、MgSO4和泥沙,进行以下操作可得到纯净的NaCl晶体:①加过量的NaOH溶液;②加H2O溶解;③加过量的BaCl2溶液;④过滤;⑤蒸发;⑥加过量的Na2CO3溶液;⑦加适量的稀盐酸,则正确的操作顺序是( )
A.②①⑥③④⑦⑤B.②①③⑥⑦④⑤
C.⑥②①③④⑤⑦ D.②③①⑥④⑦⑤
11.甲、乙两化工分布在某排污渠两岸(如图所示),箭头代表水流方向.若甲厂附近a处水样经检测含有的阴离子是OH﹣、SO42﹣,c处水样经检测pH=7且只含有少量的NaCl.则乙厂排放到b处水中的物质可能是( )
A.BaCl2、HCl B.H2SO4、Ba(NO3)2
C.MgSO4、NaCl D.H2SO4、MgCl2
12.从HCl、CuSO4、NaOH、Na2CO3、Na2SO4、Ca(NO3)2六种溶液中,任意取出两种溶液(分别编号为a和b)混合,得到无色澄清溶液,无其他明显现象,测得混合后溶液pH=1.仅根据上述实验现象和数据,对a、b作出的推断中,不正确的是( )
A.肯定有一种是HCl,另一种可能是NaOH溶液
B.符合上述实验现象的a、b组合可能不止一种
C.b都不可能是CuSO4溶液、Na2CO3溶液
D.b都不可能是CuSO4溶液、Na2CO3溶液、NaOH溶液
13.下列各组物质加入水中充分搅拌后,同组反应物恰好完全反应,过滤后,在滤纸上留下两种不溶物质的是( )
A.Ca(NO3)2、BaCl2、AgNO3
B.MgCl2、KOH、NaCl
C.CuSO4、Ba(OH)2、Cu(NO3)2
D.K2CO3、CuSO4、KCl
14.一定温度下,向不饱和的氯化铜溶液中加入足量的下列固体,其对应关系正确的是( )
A.B.
C.D.
15.对于复分解反应,X+2NaOH═2Y+Cu(OH)2↓,下列分析中正确的是( )
A.X一定是CuCl2 B.相对分子质量大小:X>Y
C.Y可能是H2O D.Y可能是Na2SO4
16.利用饱和碳酸钠溶液与酸反应,小科同学只做了如图甲所示的简易酸碱灭火器装置,并进行操作。操作结束后,对瓶中残留液进行如图乙所示的实验。实验现象:A试管溶液变红色,B试管中有白色沉淀生成。则残留液中含有的溶质有( )
A.盐酸 B.碳酸钠 C.硫酸钠 D.氯化钠
17.现有盐酸和CaCl2的混合溶液,向其中逐滴滴入Na2CO3溶液,生成沉淀质量与滴入Na2CO3溶液质量的变化关系如图所示。下列说法正确的是( )
A.滴加碳酸钠溶液质量为0~a g时,溶液中有三种离子
B.滴加碳酸钠溶液质量至b g时,溶液中含两种溶质
C.滴加碳酸钠溶液质量至a g时,溶液中溶质质量比原混合溶液中溶质质量小
D.滴加碳酸钠溶液质量为a~c g时,溶液呈酸性
18.小乐完成了图示甲、乙实验后,依次将反应后的溶液缓慢倒入同一洁净的废液缸中,观察到废液缸中先有气泡产生,然后又出现白色沉淀,则下列说法中,正确的是( )
A.甲实验结束后,试管中的废液含稀盐酸和CaCl2
B.乙实验结束后,试管中的废液只含NaCl溶质
C.最终,废液缸中一定含NaCl、CaCl2两种溶质
D.最终,废液缸中一定含NaCl、Na2CO3两种溶质
19.推理是化学学习中常见的思维方法,下列推理正确的是( )
A.碱性溶液能使酚酞试液变红,滴入酚酞试液后变红的溶液一定呈碱性
B.Na2CO3溶液能够使酚酞变红,所以它属于碱
C.酸能使石蕊试液变红,CO2也能使紫色的石蕊试液变红,所以CO2是酸
D.酸和碳酸盐反应产生气体,所以与酸反应能产生气体的物质里一定含有碳酸根离子
20.按如图所示装置进行实验(图中铁架台等仪器均已略去)。先在试管Ⅱ中加入试剂乙,然后在试管Ⅰ中加入试剂甲,立即塞紧橡皮塞,一段时间后,观察到试管Ⅱ中有白色沉淀生成。符合以上实验现象的一组试剂是( )
A.甲:Na2CO3、稀HCl乙:NaOH
B.甲:Zn、稀H2SO4乙:Ba(NO3)2溶液
C.甲:MgO、稀盐酸乙:AgNO3
D.甲:CuO、稀H2SO4乙:BaCl2溶液
二.填空题
21.盐中含有金属离子(或NH4+)和酸根离子,组成相似的盐具有一些相似的化学性质。
(1)硫酸铜、硝酸铜两种物质的溶液均显 色,因为它们都具有相同的阳离子;向这两种物质的溶液中分别加入NaOH溶液,有相同的实验现象发生,写出其中一个反应的化学方程式 。
(2)向硫酸铜、硝酸铜两种物质的溶液中分别加入BaCl2溶液,能发生反应的物质是 (填化学式),另外一种物质不反应。
(3)向硫酸铜溶液中,加入某纯净物的溶液,能同时将铜离子和硫酸根离子转变成沉淀,该纯净物的化学式为 。
22.酸、碱、盐的在日常生活、生产中用途广泛,请回答以下问题.
(1)碳酸钠可用于洗涤剂是因为它的水溶液呈 性(填“酸、碱、中”).碳酸钾的水溶液中能导电的粒子符号是 ;
(2)氢氧化钠是一种常见的碱,根据题意写出下列反应的化学方程式:
①用氢氧化钠溶液吸收二氧化碳气体 ;
②除去氯化钠中的氯化镁杂质 ;
在与二氧化碳反应中,下列物质代替氢氧化钠溶液也能出现同样现象的试剂是 (填编号).
A、KOH B、Ca(OH)2 C、Ba(OH)2 D、Cu(OH)2
(3)硫酸的下列用途中,不能用盐酸代替硫酸的是 (填编号)
①制氢气 ②金属除锈 ③制化肥硫酸铵.
23. 如图,几种物质是常见的盐,请回答下列问题。
(1)在碳酸钠溶液中滴入氯化钙溶液,现象是 。
(2)碳酸钙、碳酸钠均能与稀盐酸反应生成CO2,是因为碳酸钙、碳酸钠中均含有 (写离子符号)。
(3)硫酸铜溶液与氢氧化钠溶液能发生反应,该反应的化学方程式为 ;硫酸铜溶液与氯化钠溶液不能反应,其理由是 。
24.判断下列物质组合能发生复分解反应的有 (填序号)
①K2CO3+CaCl2②H2SO4+KCl ③CuO+HCl ④Fe+CuSO4⑤CO2+NaOH
⑥K2SO4+BaCl2⑦Mg(OH)2+CuSO4⑧BaCO3+NaOH.
三.实验探究题
25.实验室现有一瓶含少量水的碳酸氢铵样品,为测定其中碳酸氢铵的质量分数,某化学兴趣小组利用如图所示装置进行实验(该装置气密性良好,装置B、C中所装药品均足量,碱石灰是氧化钙和氢氧化钠的混合物)。已知:碳酸氢铵受热易分解,反应的化学方程式为:NH4HCO3NH3↑+H2O↑+CO2↑,NH3能被酸溶液吸收
部分实验步骤如下
Ⅰ.打开弹簧夹,通入一段时间的氮气;
Ⅱ.关闭弹簧夹,给碳酸氢铵样品加热
Ⅲ.当样品反应完全,…,再停止加热,直到玻璃管冷却;
N.实验完毕,测得装置B、C中药品的质量分别增加了m1、m2
请回答下列问题:
(1)NH4HCO3属于 (选填“氮肥”“磷肥”“钾肥”或“复合肥”),装置B中盛放的液体是
。
(2)装置C中发生反应的化学方程式为 。
(3)步骤Ⅲ中,停止加热前应进行的操作是 。
(4)该样品中碳酸氢铵的质量分数的表达式为 (用m1、m2的代数式表示)。
26.通常,粗盐中含有不溶性杂质(泥沙等)和可溶性杂质(氯化钙、氯化镁等)。
(1)为了除去粗盐中泥沙等不溶性杂质,可利用 的方法除去。下面提供的几组物质中,也能用该方法除去杂质的是 (选填字母序号)。
A.氯化钾中混有少量的二氧化锰
B.木炭粉末中混有少量的氧化钙
C.氯化钡中混有少量的氢氧化钡
(2)对于如何除去粗盐中可溶性的氯化镁和氯化钙、硫酸钠等杂质,同学们提出以下方案:
请回答:
a.操作中②的物质X为 ;
b.操作①②顺序能否相反? 原因是 。
27.侯氏制碱法所得的纯碱中常含有少量氯化钠,现用如图所示装置来测定纯碱样品中碳酸钠的质量分数(铁架台、铁夹等固定用装置已略去)
实验步骤如下:
①按图连接装置,并检查气密性;②准确称得盛有碱石灰(固体氢氧化钠和生石灰的混合物)的干燥管D的质量ag;③准确称得m g纯碱样品放入装置B的广口瓶中;④打开装置B的分液漏斗旋塞,缓缓滴入稀硫酸,至不再产生气泡为止;⑤打开弹簧夹,往试管A中缓缓鼓入空气数分钟,然后称得干燥管D的总质量为b g。
试回答:
(1)鼓入空气的目的是 ,装置A中试剂X最适宜选用 。
(2)实验中,是否可以去除C装置?理由是什么? 。
(3)碳酸钠的质量分数表达式 。
四.计算题
28.某溶液可能含CuSO4、HCl、MgCl2、Na2CO3中的几种,向其中加入一定溶质质量分数的Ba(OH)2溶液,反应中加入的Ba(OH)2溶液质量与产生沉淀的质量关系如图,回答下列问题。
(1)ab段生成的沉淀是: (填写物质的化学式)。
(2)某同学说该溶液中一定没有CuSO4,他的理由是 。
(3)a中溶液含有 种溶质。
(4)原溶液中含有的溶质是 。(填写物质的化学式)
29.某学校在进行植物园建设时设置了一个无土栽培区。无土栽培是利用磷酸钙、碳酸钾和氯化铵等盐类配置营养液栽培植物的一种方法。很多学生对此很感兴趣,并进行了研究和实践。
(1)营养液中的碳酸钾(K2CO3)为植物生长提供了 肥(填“氮”或“磷”或“钾”);
(2)无土栽培时,营养液浓度不宜过高,其原因是 。
(3)氯化铵(NH4Cl)中氮元素和氢元素的质量比为 ;
(4)小明在某次配制营养液时需要加入14克氮元素,如果这些氮元素都由氯化铵提供,则需要加入多少克氯化铵?(写出计算步骤)
参考答案
选择题
1.A; 2.C; 3.D; 4.B; 5.B; 6.A; 7.D; 8.D; 9.B; 10.D; 11.A; 12.D; 13.C; 14.D; 15.B; 16.C; 17.B; 18.A; 19.A; 20.B;
二.填空题
21.蓝;CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;CuSO4;Ba(OH)2; 22.碱;K+、CO32﹣;CO2+2NaOH═Na2CO3+H2O;MgCl2+2NaOH═2NaCl+Mg(OH)2↓;A;③; 23.产生白色沉淀;CO32﹣;CuSO4+2NaOH═Na2SO4+Cu(OH)2↓;没有沉淀生成; 24.①③⑥;
三.实验探究题
25.氮肥;浓硫酸;2NaOH+CO2═Na2CO3+H2O;打开弹簧夹,通入一段时间的氮气;×100%; 26.溶解、过滤、蒸发;A;碳酸钠溶液;否;.如果先加入碳酸钠,后加入的过量的氯化钡就无法除去。; 27.使B中产生的二氧化碳全部进入D中;氢氧化钠溶液;不可以,没有C装置,则会导致测定结果偏大;×100%;
四.计算题
28.Mg(OH)2;硫酸铜能与氢氧化钡反应生成了硫酸钡,图象中开始没有沉淀生成;2;HCl、MgCl2;
29.钾;防止植物细胞渗透失水;7:2;53.5g
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
