人教版九年级上册 第六单元碳和碳的氧化物的复习课件(17张PPT)
文档属性
| 名称 | 人教版九年级上册 第六单元碳和碳的氧化物的复习课件(17张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 389.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-11-12 00:00:00 | ||
图片预览

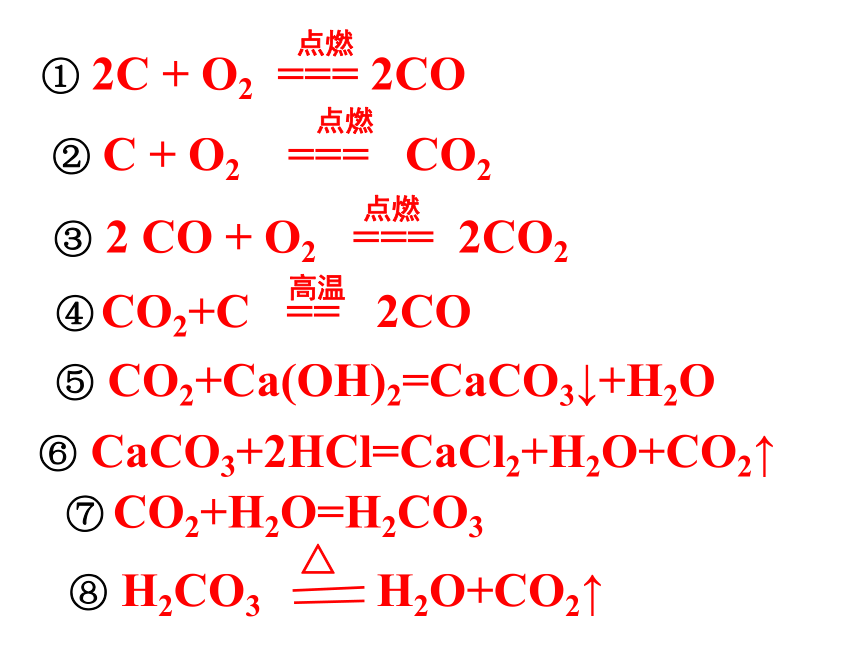



文档简介
第六单元 碳和碳的氧化物
复 习 课
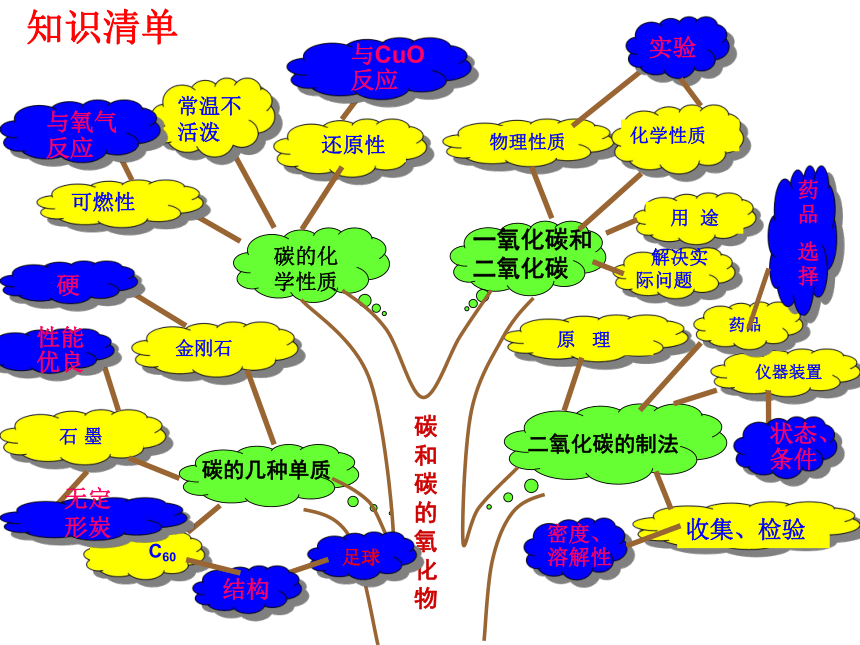
碳的几种单质
二氧化碳的制法
碳的化
学性质
一氧化碳和二氧化碳
C60
金刚石
物理性质
原 理
仪器装置
收集、检验
碳和碳的氧化物
还原性
可燃性
化学性质
用 途
知识清单
石 墨
常温不活泼
硬
性能优良
无定
形炭
药品
药品
选择
与氧气反应
与CuO反应
实验
密度、溶解性
状态、条件
足球
结构
解决实际问题
C
CO
CO2
CaCO3
CaO
Ca(OH)2
H2CO3
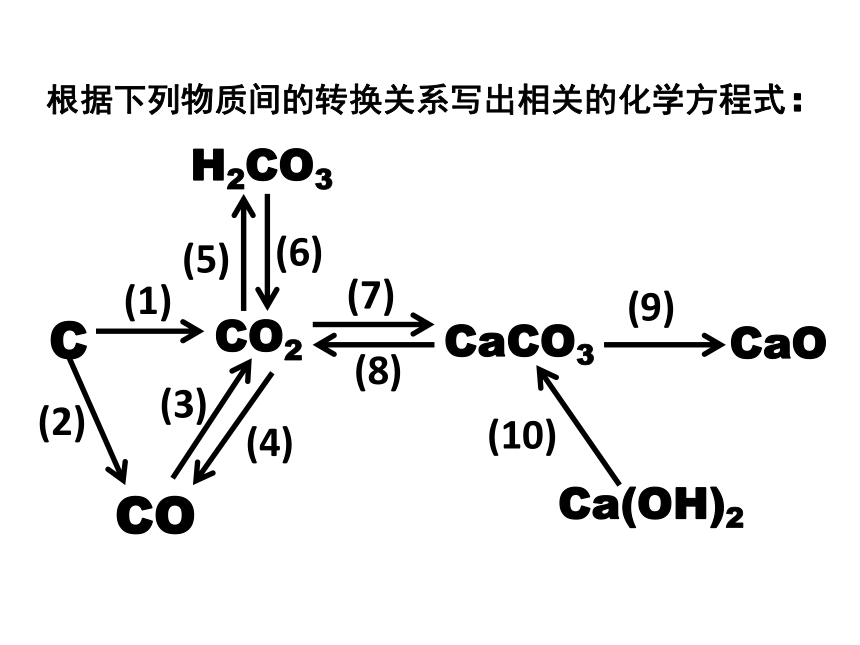
根据下列物质间的转换关系写出相关的化学方程式:
(1)
(2)
(3)
(4)
(5)
(6)
(7)
(8)
(9)
(10)
① 2C + O2 === 2CO
点燃
③ 2 CO + O2 === 2CO2
点燃
② C + O2 === CO2
点燃
④ CO2+C == 2CO
⑤ CO2+Ca(OH)2=CaCO3↓+H2O
⑥ CaCO3+2HCl=CaCl2+H2O+CO2↑
⑦ CO2+H2O=H2CO3
⑧ H2CO3 H2O+CO2↑
△
高温
4.各种碳单质相似的化学性质是
.
§6..1碳单质
1、碳元素可组成不同的单质例如
.
3、各种碳单质物理性质有差异的原因 .
2、有吸附性的碳单质是: .
吸附性属于 .
碳可燃性(燃料)
还原性(冶金)
金刚石.石墨..C60分子等
活性炭.木炭.焦炭.炭黑
木炭.活性炭
物理性质
碳原子的排列方式不同
4、碳的化学性质:
(1)常温下化学性质 ;
(2)可燃性(写出化学方程式)
①木炭在氧气充足情况下燃烧
②木炭在氧气不足情况下燃烧
(3)还原性(写出化学方程式)
①木炭还原氧化铜
稳定
C+O2 = CO2
点燃
2C+O2 = 2CO
点燃
C+2CuO = 2Cu+CO2↑
高温
②木炭还原氧化铁
碳:在反应中 氧变成 ,发生 反应,本身被 ,是 剂,具有 性。
氧化铁:在反应中 氧变成 ,发生 反应,本身被 ,是 剂,具有 性。
3C+2Fe2O3 = 4Fe+3CO2↑
高温
得到
二氧化碳
氧化
氧化
还原
还原
失去
铁
还原
氧化
还原
氧化
§6..2CO2的制取:
1.实验室制取CO2的原料是?
2.有关化学方程式?
3.收集CO2方法及原理
4.
鉴定
验满
二氧化碳
CO2
澄清的
石灰水
燃烧的木条接近瓶口,若木条熄灭,证明已经集满
涂有石灰水的玻璃片盖在瓶口
石灰石或者大理石与稀盐酸
CaCO3+2HCI=CaCI2+H2O+CO2↑
向上排空气集气法…密度比空气大.溶于水
滴有紫色石蕊的滤纸接触瓶口
A B C D E
A B C D E
所用药品名称
有关化学方程式
所选用的发生装置
所选制取的气体
D E
D
氧 气
过氧化氢溶液、二氧化锰
2H2O2=2H2O+O2↑
MnO2
B
二氧化碳
大理石(或石灰石)、稀盐酸
CaCO3+2HCl=CaCl2+CO2↑+H2O
B
所选用的收集装置
1.通过CO2灭火可知道
CO2的化学性质 .
物理性质 .
不可燃.不支持燃烧
密度比空气大
CO2+H2O=H2CO3
CO2+Ca(OH)2=CaCO3↓+H2O
H2CO3 =H2O +CO2 ↑
§6..3 CO2与CO
2.CO2溶与水生成
不稳定的酸
3.CO2与石灰水反应
5.大气中二氧化碳的产生途径:
大气中二氧化碳的消耗途径:
绿色植物的光合作用吸收二氧化碳,放出氧气。
①人和动植物的呼吸;
②煤.石油.天然气等燃料的燃烧;
减少使用煤、石油、天然气等化石燃烧,更多地利用太阳能、风能、地热等清洁能源;大力植树造林,严禁乱砍滥伐森林。
4.怎样减少温室气体的排放?
物理
性质
化学
性质
无色、无味、密度比空气略小,难溶于水的气体。
一氧化碳性质
①可燃性
②还原性
③毒性
3CO + Fe2O3 = 2Fe + 3CO2
CuO+CO = Cu+CO2
高温
吸入CO后.血红蛋白不能很好地与氧气结合.极易与血液中的血红蛋白结合生物体内缺氧
2CO + O2 == 2 CO2
点燃
还原性
联系
主要用途
毒 性
与石灰水反应
与水反应
氧化性
可燃性
水溶性
密 度
色 态 味
物质
二氧化碳与一氧化碳的性质
物理性质
化 学 性 质
二氧化碳
一氧化碳
剧 毒
无
无
难溶于水
比空气小
无色无味气体
无色无味气体
无
无
CO2+H2O====H2CO3
无
在一般情况下,既不能燃烧也不能支持燃烧
能溶于水
比空气大
点燃
2CO+O2 2CO2
CO+CuO ====Cu+CO2
△
CO2+ C ==== 2CO
高温
CO2+Ca(OH)==CaCO3 + H2O
灭火 制汽水 温室肥料 化工原料、光合作用等
燃料 冶炼金属
相互转化
2CO+O2 === CO2
点燃
CO2+ C ==== 2CO
高温
氧气和二氧化碳实验室制法的比较
物质
反应原理
实验装置图
检验方法
氧气
二氧化碳
△
2KMnO4==K2MnO4+ MnO2+O2↑
二氧化锰
2H2O2=====2H2O + O2↑
CaCO3+2HCl==CaCl2+H2O+CO2↑
将带火星的木
条放入集气瓶
内,木条复燃
,证明是氧气
将气体通入澄
清的石灰水,
石灰水变浑浊,
证明该气体是
CO2
氧气和二氧化碳实验室制法的比较
物质
验 满
步骤
注意事项
氧气
二氧化碳
用带火星的木条在瓶口检验,木条复燃,则满
用燃着的木条在瓶口检验,木条熄灭,则满
查、装、定、点、
收、离、熄
查、装(先固后液)、收
(1)反应的条件。(2)反应物的状态。
提问:1、在选择发生装置时要考虑哪些因素?
2、在选择收集装置时应以什么为依据?
主要应以物理性质两个方面:
(1)气体的密度与空气比较
(2)气体在水中的溶解性
从两个方面考虑:
(能否与空气的成分发生反应)
归纳总结
两套发生装置
三种收集方法
排水法
向下排空气法
向上排空气法
归纳总结
复 习 课
碳的几种单质
二氧化碳的制法
碳的化
学性质
一氧化碳和二氧化碳
C60
金刚石
物理性质
原 理
仪器装置
收集、检验
碳和碳的氧化物
还原性
可燃性
化学性质
用 途
知识清单
石 墨
常温不活泼
硬
性能优良
无定
形炭
药品
药品
选择
与氧气反应
与CuO反应
实验
密度、溶解性
状态、条件
足球
结构
解决实际问题
C
CO
CO2
CaCO3
CaO
Ca(OH)2
H2CO3
根据下列物质间的转换关系写出相关的化学方程式:
(1)
(2)
(3)
(4)
(5)
(6)
(7)
(8)
(9)
(10)
① 2C + O2 === 2CO
点燃
③ 2 CO + O2 === 2CO2
点燃
② C + O2 === CO2
点燃
④ CO2+C == 2CO
⑤ CO2+Ca(OH)2=CaCO3↓+H2O
⑥ CaCO3+2HCl=CaCl2+H2O+CO2↑
⑦ CO2+H2O=H2CO3
⑧ H2CO3 H2O+CO2↑
△
高温
4.各种碳单质相似的化学性质是
.
§6..1碳单质
1、碳元素可组成不同的单质例如
.
3、各种碳单质物理性质有差异的原因 .
2、有吸附性的碳单质是: .
吸附性属于 .
碳可燃性(燃料)
还原性(冶金)
金刚石.石墨..C60分子等
活性炭.木炭.焦炭.炭黑
木炭.活性炭
物理性质
碳原子的排列方式不同
4、碳的化学性质:
(1)常温下化学性质 ;
(2)可燃性(写出化学方程式)
①木炭在氧气充足情况下燃烧
②木炭在氧气不足情况下燃烧
(3)还原性(写出化学方程式)
①木炭还原氧化铜
稳定
C+O2 = CO2
点燃
2C+O2 = 2CO
点燃
C+2CuO = 2Cu+CO2↑
高温
②木炭还原氧化铁
碳:在反应中 氧变成 ,发生 反应,本身被 ,是 剂,具有 性。
氧化铁:在反应中 氧变成 ,发生 反应,本身被 ,是 剂,具有 性。
3C+2Fe2O3 = 4Fe+3CO2↑
高温
得到
二氧化碳
氧化
氧化
还原
还原
失去
铁
还原
氧化
还原
氧化
§6..2CO2的制取:
1.实验室制取CO2的原料是?
2.有关化学方程式?
3.收集CO2方法及原理
4.
鉴定
验满
二氧化碳
CO2
澄清的
石灰水
燃烧的木条接近瓶口,若木条熄灭,证明已经集满
涂有石灰水的玻璃片盖在瓶口
石灰石或者大理石与稀盐酸
CaCO3+2HCI=CaCI2+H2O+CO2↑
向上排空气集气法…密度比空气大.溶于水
滴有紫色石蕊的滤纸接触瓶口
A B C D E
A B C D E
所用药品名称
有关化学方程式
所选用的发生装置
所选制取的气体
D E
D
氧 气
过氧化氢溶液、二氧化锰
2H2O2=2H2O+O2↑
MnO2
B
二氧化碳
大理石(或石灰石)、稀盐酸
CaCO3+2HCl=CaCl2+CO2↑+H2O
B
所选用的收集装置
1.通过CO2灭火可知道
CO2的化学性质 .
物理性质 .
不可燃.不支持燃烧
密度比空气大
CO2+H2O=H2CO3
CO2+Ca(OH)2=CaCO3↓+H2O
H2CO3 =H2O +CO2 ↑
§6..3 CO2与CO
2.CO2溶与水生成
不稳定的酸
3.CO2与石灰水反应
5.大气中二氧化碳的产生途径:
大气中二氧化碳的消耗途径:
绿色植物的光合作用吸收二氧化碳,放出氧气。
①人和动植物的呼吸;
②煤.石油.天然气等燃料的燃烧;
减少使用煤、石油、天然气等化石燃烧,更多地利用太阳能、风能、地热等清洁能源;大力植树造林,严禁乱砍滥伐森林。
4.怎样减少温室气体的排放?
物理
性质
化学
性质
无色、无味、密度比空气略小,难溶于水的气体。
一氧化碳性质
①可燃性
②还原性
③毒性
3CO + Fe2O3 = 2Fe + 3CO2
CuO+CO = Cu+CO2
高温
吸入CO后.血红蛋白不能很好地与氧气结合.极易与血液中的血红蛋白结合生物体内缺氧
2CO + O2 == 2 CO2
点燃
还原性
联系
主要用途
毒 性
与石灰水反应
与水反应
氧化性
可燃性
水溶性
密 度
色 态 味
物质
二氧化碳与一氧化碳的性质
物理性质
化 学 性 质
二氧化碳
一氧化碳
剧 毒
无
无
难溶于水
比空气小
无色无味气体
无色无味气体
无
无
CO2+H2O====H2CO3
无
在一般情况下,既不能燃烧也不能支持燃烧
能溶于水
比空气大
点燃
2CO+O2 2CO2
CO+CuO ====Cu+CO2
△
CO2+ C ==== 2CO
高温
CO2+Ca(OH)==CaCO3 + H2O
灭火 制汽水 温室肥料 化工原料、光合作用等
燃料 冶炼金属
相互转化
2CO+O2 === CO2
点燃
CO2+ C ==== 2CO
高温
氧气和二氧化碳实验室制法的比较
物质
反应原理
实验装置图
检验方法
氧气
二氧化碳
△
2KMnO4==K2MnO4+ MnO2+O2↑
二氧化锰
2H2O2=====2H2O + O2↑
CaCO3+2HCl==CaCl2+H2O+CO2↑
将带火星的木
条放入集气瓶
内,木条复燃
,证明是氧气
将气体通入澄
清的石灰水,
石灰水变浑浊,
证明该气体是
CO2
氧气和二氧化碳实验室制法的比较
物质
验 满
步骤
注意事项
氧气
二氧化碳
用带火星的木条在瓶口检验,木条复燃,则满
用燃着的木条在瓶口检验,木条熄灭,则满
查、装、定、点、
收、离、熄
查、装(先固后液)、收
(1)反应的条件。(2)反应物的状态。
提问:1、在选择发生装置时要考虑哪些因素?
2、在选择收集装置时应以什么为依据?
主要应以物理性质两个方面:
(1)气体的密度与空气比较
(2)气体在水中的溶解性
从两个方面考虑:
(能否与空气的成分发生反应)
归纳总结
两套发生装置
三种收集方法
排水法
向下排空气法
向上排空气法
归纳总结
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
