2020-2021学年上海市普陀区九年级(上)期中化学试卷(word+解析答案)
文档属性
| 名称 | 2020-2021学年上海市普陀区九年级(上)期中化学试卷(word+解析答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 244.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版(试用本) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-11-13 00:00:00 | ||
图片预览



文档简介
2020-2021学年上海市普陀区九年级(上)期中化学试卷
一、选择题(共20分)1-14题只有一个正确选项,15-17题有1-2个正确选项,请将正确选项的代号用2B铅笔填涂在答题纸的相应位置上,更改答案时,用橡皮擦去,重新填涂。
1.(1分)属于化学变化的是( )
A.玻璃破碎
B.蜡烛熔化
C.水的蒸发
D.酒精燃烧
2.(1分)属于氧化物的是( )
A.Na2CO3
B.P2O5
C.O3
D.CaCO3
3.(1分)属于浊液的是( )
A.糖水
B.泥水
C.盐水
D.汽水
4.(1分)试剂标签对应的化学式书写错误的是( )
A.
B.
C.
D.
5.(1分)我国推广使用的加碘食盐中加入的是碘酸钾(KIO3).碘酸钾中碘元素的化合价为( )
A.+1
B.+3
C.+5
D.+7
6.(1分)化学用语表示正确的是( )
A.2个氢分子:2H
B.2个氧原子:O2
C.水分子:H2O2
D.+1价的钠元素:
7.(1分)有关物质性质对应用途错误的是( )
A.氮气难溶于水﹣﹣用作冷冻剂
B.氧气有助燃性﹣﹣用作氧炔焰
C.稀有气体通电发有色光﹣﹣制霓虹灯
D.生石灰能与水反应﹣﹣作干燥剂
8.(1分)红磷在氧气中燃烧的化学方程式,书写正确的是( )
A.P+O2P2O5
B.4P+5O2═2P2O5
C.4P+5O22P2O5
D.4P+5O2P2O5
9.(1分)实验现象描述正确的是( )
A.氢氧化钠与硫酸铜溶液反应,产生蓝色的氢氧化铜沉淀
B.硫在空气中燃烧,产生明亮的蓝紫色火焰
C.大理石上滴加稀盐酸,产生大量气泡
D.红磷在空气中燃烧,产生大量白雾
10.(1分)华为开创了“中国芯”时代。“中国芯”的主要材料是高纯度的单质硅,高温下氢气与四氯化硅反应制硅的化学方程式为:2H2+SiCl4Si+4X,其中X的化学式为( )
A.Cl2
B.HCl
C.H2O
D.SiH4
11.(1分)关于NH4NO3的分析正确的是( )
A.名称:硝酸氨
B.摩尔质量:80g
C.含有两种原子团
D.该物质中氮元素的化合价相同
12.(1分)根据化学方程式S+O2SO2,无法获得的信息是( )
A.反应前后反应物和生成物的种类
B.参加反应硫和二氧化硫的质量比
C.反应发生所需要的条件
D.化学反应速率的快慢
13.(1分)关于原子和分子,说法正确的是( )
A.同种分子构成纯净物,不同种分子构成混合物
B.分子的质量和体积一定比原子大
C.分子可分,原子不可分
D.分子个数相等的任何物质具有相同的质量
14.(1分)关于物质的量说法正确的是( )
A.摩尔是国际七个基本物理量之一
B.1
摩尔任何物质都含有
6.02×1023个微粒
C.物质的量就是物质的质量
D.物质的量表示一定量数目的微粒的集合体
15.(1分)鉴别物质的方法或试剂错误的是( )
选项
待鉴别的物质
方法或试剂
A
水和5%的双氧水
二氧化锰
B
氢氧化钠溶液和硫酸铜溶液
观察颜色
C
氮气和二氧化碳
燃烧的木条
D
氢氧化钠和澄清石灰水
酚酞
A.A
B.B
C.C
D.D
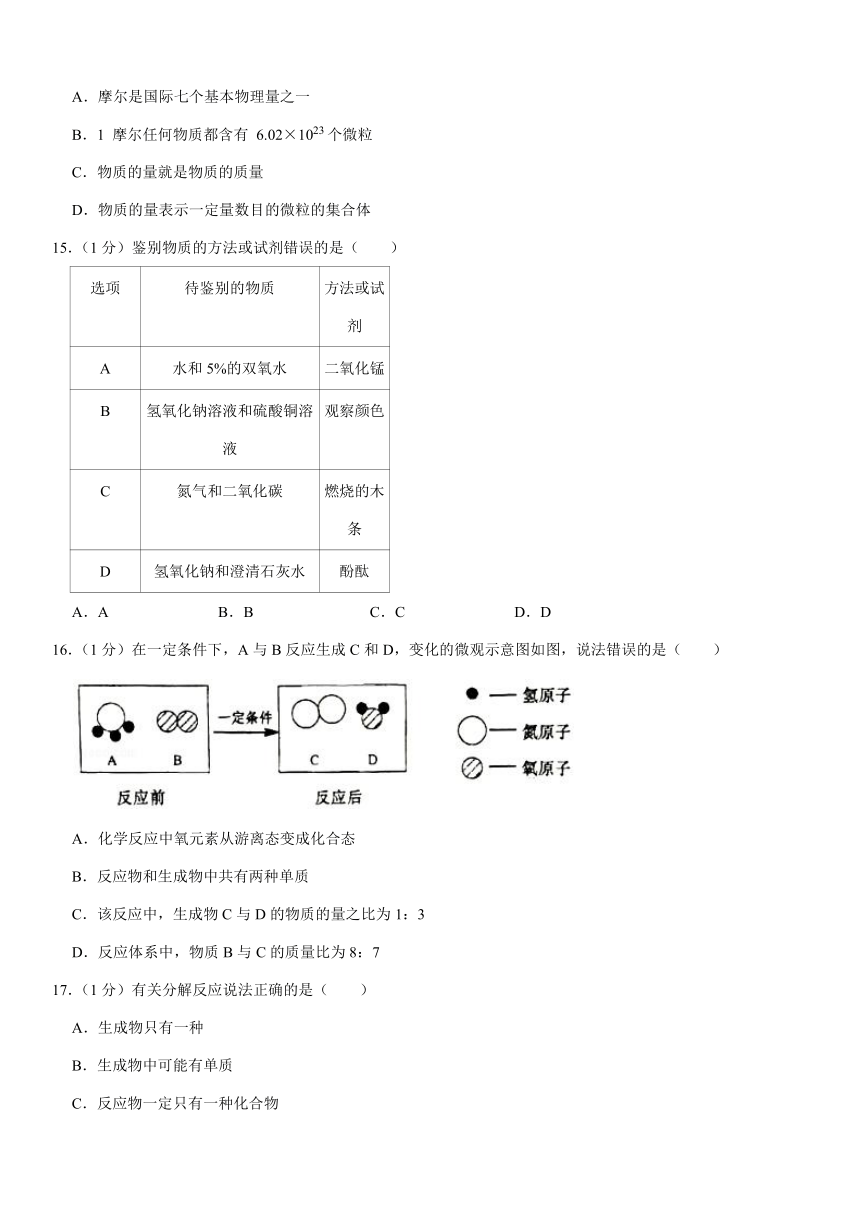
16.(1分)在一定条件下,A与B反应生成C和D,变化的微观示意图如图,说法错误的是( )
A.化学反应中氧元素从游离态变成化合态
B.反应物和生成物中共有两种单质
C.该反应中,生成物C与D的物质的量之比为1:3
D.反应体系中,物质B与C的质量比为8:7
17.(1分)有关分解反应说法正确的是( )
A.生成物只有一种
B.生成物中可能有单质
C.反应物一定只有一种化合物
D.反应后元素的化合价一定改变
二、简答题(共30分)请根据要求在答题纸的相应位置作答。
18.(7分)氧气是一种与人类生活密切相关的气体,请回答下列问题。
①空气中各组分的沸点如下表所示:
组分
氮气
氧气
二氧化碳
氩气
氖气
氦气
沸点(℃)
﹣196
﹣183
﹣78.4
﹣186
﹣246
﹣267
根据以上数据分析可知,将空气加压降温至约﹣200℃时,空气变为液态,升温至约﹣196℃时,
逸出。通过此方法得到的氧气是
(选填“纯净物”或“混合物”)。
②氧气的化学性质十分活泼,能与许多物质发生反应。例如:铁丝氧气中燃烧的现象是剧烈燃烧,
,并放出大量热。发生反应的化学方程式为:
。
③收集氧气可采用排水集气法,因为氧气具有
的性质。甲同学欲收集体积分数为40%的氧气,他先往集气瓶中注入40%体积的水(如图所示),乙同学认为该方法得到的氧气体积分数不是40%,原因是
。
19.(10分)人类生活离不开水,请回答有关问题。
①某自来水厂净化水的大致流程如图:
Ⅰ.絮凝反应处理中会使用净水剂处理微小悬浮物,常用的净水剂有
或氯化铁。
Ⅱ.氯化铁放入水中可与水反应生成Fe(OH)3,Fe(OH)3由
种元素组成,其摩尔质量为
,1mol
Fe(OH)3中约含有
个铁原子。
Ⅲ.消毒处理中常用的消毒剂是
。
②通过如图两个实验可以验证水的组成:
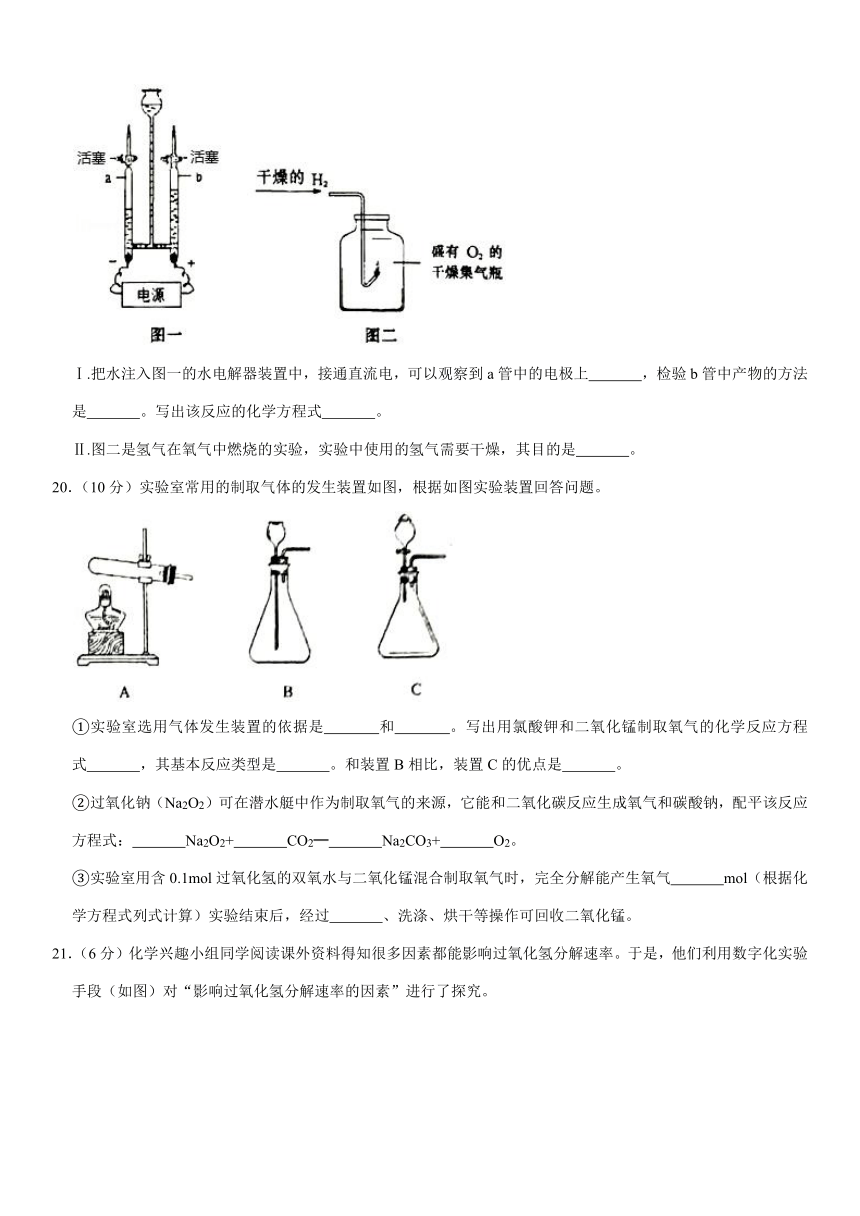
Ⅰ.把水注入图一的水电解器装置中,接通直流电,可以观察到a管中的电极上
,检验b管中产物的方法是
。写出该反应的化学方程式
。
Ⅱ.图二是氢气在氧气中燃烧的实验,实验中使用的氢气需要干燥,其目的是
。
20.(10分)实验室常用的制取气体的发生装置如图,根据如图实验装置回答问题。
①实验室选用气体发生装置的依据是
和
。写出用氯酸钾和二氧化锰制取氧气的化学反应方程式
,其基本反应类型是
。和装置B相比,装置C的优点是
。
②过氧化钠(Na2O2)可在潜水艇中作为制取氧气的来源,它能和二氧化碳反应生成氧气和碳酸钠,配平该反应方程式:
Na2O2+
CO2═
Na2CO3+
O2。
③实验室用含0.1mol过氧化氢的双氧水与二氧化锰混合制取氧气时,完全分解能产生氧气
mol(根据化学方程式列式计算)实验结束后,经过
、洗涤、烘干等操作可回收二氧化锰。
21.(6分)化学兴趣小组同学阅读课外资料得知很多因素都能影响过氧化氢分解速率。于是,他们利用数字化实验手段(如图)对“影响过氧化氢分解速率的因素”进行了探究。
①按下表分组进行实验一,在同一温度下通过压强传感器得到的数据如实验一所示。
实验一
药品
第一组
4%
H2O2溶液15mL
第二组
4%
H2O2溶液15mL、0.2g
MnO2粉末
第三组
4%
H2O2溶液15mL、0.2g
FeCl3粉末
Ⅰ.实验一中设计第一组实验的目的是
。经过分组实验,同学们从实验一中得出结论:在其他条件相同的情况下,
的催化效果最好.
Ⅱ.选用0.2g
MnO2粉末做催化剂,同学们又分别做了实验二和实验三,得到的数据如图,通过分析,影响该反应速率的外界因素除催化剂外,还有
。
Ⅲ.实验一与实验二中4%的过氧化氢溶液与0.2g
MnO2粉末混合后产生的气体压强有明显不同(见图中A点和B点),可能的原因是
。
②实验反思:同学们通过研究讨论,认为还可以研究
对双氧水分解速度的影响。(写出一点即可)
2020-2021学年上海市普陀区九年级(上)期中化学试卷
试题解析
一、选择题(共20分)1-14题只有一个正确选项,15-17题有1-2个正确选项,请将正确选项的代号用2B铅笔填涂在答题纸的相应位置上,更改答案时,用橡皮擦去,重新填涂。
1.【答案】D
【解答】解:A、玻璃破碎没有新物质生成,属于物理变化;故选项错误;
B、蜡烛熔化没有新物质生成,属于物理变化;故选项错误;
C、水的蒸发没有新物质生成,属于物理变化;故选项错误;
D、酒精燃烧生成二氧化碳和水,属于化学变化;故选项正确;
故选:D。
2.【答案】B
【解答】解:A、该物质含有三种元素,不是氧化物,说法错误;
B、该物质是由两种元素组成、其中一种是氧元素的化合物,属于氧化物,说法正确;
C、该物质只含有一种元素,属于单质,说法错误;
D、该物质含有三种元素,不是氧化物,说法错误;
故选:B。
3.【答案】B
【解答】解:A、糖水是蔗糖的水溶液,属于溶液,故选项错误。
B、泥难溶于水,泥水是不溶性的固体小颗粒悬浮于液体中形成的混合物,属于悬浊液,故选项正确。
C、盐水是氯化钠的水溶液,属于溶液,故选项错误。
D、汽水可看作是碳酸的水溶液,属于溶液,故选项错误。
故选:B。
4.【答案】A
【解答】解:A、硫化钾中钾元素显+1价,硫元素显﹣2价,其化学式为:K2S,故选项化学式书写错误。
B、氢氧化钠中钠元素显+1价,氢氧根显﹣1价,其化学式为:NaOH,故选项化学式书写正确。
C、氯化钙中钙元素显+2价,氯元素显﹣1价,其化学式为:CaCl2,故选项化学式书写正确。
D、氧化镁中镁元素显+2价,氧元素显﹣2价,其化学式为:MgO,故选项化学式书写正确。
故选:A。
5.【答案】C
【解答】解:钾元素显+1价,氧元素显﹣2价,设碘元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)+x+(﹣2)×3=0,则x=+5价。
故选:C。
6.【答案】D
【解答】解:A、2个氢分子表示为2H2,说法错误;
B、2个氧原子表示为2O,说法错误;
C、水分子的化学式为H2O,说法错误;
D、+1价的钠元素表示为,说法正确;
故选:D。
7.【答案】A
【解答】解:A、液氮汽化吸热,所以液氮用作冷冻剂,而不是因为氮气难溶于水,故A错误;
B、氧气具有助燃性,所以氧气用作氧炔焰,故B正确;
C、稀有气体通电发出不同颜色的光,所以稀有气体制霓虹灯,故C正确;
D、生石灰能与水反应,所以生石灰用作干燥剂,故D正确。
故选:A。
8.【答案】C
【解答】解:红磷燃烧生成五氧化二磷,反应的化学方程式为:4P+5O22P2O5。
故选:C。
9.【答案】C
【解答】解:A、氢氧化钠溶液与硫酸铜溶液反应生成氢氧化铜蓝色沉淀和硫酸钠,产生蓝色的氢氧化铜沉淀是实验结论而不是实验现象,故选项说法错误。
B、硫在空气中燃烧,产生淡蓝色火焰,故选项说法错误。
C、大理石的主要成分是碳酸钙,碳酸钙与稀盐酸反应生成二氧化碳气体,大理石上滴加稀盐酸,产生大量气泡,故选项说法正确。
D、红磷在空气中燃烧,产生大量的白烟,而不是白雾,故选项说法错误.
故选:C。
10.【答案】B
【解答】解:由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式,反应前氢、硅、氯原子个数分别为4、1、4,反应后的生成物中氢、硅、氯原子个数分别为0、1、4,根据反应前后原子种类、数目不变,则4X分子中含有4个氢原子和4个氯原子,则每个X分子由1个氢原子和1个氯原子构成,则物质X的化学式为HCl。
故选:B。
11.【答案】C
【解答】解:A、NH4NO3从右向左读,读作硝酸铵,故选项说法错误。
B、摩尔质量的单位为g/mol,硝酸铵的摩尔质量是80g/mol,故选项说法错误。
C、由硝酸铵的化学式可知,含有铵根和硝酸根两种原子团,故选项说法正确。
D、硝酸铵(NH4NO3)中铵根显+1价,氢元素显+1价,设铵根中氮元素的化合价是x,由原子团中元素的化合价代数和等于原子团的化合价,可得:x+(+1)×4=+1,则x=﹣3价。硝酸根显﹣1价,氧元素显﹣2价,设硝酸根中氮元素的化合价是y,由原子团中元素的化合价代数和等于原子团的化合价,可得:y+(﹣2)×3=﹣1,则y=+5价。故选项说法错误。
故选:C。
12.【答案】D
【解答】解:A、由化学方程式S+O2SO2,可以确定反应前后反应物(硫和氧气)和生成物(二氧化硫)的种类,故选项说法正确。
B、由化学方程式S+O2SO2,每32份质量的硫和32份质量的氧气在点燃条件下恰好反应生成64份质量的二氧化硫,可以计算出参加反应硫和二氧化硫的质量比,故选项说法正确。
C、由化学方程式S+O2SO2,可以确定反应发生所需要的条件是点燃,故选项说法正确。
D、由化学方程式,无法确定化学反应速率的快慢,故选项说法错误。
故选:D。
13.【答案】A
【解答】解:A、同种分子构成纯净物,不同种分子构成混合物,该选项说法正确;
B、分子的质量和体积不一定比原子大,例如水分子质量小于汞原子质量,该选项说法不正确;
C、化学变化中分子可分,原子不可分,该选项说法不正确;
D、分子个数相等的物质,质量不一定相等,例如1个水分子质量和1个氧分子质量不相等,该选项说法不正确。
故选:A。
14.【答案】D
【解答】解:A、物质的量是一种物理量,其单位是摩尔(mol),而非摩尔是基本物理量之一。错误;
B、1摩尔物质大约含有6.02×1023个该物质的微粒,是大约,而非准确数。错误;
C、物质的量是用来描述微观粒子的数量,与物质的质量完全不同,错误;
D、1mol任何物质的微粒个数约为6.02×1023个,表示一定量数目的微粒的集合体,故正确;
故选:D。
15.【答案】CD
【解答】解:A、取样品,加入二氧化锰,有气泡产生的是双氧水,没有明显现象的是水,现象不同,可以鉴别,故A正确;
B、取样品,观察颜色,无色溶液的是氢氧化钠,蓝色溶液的是硫酸铜,现象不同,可以鉴别,故B正确;
C、氮气和二氧化碳都不具有助燃性,燃着的木条都会熄灭,现象相同,不能鉴别,故C错误;
D、氢氧化钠和澄清石灰水都显碱性,都能使酚酞变红色,现象相同,不能鉴别,故D错误。
故选:CD。
16.【答案】D
【解答】解:由反应的微观示意图可知,该反应是氨气和氧气在点燃时生成了氮气和水,化学方程式为:4NH3+3O22N2+6H2O。
A.在反应前,氧元素存在于氧气这种单质中,在反应后,氧元素存在于水这种化合物中,即化学反应中氧元素从游离态变成化合态,选项说法正确;
B.由化学方程式可知,反应物中的氧气与生成物中的氮气均属于单质,即反应物和生成物中共有两种单质,选项说法正确;
C.由化学方程式可知,该反应中,生成物C(N2)与D(H2O)的物质的量之比为:2:6=1:3,选项说法正确;
D.反应体系中,物质B(O2)与C(N2)的质量比为12:7,选项说法错误。
故选:D。
17.【答案】BC
【解答】解:A、分解反应是一种物质反应后生成两种或两种以上的物质,其特点可总结为“一变多”,生成物是两种或两种以上,故选项说法错误。
B、分解反应的生成物中可能有单质,如水分解生成氢气和氧气,故选项说法正确。
C、分解反应:一种物质反应后生成两种或两种以上的物质,其特点可总结为“一变多”,反应物中只有一种,至少含有两种元素,反应物一定只有一种化合物,故选项说法正确。
D、反应后元素的化合价不一定改变,如碳酸分解生成水和二氧化碳,故选项说法错误。
故选:BC。
二、简答题(共30分)请根据要求在答题纸的相应位置作答。
18.【答案】①氮气;混合物。
②火星四射;3Fe+2O2Fe3O4。
③不易溶于水;剩余的瓶内60%的容积中含有空气,空气中含有氧气。
【解答】解:①根据以上数据分析可知,将空气加压降温至约﹣200℃时,空气变为液态,升温至约﹣196℃时,沸点低的氮气逸出。通过此方法得到的氧气中含有多种物质,是混合物,故填:氮气;混合物。
②铁丝氧气中燃烧的现象是剧烈燃烧,火星四射,并放出大量热。发生反应的化学方程式为:3Fe+2O2Fe3O4;故填:火星四射;3Fe+2O2Fe3O4。
③收集氧气可采用排水集气法,因为氧气具有不易溶于水的性质。欲收集体积分数为40%的氧气,先往集气瓶中注入40%体积的水,该方法得到的氧气体积分数不是40%,是因为剩余的瓶内60%的容积中含有空气,空气中含有氧气,故填:不易溶于水;剩余的瓶内60%的容积中含有空气,空气中含有氧气。
19.【答案】①Ⅰ、明矾;
Ⅱ、3;107g/mol;6.02×1023;
Ⅲ、氯气(合理即可);
②Ⅰ、产生的气泡速率快;打开活塞,将带火星的靠近管口,带火星的木条复燃,说明是氧气;2H2O2H2↑+O2↑;
Ⅱ、验证氢气燃烧生成水。
【解答】解:①Ⅰ、明矾溶于水可以吸附水中的悬浮杂质而加速其沉降,所以絮凝反应处理中会使用净水剂处理微小悬浮物,常用的净水剂有明矾或氯化铁,故填:明矾;
Ⅱ、Fe(OH)3由铁、氢、氧三种元素组成,其摩尔质量为:(56+16×3+1×3)g/mol=107g/mol,1molFe(OH)3中约含有铁原子的个数为:6.02×1023×1=6.02×1023;故填:3;107g/mol;6.02×1023;
Ⅲ、消毒处理中常用的消毒剂是氯气、二氧化氯等;故填:氯气;
②Ⅰ、由图一可知,a管内的气体体积较大,是氢气,b管内的气体体积较小,是氧气,实验中观察到a管中的电极上产生气泡的速率较快,氧气具有助燃性,所以可用带火星的木条来检验,检验方法是打开活塞,将带火星的靠近管口,带火星的木条复燃,说明是氧气;该反应的化学方程式为:2H2O2H2↑+O2↑;故填:产生的气泡速率快;打开活塞,将带火星的靠近管口,带火星的木条复燃,说明是氧气;2H2O2H2↑+O2↑;
Ⅱ、氢气燃烧生成水,所以验证氢气燃烧有水生成时,氢气必须是干燥的,否则无法验证氢气燃烧生成水;故填:验证氢气燃烧生成水。
20.【答案】①反应物状态;反应条件;2KClO32KCl+3O2↑;分解反应;能够控制反应速率。
②2;2;2;1.
③0.05;过滤。
【解答】解:①实验室选用气体发生装置的依据是反应物状态和反应条件;
用氯酸钾和二氧化锰制取氧气的化学反应方程式:2KClO32KCl+3O2↑,其基本反应类型是分解反应;
和装置B相比,装置C的优点是通过分液漏斗能够控制液体药品流量,从而能够控制反应速率。
故填:反应物状态;反应条件;2KClO32KCl+3O2↑;分解反应;能够控制反应速率。
②该反应方程式:2Na2O2+2CO2═2Na2CO3+O2。
故填:2;2;2;1.
③设生成氧气的物质的量为x,
2H2O22H2O+O2↑,
2
1
0.1mol
x
=,
x=0.05mol,
实验结束后,经过过滤、洗涤、烘干等操作可回收二氧化锰。
故填:0.05;过滤。
21.【答案】Ⅰ.进行对比;二氧化锰。
Ⅱ.过氧化氢溶液浓度、温度。
Ⅲ.温度不同。
②催化剂形状。
【解答】解:Ⅰ.实验一中设计第一组实验的目的是进行对比;
经过分组实验,同学们从实验一中得出结论:在其他条件相同的情况下,二氧化锰的催化效果最好,是因为单位时间内利用二氧化锰产生气体比氯化铁多。
故填:进行对比;二氧化锰。
Ⅱ.通过分析,影响该反应速率的外界因素除催化剂外,还有过氧化氢溶液浓度、温度。
故填:过氧化氢溶液浓度、温度。
Ⅲ.实验一与实验二中4%的过氧化氢溶液与0.2g
MnO2粉末混合后产生的气体压强有明显不同(见图中A点和B点),可能的原因是温度不同。
故填:温度不同。
②实验反思:同学们通过研究讨论,认为还可以研究催化剂形状对双氧水分解速度的影响。
故填:催化剂形状。
一、选择题(共20分)1-14题只有一个正确选项,15-17题有1-2个正确选项,请将正确选项的代号用2B铅笔填涂在答题纸的相应位置上,更改答案时,用橡皮擦去,重新填涂。
1.(1分)属于化学变化的是( )
A.玻璃破碎
B.蜡烛熔化
C.水的蒸发
D.酒精燃烧
2.(1分)属于氧化物的是( )
A.Na2CO3
B.P2O5
C.O3
D.CaCO3
3.(1分)属于浊液的是( )
A.糖水
B.泥水
C.盐水
D.汽水
4.(1分)试剂标签对应的化学式书写错误的是( )
A.
B.
C.
D.
5.(1分)我国推广使用的加碘食盐中加入的是碘酸钾(KIO3).碘酸钾中碘元素的化合价为( )
A.+1
B.+3
C.+5
D.+7
6.(1分)化学用语表示正确的是( )
A.2个氢分子:2H
B.2个氧原子:O2
C.水分子:H2O2
D.+1价的钠元素:
7.(1分)有关物质性质对应用途错误的是( )
A.氮气难溶于水﹣﹣用作冷冻剂
B.氧气有助燃性﹣﹣用作氧炔焰
C.稀有气体通电发有色光﹣﹣制霓虹灯
D.生石灰能与水反应﹣﹣作干燥剂
8.(1分)红磷在氧气中燃烧的化学方程式,书写正确的是( )
A.P+O2P2O5
B.4P+5O2═2P2O5
C.4P+5O22P2O5
D.4P+5O2P2O5
9.(1分)实验现象描述正确的是( )
A.氢氧化钠与硫酸铜溶液反应,产生蓝色的氢氧化铜沉淀
B.硫在空气中燃烧,产生明亮的蓝紫色火焰
C.大理石上滴加稀盐酸,产生大量气泡
D.红磷在空气中燃烧,产生大量白雾
10.(1分)华为开创了“中国芯”时代。“中国芯”的主要材料是高纯度的单质硅,高温下氢气与四氯化硅反应制硅的化学方程式为:2H2+SiCl4Si+4X,其中X的化学式为( )
A.Cl2
B.HCl
C.H2O
D.SiH4
11.(1分)关于NH4NO3的分析正确的是( )
A.名称:硝酸氨
B.摩尔质量:80g
C.含有两种原子团
D.该物质中氮元素的化合价相同
12.(1分)根据化学方程式S+O2SO2,无法获得的信息是( )
A.反应前后反应物和生成物的种类
B.参加反应硫和二氧化硫的质量比
C.反应发生所需要的条件
D.化学反应速率的快慢
13.(1分)关于原子和分子,说法正确的是( )
A.同种分子构成纯净物,不同种分子构成混合物
B.分子的质量和体积一定比原子大
C.分子可分,原子不可分
D.分子个数相等的任何物质具有相同的质量
14.(1分)关于物质的量说法正确的是( )
A.摩尔是国际七个基本物理量之一
B.1
摩尔任何物质都含有
6.02×1023个微粒
C.物质的量就是物质的质量
D.物质的量表示一定量数目的微粒的集合体
15.(1分)鉴别物质的方法或试剂错误的是( )
选项
待鉴别的物质
方法或试剂
A
水和5%的双氧水
二氧化锰
B
氢氧化钠溶液和硫酸铜溶液
观察颜色
C
氮气和二氧化碳
燃烧的木条
D
氢氧化钠和澄清石灰水
酚酞
A.A
B.B
C.C
D.D
16.(1分)在一定条件下,A与B反应生成C和D,变化的微观示意图如图,说法错误的是( )
A.化学反应中氧元素从游离态变成化合态
B.反应物和生成物中共有两种单质
C.该反应中,生成物C与D的物质的量之比为1:3
D.反应体系中,物质B与C的质量比为8:7
17.(1分)有关分解反应说法正确的是( )
A.生成物只有一种
B.生成物中可能有单质
C.反应物一定只有一种化合物
D.反应后元素的化合价一定改变
二、简答题(共30分)请根据要求在答题纸的相应位置作答。
18.(7分)氧气是一种与人类生活密切相关的气体,请回答下列问题。
①空气中各组分的沸点如下表所示:
组分
氮气
氧气
二氧化碳
氩气
氖气
氦气
沸点(℃)
﹣196
﹣183
﹣78.4
﹣186
﹣246
﹣267
根据以上数据分析可知,将空气加压降温至约﹣200℃时,空气变为液态,升温至约﹣196℃时,
逸出。通过此方法得到的氧气是
(选填“纯净物”或“混合物”)。
②氧气的化学性质十分活泼,能与许多物质发生反应。例如:铁丝氧气中燃烧的现象是剧烈燃烧,
,并放出大量热。发生反应的化学方程式为:
。
③收集氧气可采用排水集气法,因为氧气具有
的性质。甲同学欲收集体积分数为40%的氧气,他先往集气瓶中注入40%体积的水(如图所示),乙同学认为该方法得到的氧气体积分数不是40%,原因是
。
19.(10分)人类生活离不开水,请回答有关问题。
①某自来水厂净化水的大致流程如图:
Ⅰ.絮凝反应处理中会使用净水剂处理微小悬浮物,常用的净水剂有
或氯化铁。
Ⅱ.氯化铁放入水中可与水反应生成Fe(OH)3,Fe(OH)3由
种元素组成,其摩尔质量为
,1mol
Fe(OH)3中约含有
个铁原子。
Ⅲ.消毒处理中常用的消毒剂是
。
②通过如图两个实验可以验证水的组成:
Ⅰ.把水注入图一的水电解器装置中,接通直流电,可以观察到a管中的电极上
,检验b管中产物的方法是
。写出该反应的化学方程式
。
Ⅱ.图二是氢气在氧气中燃烧的实验,实验中使用的氢气需要干燥,其目的是
。
20.(10分)实验室常用的制取气体的发生装置如图,根据如图实验装置回答问题。
①实验室选用气体发生装置的依据是
和
。写出用氯酸钾和二氧化锰制取氧气的化学反应方程式
,其基本反应类型是
。和装置B相比,装置C的优点是
。
②过氧化钠(Na2O2)可在潜水艇中作为制取氧气的来源,它能和二氧化碳反应生成氧气和碳酸钠,配平该反应方程式:
Na2O2+
CO2═
Na2CO3+
O2。
③实验室用含0.1mol过氧化氢的双氧水与二氧化锰混合制取氧气时,完全分解能产生氧气
mol(根据化学方程式列式计算)实验结束后,经过
、洗涤、烘干等操作可回收二氧化锰。
21.(6分)化学兴趣小组同学阅读课外资料得知很多因素都能影响过氧化氢分解速率。于是,他们利用数字化实验手段(如图)对“影响过氧化氢分解速率的因素”进行了探究。
①按下表分组进行实验一,在同一温度下通过压强传感器得到的数据如实验一所示。
实验一
药品
第一组
4%
H2O2溶液15mL
第二组
4%
H2O2溶液15mL、0.2g
MnO2粉末
第三组
4%
H2O2溶液15mL、0.2g
FeCl3粉末
Ⅰ.实验一中设计第一组实验的目的是
。经过分组实验,同学们从实验一中得出结论:在其他条件相同的情况下,
的催化效果最好.
Ⅱ.选用0.2g
MnO2粉末做催化剂,同学们又分别做了实验二和实验三,得到的数据如图,通过分析,影响该反应速率的外界因素除催化剂外,还有
。
Ⅲ.实验一与实验二中4%的过氧化氢溶液与0.2g
MnO2粉末混合后产生的气体压强有明显不同(见图中A点和B点),可能的原因是
。
②实验反思:同学们通过研究讨论,认为还可以研究
对双氧水分解速度的影响。(写出一点即可)
2020-2021学年上海市普陀区九年级(上)期中化学试卷
试题解析
一、选择题(共20分)1-14题只有一个正确选项,15-17题有1-2个正确选项,请将正确选项的代号用2B铅笔填涂在答题纸的相应位置上,更改答案时,用橡皮擦去,重新填涂。
1.【答案】D
【解答】解:A、玻璃破碎没有新物质生成,属于物理变化;故选项错误;
B、蜡烛熔化没有新物质生成,属于物理变化;故选项错误;
C、水的蒸发没有新物质生成,属于物理变化;故选项错误;
D、酒精燃烧生成二氧化碳和水,属于化学变化;故选项正确;
故选:D。
2.【答案】B
【解答】解:A、该物质含有三种元素,不是氧化物,说法错误;
B、该物质是由两种元素组成、其中一种是氧元素的化合物,属于氧化物,说法正确;
C、该物质只含有一种元素,属于单质,说法错误;
D、该物质含有三种元素,不是氧化物,说法错误;
故选:B。
3.【答案】B
【解答】解:A、糖水是蔗糖的水溶液,属于溶液,故选项错误。
B、泥难溶于水,泥水是不溶性的固体小颗粒悬浮于液体中形成的混合物,属于悬浊液,故选项正确。
C、盐水是氯化钠的水溶液,属于溶液,故选项错误。
D、汽水可看作是碳酸的水溶液,属于溶液,故选项错误。
故选:B。
4.【答案】A
【解答】解:A、硫化钾中钾元素显+1价,硫元素显﹣2价,其化学式为:K2S,故选项化学式书写错误。
B、氢氧化钠中钠元素显+1价,氢氧根显﹣1价,其化学式为:NaOH,故选项化学式书写正确。
C、氯化钙中钙元素显+2价,氯元素显﹣1价,其化学式为:CaCl2,故选项化学式书写正确。
D、氧化镁中镁元素显+2价,氧元素显﹣2价,其化学式为:MgO,故选项化学式书写正确。
故选:A。
5.【答案】C
【解答】解:钾元素显+1价,氧元素显﹣2价,设碘元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)+x+(﹣2)×3=0,则x=+5价。
故选:C。
6.【答案】D
【解答】解:A、2个氢分子表示为2H2,说法错误;
B、2个氧原子表示为2O,说法错误;
C、水分子的化学式为H2O,说法错误;
D、+1价的钠元素表示为,说法正确;
故选:D。
7.【答案】A
【解答】解:A、液氮汽化吸热,所以液氮用作冷冻剂,而不是因为氮气难溶于水,故A错误;
B、氧气具有助燃性,所以氧气用作氧炔焰,故B正确;
C、稀有气体通电发出不同颜色的光,所以稀有气体制霓虹灯,故C正确;
D、生石灰能与水反应,所以生石灰用作干燥剂,故D正确。
故选:A。
8.【答案】C
【解答】解:红磷燃烧生成五氧化二磷,反应的化学方程式为:4P+5O22P2O5。
故选:C。
9.【答案】C
【解答】解:A、氢氧化钠溶液与硫酸铜溶液反应生成氢氧化铜蓝色沉淀和硫酸钠,产生蓝色的氢氧化铜沉淀是实验结论而不是实验现象,故选项说法错误。
B、硫在空气中燃烧,产生淡蓝色火焰,故选项说法错误。
C、大理石的主要成分是碳酸钙,碳酸钙与稀盐酸反应生成二氧化碳气体,大理石上滴加稀盐酸,产生大量气泡,故选项说法正确。
D、红磷在空气中燃烧,产生大量的白烟,而不是白雾,故选项说法错误.
故选:C。
10.【答案】B
【解答】解:由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式,反应前氢、硅、氯原子个数分别为4、1、4,反应后的生成物中氢、硅、氯原子个数分别为0、1、4,根据反应前后原子种类、数目不变,则4X分子中含有4个氢原子和4个氯原子,则每个X分子由1个氢原子和1个氯原子构成,则物质X的化学式为HCl。
故选:B。
11.【答案】C
【解答】解:A、NH4NO3从右向左读,读作硝酸铵,故选项说法错误。
B、摩尔质量的单位为g/mol,硝酸铵的摩尔质量是80g/mol,故选项说法错误。
C、由硝酸铵的化学式可知,含有铵根和硝酸根两种原子团,故选项说法正确。
D、硝酸铵(NH4NO3)中铵根显+1价,氢元素显+1价,设铵根中氮元素的化合价是x,由原子团中元素的化合价代数和等于原子团的化合价,可得:x+(+1)×4=+1,则x=﹣3价。硝酸根显﹣1价,氧元素显﹣2价,设硝酸根中氮元素的化合价是y,由原子团中元素的化合价代数和等于原子团的化合价,可得:y+(﹣2)×3=﹣1,则y=+5价。故选项说法错误。
故选:C。
12.【答案】D
【解答】解:A、由化学方程式S+O2SO2,可以确定反应前后反应物(硫和氧气)和生成物(二氧化硫)的种类,故选项说法正确。
B、由化学方程式S+O2SO2,每32份质量的硫和32份质量的氧气在点燃条件下恰好反应生成64份质量的二氧化硫,可以计算出参加反应硫和二氧化硫的质量比,故选项说法正确。
C、由化学方程式S+O2SO2,可以确定反应发生所需要的条件是点燃,故选项说法正确。
D、由化学方程式,无法确定化学反应速率的快慢,故选项说法错误。
故选:D。
13.【答案】A
【解答】解:A、同种分子构成纯净物,不同种分子构成混合物,该选项说法正确;
B、分子的质量和体积不一定比原子大,例如水分子质量小于汞原子质量,该选项说法不正确;
C、化学变化中分子可分,原子不可分,该选项说法不正确;
D、分子个数相等的物质,质量不一定相等,例如1个水分子质量和1个氧分子质量不相等,该选项说法不正确。
故选:A。
14.【答案】D
【解答】解:A、物质的量是一种物理量,其单位是摩尔(mol),而非摩尔是基本物理量之一。错误;
B、1摩尔物质大约含有6.02×1023个该物质的微粒,是大约,而非准确数。错误;
C、物质的量是用来描述微观粒子的数量,与物质的质量完全不同,错误;
D、1mol任何物质的微粒个数约为6.02×1023个,表示一定量数目的微粒的集合体,故正确;
故选:D。
15.【答案】CD
【解答】解:A、取样品,加入二氧化锰,有气泡产生的是双氧水,没有明显现象的是水,现象不同,可以鉴别,故A正确;
B、取样品,观察颜色,无色溶液的是氢氧化钠,蓝色溶液的是硫酸铜,现象不同,可以鉴别,故B正确;
C、氮气和二氧化碳都不具有助燃性,燃着的木条都会熄灭,现象相同,不能鉴别,故C错误;
D、氢氧化钠和澄清石灰水都显碱性,都能使酚酞变红色,现象相同,不能鉴别,故D错误。
故选:CD。
16.【答案】D
【解答】解:由反应的微观示意图可知,该反应是氨气和氧气在点燃时生成了氮气和水,化学方程式为:4NH3+3O22N2+6H2O。
A.在反应前,氧元素存在于氧气这种单质中,在反应后,氧元素存在于水这种化合物中,即化学反应中氧元素从游离态变成化合态,选项说法正确;
B.由化学方程式可知,反应物中的氧气与生成物中的氮气均属于单质,即反应物和生成物中共有两种单质,选项说法正确;
C.由化学方程式可知,该反应中,生成物C(N2)与D(H2O)的物质的量之比为:2:6=1:3,选项说法正确;
D.反应体系中,物质B(O2)与C(N2)的质量比为12:7,选项说法错误。
故选:D。
17.【答案】BC
【解答】解:A、分解反应是一种物质反应后生成两种或两种以上的物质,其特点可总结为“一变多”,生成物是两种或两种以上,故选项说法错误。
B、分解反应的生成物中可能有单质,如水分解生成氢气和氧气,故选项说法正确。
C、分解反应:一种物质反应后生成两种或两种以上的物质,其特点可总结为“一变多”,反应物中只有一种,至少含有两种元素,反应物一定只有一种化合物,故选项说法正确。
D、反应后元素的化合价不一定改变,如碳酸分解生成水和二氧化碳,故选项说法错误。
故选:BC。
二、简答题(共30分)请根据要求在答题纸的相应位置作答。
18.【答案】①氮气;混合物。
②火星四射;3Fe+2O2Fe3O4。
③不易溶于水;剩余的瓶内60%的容积中含有空气,空气中含有氧气。
【解答】解:①根据以上数据分析可知,将空气加压降温至约﹣200℃时,空气变为液态,升温至约﹣196℃时,沸点低的氮气逸出。通过此方法得到的氧气中含有多种物质,是混合物,故填:氮气;混合物。
②铁丝氧气中燃烧的现象是剧烈燃烧,火星四射,并放出大量热。发生反应的化学方程式为:3Fe+2O2Fe3O4;故填:火星四射;3Fe+2O2Fe3O4。
③收集氧气可采用排水集气法,因为氧气具有不易溶于水的性质。欲收集体积分数为40%的氧气,先往集气瓶中注入40%体积的水,该方法得到的氧气体积分数不是40%,是因为剩余的瓶内60%的容积中含有空气,空气中含有氧气,故填:不易溶于水;剩余的瓶内60%的容积中含有空气,空气中含有氧气。
19.【答案】①Ⅰ、明矾;
Ⅱ、3;107g/mol;6.02×1023;
Ⅲ、氯气(合理即可);
②Ⅰ、产生的气泡速率快;打开活塞,将带火星的靠近管口,带火星的木条复燃,说明是氧气;2H2O2H2↑+O2↑;
Ⅱ、验证氢气燃烧生成水。
【解答】解:①Ⅰ、明矾溶于水可以吸附水中的悬浮杂质而加速其沉降,所以絮凝反应处理中会使用净水剂处理微小悬浮物,常用的净水剂有明矾或氯化铁,故填:明矾;
Ⅱ、Fe(OH)3由铁、氢、氧三种元素组成,其摩尔质量为:(56+16×3+1×3)g/mol=107g/mol,1molFe(OH)3中约含有铁原子的个数为:6.02×1023×1=6.02×1023;故填:3;107g/mol;6.02×1023;
Ⅲ、消毒处理中常用的消毒剂是氯气、二氧化氯等;故填:氯气;
②Ⅰ、由图一可知,a管内的气体体积较大,是氢气,b管内的气体体积较小,是氧气,实验中观察到a管中的电极上产生气泡的速率较快,氧气具有助燃性,所以可用带火星的木条来检验,检验方法是打开活塞,将带火星的靠近管口,带火星的木条复燃,说明是氧气;该反应的化学方程式为:2H2O2H2↑+O2↑;故填:产生的气泡速率快;打开活塞,将带火星的靠近管口,带火星的木条复燃,说明是氧气;2H2O2H2↑+O2↑;
Ⅱ、氢气燃烧生成水,所以验证氢气燃烧有水生成时,氢气必须是干燥的,否则无法验证氢气燃烧生成水;故填:验证氢气燃烧生成水。
20.【答案】①反应物状态;反应条件;2KClO32KCl+3O2↑;分解反应;能够控制反应速率。
②2;2;2;1.
③0.05;过滤。
【解答】解:①实验室选用气体发生装置的依据是反应物状态和反应条件;
用氯酸钾和二氧化锰制取氧气的化学反应方程式:2KClO32KCl+3O2↑,其基本反应类型是分解反应;
和装置B相比,装置C的优点是通过分液漏斗能够控制液体药品流量,从而能够控制反应速率。
故填:反应物状态;反应条件;2KClO32KCl+3O2↑;分解反应;能够控制反应速率。
②该反应方程式:2Na2O2+2CO2═2Na2CO3+O2。
故填:2;2;2;1.
③设生成氧气的物质的量为x,
2H2O22H2O+O2↑,
2
1
0.1mol
x
=,
x=0.05mol,
实验结束后,经过过滤、洗涤、烘干等操作可回收二氧化锰。
故填:0.05;过滤。
21.【答案】Ⅰ.进行对比;二氧化锰。
Ⅱ.过氧化氢溶液浓度、温度。
Ⅲ.温度不同。
②催化剂形状。
【解答】解:Ⅰ.实验一中设计第一组实验的目的是进行对比;
经过分组实验,同学们从实验一中得出结论:在其他条件相同的情况下,二氧化锰的催化效果最好,是因为单位时间内利用二氧化锰产生气体比氯化铁多。
故填:进行对比;二氧化锰。
Ⅱ.通过分析,影响该反应速率的外界因素除催化剂外,还有过氧化氢溶液浓度、温度。
故填:过氧化氢溶液浓度、温度。
Ⅲ.实验一与实验二中4%的过氧化氢溶液与0.2g
MnO2粉末混合后产生的气体压强有明显不同(见图中A点和B点),可能的原因是温度不同。
故填:温度不同。
②实验反思:同学们通过研究讨论,认为还可以研究催化剂形状对双氧水分解速度的影响。
故填:催化剂形状。
同课章节目录
