湖北省汉川市官备塘中学2020年九年级化学上册第5单元 课题2 如何正确书写化学方程式 能力提升卷(无答案)
文档属性
| 名称 | 湖北省汉川市官备塘中学2020年九年级化学上册第5单元 课题2 如何正确书写化学方程式 能力提升卷(无答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 104.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-11-14 00:00:00 | ||
图片预览



文档简介
课题2《如何正确书写化学方程式》能力提升卷
1.下列说法正确的是( )
A.原子团在化学反应中,有时是可以拆开的
B.配平化学方程式时,有时可改动化学式中的小字码,但不常用
C.化学方程式配平是为了计算的方便
D.化学方程式中的“↓”表示生成是固体,因此反应中只要有固体生成就必须标示“↓”
2.下列化学方程式书写和配平没有错误或遗漏的是( )
A.2H2O2═2H2O+O2
B.2A1+O3═A12O3
C.S+O2↑SO2↑
D.2KMnO4K2MnO4+MnO2+O2↑
3.下列化学方程式书写正确的是( )
A.4P+5O22P2O5
B.3Fe+2OFe2O3
C.Mg+OMgO2
D.H2OH2↑+O2↑
4.如图是某化学反应的微观示意图。下列说法中正确的是( )
A.丙物质含有3个原子
B.物质乙、丙都属于氧化物
C.该反应前后,原子的种类不变
D.该反应属于化合反应
5.在化学方程式aCu+bHNO3═cCu(NO3)2+dNO↑+eH2O中,各化学式前的化学计量
数之间的关系正确的是( )
A.3b=6c+d
B.2e=b
C.c+d=b
D.d+e=a
三硝酸甘油酯是一种安全性炸药其化学式为C3H5N3O9,是著名的发明家诺贝尔
经过长期的研究与试验发明的.这种炸药发生爆炸的反应方程式为,该反应中x、y分别是( )
A.6
2
B.4
6
C.5
5
D.2
8
7.物质X燃烧的化学方程式为:X+2O2===CO2+2H2O,推求X的化学式为(
)
A、CH4
B、C2H5OH
C、CH3OH
D、CH3COOH
8.在4Cu
+
10HNO3
=
4Cu(NO3)3
+
X+5H2O反应方程式中,X的化学式为(
)
A
NO
B
NO2
C
N2O
D
N2O3
9.下列实验现象的描述与相应化学方程式的书写都正确的是
A.铁丝在空气中剧烈燃烧,火星四射生成黑色固体:3Fe+2O2Fe3O4
B.水受热至沸腾,产生水蒸气.2H2O2H2↑+O2↑
C.硫在氧气中燃烧产生蓝紫色火焰.S
+O2S
O2
D.烤羊肉串时,看到木炭发红光,放出大量的热:C+O2CO2
10.某化学反应前后分子变化的微观示意图如图所示。下列说法不正确的是
A.该反应在反应前后分子的数目没有变化
B.反应的本质是原子的重新组合过程
C.示意图中的各物质均属于化合物
D.该图示表示的化学方程式为CH4+2O22H2O+CO2
11.下列应用及相应的原理(用化学方程式表示)都正确的是(
)
A.测定空气中氧气含量:4Fe+3O22Fe2O3
B.用二氧化碳做碳酸饮料:CO2+H2O=H2CO3
C.实验室用过氧化氢溶液制取氧气:2H2O2=H2O+O2↑
D.田径运动会上用红磷做发令枪的弹药:S+O2SO2
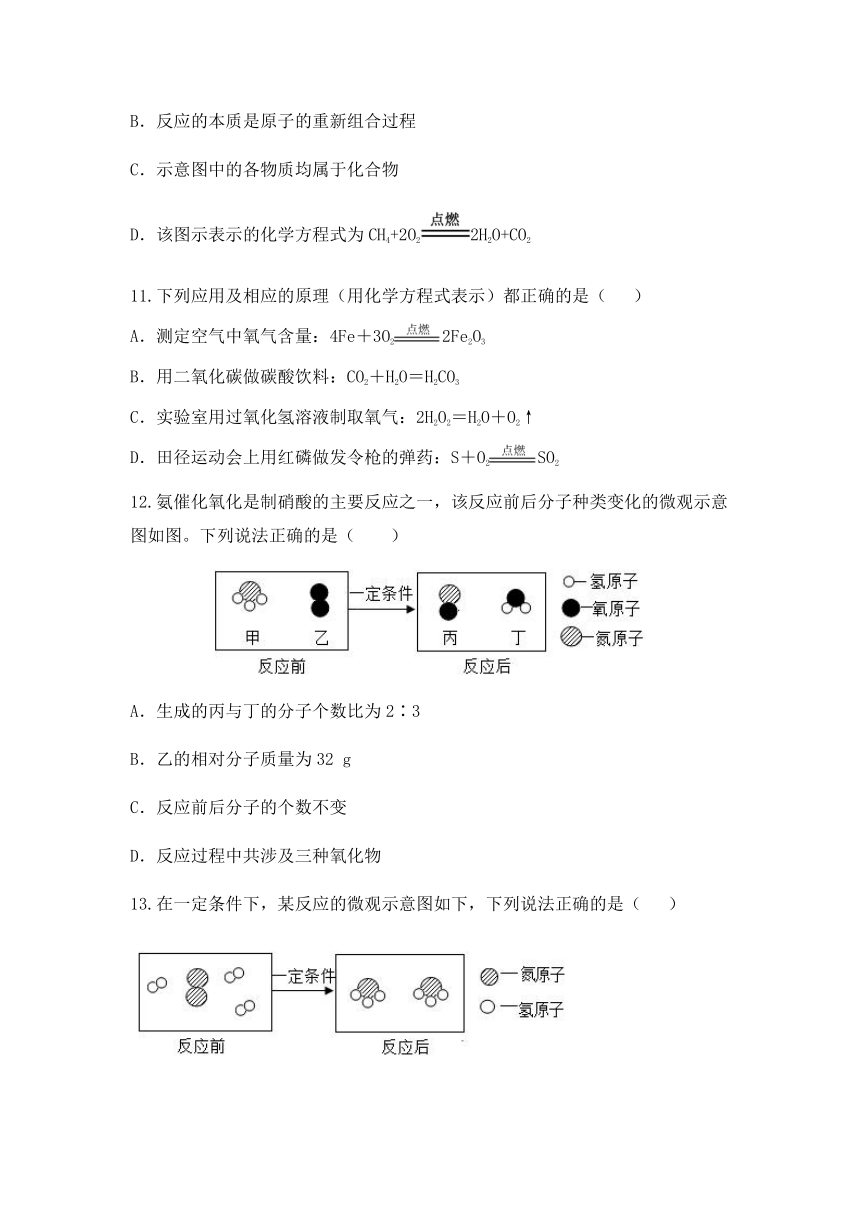
12.氨催化氧化是制硝酸的主要反应之一,该反应前后分子种类变化的微观示意图如图。下列说法正确的是(
)
A.生成的丙与丁的分子个数比为2∶3
B.乙的相对分子质量为32
g
C.反应前后分子的个数不变
D.反应过程中共涉及三种氧化物
13.在一定条件下,某反应的微观示意图如下,下列说法正确的是(
)
A.该反应属于分解反应
B.反应前后各元素的化合价都未发生改变
C.反应前后分子的种类和个数没变
D.该反应的化学方程式为:
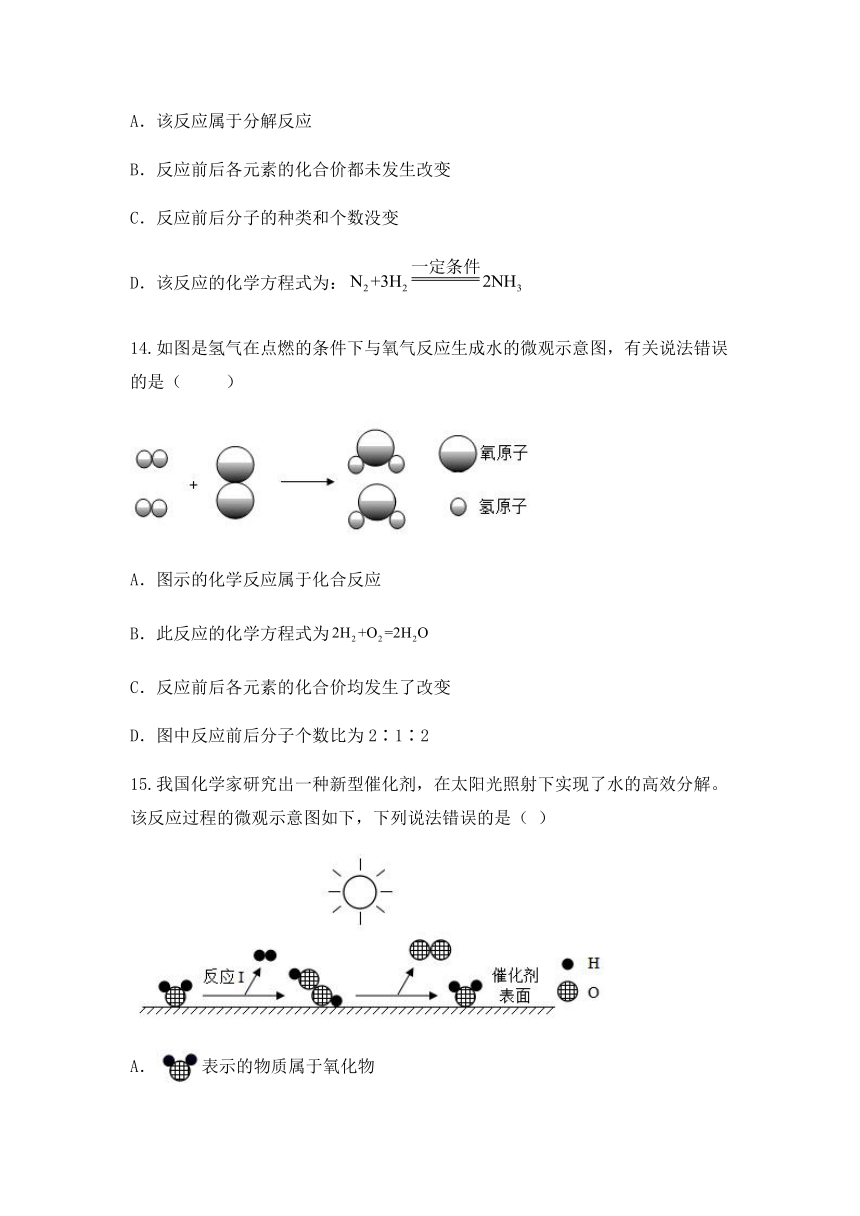
14.如图是氢气在点燃的条件下与氧气反应生成水的微观示意图,有关说法错误的是(
)
A.图示的化学反应属于化合反应
B.此反应的化学方程式为
C.反应前后各元素的化合价均发生了改变
D.图中反应前后分子个数比为2∶1∶2
15.我国化学家研究出一种新型催化剂,在太阳光照射下实现了水的高效分解。该反应过程的微观示意图如下,下列说法错误的是(
)
A.表示的物质属于氧化物
B.反应I
的化学方程式为
C.反应II
中,反应前后原子的种类和数目均不变
D.该成果对氢能源的推广应用有重要的实践意义
16.书写化学方程式应遵循两个原则,填写下面两个化学方程式错误的原因。
(1)Cu+O2CuO2违背了___________________________。
(2)H2OH2↑+O2
↑违背了___________________________。
17.用化学符号填空:
(1)氢元素:
。
(2)3个二氧化硫分子:
。
(3)二氧化碳:
。
(4)2个氧原子:
。
(5)带2个单位正电荷的钙离子:
。
(6)带1个单位负电荷的氢氧根离子:
。
(7)带3个单位正电荷的铝离子:
。
(8)带1个单位正电荷的铵根离子:
。
18.配平下列化学方程式:
(1)
C2H4
+
O2
——__CO2
+
H2O
(2)
Al
+
H2SO4
——
Al
2(SO4)3
+
H2
(3)
NH3+
O2
——
NO+
H2O
(4)
KClO3——
KCl+
O2
H2O+
C——
CO+
H2
MnO2+
HCl——
MnCl2+
H2O+
Cl2
H2S+
SO2——
H2O+
S
H2S+
O2——
H2O+
SO2
Al2O3+
H2SO4——
Al2(SO4)3+
H2O
Na+
H2O——___NaOH+___H2
19.配平下列化学方程式
(1)
A1+
Fe2O3﹣﹣
Fe+
A12O3
(2)
C3H6
+
O2
CO2
+
H2O
(3)
Al+
HCl﹣﹣
AlCl3
+
H2↑
(4)
NH3
+
O2
NO+
H2O
(5)
Fe2O3
+
CO
Fe+
CO2
20.配平下列化学方程式。
(1)______H2O2______H2O+______O2↑
(2)______Fe+______O2______Fe3O4
(3)______C6H6+______O2______CO2+______H2O
(4)______Fe+______CuSO4______Cu+______FeSO4[
(5)______H2O______H2↑+______O2↑
(6)______Fe2O3
+______CO______Fe
+
______CO2
(7)______C2H5OH+______O2______CO2
+______H2O
21.配平下列化学方程式:
(1)_____CO+____Fe3O4____Fe+____CO2
(2)____CH3OH+____O2____CO2+____H2O
(3)____Al+____HCl____AlCl3+____
H2↑
(4)_____C3H8+____O2_____CO2+
____H2O;
(5)____Mg+____
N2_______Mg3N2
;
(6)____FeS+_____O2____Fe2O3+
_____SO2
。
22.写出下列化学方程式
(1)木炭在空气中燃烧:____________________________________;
(2)硫在空气中燃烧:_______________________________________;
(3)红磷在空气中燃烧:____________________________________;
(4)铁丝在氧气中燃烧:____________________________________;
(5)氢气在空气中燃烧:
__________________________________;
(6)镁条在空气中燃烧:___________________________________;
(7)水通电分解:_________________________________________;
(8)氯酸钾和二氧化锰共热制氧气:________________________;
(9)高锰酸钾制氧气:_____________________________________;
(19)过氧化氢制氧气:____________________________________。
补充训练
一、化学方程式的配平
01.[
]Fe3O4+[
]CO=[
]Fe+[
]CO2
02.[
]I2O5+[
]CO=[
]I2+[
]CO2
03.[
]WO3+[
]CO=[
]W+[
]CO2
04.[
]C+[
]Fe2O3=[
]Fe+[
]CO2
05.[
]C+[
]Fe3O4=[
]Fe+[
]CO2
06.[
]H2+[
]Fe2O3=[
]Fe+[
]H2O
07.[
]H2+[
]Fe3O4=[
]Fe+[
]H2O
08.[
]H2+[
]WO3=[
]W+[
]H2O
09.[
]CO+[
]FexOy=[
]Fe+[
]CO2
10.[
]C+[
]FexOy=[
]Fe+[
]CO2
11.[
]H2+[
]FexOy=[
]Fe+[
]H2O
12.[
]Fe+[
]H2O=[
]Fe3O4+[
]H2
13.[
]Al+[
]H2SO4=[
]Al2(SO4)3+[
]H2
14.[
]Fe2O3+[
]HCl=[
]FeCl3+[
]H2O
15.[
]FeO+[
]HCl=[
]FeCl2+[
]H2O
16.[
]NaOH+[
]CO2=[
]Na2CO3+[
]H2O
17.[
]NaOH+[
]SO2=[
]Na2SO3+[
]H2O
18.[
]KOH+[
]CO2=[
]K2CO3+[
]H2O
19.[
]Al(OH)3+[
]HCl=[
]AlCl3+[
]H2O
20.[
]C4H10+[
]O2=[
]CO2+[
]H2O
21.[
]C2H6+[
]O2=[
]CO2+[
]H2O
22.[
]C2H2+[
]O2=[
]CO2+[
]H2O
23.[
]C3H8+[
]O2=[
]CO2+[
]H2O
24.[
]FeS2+[
]O2=[
]Fe2O3+[
]SO2
25.[
]H2O=[
]
O2+[
]H2
26.[
]Si+[
]Cl2=[
]SiCl4
27.[
]MnO2+[
]HCl=[
]MnCl2+[
]Cl2+[
]H2O
28.[
]Cl2+[
]Ca(OH)2=[
]CaCl2+[
]Ca(ClO)2+[
]H2O
二、化学方程式的书写
1.发射卫星的火箭用联氨【N2H4】作燃料,以四氧化二氮【N2O4】作氧化剂,燃烧尾气由氮气和水蒸气组成。试写出反应的化学方程式:_________________________________。
2.用粮食作原料酿酒时,往往发现制得的酒发酸,这实际上是因为酒精【C2H5OH】在酶的作用下与空气中的氧气作用,生成了醋酸【CH3COOH】和水。
请写出该反应的化学方程式:_____________________________________________。
3.工业上常用接触法制硫酸,所使用的原料是硫铁矿【FeS】。在高温下,将硫铁矿的粉末与氧气充分反应生成三氧化二铁和二氧化硫,再经过一系列转化可生成硫酸。试写出硫铁矿与氧气反应的化学方程式:_________________________________。
4.壁画颜料中的铅白【Pb2(OH)2CO3】由于受到空气中硫化氢气体的作用而变成黑色硫化铅【PbS】,影响画面的色泽。当用双氧水处理时就可以使黑色的硫化铅氧化成白色硫酸铅【PbSO4】和水。
试写出双氧水处理硫化铅的化学方程式:_________________________________。
5.哥伦比亚号航天飞机曾用金属铝和高氯酸铵【NH4ClO4】的混合物作为固体燃料。加热铝粉使其被氧气氧化,放出大量的热,促使混合物中的高氯酸铵受热分解,同时生成四种气体:两种气体是空气中的主要成分,一种气体是Cl2,还有一种气体是化合物(常温下是液态),因而产生巨大的推动力。
试写出其中涉及的化学方程式:
(1)铝粉被氧气氧化成三氧化二铝:_______________________________。
(2)高氯酸铵受热分解:_______________________________。
6.在通常情况下,碳单质的化学性质稳定,但在常温下石墨可与一种叫高氯酸【HClO4】的物质发生反应,产物除水是液体外,其余都是气体,一种是有毒的氯气,一种是无色无毒的化合物。
请写出此反应的化学方程式:_____________________________。
7.砷化氢AsH3是一种很强的还原剂,在室温下它能在空气中自燃,其氧化产物是砒霜【As2O3】。
写出该反应的化学方程式:_______________________________。
8.将黑色氧化铜粉末装入试管中加热,通入氨气则生成红色的铜,水和一种气体单质。
该反应的化学方程式:_______________________________。
9.镁是一种很活泼的金属。点燃后,它不仅能和氧气发生反应,而且能在氮气和二氧化碳中燃烧。已知镁在氮气中燃烧会化合成一种新物质,其中氮元素的化合价为﹣3价。在二氧化碳中燃烧会生成一种白色固体和一种黑色固体。
试写出这两个反应的化学方程式。
(1)在氮气中燃烧:___________________________________;
(2)在二氧化碳中燃烧:_______________________________。
10.河水里的微生物使有机物【以C6H10O5表示】转化为二氧化碳和水的过程中所需要的氧气量叫做生化需氧量。
试写出该反应的化学方程式:_____________________________。
11.CaCO3在高温条件下分解的化学方程式为:CaCO3CaO+CO2↑。碳酸锂(其中锂为﹢1价)是手机中锂电池的主要成份,它在高温下分解的反应与碳酸钙相似。
试写出碳酸锂分解的化学反应方程式:_____________________________________。
12.过氧乙酸【C2H4O3】是人们广泛使用的消毒剂,它无色且有辛辣味,具有强氧化性,温度稍高即分解放出氧气,同时生成醋酸【C2H4O2】。
试写出过氧乙酸分解的化学方程式:_______________________________________。
13.根据下列反应事实写出相应的化学方程式。
(1)双氧水在二氧化锰的催化作用下生成水和氧气:______________________________________。
(2)在尘埃的作用下,二氧化硫和氧气反应生成三氧化硫(SO3):___________________________。
(3)Cu和AgNO3溶液反应,生成Cu(NO3)2溶液和Ag:__________________________________。
(4)少量CuSO4溶液滴入NaOH稀溶液中生成Cu(OH)2沉淀和Na2SO4溶液:___________________。
(5)一氧化碳和四氧化三铁(Fe3O4)在高温下反应,生成铁和二氧化碳:_________________________。
1.下列说法正确的是( )
A.原子团在化学反应中,有时是可以拆开的
B.配平化学方程式时,有时可改动化学式中的小字码,但不常用
C.化学方程式配平是为了计算的方便
D.化学方程式中的“↓”表示生成是固体,因此反应中只要有固体生成就必须标示“↓”
2.下列化学方程式书写和配平没有错误或遗漏的是( )
A.2H2O2═2H2O+O2
B.2A1+O3═A12O3
C.S+O2↑SO2↑
D.2KMnO4K2MnO4+MnO2+O2↑
3.下列化学方程式书写正确的是( )
A.4P+5O22P2O5
B.3Fe+2OFe2O3
C.Mg+OMgO2
D.H2OH2↑+O2↑
4.如图是某化学反应的微观示意图。下列说法中正确的是( )
A.丙物质含有3个原子
B.物质乙、丙都属于氧化物
C.该反应前后,原子的种类不变
D.该反应属于化合反应
5.在化学方程式aCu+bHNO3═cCu(NO3)2+dNO↑+eH2O中,各化学式前的化学计量
数之间的关系正确的是( )
A.3b=6c+d
B.2e=b
C.c+d=b
D.d+e=a
三硝酸甘油酯是一种安全性炸药其化学式为C3H5N3O9,是著名的发明家诺贝尔
经过长期的研究与试验发明的.这种炸药发生爆炸的反应方程式为,该反应中x、y分别是( )
A.6
2
B.4
6
C.5
5
D.2
8
7.物质X燃烧的化学方程式为:X+2O2===CO2+2H2O,推求X的化学式为(
)
A、CH4
B、C2H5OH
C、CH3OH
D、CH3COOH
8.在4Cu
+
10HNO3
=
4Cu(NO3)3
+
X+5H2O反应方程式中,X的化学式为(
)
A
NO
B
NO2
C
N2O
D
N2O3
9.下列实验现象的描述与相应化学方程式的书写都正确的是
A.铁丝在空气中剧烈燃烧,火星四射生成黑色固体:3Fe+2O2Fe3O4
B.水受热至沸腾,产生水蒸气.2H2O2H2↑+O2↑
C.硫在氧气中燃烧产生蓝紫色火焰.S
+O2S
O2
D.烤羊肉串时,看到木炭发红光,放出大量的热:C+O2CO2
10.某化学反应前后分子变化的微观示意图如图所示。下列说法不正确的是
A.该反应在反应前后分子的数目没有变化
B.反应的本质是原子的重新组合过程
C.示意图中的各物质均属于化合物
D.该图示表示的化学方程式为CH4+2O22H2O+CO2
11.下列应用及相应的原理(用化学方程式表示)都正确的是(
)
A.测定空气中氧气含量:4Fe+3O22Fe2O3
B.用二氧化碳做碳酸饮料:CO2+H2O=H2CO3
C.实验室用过氧化氢溶液制取氧气:2H2O2=H2O+O2↑
D.田径运动会上用红磷做发令枪的弹药:S+O2SO2
12.氨催化氧化是制硝酸的主要反应之一,该反应前后分子种类变化的微观示意图如图。下列说法正确的是(
)
A.生成的丙与丁的分子个数比为2∶3
B.乙的相对分子质量为32
g
C.反应前后分子的个数不变
D.反应过程中共涉及三种氧化物
13.在一定条件下,某反应的微观示意图如下,下列说法正确的是(
)
A.该反应属于分解反应
B.反应前后各元素的化合价都未发生改变
C.反应前后分子的种类和个数没变
D.该反应的化学方程式为:
14.如图是氢气在点燃的条件下与氧气反应生成水的微观示意图,有关说法错误的是(
)
A.图示的化学反应属于化合反应
B.此反应的化学方程式为
C.反应前后各元素的化合价均发生了改变
D.图中反应前后分子个数比为2∶1∶2
15.我国化学家研究出一种新型催化剂,在太阳光照射下实现了水的高效分解。该反应过程的微观示意图如下,下列说法错误的是(
)
A.表示的物质属于氧化物
B.反应I
的化学方程式为
C.反应II
中,反应前后原子的种类和数目均不变
D.该成果对氢能源的推广应用有重要的实践意义
16.书写化学方程式应遵循两个原则,填写下面两个化学方程式错误的原因。
(1)Cu+O2CuO2违背了___________________________。
(2)H2OH2↑+O2
↑违背了___________________________。
17.用化学符号填空:
(1)氢元素:
。
(2)3个二氧化硫分子:
。
(3)二氧化碳:
。
(4)2个氧原子:
。
(5)带2个单位正电荷的钙离子:
。
(6)带1个单位负电荷的氢氧根离子:
。
(7)带3个单位正电荷的铝离子:
。
(8)带1个单位正电荷的铵根离子:
。
18.配平下列化学方程式:
(1)
C2H4
+
O2
——__CO2
+
H2O
(2)
Al
+
H2SO4
——
Al
2(SO4)3
+
H2
(3)
NH3+
O2
——
NO+
H2O
(4)
KClO3——
KCl+
O2
H2O+
C——
CO+
H2
MnO2+
HCl——
MnCl2+
H2O+
Cl2
H2S+
SO2——
H2O+
S
H2S+
O2——
H2O+
SO2
Al2O3+
H2SO4——
Al2(SO4)3+
H2O
Na+
H2O——___NaOH+___H2
19.配平下列化学方程式
(1)
A1+
Fe2O3﹣﹣
Fe+
A12O3
(2)
C3H6
+
O2
CO2
+
H2O
(3)
Al+
HCl﹣﹣
AlCl3
+
H2↑
(4)
NH3
+
O2
NO+
H2O
(5)
Fe2O3
+
CO
Fe+
CO2
20.配平下列化学方程式。
(1)______H2O2______H2O+______O2↑
(2)______Fe+______O2______Fe3O4
(3)______C6H6+______O2______CO2+______H2O
(4)______Fe+______CuSO4______Cu+______FeSO4[
(5)______H2O______H2↑+______O2↑
(6)______Fe2O3
+______CO______Fe
+
______CO2
(7)______C2H5OH+______O2______CO2
+______H2O
21.配平下列化学方程式:
(1)_____CO+____Fe3O4____Fe+____CO2
(2)____CH3OH+____O2____CO2+____H2O
(3)____Al+____HCl____AlCl3+____
H2↑
(4)_____C3H8+____O2_____CO2+
____H2O;
(5)____Mg+____
N2_______Mg3N2
;
(6)____FeS+_____O2____Fe2O3+
_____SO2
。
22.写出下列化学方程式
(1)木炭在空气中燃烧:____________________________________;
(2)硫在空气中燃烧:_______________________________________;
(3)红磷在空气中燃烧:____________________________________;
(4)铁丝在氧气中燃烧:____________________________________;
(5)氢气在空气中燃烧:
__________________________________;
(6)镁条在空气中燃烧:___________________________________;
(7)水通电分解:_________________________________________;
(8)氯酸钾和二氧化锰共热制氧气:________________________;
(9)高锰酸钾制氧气:_____________________________________;
(19)过氧化氢制氧气:____________________________________。
补充训练
一、化学方程式的配平
01.[
]Fe3O4+[
]CO=[
]Fe+[
]CO2
02.[
]I2O5+[
]CO=[
]I2+[
]CO2
03.[
]WO3+[
]CO=[
]W+[
]CO2
04.[
]C+[
]Fe2O3=[
]Fe+[
]CO2
05.[
]C+[
]Fe3O4=[
]Fe+[
]CO2
06.[
]H2+[
]Fe2O3=[
]Fe+[
]H2O
07.[
]H2+[
]Fe3O4=[
]Fe+[
]H2O
08.[
]H2+[
]WO3=[
]W+[
]H2O
09.[
]CO+[
]FexOy=[
]Fe+[
]CO2
10.[
]C+[
]FexOy=[
]Fe+[
]CO2
11.[
]H2+[
]FexOy=[
]Fe+[
]H2O
12.[
]Fe+[
]H2O=[
]Fe3O4+[
]H2
13.[
]Al+[
]H2SO4=[
]Al2(SO4)3+[
]H2
14.[
]Fe2O3+[
]HCl=[
]FeCl3+[
]H2O
15.[
]FeO+[
]HCl=[
]FeCl2+[
]H2O
16.[
]NaOH+[
]CO2=[
]Na2CO3+[
]H2O
17.[
]NaOH+[
]SO2=[
]Na2SO3+[
]H2O
18.[
]KOH+[
]CO2=[
]K2CO3+[
]H2O
19.[
]Al(OH)3+[
]HCl=[
]AlCl3+[
]H2O
20.[
]C4H10+[
]O2=[
]CO2+[
]H2O
21.[
]C2H6+[
]O2=[
]CO2+[
]H2O
22.[
]C2H2+[
]O2=[
]CO2+[
]H2O
23.[
]C3H8+[
]O2=[
]CO2+[
]H2O
24.[
]FeS2+[
]O2=[
]Fe2O3+[
]SO2
25.[
]H2O=[
]
O2+[
]H2
26.[
]Si+[
]Cl2=[
]SiCl4
27.[
]MnO2+[
]HCl=[
]MnCl2+[
]Cl2+[
]H2O
28.[
]Cl2+[
]Ca(OH)2=[
]CaCl2+[
]Ca(ClO)2+[
]H2O
二、化学方程式的书写
1.发射卫星的火箭用联氨【N2H4】作燃料,以四氧化二氮【N2O4】作氧化剂,燃烧尾气由氮气和水蒸气组成。试写出反应的化学方程式:_________________________________。
2.用粮食作原料酿酒时,往往发现制得的酒发酸,这实际上是因为酒精【C2H5OH】在酶的作用下与空气中的氧气作用,生成了醋酸【CH3COOH】和水。
请写出该反应的化学方程式:_____________________________________________。
3.工业上常用接触法制硫酸,所使用的原料是硫铁矿【FeS】。在高温下,将硫铁矿的粉末与氧气充分反应生成三氧化二铁和二氧化硫,再经过一系列转化可生成硫酸。试写出硫铁矿与氧气反应的化学方程式:_________________________________。
4.壁画颜料中的铅白【Pb2(OH)2CO3】由于受到空气中硫化氢气体的作用而变成黑色硫化铅【PbS】,影响画面的色泽。当用双氧水处理时就可以使黑色的硫化铅氧化成白色硫酸铅【PbSO4】和水。
试写出双氧水处理硫化铅的化学方程式:_________________________________。
5.哥伦比亚号航天飞机曾用金属铝和高氯酸铵【NH4ClO4】的混合物作为固体燃料。加热铝粉使其被氧气氧化,放出大量的热,促使混合物中的高氯酸铵受热分解,同时生成四种气体:两种气体是空气中的主要成分,一种气体是Cl2,还有一种气体是化合物(常温下是液态),因而产生巨大的推动力。
试写出其中涉及的化学方程式:
(1)铝粉被氧气氧化成三氧化二铝:_______________________________。
(2)高氯酸铵受热分解:_______________________________。
6.在通常情况下,碳单质的化学性质稳定,但在常温下石墨可与一种叫高氯酸【HClO4】的物质发生反应,产物除水是液体外,其余都是气体,一种是有毒的氯气,一种是无色无毒的化合物。
请写出此反应的化学方程式:_____________________________。
7.砷化氢AsH3是一种很强的还原剂,在室温下它能在空气中自燃,其氧化产物是砒霜【As2O3】。
写出该反应的化学方程式:_______________________________。
8.将黑色氧化铜粉末装入试管中加热,通入氨气则生成红色的铜,水和一种气体单质。
该反应的化学方程式:_______________________________。
9.镁是一种很活泼的金属。点燃后,它不仅能和氧气发生反应,而且能在氮气和二氧化碳中燃烧。已知镁在氮气中燃烧会化合成一种新物质,其中氮元素的化合价为﹣3价。在二氧化碳中燃烧会生成一种白色固体和一种黑色固体。
试写出这两个反应的化学方程式。
(1)在氮气中燃烧:___________________________________;
(2)在二氧化碳中燃烧:_______________________________。
10.河水里的微生物使有机物【以C6H10O5表示】转化为二氧化碳和水的过程中所需要的氧气量叫做生化需氧量。
试写出该反应的化学方程式:_____________________________。
11.CaCO3在高温条件下分解的化学方程式为:CaCO3CaO+CO2↑。碳酸锂(其中锂为﹢1价)是手机中锂电池的主要成份,它在高温下分解的反应与碳酸钙相似。
试写出碳酸锂分解的化学反应方程式:_____________________________________。
12.过氧乙酸【C2H4O3】是人们广泛使用的消毒剂,它无色且有辛辣味,具有强氧化性,温度稍高即分解放出氧气,同时生成醋酸【C2H4O2】。
试写出过氧乙酸分解的化学方程式:_______________________________________。
13.根据下列反应事实写出相应的化学方程式。
(1)双氧水在二氧化锰的催化作用下生成水和氧气:______________________________________。
(2)在尘埃的作用下,二氧化硫和氧气反应生成三氧化硫(SO3):___________________________。
(3)Cu和AgNO3溶液反应,生成Cu(NO3)2溶液和Ag:__________________________________。
(4)少量CuSO4溶液滴入NaOH稀溶液中生成Cu(OH)2沉淀和Na2SO4溶液:___________________。
(5)一氧化碳和四氧化三铁(Fe3O4)在高温下反应,生成铁和二氧化碳:_________________________。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
