安徽省合肥第六高中2020-2021学年高二上学期期中考试化学试题 PDF版含答案
文档属性
| 名称 | 安徽省合肥第六高中2020-2021学年高二上学期期中考试化学试题 PDF版含答案 |

|
|
| 格式 | |||
| 文件大小 | 784.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-11-16 00:00:00 | ||
图片预览



文档简介
C. 2-丁 醇
2 019 级 高二 上学 期化 学期 中考试
D. 2-甲基-3-丁炔
化 学试 题
.用 CH4催化 还原 NOx可以 消除 氮氧 化物 的污 染。 例如 :
(分值: 100 分 时长:90 分钟 ) 4
1
① CH4(g)+4NO2(g) 4NO(g)+CO2(g)+2H2O(g) ΔH=?574 kJ· mol?
可 能 用 到的 原 子 量 :H-1 C-12 O-16 S-32
1
② CH4(g)+4NO(g) 2N2(g)+CO2(g)+2H2O(g) ΔH=?1 160 kJ· mol?
一 .选 择 题 (每 小 题3分 , 共48分 )
下列 说法 不正 确的 是 ( )
1. 化学 与人类 生产 生活 及健 康 密切 相关 ,下 列说 法正 确的 是( )
1
A. 由反 应① 可推 知: CH4(g)+4NO2(g) 4NO(g)+CO2(g)+2H2O(l) ΔH=?Q,Q>574 kJ· mol?
A.新型 冠状 病毒 由C、H、O三种 元素 组成 B.等物 质的 量的 甲烷 分别 参加 反应 ① 、② ,反 应转 移的 电子 数不 同
B. 变质 的油 脂有 难闻 的特 殊气 味, 是由 于油 脂发 生了 水解 反应 C.若用 4.48 L (已 折算 成标准 状况 下体 积 )CH4还原 NO2至 N2,则 放出 的热 量为 173.4 kJ
C. 浸泡 过高 锰酸 钾溶 液的 硅藻 土放 于水 果箱 内是 为了 延长 水果 保鲜 期 D. 若用 4.48 L (已 折算 成标准 状况 下体 积 )CH4还原 NO2至 N2,则 整个 过程 中转 移的 电子 总物 质的 量
D.84消毒 液是 以NaClO为主 要有 效成 分的 消毒 液, 与医 用酒 精混 合可 以提 升消 毒效 果
为 1.6 mol
2.下列 说法 或表 示方 法不 正确 的是( ) 5.某有 机物A是农 药生 产中 的一 种中 间体 ,其 结构 简式 如图 ,下 列叙 述 错误 的是 ( )
A.盖斯 定律 实质 上是 能量 守恒 定律 的体 现
+ - -
B.在稀 溶液 中:H (aq)+OH (aq)=H2O(l) ΔH=-57.3 kJ ·mol 1,含0.5 mol H2SO4的浓 硫酸 与含1 mol
NaOH的溶 液混 合, 放出 的热 量大 于57.3 kJ
C. 由C(石墨 ,s)=== C(金刚 石,s) Δ H>0,可 知, 石墨 比金 刚石 稳定
- - A. 有机 物A属于 芳香 族化 合物
D.H2(g)的燃 烧热ΔH=-285.8 kJ ·mol 1,则2H2O(l)= ==2H2(g)+O2(g) ΔH=285.8 kJ ·mol 1
B.有机 物A不 可以 和Br2的CCl4溶液 发生 加成 反应
3.下 列有 机物 命名 错误 的是 ( )
C.有机 物A和浓 硫酸 混合 加热 ,可 以发 生消 去反 应
A. 1,2,4-三甲 苯 D.1mol A和足 量的NaOH溶液 反应 ,最 多可 以消 耗3mol NaOH
5 ?1
6.在298K、1.01 10 P a? 下 ,将32g S O2通入750mL 1mol L? 的KOH溶液 中充 分反 应 ,测得 反应
?
放出 1
xkJ的热 量 。已知 在该 条件 下 ,1 mo l S O 通入1L 2mol L? 的KOH溶液 中充 分反 应放 出yk J的
B. 2-甲基-2-氯丙 烷 2
热量 。则S O2与KOH溶液 反应 生成KHS O3的热 化学 方程 式正 确的 是( )
?1
A.SO g KOH aq KHSO aq2? ? ? ? ? ?? ? 3 , ? ? ? ? ?H x y? ?4 kJ mol
高二年级化学试卷 第1页 共12页 高二年级化学试卷 第2页 共12页
?1
B. A.物质 的二 氯代 物有 种
SO g KOH aq KHSO aq2? ? ? ? ? ?? ? 3 ,? ? ? ? ?H x y? ?2 kJ mol d 6
. 物质 的分 子式 为
?1 B b C10H12
C.SO g KOH aq KHSO aq2? ? ? ? ? ?? ? 3 ,? ? ? ? ?H y x? ?2 kJ mol
C. 物质c与物 质d互为 同分 异构 体
?1
D.SO g KOH aq KHSO aq2? ? ? ? ? ?? ? 3 ,? ? ? ? ?H x y? ?8 2 kJ mol D.a最多 有10个原 子共 平面
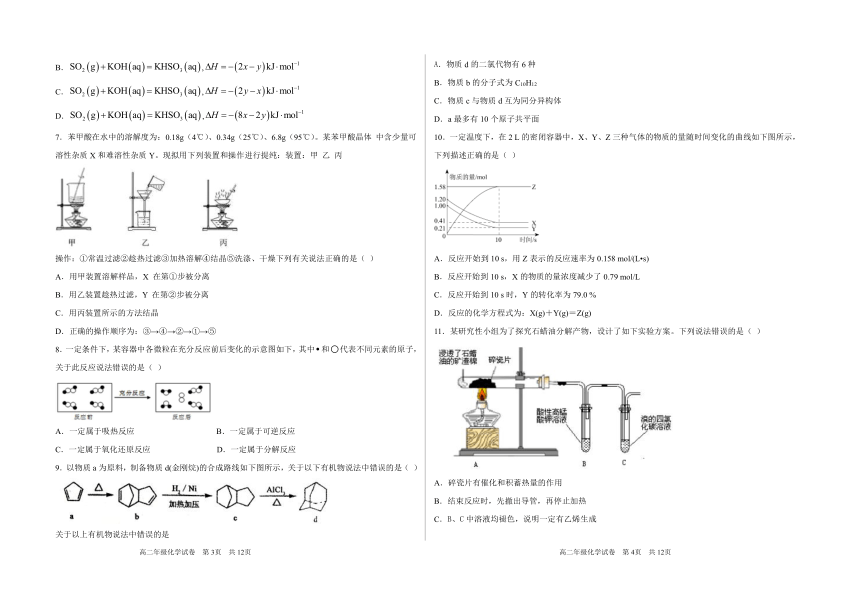
7.苯甲 酸在 水中 的溶 解度 为:0.18g(4℃)、0.34g(25℃)、6.8g(95℃ )。某 苯甲 酸晶 体 中含 少量 可 10.一定 温度 下,在2 L的密 闭容 器中 ,X、Y、Z三种 气体 的物 质的 量随 时间 变化 的曲 线如 下图 所示 ,
溶性 杂质X和难 溶性 杂质Y。现 拟用 下列 装置 和操 作进 行提 纯: 装置 : 甲 乙 丙 下列 描述 正确 的是 ( )
操作 :① 常温 过滤 ②趁热 过滤 ③ 加热 溶解 ④结晶 ⑤ 洗涤 、干 燥下 列有 关说 法正 确的 是( ) A. 反应 开始 到10 s,用Z表示 的反 应速 率为0.158 mol/(L ?s)
A.用甲 装置 溶解 样品 ,X 在第 ①步被 分离 B. 反应 开始 到10 s,X的物 质的 量浓 度减 少了0.79 mol/L
B. 用乙 装置 趁热 过滤 ,Y 在第 ② 步被 分离 C. 反应 开始 到10 s时,Y的转 化率 为79.0 %
C. 用丙 装置 所示 的方 法结 晶 D. 反应 的化 学方 程式 为:X(g)+Y(g)=Z(g)
D.正确 的操 作顺 序为 : ③→④→②→①→⑤ 11. 某研 究性 小组 为了 探究 石蜡 油分 解产 物, 设计 了如 下实 验方 案。 下列 说法 错误 的是 ( )
8.一定 条件 下,某容 器中 各微 粒在 充分 反应 前后 变化 的示 意图 如下 ,其中?和?代表 不同 元素 的原 子,
关于 此反 应说 法错 误的 是( )
A.一定 属于 吸热 反应 B.一定 属于 可逆 反应
C. 一定 属于 氧化 还原 反应 D. 一定 属于 分解 反应
9.以物 质a为原 料,制备 物质d(金刚 烷)的合 成路 线如 下图 所示 ,关于 以下 有机 物说 法中 错误 的是( )
A. 碎瓷 片有 催化 和积 蓄热 量的 作用
B. 结束 反应 时, 先撤 出导 管, 再停 止加 热
C. B、C 中溶 液均 褪色 ,说明 一定 有乙 烯生 成
关于 以上 有机 物说 法中 错误 的是
高二年级化学试卷 第3页 共12页 高二年级化学试卷 第4页 共12页
D.石蜡 油是 液态 烷烃 v(KMnO4)=2.5×10-4mol·L-1·s-1
-1
12. 一定 温度 下, 向 10 mL 0.40 mol· L H2O2溶液 中加 入适 量 FeCl3溶液 ,不 同时 刻测 得生 成 O2的体 14.最新 报道 :科学 家首 次用 X 射线 激光 技术 观察 到 CO 与 O 在催 化剂 表面 形成 化学 键的 过程 .反应 过
积( 已折 算为 标准 状况 )如 下左 表所 示。 程的 示意 图如 下 ,下列 说法 正确 的是 ( )
t/ min 0 2 4 6
V(O2) / mL 0 9.9 17.2 22.4
3+ 2+ + 2+ + 3+
资料 显示 ,反应 分两 步进 行:① 2Fe +H2O2=2Fe +O2↑+2H② H2O2+2Fe +2H = 2H2O+2Fe ,反应 过程 中能
量变 化如 上右 图所 示。 下列 说法 不正 确的 是( ) A. CO 和 O 生成 CO2是吸 热反 应
-2 -1 -1
A.0~ 6 min 的平 均反 应速 率:v(H2O2)=3.33×10 mol·L · min B.在该 过程 中, CO 断键 形成 C 和 O
3+
B. Fe 的作 用是 增大 过氧 化氢 的分 解速 率 C.同物 质的 量的 CO 和 O 反应 比 CO 与 O2反应 放出 更多 热量
C. 反应 ①是吸 热反 应、 反应 ② 是放 热反 应 D. 状态 Ⅰ→ 状态 Ⅲ表示 CO 与 O2反应 的过 程
D.反应 2H2O2(aq)= 2H2O(l)+O2(g)的△H=E1-E2<0 15.一定 条件 下, 在水 溶液 中1molC l-、ClOx-(x= 1,2,3,4)的能 量(kJ)相对 大小 如图 所示 。下 列有 关
13. 以反 应5H2C2O4+2MnO4-+6H+=10CO2↑+2Mn2++8H2O为例 探究“外界 条件 对化 学反 应速 率的 影响”。 说法 正确 的是 ( )
实验 时, 分别 量取H2C2O4溶液 和酸 性KMnO4溶液 ,迅 速混 合并 开始 计时 ,通 过测 定溶 液褪 色所 需时
间来 判断 反应 的快 慢。 下列 说法 不正 确的 是( )
H2C2O4溶液 酸性KMnO4溶液
编号 温度/℃
浓度/mol/L 体积/mL 浓度/mol/L 体积/mL
① 0.10 2.0 0.010 4.0 25
② 0.20 2.0 0.010 4.0 25
③ 0.20 2.0 0.010 4.0 50 A. 这些 离子 中氧化 性 最强 的是E
A.实验 ① 、② 、③ 所加 的H2C2O4溶液 均要 过量 B.A,B,C,D,E五种 微粒 中C最稳 定
B. 实验 ①和 ②起初 反应 均很 慢, 过了 一会 儿速 率突 然增 大, 可能 是生 成的Mn2+对反 应起 催化 作用 C.C→ B+D的反 应, 反应 物的 总键 能 小于生 成物 的总 键能
C.实验 ①和实 验 ②是探 究浓 度对 化学 反应 速率 的影 响 ,实验 ② 和③ 是探 究温 度对 化学 反应 速率 的影 响 D.B→A+D是吸 热反 应
-1 -1
D.实验 ① 测得KMnO4溶液 的褪 色时 间为40 s,则 这段 时间 内平 均反 应速 率 16 . 把 温 度 为 20 ℃ , 浓 度 为 1.0 mol · L 的 H2SO4和 2.2 mol· L 的 碱 溶 液 各 50 mL 混 合 ( 溶 液 密 度 均
高二年级化学试卷 第5页 共12页 高二年级化学试卷 第6页 共12页
-1 -1 -1
为 l g· mL ,比 热容 为 4.184 kJ·K ·kg ),轻 轻搅 动。 测得 酸碱 混合 液的 温度 变化 数据 如下 :
② 已知C能与NaHCO3溶液 发生 反应 ,且C分子 的核 磁共 振氢 谱有4个峰 ,峰面 积之 比是1:1:1:3,
则C的结 构简 式是__________________。
+ - -1 18.(16分 ).研究 化学 反应 中的 能量 变化 和反 应原 理对 工业 生产 具有 十分 重要 的意 义。
则反 应 NH3·H2O=NH4+OH的焓 变约 为(单位 :kJ·mol )( )
I已知 一定 条件 下, 工业 合成 氨反 应的 能量 变化 如下 图:
A.2.1 B. 4.2 C.52.7 D.缺 少数 据无 法计 算
二 、非 选 择 题( 共52分 )
17.(8分)核磁 共振 氢谱 图是 研究 有机 物结 构的 常用 方法 :
(1)根据 核磁 共振 氢谱 图可 以确 定有 机物 分子 中氢 原子 的种 类和 数目 。例 如: 乙醚 的结 构式 为
,其 核磁 共振 氢谱 如下 左图 。
( 1) 写出 工业 合成 氨反 应的 热化 学方 程式 _______________________________
( 2) 在一 定温 度下 ,体 积为2 L的密 闭容 器中 加入1.2molN2、3.2 molH2,N2和H2之间 发生 反应 :
催化剂
N2(g) +3H2(g)????????????
高温高压 2NH3(g),如 图所 示。
若化合 物A和B的分 子式 都是C2H4Br2,A的核 磁共 振氢 谱如 上右 图所 示, 则A的结 构简 式为
_____________。
(2)有机 物C常用 于食 品行 业 。已知9.0gC在足 量O2中充 分燃 烧 ,将生 成的 混合 气体 依次 通过 足量 的浓
硫酸 和碱 石灰 ,分 别增 重5.4g和13.2g,经 检验 剩余 气体 为O2。
①C分子 的质 谱图 如图 所示 ,从 图中 可知 其相 对分 子质 量是______________,则C的分 子式 是
___________________。
①曲线_________(填“ X”、“Y”或“Z ”)表示NH3的物 质的 量浓 度随 时间 的变 化曲 线。
②0~4mi n内, 以NH3的浓 度变 化表 示的 平均 反应 速率 为_______________。
③下列 措施 能使 该反 应的 化学 反应 速率 加快 的是__________(填编 号 ,下同 ),能使 平衡 正向 移动 的是
高二年级化学试卷 第7页 共12页 高二年级化学试卷 第8页 共12页
_______。 —
相对 分子 质量 沸点/℃ 密度/(g·cm 3) 水中 溶解 性
A 通入H2 B减小 容器 体积 C 升高 温度 D 通入Ar使压 强增 大
正丁 醇 74 117.2 0.8109 微溶
④对于 该反 应, 下列 说法 能判 定达 到平 衡状 态的 是 ________________。
A. v逆(N2)=2v正(NH3) 正丁 醚 130 142.0 0.7704 几乎 不溶
B. 断裂 3mol 的 H-H 键同 时形 成 6mol 的 N-H 键 合成 反应 :
C. 混合 气体 的压 强保 持不 变 ① 将6 mL浓硫 酸和37 g正丁 醇, 按一 定顺 序添 加到A中, 并加 几粒 沸石 。
D. 混合 气体 的平 均相 对分 子质 量保 持不 变 ② 加热A中反 应液 ,迅 速升 温至135℃,维 持反 应一 段时 间。
E. 混合 气体 的密 度不 再改 变 分离 提纯 :
Ⅱ我国 学者 结合 实验 与计 算机 模拟 结果 ,研 究 C6H6(g)+C H3OH(g) C7H8(g)+ H2O(g)在固 体酸(HB)催化 ③ 待A中液 体冷 却后 将其 缓慢 倒入 盛有70 mL水的 分液 漏斗 中, 振摇 后静 置, 分液 得粗 产物 。
剂表 面进 行的 反应 历程 如图 所示 。其 中吸 附在 固体 酸(HB)表面 的物 种用?
*标注 。 ④ 粗产 物依 次用40 mL水 、20 mL NaOH溶液 和40 mL水洗 涤,分液 后加 入约3 g无水 氯化 钙颗 粒,静
置一 段时 间后 弃去 氯化 钙。
⑤ 将上 述处 理过 的粗 产物 进行 蒸馏 ,收 集馏 分, 得纯 净正 丁醚11 g。
请回 答:
(1)步 骤 ①中浓 硫酸 和正 丁醇 的添 加顺 序为_____________________________。
(2)步骤 ③的目 的是 初步 洗去_____,振摇 后静 置,粗产 物应 在分 液漏 斗的____口(填“ 上” 或“ 下” )
分离 出。
(3) 该反 应的 活化 能E为_________kJ ·mol-1。 (3)步 骤 ④中最 后一 次水 洗的 作用 为___________________________________。
(4)C6H6*在催 化剂 表面 转化 为C7H8*的反 应方 程式 为____________________________。 (4)步 骤 ⑤中, 加热 蒸馏 时应 收集________(填 选项 字母 )左 右温 度的 馏分 。
19(13分). 正丁 醚常 用作 有机 反应 的溶 剂。 实验 室制 备正 丁醚 的反 应和 主要 实验 装置 如下 : a. 100℃ b. 117℃ c. 135℃ d . 142℃
2CH3CH2CH2CH2OH (CH3CH2CH2CH2)2O+H2O (5)反应 过程 中会 观察 到分 水器 中收 集到 液体 物质 ,且分 为上 下两 层 ,随着 反应 的进 行,分水 器中 液
体逐 渐增 多至 充满 液体 时, 上层 液体 会从 左侧 支管 自动 流回A。分 水器 中上 层液 体的 主要 成分 是
___________。
(6)本实 验中 ,正丁 醚的 产率 为_________%。(保留2位有 效数 字)(产率 等于 实际 产量 与理 论产 量的
比值 )
20.(15分 )物质G是一 种可 降解 的高 分子 有机 材料 ,以 物质A为原 料合 成G的流 程如 图所 示:
反应 物和 产物 的相 关数 据如 下:
高二年级化学试卷 第9页 共12页 高二年级化学试卷 第10页 共12页
回答 下列 问题 :
(1)F转化 为G的反 应类 型为____________, D 所含 官能 团的 名称 为_____________。
(2)B的名 称为________________,B转化 为C的反 应条 件为____________________。
(3)F分子 之间 可以 形成 多种 酯, 写出F形成 的一 种六 元环 酯的 结构 简式 :____________。
(4)写出E转化 为F的第 i 步反 应的 化学 方程 式:_______________________________。
(5)C有多 种同 分异 构体 ,能 够发 生水 解反 应的 结构 共有______种, 其中 核磁 共振 氢谱 有3种峰 ,峰 的
面积 之比 为1:1:6的结 构简 式为_______________(不考 虑立 体异 构)。
(6)氯丁 橡胶 是目 前常 用的 橡胶 ,试以A为原 料 ,设计 制备 氯丁 橡胶 单体(CH2=CCl-C H=CH2)的合 成路
线图(其他 试剂 任选)______________________________________。
高二年级化学试卷 第11页 共12页 高二年级化学试卷 第12页 共12页
2019级高二上学期化学期中考试
参考答案
1-5.CDD BC
6-10.A AADC
11-16.C DDCCB
17.BrCH2CH2Br(2分) 90(2分 ) C3H6O3 (2分 ) (2分)
18.I(1)N2(g)+3H2(g) 2NH3(g) ?H=2(a-b)kJ/ mol (2分)
(2) ①Y (2分 ) ②0.2 mol/(L ·min) (2分 ) ③ABC (2分)AB(2分) ④C D
(2分)
Ⅱ①-161.9 (2分) ②C6H6*+H2O+CH3B=C7H8*+H2O+HB (C6H6*+CH3B=C7H8*+HB )
(2分)
19(1)先加 入正 丁醇 ,再 加入 浓硫 酸( 2 分 )
(2) 浓硫 酸(1分 ) 上 (1分)
(1) 洗去 有机 层中 残留 的NaOH及中 和反 应生 成的 盐 (2分 )
(2)d(2分 )
(3) 正丁 醇(2分 )
(4)34(3分)
20.缩聚 反应 (1 分) 羟基 、溴原 子键 (1 分 ) 1,4-二溴-2-丁烯 (1 分 ) NaOH水溶
液、 加热 (1 分 ) (2 分)
H O2
HOOC-C HBr-CH2-COOH +3NaOH? NaOOC-CH OH-C H2-C OONa+N aBr +2H2O(2 分)
?
4(2 分) HCOOC H(CH3)2(2 分 )
(3 分 )
2 019 级 高二 上学 期化 学期 中考试
D. 2-甲基-3-丁炔
化 学试 题
.用 CH4催化 还原 NOx可以 消除 氮氧 化物 的污 染。 例如 :
(分值: 100 分 时长:90 分钟 ) 4
1
① CH4(g)+4NO2(g) 4NO(g)+CO2(g)+2H2O(g) ΔH=?574 kJ· mol?
可 能 用 到的 原 子 量 :H-1 C-12 O-16 S-32
1
② CH4(g)+4NO(g) 2N2(g)+CO2(g)+2H2O(g) ΔH=?1 160 kJ· mol?
一 .选 择 题 (每 小 题3分 , 共48分 )
下列 说法 不正 确的 是 ( )
1. 化学 与人类 生产 生活 及健 康 密切 相关 ,下 列说 法正 确的 是( )
1
A. 由反 应① 可推 知: CH4(g)+4NO2(g) 4NO(g)+CO2(g)+2H2O(l) ΔH=?Q,Q>574 kJ· mol?
A.新型 冠状 病毒 由C、H、O三种 元素 组成 B.等物 质的 量的 甲烷 分别 参加 反应 ① 、② ,反 应转 移的 电子 数不 同
B. 变质 的油 脂有 难闻 的特 殊气 味, 是由 于油 脂发 生了 水解 反应 C.若用 4.48 L (已 折算 成标准 状况 下体 积 )CH4还原 NO2至 N2,则 放出 的热 量为 173.4 kJ
C. 浸泡 过高 锰酸 钾溶 液的 硅藻 土放 于水 果箱 内是 为了 延长 水果 保鲜 期 D. 若用 4.48 L (已 折算 成标准 状况 下体 积 )CH4还原 NO2至 N2,则 整个 过程 中转 移的 电子 总物 质的 量
D.84消毒 液是 以NaClO为主 要有 效成 分的 消毒 液, 与医 用酒 精混 合可 以提 升消 毒效 果
为 1.6 mol
2.下列 说法 或表 示方 法不 正确 的是( ) 5.某有 机物A是农 药生 产中 的一 种中 间体 ,其 结构 简式 如图 ,下 列叙 述 错误 的是 ( )
A.盖斯 定律 实质 上是 能量 守恒 定律 的体 现
+ - -
B.在稀 溶液 中:H (aq)+OH (aq)=H2O(l) ΔH=-57.3 kJ ·mol 1,含0.5 mol H2SO4的浓 硫酸 与含1 mol
NaOH的溶 液混 合, 放出 的热 量大 于57.3 kJ
C. 由C(石墨 ,s)=== C(金刚 石,s) Δ H>0,可 知, 石墨 比金 刚石 稳定
- - A. 有机 物A属于 芳香 族化 合物
D.H2(g)的燃 烧热ΔH=-285.8 kJ ·mol 1,则2H2O(l)= ==2H2(g)+O2(g) ΔH=285.8 kJ ·mol 1
B.有机 物A不 可以 和Br2的CCl4溶液 发生 加成 反应
3.下 列有 机物 命名 错误 的是 ( )
C.有机 物A和浓 硫酸 混合 加热 ,可 以发 生消 去反 应
A. 1,2,4-三甲 苯 D.1mol A和足 量的NaOH溶液 反应 ,最 多可 以消 耗3mol NaOH
5 ?1
6.在298K、1.01 10 P a? 下 ,将32g S O2通入750mL 1mol L? 的KOH溶液 中充 分反 应 ,测得 反应
?
放出 1
xkJ的热 量 。已知 在该 条件 下 ,1 mo l S O 通入1L 2mol L? 的KOH溶液 中充 分反 应放 出yk J的
B. 2-甲基-2-氯丙 烷 2
热量 。则S O2与KOH溶液 反应 生成KHS O3的热 化学 方程 式正 确的 是( )
?1
A.SO g KOH aq KHSO aq2? ? ? ? ? ?? ? 3 , ? ? ? ? ?H x y? ?4 kJ mol
高二年级化学试卷 第1页 共12页 高二年级化学试卷 第2页 共12页
?1
B. A.物质 的二 氯代 物有 种
SO g KOH aq KHSO aq2? ? ? ? ? ?? ? 3 ,? ? ? ? ?H x y? ?2 kJ mol d 6
. 物质 的分 子式 为
?1 B b C10H12
C.SO g KOH aq KHSO aq2? ? ? ? ? ?? ? 3 ,? ? ? ? ?H y x? ?2 kJ mol
C. 物质c与物 质d互为 同分 异构 体
?1
D.SO g KOH aq KHSO aq2? ? ? ? ? ?? ? 3 ,? ? ? ? ?H x y? ?8 2 kJ mol D.a最多 有10个原 子共 平面
7.苯甲 酸在 水中 的溶 解度 为:0.18g(4℃)、0.34g(25℃)、6.8g(95℃ )。某 苯甲 酸晶 体 中含 少量 可 10.一定 温度 下,在2 L的密 闭容 器中 ,X、Y、Z三种 气体 的物 质的 量随 时间 变化 的曲 线如 下图 所示 ,
溶性 杂质X和难 溶性 杂质Y。现 拟用 下列 装置 和操 作进 行提 纯: 装置 : 甲 乙 丙 下列 描述 正确 的是 ( )
操作 :① 常温 过滤 ②趁热 过滤 ③ 加热 溶解 ④结晶 ⑤ 洗涤 、干 燥下 列有 关说 法正 确的 是( ) A. 反应 开始 到10 s,用Z表示 的反 应速 率为0.158 mol/(L ?s)
A.用甲 装置 溶解 样品 ,X 在第 ①步被 分离 B. 反应 开始 到10 s,X的物 质的 量浓 度减 少了0.79 mol/L
B. 用乙 装置 趁热 过滤 ,Y 在第 ② 步被 分离 C. 反应 开始 到10 s时,Y的转 化率 为79.0 %
C. 用丙 装置 所示 的方 法结 晶 D. 反应 的化 学方 程式 为:X(g)+Y(g)=Z(g)
D.正确 的操 作顺 序为 : ③→④→②→①→⑤ 11. 某研 究性 小组 为了 探究 石蜡 油分 解产 物, 设计 了如 下实 验方 案。 下列 说法 错误 的是 ( )
8.一定 条件 下,某容 器中 各微 粒在 充分 反应 前后 变化 的示 意图 如下 ,其中?和?代表 不同 元素 的原 子,
关于 此反 应说 法错 误的 是( )
A.一定 属于 吸热 反应 B.一定 属于 可逆 反应
C. 一定 属于 氧化 还原 反应 D. 一定 属于 分解 反应
9.以物 质a为原 料,制备 物质d(金刚 烷)的合 成路 线如 下图 所示 ,关于 以下 有机 物说 法中 错误 的是( )
A. 碎瓷 片有 催化 和积 蓄热 量的 作用
B. 结束 反应 时, 先撤 出导 管, 再停 止加 热
C. B、C 中溶 液均 褪色 ,说明 一定 有乙 烯生 成
关于 以上 有机 物说 法中 错误 的是
高二年级化学试卷 第3页 共12页 高二年级化学试卷 第4页 共12页
D.石蜡 油是 液态 烷烃 v(KMnO4)=2.5×10-4mol·L-1·s-1
-1
12. 一定 温度 下, 向 10 mL 0.40 mol· L H2O2溶液 中加 入适 量 FeCl3溶液 ,不 同时 刻测 得生 成 O2的体 14.最新 报道 :科学 家首 次用 X 射线 激光 技术 观察 到 CO 与 O 在催 化剂 表面 形成 化学 键的 过程 .反应 过
积( 已折 算为 标准 状况 )如 下左 表所 示。 程的 示意 图如 下 ,下列 说法 正确 的是 ( )
t/ min 0 2 4 6
V(O2) / mL 0 9.9 17.2 22.4
3+ 2+ + 2+ + 3+
资料 显示 ,反应 分两 步进 行:① 2Fe +H2O2=2Fe +O2↑+2H② H2O2+2Fe +2H = 2H2O+2Fe ,反应 过程 中能
量变 化如 上右 图所 示。 下列 说法 不正 确的 是( ) A. CO 和 O 生成 CO2是吸 热反 应
-2 -1 -1
A.0~ 6 min 的平 均反 应速 率:v(H2O2)=3.33×10 mol·L · min B.在该 过程 中, CO 断键 形成 C 和 O
3+
B. Fe 的作 用是 增大 过氧 化氢 的分 解速 率 C.同物 质的 量的 CO 和 O 反应 比 CO 与 O2反应 放出 更多 热量
C. 反应 ①是吸 热反 应、 反应 ② 是放 热反 应 D. 状态 Ⅰ→ 状态 Ⅲ表示 CO 与 O2反应 的过 程
D.反应 2H2O2(aq)= 2H2O(l)+O2(g)的△H=E1-E2<0 15.一定 条件 下, 在水 溶液 中1molC l-、ClOx-(x= 1,2,3,4)的能 量(kJ)相对 大小 如图 所示 。下 列有 关
13. 以反 应5H2C2O4+2MnO4-+6H+=10CO2↑+2Mn2++8H2O为例 探究“外界 条件 对化 学反 应速 率的 影响”。 说法 正确 的是 ( )
实验 时, 分别 量取H2C2O4溶液 和酸 性KMnO4溶液 ,迅 速混 合并 开始 计时 ,通 过测 定溶 液褪 色所 需时
间来 判断 反应 的快 慢。 下列 说法 不正 确的 是( )
H2C2O4溶液 酸性KMnO4溶液
编号 温度/℃
浓度/mol/L 体积/mL 浓度/mol/L 体积/mL
① 0.10 2.0 0.010 4.0 25
② 0.20 2.0 0.010 4.0 25
③ 0.20 2.0 0.010 4.0 50 A. 这些 离子 中氧化 性 最强 的是E
A.实验 ① 、② 、③ 所加 的H2C2O4溶液 均要 过量 B.A,B,C,D,E五种 微粒 中C最稳 定
B. 实验 ①和 ②起初 反应 均很 慢, 过了 一会 儿速 率突 然增 大, 可能 是生 成的Mn2+对反 应起 催化 作用 C.C→ B+D的反 应, 反应 物的 总键 能 小于生 成物 的总 键能
C.实验 ①和实 验 ②是探 究浓 度对 化学 反应 速率 的影 响 ,实验 ② 和③ 是探 究温 度对 化学 反应 速率 的影 响 D.B→A+D是吸 热反 应
-1 -1
D.实验 ① 测得KMnO4溶液 的褪 色时 间为40 s,则 这段 时间 内平 均反 应速 率 16 . 把 温 度 为 20 ℃ , 浓 度 为 1.0 mol · L 的 H2SO4和 2.2 mol· L 的 碱 溶 液 各 50 mL 混 合 ( 溶 液 密 度 均
高二年级化学试卷 第5页 共12页 高二年级化学试卷 第6页 共12页
-1 -1 -1
为 l g· mL ,比 热容 为 4.184 kJ·K ·kg ),轻 轻搅 动。 测得 酸碱 混合 液的 温度 变化 数据 如下 :
② 已知C能与NaHCO3溶液 发生 反应 ,且C分子 的核 磁共 振氢 谱有4个峰 ,峰面 积之 比是1:1:1:3,
则C的结 构简 式是__________________。
+ - -1 18.(16分 ).研究 化学 反应 中的 能量 变化 和反 应原 理对 工业 生产 具有 十分 重要 的意 义。
则反 应 NH3·H2O=NH4+OH的焓 变约 为(单位 :kJ·mol )( )
I已知 一定 条件 下, 工业 合成 氨反 应的 能量 变化 如下 图:
A.2.1 B. 4.2 C.52.7 D.缺 少数 据无 法计 算
二 、非 选 择 题( 共52分 )
17.(8分)核磁 共振 氢谱 图是 研究 有机 物结 构的 常用 方法 :
(1)根据 核磁 共振 氢谱 图可 以确 定有 机物 分子 中氢 原子 的种 类和 数目 。例 如: 乙醚 的结 构式 为
,其 核磁 共振 氢谱 如下 左图 。
( 1) 写出 工业 合成 氨反 应的 热化 学方 程式 _______________________________
( 2) 在一 定温 度下 ,体 积为2 L的密 闭容 器中 加入1.2molN2、3.2 molH2,N2和H2之间 发生 反应 :
催化剂
N2(g) +3H2(g)????????????
高温高压 2NH3(g),如 图所 示。
若化合 物A和B的分 子式 都是C2H4Br2,A的核 磁共 振氢 谱如 上右 图所 示, 则A的结 构简 式为
_____________。
(2)有机 物C常用 于食 品行 业 。已知9.0gC在足 量O2中充 分燃 烧 ,将生 成的 混合 气体 依次 通过 足量 的浓
硫酸 和碱 石灰 ,分 别增 重5.4g和13.2g,经 检验 剩余 气体 为O2。
①C分子 的质 谱图 如图 所示 ,从 图中 可知 其相 对分 子质 量是______________,则C的分 子式 是
___________________。
①曲线_________(填“ X”、“Y”或“Z ”)表示NH3的物 质的 量浓 度随 时间 的变 化曲 线。
②0~4mi n内, 以NH3的浓 度变 化表 示的 平均 反应 速率 为_______________。
③下列 措施 能使 该反 应的 化学 反应 速率 加快 的是__________(填编 号 ,下同 ),能使 平衡 正向 移动 的是
高二年级化学试卷 第7页 共12页 高二年级化学试卷 第8页 共12页
_______。 —
相对 分子 质量 沸点/℃ 密度/(g·cm 3) 水中 溶解 性
A 通入H2 B减小 容器 体积 C 升高 温度 D 通入Ar使压 强增 大
正丁 醇 74 117.2 0.8109 微溶
④对于 该反 应, 下列 说法 能判 定达 到平 衡状 态的 是 ________________。
A. v逆(N2)=2v正(NH3) 正丁 醚 130 142.0 0.7704 几乎 不溶
B. 断裂 3mol 的 H-H 键同 时形 成 6mol 的 N-H 键 合成 反应 :
C. 混合 气体 的压 强保 持不 变 ① 将6 mL浓硫 酸和37 g正丁 醇, 按一 定顺 序添 加到A中, 并加 几粒 沸石 。
D. 混合 气体 的平 均相 对分 子质 量保 持不 变 ② 加热A中反 应液 ,迅 速升 温至135℃,维 持反 应一 段时 间。
E. 混合 气体 的密 度不 再改 变 分离 提纯 :
Ⅱ我国 学者 结合 实验 与计 算机 模拟 结果 ,研 究 C6H6(g)+C H3OH(g) C7H8(g)+ H2O(g)在固 体酸(HB)催化 ③ 待A中液 体冷 却后 将其 缓慢 倒入 盛有70 mL水的 分液 漏斗 中, 振摇 后静 置, 分液 得粗 产物 。
剂表 面进 行的 反应 历程 如图 所示 。其 中吸 附在 固体 酸(HB)表面 的物 种用?
*标注 。 ④ 粗产 物依 次用40 mL水 、20 mL NaOH溶液 和40 mL水洗 涤,分液 后加 入约3 g无水 氯化 钙颗 粒,静
置一 段时 间后 弃去 氯化 钙。
⑤ 将上 述处 理过 的粗 产物 进行 蒸馏 ,收 集馏 分, 得纯 净正 丁醚11 g。
请回 答:
(1)步 骤 ①中浓 硫酸 和正 丁醇 的添 加顺 序为_____________________________。
(2)步骤 ③的目 的是 初步 洗去_____,振摇 后静 置,粗产 物应 在分 液漏 斗的____口(填“ 上” 或“ 下” )
分离 出。
(3) 该反 应的 活化 能E为_________kJ ·mol-1。 (3)步 骤 ④中最 后一 次水 洗的 作用 为___________________________________。
(4)C6H6*在催 化剂 表面 转化 为C7H8*的反 应方 程式 为____________________________。 (4)步 骤 ⑤中, 加热 蒸馏 时应 收集________(填 选项 字母 )左 右温 度的 馏分 。
19(13分). 正丁 醚常 用作 有机 反应 的溶 剂。 实验 室制 备正 丁醚 的反 应和 主要 实验 装置 如下 : a. 100℃ b. 117℃ c. 135℃ d . 142℃
2CH3CH2CH2CH2OH (CH3CH2CH2CH2)2O+H2O (5)反应 过程 中会 观察 到分 水器 中收 集到 液体 物质 ,且分 为上 下两 层 ,随着 反应 的进 行,分水 器中 液
体逐 渐增 多至 充满 液体 时, 上层 液体 会从 左侧 支管 自动 流回A。分 水器 中上 层液 体的 主要 成分 是
___________。
(6)本实 验中 ,正丁 醚的 产率 为_________%。(保留2位有 效数 字)(产率 等于 实际 产量 与理 论产 量的
比值 )
20.(15分 )物质G是一 种可 降解 的高 分子 有机 材料 ,以 物质A为原 料合 成G的流 程如 图所 示:
反应 物和 产物 的相 关数 据如 下:
高二年级化学试卷 第9页 共12页 高二年级化学试卷 第10页 共12页
回答 下列 问题 :
(1)F转化 为G的反 应类 型为____________, D 所含 官能 团的 名称 为_____________。
(2)B的名 称为________________,B转化 为C的反 应条 件为____________________。
(3)F分子 之间 可以 形成 多种 酯, 写出F形成 的一 种六 元环 酯的 结构 简式 :____________。
(4)写出E转化 为F的第 i 步反 应的 化学 方程 式:_______________________________。
(5)C有多 种同 分异 构体 ,能 够发 生水 解反 应的 结构 共有______种, 其中 核磁 共振 氢谱 有3种峰 ,峰 的
面积 之比 为1:1:6的结 构简 式为_______________(不考 虑立 体异 构)。
(6)氯丁 橡胶 是目 前常 用的 橡胶 ,试以A为原 料 ,设计 制备 氯丁 橡胶 单体(CH2=CCl-C H=CH2)的合 成路
线图(其他 试剂 任选)______________________________________。
高二年级化学试卷 第11页 共12页 高二年级化学试卷 第12页 共12页
2019级高二上学期化学期中考试
参考答案
1-5.CDD BC
6-10.A AADC
11-16.C DDCCB
17.BrCH2CH2Br(2分) 90(2分 ) C3H6O3 (2分 ) (2分)
18.I(1)N2(g)+3H2(g) 2NH3(g) ?H=2(a-b)kJ/ mol (2分)
(2) ①Y (2分 ) ②0.2 mol/(L ·min) (2分 ) ③ABC (2分)AB(2分) ④C D
(2分)
Ⅱ①-161.9 (2分) ②C6H6*+H2O+CH3B=C7H8*+H2O+HB (C6H6*+CH3B=C7H8*+HB )
(2分)
19(1)先加 入正 丁醇 ,再 加入 浓硫 酸( 2 分 )
(2) 浓硫 酸(1分 ) 上 (1分)
(1) 洗去 有机 层中 残留 的NaOH及中 和反 应生 成的 盐 (2分 )
(2)d(2分 )
(3) 正丁 醇(2分 )
(4)34(3分)
20.缩聚 反应 (1 分) 羟基 、溴原 子键 (1 分 ) 1,4-二溴-2-丁烯 (1 分 ) NaOH水溶
液、 加热 (1 分 ) (2 分)
H O2
HOOC-C HBr-CH2-COOH +3NaOH? NaOOC-CH OH-C H2-C OONa+N aBr +2H2O(2 分)
?
4(2 分) HCOOC H(CH3)2(2 分 )
(3 分 )
同课章节目录
