沪教版九上化学 5.2 金属矿物 铁的治练 课件(21张ppt)
文档属性
| 名称 | 沪教版九上化学 5.2 金属矿物 铁的治练 课件(21张ppt) |

|
|
| 格式 | ppt | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-11-16 00:00:00 | ||
图片预览








文档简介
第二节 金属矿物 铁的冶炼
一、金属矿物
铜的矿物
对比Fe2O3和Fe的组成,如何使Fe2O3转变成Fe 呢?
金属铁的冶炼,是把它们的矿物跟易得氧的物质一起高温反应,以夺氧的方式还原铁的氧化物。通常使用的还原剂是CO。以赤铁矿为例,其化学方程式为:
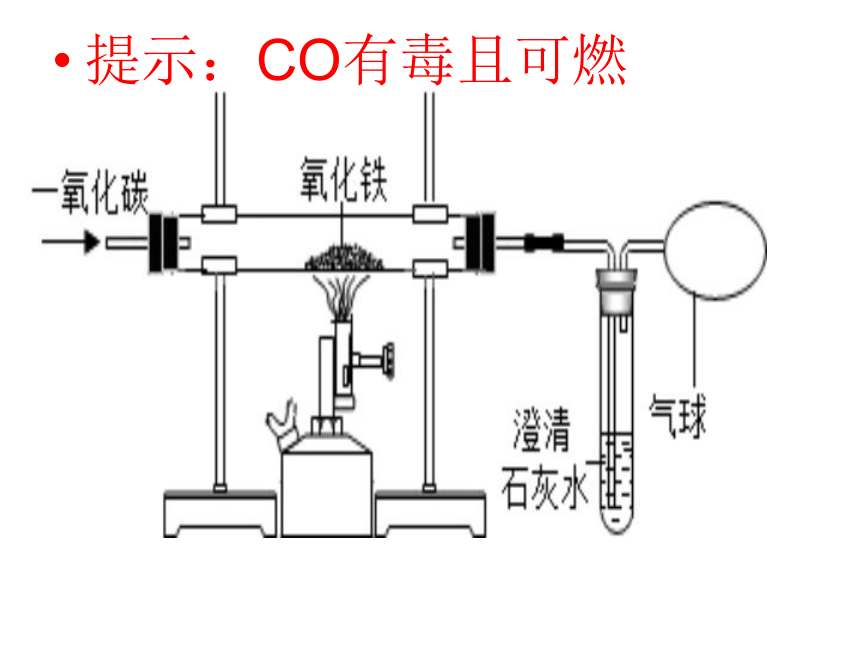
提示:CO有毒且可燃
(1)、检查装置的气密性;
(2)、装入药品;
(3)、向玻璃管内通入一氧化碳气体;
(4)、给氧化铁加热;
(5)、停止加热;
(6)、待玻璃管冷却后停止通一氧化碳。
1、红棕色的固体逐渐变成黑色
2、澄清的石灰水变浑浊。
铁、四氧化三铁性质对比表
工业炼铁的主要设备、原料、主要反应、产品各是什么?各原料的作用又是如何的呢?
1、炼铁的主要设备是:
2、炼铁的原料及作用:
(1)铁矿石:
(2)焦 炭:
(3)石灰石:
(4)空 气:
定量研究
四、交流与讨论
例题:
某钢铁公司用490万吨含氧化铁60%的赤铁矿炼铁,所得生铁中最多含铁多少万吨?
①完成学案纸:一、自主学习
②预习书123—124页
自然界以单质形式存在的银
自然界以单质形式存在的金
黄铜矿
孔雀石
斑铜矿
赤铜矿
铝的矿物
铝土矿
明矾石
水铝石
使金属矿物变成金属的过程,叫做金属的冶炼
金属的冶炼
磁铁矿的主要成分为Fe3O4
黄铁矿的主要成分是FeS2
铁的几种矿石
赤铁矿(主要成分为Fe2O3)
褐铁矿(Fe2O3·xH2O)
菱铁矿主要成分是FeCO3
主要成分含铁量37%—55%
含铁量70%
含铁量72.4%
含铁量46.7%
含铁量48.3%
二、铁的冶炼
3CO+Fe2O3==2Fe+3CO2
高温
小结
1、实验步骤
CO
早出晚归:
酒精喷灯
迟到早退:
排出装置内的空气,防止加热时CO与空气混合,
可能会发生爆炸
防止生成的铁重新被氧化
防止石灰水倒吸,玻璃管炸裂
2、实验现象
3、化学方程式
3CO+Fe2O3===2Fe+3CO2
CO2+Ca(OH)2===CaCO3 +H2O
高温
不冒气泡
能
黑色
四氧化三铁
冒气泡
能
黑色
铁粉
加盐酸中是否冒气泡
是否能被磁铁吸引
颜色
粉末
高炉
提供铁元素
a、燃烧放热、维持高温
b、制还原剂CO
制造炉渣
提供氧气
4、主要反应
C+O2===CO2
C+CO2===2CO
3CO+Fe2O3===2Fe+3CO2
高温
高温
点燃
5、产物:生铁
金属冶炼方法小结
1、热分解法
有些不活泼金属仅用热分解法就能制得。
2HgO == 2Hg + O2↑
2Ag2O == 4Ag + O2↑
2Al2O3====4Al+3O2↑
2NaCl====2Na+Cl2↑
2.电解法
在金属活动性顺序中,钾、钠、钙、铝等几种金属活动性很强,这些金属都很容易失去电子,因此不能用一般的方法和还原剂使其从化合物中还原出来,而只能用通电分解其熔融盐或氧化物的方法来冶炼。
通电
通电
3.热还原法
多数金属的冶炼过程属于热还原法。常用的还原剂有焦炭、一氧化碳、氢气等。
Fe2O3+3CO == 2Fe+3CO2
高温
CuO+ H2 == Cu+H2O
高温
一、金属矿物
铜的矿物
对比Fe2O3和Fe的组成,如何使Fe2O3转变成Fe 呢?
金属铁的冶炼,是把它们的矿物跟易得氧的物质一起高温反应,以夺氧的方式还原铁的氧化物。通常使用的还原剂是CO。以赤铁矿为例,其化学方程式为:
提示:CO有毒且可燃
(1)、检查装置的气密性;
(2)、装入药品;
(3)、向玻璃管内通入一氧化碳气体;
(4)、给氧化铁加热;
(5)、停止加热;
(6)、待玻璃管冷却后停止通一氧化碳。
1、红棕色的固体逐渐变成黑色
2、澄清的石灰水变浑浊。
铁、四氧化三铁性质对比表
工业炼铁的主要设备、原料、主要反应、产品各是什么?各原料的作用又是如何的呢?
1、炼铁的主要设备是:
2、炼铁的原料及作用:
(1)铁矿石:
(2)焦 炭:
(3)石灰石:
(4)空 气:
定量研究
四、交流与讨论
例题:
某钢铁公司用490万吨含氧化铁60%的赤铁矿炼铁,所得生铁中最多含铁多少万吨?
①完成学案纸:一、自主学习
②预习书123—124页
自然界以单质形式存在的银
自然界以单质形式存在的金
黄铜矿
孔雀石
斑铜矿
赤铜矿
铝的矿物
铝土矿
明矾石
水铝石
使金属矿物变成金属的过程,叫做金属的冶炼
金属的冶炼
磁铁矿的主要成分为Fe3O4
黄铁矿的主要成分是FeS2
铁的几种矿石
赤铁矿(主要成分为Fe2O3)
褐铁矿(Fe2O3·xH2O)
菱铁矿主要成分是FeCO3
主要成分含铁量37%—55%
含铁量70%
含铁量72.4%
含铁量46.7%
含铁量48.3%
二、铁的冶炼
3CO+Fe2O3==2Fe+3CO2
高温
小结
1、实验步骤
CO
早出晚归:
酒精喷灯
迟到早退:
排出装置内的空气,防止加热时CO与空气混合,
可能会发生爆炸
防止生成的铁重新被氧化
防止石灰水倒吸,玻璃管炸裂
2、实验现象
3、化学方程式
3CO+Fe2O3===2Fe+3CO2
CO2+Ca(OH)2===CaCO3 +H2O
高温
不冒气泡
能
黑色
四氧化三铁
冒气泡
能
黑色
铁粉
加盐酸中是否冒气泡
是否能被磁铁吸引
颜色
粉末
高炉
提供铁元素
a、燃烧放热、维持高温
b、制还原剂CO
制造炉渣
提供氧气
4、主要反应
C+O2===CO2
C+CO2===2CO
3CO+Fe2O3===2Fe+3CO2
高温
高温
点燃
5、产物:生铁
金属冶炼方法小结
1、热分解法
有些不活泼金属仅用热分解法就能制得。
2HgO == 2Hg + O2↑
2Ag2O == 4Ag + O2↑
2Al2O3====4Al+3O2↑
2NaCl====2Na+Cl2↑
2.电解法
在金属活动性顺序中,钾、钠、钙、铝等几种金属活动性很强,这些金属都很容易失去电子,因此不能用一般的方法和还原剂使其从化合物中还原出来,而只能用通电分解其熔融盐或氧化物的方法来冶炼。
通电
通电
3.热还原法
多数金属的冶炼过程属于热还原法。常用的还原剂有焦炭、一氧化碳、氢气等。
Fe2O3+3CO == 2Fe+3CO2
高温
CuO+ H2 == Cu+H2O
高温
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
