沪教版九上化学 5.3 金属防护和废金属回收 课件(15张ppt)
文档属性
| 名称 | 沪教版九上化学 5.3 金属防护和废金属回收 课件(15张ppt) |

|
|
| 格式 | ppt | ||
| 文件大小 | 2.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-11-16 00:00:00 | ||
图片预览






文档简介
第三节 金属防护和废金属回收
※钢铁有什么用途
面临钢铁的最大问题是什么呢?
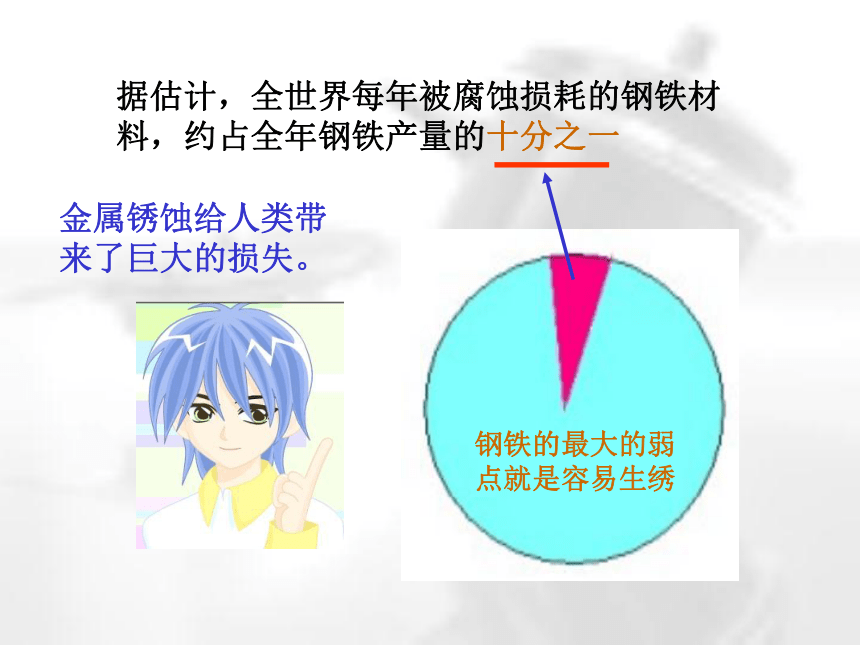
据估计,全世界每年被腐蚀损耗的钢铁材料,约占全年钢铁产量的十分之一
钢铁的最大的弱点就是容易生绣
金属锈蚀给人类带来了巨大的损失。
铁轨的锈蚀
铁钉的生锈
各种铁制品的锈蚀
如何防锈?
探究实验一:铁生锈的条件
一半在水中
全浸没在煮沸迅速冷却的水中
干燥空气中
① ② ③
三天后
铁在空气、水的界面处生锈
铁未生锈
铁未生锈
① ② ③
一半在水中
全浸没在煮沸迅速冷却的水中
干燥空气中
探究实验二:
一半在水中
食盐水中
浸没过稀硫酸
④ ⑤ ①
三天后
铁钉严重锈蚀
浸没在食盐水中的铁钉几乎完全锈蚀
铁钉在空气与水的界面处生锈
④ ⑤ ①
浸没过稀硫酸
食盐水中
一半在水中
铁生锈的应用:
食品包装盒中常放有一小袋粉末状物质,该物质对食品同时具有防潮和防氧化作用。玲玲同学从超市购买的食品包装盒中取出装有粉末状物质的小袋,撕开后发现袋里有板结的铁锈。试推测粉末状物质是什么?其作用原理是什么?
铝比铁更容易跟氧气和其他物质发生化学反应。铝在空气中与氧气反应,生成的氧化铝形成一层致密而结实的膜覆盖在铝的表面,防止铝继续与氧气反应,从而起到“自我保护”的作用。
所谓“电化铝”是指用特殊方法使铝表面形成加厚的氧化铝保护层的铝材料。
铁锈
(Fe2O3)
氧化铝
(Al2O3)
结构特点
若不除去结果
疏松多孔
完全锈蚀
致密结实
使铝“自我保护”
怎么防止钢铁的生锈呢?
在车船的表面喷油漆
在机械表面涂防锈油
在面盆、杯子、等表面烧涂搪瓷
此外,还可以在钢铁表面镀上一层能起保护作用的其他金属。
如:在钢铁表面镀锡、镀锌、和镀铬
镀铜
阅读课本P129
1、小结本节的内容
2、课本的练习
P130第1至4题
某市一家大型化工厂处理回收含铜废料的生产流程如下:
含铜废物
黑色固体及残留物
硫酸铜、水及不溶物
滤液
浅绿色溶液及红色沉淀物
红色粉末
灼烧
(1)
稀硫酸、加热
(2)
过滤
铁屑
过滤
过程⑴得到的残留物不溶于水和稀硫酸。请写出上述生产流程中与铜直接有关的化学方程式。
⑴____________________________________________________
⑵____________________________________________________
⑶____________________________________________________
2Cu+O2 2CuO
△
CuO+H2SO4=CuSO4+H2O
Fe+CuSO4=FeSO4+Cu
※钢铁有什么用途
面临钢铁的最大问题是什么呢?
据估计,全世界每年被腐蚀损耗的钢铁材料,约占全年钢铁产量的十分之一
钢铁的最大的弱点就是容易生绣
金属锈蚀给人类带来了巨大的损失。
铁轨的锈蚀
铁钉的生锈
各种铁制品的锈蚀
如何防锈?
探究实验一:铁生锈的条件
一半在水中
全浸没在煮沸迅速冷却的水中
干燥空气中
① ② ③
三天后
铁在空气、水的界面处生锈
铁未生锈
铁未生锈
① ② ③
一半在水中
全浸没在煮沸迅速冷却的水中
干燥空气中
探究实验二:
一半在水中
食盐水中
浸没过稀硫酸
④ ⑤ ①
三天后
铁钉严重锈蚀
浸没在食盐水中的铁钉几乎完全锈蚀
铁钉在空气与水的界面处生锈
④ ⑤ ①
浸没过稀硫酸
食盐水中
一半在水中
铁生锈的应用:
食品包装盒中常放有一小袋粉末状物质,该物质对食品同时具有防潮和防氧化作用。玲玲同学从超市购买的食品包装盒中取出装有粉末状物质的小袋,撕开后发现袋里有板结的铁锈。试推测粉末状物质是什么?其作用原理是什么?
铝比铁更容易跟氧气和其他物质发生化学反应。铝在空气中与氧气反应,生成的氧化铝形成一层致密而结实的膜覆盖在铝的表面,防止铝继续与氧气反应,从而起到“自我保护”的作用。
所谓“电化铝”是指用特殊方法使铝表面形成加厚的氧化铝保护层的铝材料。
铁锈
(Fe2O3)
氧化铝
(Al2O3)
结构特点
若不除去结果
疏松多孔
完全锈蚀
致密结实
使铝“自我保护”
怎么防止钢铁的生锈呢?
在车船的表面喷油漆
在机械表面涂防锈油
在面盆、杯子、等表面烧涂搪瓷
此外,还可以在钢铁表面镀上一层能起保护作用的其他金属。
如:在钢铁表面镀锡、镀锌、和镀铬
镀铜
阅读课本P129
1、小结本节的内容
2、课本的练习
P130第1至4题
某市一家大型化工厂处理回收含铜废料的生产流程如下:
含铜废物
黑色固体及残留物
硫酸铜、水及不溶物
滤液
浅绿色溶液及红色沉淀物
红色粉末
灼烧
(1)
稀硫酸、加热
(2)
过滤
铁屑
过滤
过程⑴得到的残留物不溶于水和稀硫酸。请写出上述生产流程中与铜直接有关的化学方程式。
⑴____________________________________________________
⑵____________________________________________________
⑶____________________________________________________
2Cu+O2 2CuO
△
CuO+H2SO4=CuSO4+H2O
Fe+CuSO4=FeSO4+Cu
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
