2020-2021学年北京市朝阳区高三(上)期中化学试卷 含答案解析
文档属性
| 名称 | 2020-2021学年北京市朝阳区高三(上)期中化学试卷 含答案解析 |

|
|
| 格式 | zip | ||
| 文件大小 | 533.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-11-17 00:00:00 | ||
图片预览


文档简介
2020-2021学年北京市朝阳区高三(上)期中化学试卷
一、本部分共14题,每题3分,共42分。在每题列出的四个选项中,选出最符合题目要求的一项。
1.(3分)2020年7月23日我国首个火星探测器“天问一号”发射成功。火星车所涉及的下列材料中属于金属材料的是( )
A.探测仪镜头材料﹣﹣二氧化硅
B.车轮材料﹣﹣钛合金
C.温控涂层材料﹣﹣聚酰胺
D.太阳能电池复合材料﹣﹣石墨纤维和硅
2.(3分)下列有关化学用语表述正确的是( )
A.中子数为16的硫原子:S
B.纯碱的化学式:NaHCO3
C.CO2的电子式:
D.Al3+的结构示意图:
3.(3分)设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.常温下,将7.1g
Cl2通入水中,转移的电子数为0.1NA
B.1L
0.1mol?L﹣1乙酸溶液中含H+的数目为0.1NA
C.标准状况下,22.4L
CH4完全燃烧后恢复至原状态,所得产物中气体分子数为3NA
D.25℃时,1L
pH=11的Na2CO3溶液中由水电离出的OH﹣的数目为0.001NA
4.(3分)下列实验所涉及反应的离子方程式不正确的是( )
A.向氯化铁溶液中加入铁粉:2Fe3++Fe═3Fe2+
B.向硫酸铝溶液中加入过量氨水:Al3++4OH﹣═AlO2﹣+2H2O
C.向草酸溶液中滴加几滴高锰酸钾酸性溶液:2MnO4﹣+5H2C2O4+6H+═2Mn2++10CO2↑+8H2O
D.向海带灰浸出液中滴加几滴硫酸酸化的过氧化氢溶液:2I﹣+H2O2+2H+═I2+2H2O
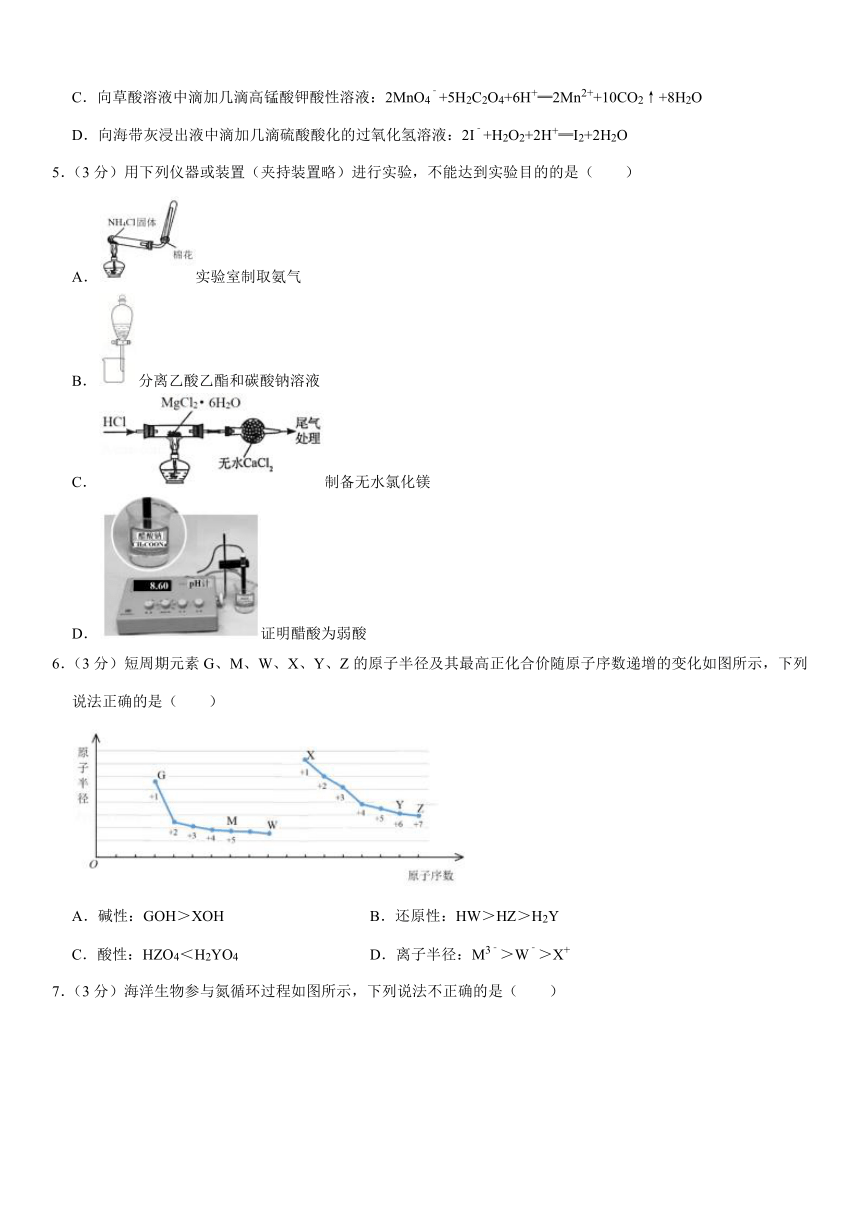
5.(3分)用下列仪器或装置(夹持装置略)进行实验,不能达到实验目的的是( )
A.实验室制取氨气
B.分离乙酸乙酯和碳酸钠溶液
C.制备无水氯化镁
D.证明醋酸为弱酸
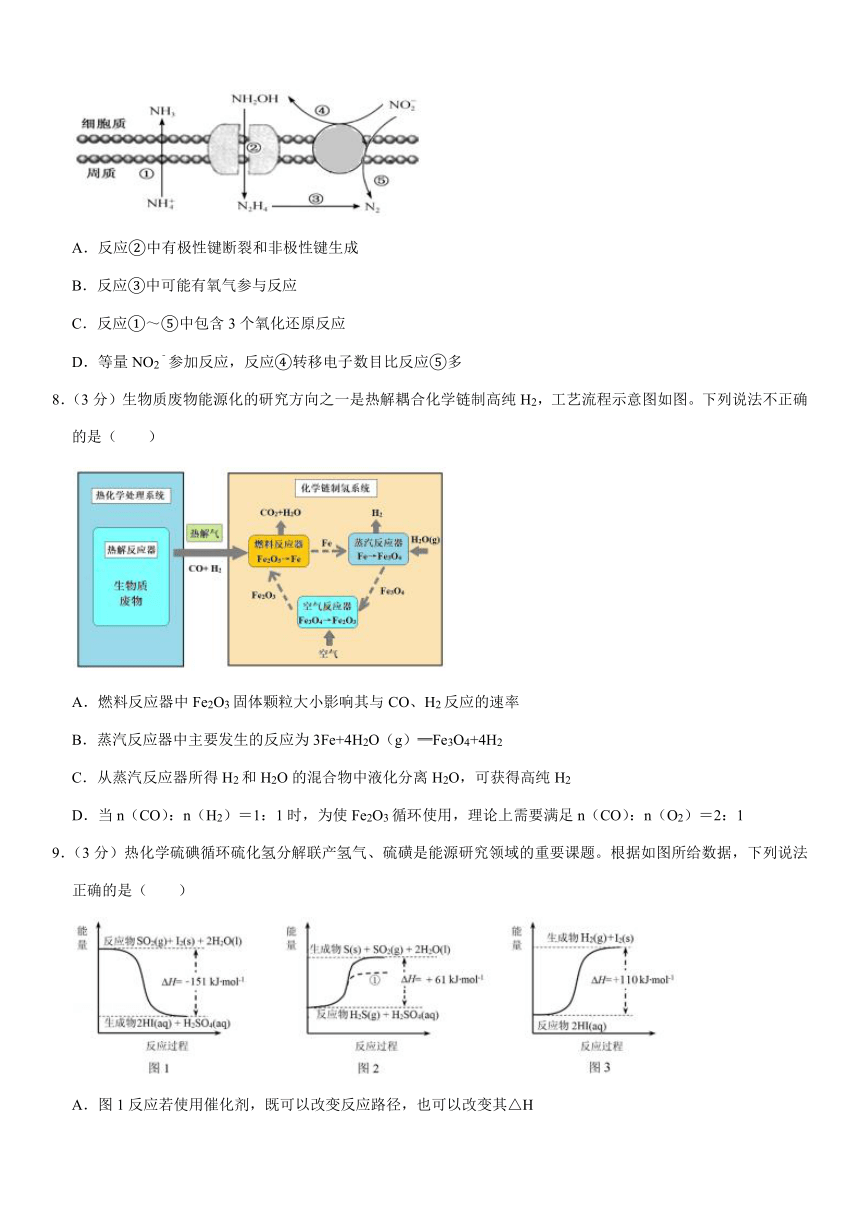
6.(3分)短周期元素G、M、W、X、Y、Z的原子半径及其最高正化合价随原子序数递增的变化如图所示,下列说法正确的是( )
A.碱性:GOH>XOH
B.还原性:HW>HZ>H2Y
C.酸性:HZO4<H2YO4
D.离子半径:M3﹣>W﹣>X+
7.(3分)海洋生物参与氮循环过程如图所示,下列说法不正确的是( )
A.反应②中有极性键断裂和非极性键生成
B.反应③中可能有氧气参与反应
C.反应①~⑤中包含3个氧化还原反应
D.等量NO2﹣参加反应,反应④转移电子数目比反应⑤多
8.(3分)生物质废物能源化的研究方向之一是热解耦合化学链制高纯H2,工艺流程示意图如图。下列说法不正确的是( )
A.燃料反应器中Fe2O3固体颗粒大小影响其与CO、H2反应的速率
B.蒸汽反应器中主要发生的反应为3Fe+4H2O(g)═Fe3O4+4H2
C.从蒸汽反应器所得H2和H2O的混合物中液化分离H2O,可获得高纯H2
D.当n(CO):n(H2)=1:1时,为使Fe2O3循环使用,理论上需要满足n(CO):n(O2)=2:1
9.(3分)热化学硫碘循环硫化氢分解联产氢气、硫磺是能源研究领域的重要课题。根据如图所给数据,下列说法正确的是( )
A.图1反应若使用催化剂,既可以改变反应路径,也可以改变其△H
B.图2中若H2O的状态为气态,则能量变化曲线可能为①
C.图3反应中反应物的总能量比生成物的总能量高
D.由图1、图2和图3可知,H2S(g)═H2(g)+S(s)△H=+20kJ?mol﹣1
10.(3分)实验小组同学制备KClO3并探究其性质,过程如图下列说法不正确的是( )
A.可用饱和NaCl溶液净化氯气
B.生成KClO3的离子方程式为3Cl2+6OH﹣ClO3﹣+5Cl﹣+3H2O
C.推测若取少量无色溶液a于试管中,滴加稀H2SO4后,溶液仍为无色
D.上述实验说明碱性条件下氧化性Cl2>KClO3,酸性条件下氧化性:Cl2<KClO3
11.(3分)25℃时,在20mL
0.1mol?L﹣1CH3COOH溶液中逐滴加入0.1mol?L﹣1NaOH溶液,pH变化曲线如图所示,下列说法不正确的是( )
A.若用10mL
H2O代替10mL
NaOH溶液,所得溶液pH小于a点
B.b点溶液中微粒浓度:c(Na+)>c(CH3COO﹣)>c(CH3COOH)
C.a点→c点的过程中n(CH3COO﹣)持续增大
D.若向a点对应的溶液中滴加1滴0.1mol?L﹣1NaOH溶液或1滴0.1mol?L﹣1醋酸溶液,pH变化均不大
12.(3分)向体积为10L的恒容密闭容器中通入1.1mol
CH4(g)和1.1mol
H2O(g)制备H2,反应原理为CH4(g)+H2O(g)?CO(g)+3H2(g)△H=+206.2kJ?mol﹣1。在不同温度(Ta、Tb)下测得容器中n(CO)随时间的变化曲线如图所示,下列说法正确的是( )
A.温度Ta<Tb
B.Ta时,0~4min内v(CH4)=0.25mol?L﹣1?min﹣1
C.Tb时,若改为恒温恒压容器,平衡时n(CO)>0.6mol
D.Tb时,平衡时再充入1.1mol
CH4,平衡常数增大
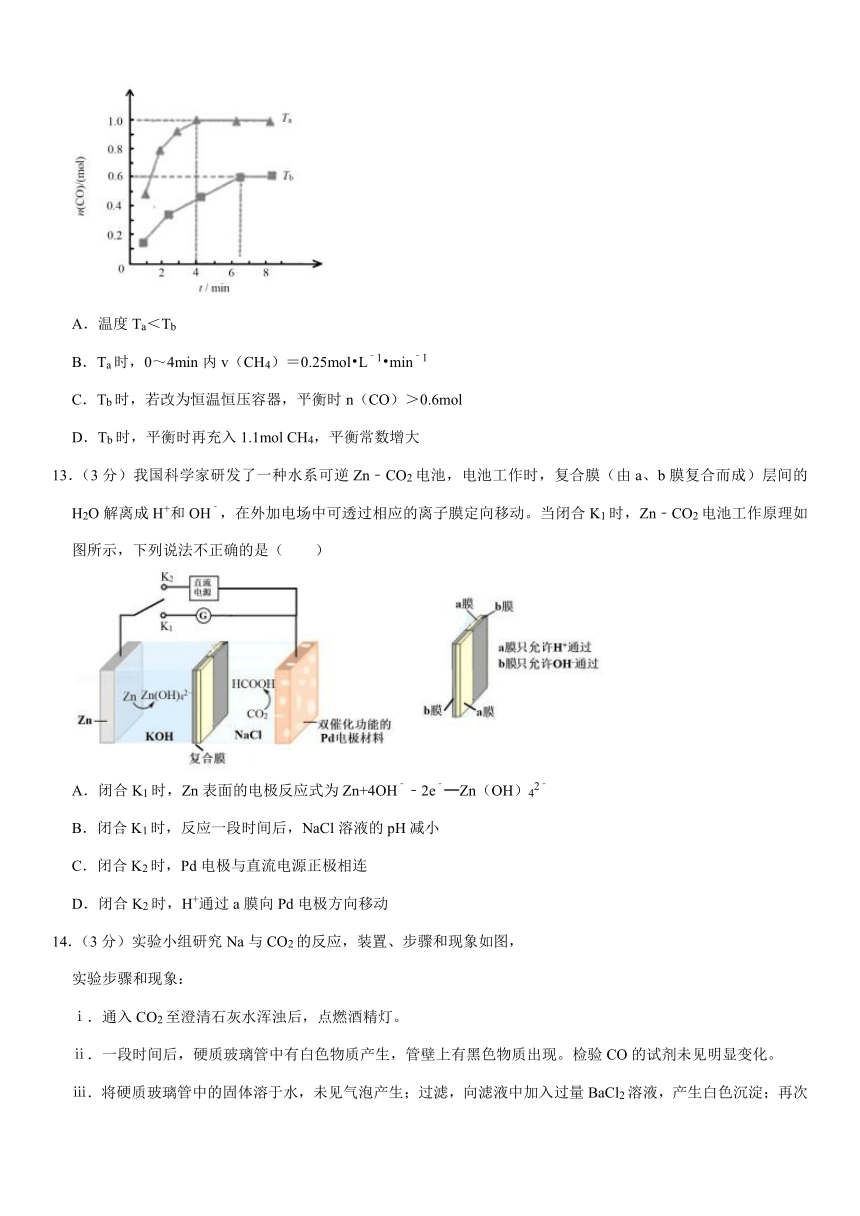
13.(3分)我国科学家研发了一种水系可逆Zn﹣CO2电池,电池工作时,复合膜(由a、b膜复合而成)层间的H2O解离成H+和OH﹣,在外加电场中可透过相应的离子膜定向移动。当闭合K1时,Zn﹣CO2电池工作原理如图所示,下列说法不正确的是( )
A.闭合K1时,Zn表面的电极反应式为Zn+4OH﹣﹣2e﹣═Zn(OH)42﹣
B.闭合K1时,反应一段时间后,NaCl溶液的pH减小
C.闭合K2时,Pd电极与直流电源正极相连
D.闭合K2时,H+通过a膜向Pd电极方向移动
14.(3分)实验小组研究Na与CO2的反应,装置、步骤和现象如图,
实验步骤和现象:
ⅰ.通入CO2至澄清石灰水浑浊后,点燃酒精灯。
ⅱ.一段时间后,硬质玻璃管中有白色物质产生,管壁上有黑色物质出现。检验CO的试剂未见明显变化。
ⅲ.将硬质玻璃管中的固体溶于水,未见气泡产生;过滤,向滤液中加入过量BaCl2溶液,产生白色沉淀;再次过滤,滤液呈碱性;取白色沉淀加入盐酸,产生气体。
ⅳ.将管壁上的黑色物质与浓硫酸混合加热,生成能使品红溶液褪色的气体。
下列说法不正确的是( )
A.步骤ⅰ的目的是排除O2的干扰
B.步骤ⅲ证明白色物质是Na2CO3
C.步骤ⅳ发生反应的化学方程式为C+2H2SO4(浓)CO2↑+2SO2↑+2H2O
D.根据以上实验推测:CO2与金属K也可以发生反应并被还原
二、解答题(共5小题,满分58分)
15.(10分)中国传统的农具、兵器曾大量使用铁,铁器的修复是文物保护的重要课题。
(1)潮湿环境中,铁器发生电化学腐蚀的负极反应式是
。
(2)铁器表面氧化层的成分有多种,性质如下:
成分
Fe3O4
FeO(OH)
FeOCl
性质
致密
疏松
疏松
①Fe(OH)2被空气氧化为Fe3O4的化学方程式是
。
②在有氧条件下,Fe3O4在含Cl﹣溶液中会转化为FeOCl,将相关反应的离子方程式补充完整:
4Fe3O4+O2+
+
H2O═
FeOCl+
。
(3)化学修复可以使FeOCl转化为Fe3O4致密保护层:用Na2SO3和NaOH混合溶液浸泡锈蚀的铁器,一段时间后取出,再用NaOH溶液反复洗涤。
①FeOCl在NaOH的作用下转变为FeO(OH),推测溶解度FeOCl
FeO(OH)(填“>”或“<”)。
②Na2SO3的作用是
。
③检验FeOCl转化完全的操作和现象是
。
16.(10分)硝酸是重要的化工原料,工业生产硝酸的流程如下图所示:
CH4H2NH3NONO2HNO3
已知:ⅰ.HNO3受热易分解为NO2、O2等物质;
ⅱ.原子利用率=。
(1)步骤Ⅰ:制高纯氢
①反应器中初始反应的生成物有两种,且物质的量之比为1:4,甲烷与水蒸气反应的化学方程式是
。
②所得H2中含有少量CO气体,影响后续反应催化剂活性,可利用如下反应吸收CO:[Cu(NH3)2]Ac(aq)+CO(g)+NH3(g)?[Cu(NH3)3]Ac?CO(aq)△H<0
(注:Ac﹣代表CH3COO﹣)
利于CO被吸收的反应条件有
(写出两点)。
(2)步骤Ⅱ:合成氨
①工业合成氨时,每生成1mol
NH3(g)放出46.1kJ热量,则合成氨的热化学方程式是
。
②用如图所示装置实现电化学合成氨。产生NH3的电极反应式是
。
(3)步骤Ⅲ和步骤Ⅳ均是放热反应,步骤Ⅴ在反应前需将NO2冷却。
①步骤Ⅴ的化学方程式是
。
②冷却NO2有利于提高HNO3产率,原因是
(写出一点即可)。
③提高由NH3转化为HNO3的整个过程中氮原子利用率的措施是
。
17.(12分)研究人员从处理废旧线路板后的固体残渣(含SnO2、PbO2等)中进一步回收金属锡(Sn),一种回收流程如图。
已知:ⅰ.50Sn、82Pb为ⅣA族元素。
ⅱ.SnO2、PbO2与强碱反应生成盐和水。
(1)Sn在空气中不反应,Pb在空气中表面生成一层氧化膜,结合原子结构解释原因
。
(2)SnO2与NaOH反应的化学方程式为
。
(3)滤液1中加入Na2S的目的是除铅,将相关方程式补充完整:
Na2PbO3+
Na2S+
═PbS↓+S↓+
(4)不同溶剂中Na2SnO3的溶解度随温度变化如图。
①相同温度下,Na2SnO3的溶解度随NaOH浓度增大而减小,结合平衡移动原理解释原因:
。
②操作Ⅲ的具体方法为
。
(5)测定粗锡中Sn的纯度:在强酸性环境中将ag粗锡样品溶解(此时Sn全部转化成Sn2+),迅速加入过量NH4Fe(SO4)2溶液,以二苯胺磺酸钠为指示剂,用cmol?L﹣1K2Cr2O7标准溶液滴定至终点。平行测定三次,消耗K2Cr2O7溶液的体积平均为vmL,计算Sn的纯度(Sn的摩尔质量为119g?mol﹣1)。
已知:Sn2++2Fe3+═Sn4++2Fe2+
Cr2O72﹣+6Fe2++14H+═2Cr3++6Fe3++7H2O
①溶解粗锡时不宜选用浓盐酸,理由是
。
②粗锡样品中Sn的纯度为
(用质量分数表示)。
18.(12分)将CO2转化成C2H4可以变废为宝、改善环境。以CO2、C2H6为原料合成C2H4涉及的主要反应如下:
Ⅰ.CO2(g)+C2H6(g)?C2H4(g)+H2O(g)+CO(g)△H=+177kJ?mol﹣1(主反应)
Ⅱ.C2H6(g)?CH4(g)+H2(g)+C(s)△H=+9kJ?mol﹣1(副反应)
(1)反应Ⅰ的反应历程可分为如下两步:
ⅰ.C2H6(g)?C2H4(g)+H2(g)△H1=+136kJ?mol﹣1(反应速率较快)
ⅱ.H2(g)+CO2(g)?H2O(g)+CO(g)△H2(反应速率较慢)
①△H2=
kJ?mol﹣1
②相比于提高c(C2H6),提高c(CO2)对反应Ⅰ速率影响更大,原因是
。
(2)0.1MPa时向密闭容器中充入CO2和C2H6,温度对催化剂K﹣Fe﹣Mn/Si﹣2性能的影响如图所示。
①工业生产中反应Ⅰ选择800℃,原因是
。
②800℃时,不同的CO2和C2H6体积比对反应影响的实验数据如下表:
v(CO2)/v(C2H6)
平衡时有机产物的质量分数
CH4
C2H4
15.0/15.0
7.7
92.3
20.0/10.0
6.4
93.6
24.0/6.0
4.5
95.5
a.随增大,CO2转化率将
(填“增大”或“减小”)。
b.解释对产物中C2H4的质量分数影响的原因:
。
(3)我国科学家使用电化学的方法(装置如图)用C2H6和CO2合成了C2H4。
①N是电源的
极。
②阳极电极反应式是
。
19.(14分)久置的Na2S固体会潮解、变质、颜色变黄,探究Na2S变质的产物。
资料:ⅰ.Na2S能与S反应生成Na2Sx(黄色),Na2Sx与酸反应生成S和H2S;
ⅱ.BaS、BaSx均易溶于水,H2S可溶于水,BaS2O3微溶于水;
ⅲ.白色的Ag2S2O3难溶于水,且易转化为黑色Ag2S。
将久置的Na2S固体溶于水,溶液呈黄色。取黄色溶液,滴加稀硫酸,产生白色沉淀(经检验该沉淀含S)。
(1)推测Na2S变质的产物含有Na2Sx,实验证据是
。
(2)研究白色沉淀产生的途径,实验小组同学进行如下假设:
途径一:白色沉淀由Na2Sx与稀硫酸反应产生。
途径二:Na2S变质的产物中可能含有Na2S2O3,白色沉淀由Na2S2O3与稀硫酸反应产生。
途径三:Na2S变质的产物中可能含有Na2SO3,白色沉淀由……。
①Na2S2O3与稀硫酸反应的化学方程式是
。
②请将途径三补充完全:
。
(3)为检验Na2S变质的产物中是否含有Na2S2O3,设计实验:
①取黄色溶液,向其中滴加AgNO3溶液,产生黑色沉淀。由此得出结论:Na2S变质的产物中含Na2S2O3。有同学认为得出该结论的理由不充分,原因是
。
②改进实验,方案和现象如下:
实验一:
实验二:
a.实验一的目的是
。
b.试剂1是
,试剂2是
。
(4)检验Na2S变质的产物中是否含有Na2SO4:取黄色溶液,加入过量稀盐酸,产生白色沉淀。离心沉降(分离固体)后向溶液中滴加BaCl2溶液,产生白色沉淀。你认为能否根据实验现象得出结论?说明理由:
。
2020-2021学年北京市朝阳区高三(上)期中化学试卷
试题解析
一、本部分共14题,每题3分,共42分。在每题列出的四个选项中,选出最符合题目要求的一项。
1.【答案】B
【解答】解:A.二氧化硅属于非金属氧化物,不是金属材料,故A错误;
B.钛合金是钛的合金,属于金属材料,故B正确;
C.聚酰胺属于有机高分子材料,不是金属材料,故C错误;
D.水泥属于无机硅酸盐材料,不是金属材料,故D错误;
故选:B。
2.【答案】A
【解答】解:A.中子数为16的硫离子的质量数是16+16=32,所以中子数为16的硫原子:S,故A正确;
B.纯碱是Na2CO3的俗名,故B错误;
C.二氧化碳为共价化合物,其分子中含有两个碳氧双键,二氧化碳的电子式为:,故C错误;
D.铝离子的核外有10个电子,铝离子的结构示意图为:,故D错误;
故选:A。
3.【答案】D
【解答】解:A.7.1g
Cl2的物质的量为:=0.1mol,由于反应后溶液中还存在Cl2,则转移电子的物质的量小于0.1mol,转移的电子数小于0.1NA,故A错误;
B.1L
0.1mol?L﹣1乙酸溶液中含有乙酸的物质的量为:0.1mol/L×1L=0.1mol,乙酸为弱酸,只能部分电离出氢离子,则溶液中含H+的数目小于0.1NA,故B错误;
C.标准状况下,22.4L
CH4为1mol,完全燃烧生成1mol二氧化碳和2mol水,由于标况下水为液态,则所得产物中气体分子数为NA,故C错误;
D.Na2CO3溶液中的OH﹣完全来自水的电离,该溶液中OH﹣的浓度为0.001mol/L,由水电离出的OH﹣的物质的量为:0.001mol/L×1L=0.001mol,数目为0.001NA,故D正确;
故选:D。
4.【答案】B
【解答】解:A.氯化铁溶液中加入铁粉会生成氯化亚铁,其反应的离子方程式为:2Fe3++Fe=3Fe2+,故A正确;
B.硫酸铝溶液中加入过量氨水的离子反应为Al3++3NH3?H2O=Al(OH)3↓+3NH4+,故B错误;
C.高锰酸钾酸性溶液与草酸溶液反应,离子方程式:2MnO4﹣+5H2C2O4+6H+═2Mn2++10CO2↑+8H2O,故C正确;
D.用过氧化氢从酸化的海带灰浸出液中提取碘,双氧水与过氧化氢发生氧化还原反应,反应的离子方程式为:2I﹣+H2O2+2H+═I2+2H2O,故D正确;
故选:B。
5.【答案】A
【解答】解:A.加热氯化铵分解,在试管口化合生成氯化铵,不能制备氨气,应选氯化铵与碱石灰加热制备,故A错误;
B.乙酸乙酯和碳酸钠溶液分层,可选分液漏斗分离,故B正确;
C.在HCl气体中可抑制镁离子水解,可制备无水氯化镁,故C正确;
D.醋酸钠水解显碱性,测定盐溶液的pH可证明醋酸为弱酸,故D正确;
故选:A。
6.【答案】D
【解答】解:A.金属性Na>Li,NaOH的碱性比LiOH强,故A错误;
B.非金属性F>Cl>S,元素的非金属性越强,对应的氢化物的还原性越弱,故B错误;
C.非金属性Cl>S,非金属性越强,对应的最高价氧化物的水化物的酸性越强,故C错误;
D.三种离子具有相同的核外电子排布,核电荷数越大离子半径越小,故D正确。
故选:D。
7.【答案】C
【解答】解:A.反应②中,NH2OH中存在极性键,反应时有极性键断裂,生成物N2H4中含有非极性键,则反应中有N﹣N非极性键生成,故A正确;
B.反应③N2H4中N元素的化合价升高,被氧化,氧气可以氧化N2H4,则可能有氧气参与反应,故B正确;
C.反应②③④⑤中,都存在N元素化合价的变化,均属于氧化还原反应,所以反应①~⑤中包含4个氧化还原反应,故C错误;
D.反应④中N元素的化合价从+3价降低到﹣3价,反应⑤中N元素的化合价从+3价降低到0价,则等量NO2﹣参加反应,反应④转移电子数目比反应⑤多,故D正确。
故选:C。
8.【答案】D
【解答】解:A.燃料反应器中Fe2O3固体颗粒越小,接触面积越大,反应速率越快,故A正确;
B.根据图示,蒸汽反应器中铁和水蒸气反应生成四氧化三铁和氢气,发生的反应为3Fe+4H2O(g)═Fe3O4+4H2,故B正确;
C.H2O的沸点比H2高得多,从蒸汽反应器所得H2和H2O的混合物中液化分离H2O,可获得高纯H2,故C正确;
D.根据氧元素守恒分析,反应体系有水蒸气通入,为使Fe2O3循环使用,理论上需要满足n(CO):n(O2)>2:1,故D错误;
故选:D。
9.【答案】D
【解答】解:A.图1反应若使用催化剂,可以改变反应路径,不改变其△H,焓变和反应路径无关,故A错误;
B.该反应反应物的总能量大于生成物的总能量,为吸热反应,而液态水转化为气态水还要吸收热量,所以能量变化曲线还要在生成物上方,故B错误;
C.该图象表示的反应物的总能量比生成物的总能量低,为吸热反应,故C错误;
D.已知①SO2(g)+I2(s)+2H2O(l)═2HI(aq)+H2S
O4(aq)△H1=﹣151kJ?mol﹣1,
②H2S
(g)+H2S
O4(aq)═S(s)+SO2(g)+2H2O(l)△H3=+61kJ?mol﹣1,
③2HI(aq)═H2(g)+I2(s)△H2=+110kJ?mol﹣1,
根据盖斯定律由①+②+③可得反应H2S
(g)=H2(g)+S(s),由此计算反应的△H,则△H=△H1+△H2﹣△H3=(61kJ?mol﹣1)+(﹣151kJ?mol﹣1)+(110kJ?mol﹣1)=20kJ?mol﹣1,此反应的热化学方程式为H2S
(g)=H2(g)+S(s)△H=+20kJ?mol﹣1,故D正确;
故选:D。
10.【答案】C
【解答】解:A.浓盐酸易挥发,可用饱和NaCl溶液净化氯气,故A正确;
B.生成KClO3时只有Cl元素的化合价变化,离子方程式为3Cl2+6OH﹣ClO3﹣+5Cl﹣+3H2O,故B正确;
C.若取少量无色溶液a于试管中,滴加稀H2SO4后,Cl﹣、IO3﹣发生氧化还原反应生成碘,溶液为黄色,故C错误;
D.由氯气与KOH的反应、氯酸钾与盐酸的反应,结合氧化剂的氧化性大于氧化产物的氧化性可知,上述实验说明碱性条件下氧化性Cl2>KClO3,酸性条件下氧化性:Cl2<KClO3,故D正确;
故选:C。
11.【答案】B
【解答】解:A.a点溶质CH3COOH和CH3COONa的混合液,pH=5,若用10mL
H2O代替10mL
NaOH溶液,开始pH=3,仅仅稀释0.5倍,pH<4,故A正确;
B.b点溶液pH=7,c(H+)=c(OH﹣),满足c(Na+)+c(H+)=c(OH﹣)+c(CH3COO﹣),b点时有c(CH3COO﹣)=c(Na+),故B错误;
C.a点是c(H+)=10﹣4mol/L,a
点溶液中
c(CH3COO﹣)约为
10﹣4mol?L﹣1,c点溶液为二者恰好反应点,c(CH3COO﹣)>c(Na+)≈0.05mol?L﹣1,a点→c点的过程中n(CH3COO﹣)持续增大,故C正确;
D.醋酸的电离是可逆反应:CH3COOH?CH3COO﹣+H+,向a点对应的溶液中滴加1滴0.1mol?L﹣1NaOH溶液或1滴0.1mol?L﹣1醋酸溶液,平衡正向移动,且量很小,氢离子浓度基本不变,所以pH变化均不大,故D正确;
故选:B。
12.【答案】C
【解答】解:A.根据“先拐先平数值大”知,其它条件相同时温度高的先达到平衡状态,根据图知Ta条件下先达到平衡状态,所以Ta>Tb,故A错误;
B.Ta时,0~4min内v(CO)==mol?L﹣1?min﹣1=0.0125mol?L﹣1?min﹣1,相同时间内v(CH4)=v(CO)=0.0125mol?L﹣1?min﹣1,故B错误;
C.图中Tb时为恒温恒容条件下发生的反应,随着反应进行气体物质的量增大导致容器内压强增大,如果改为恒温恒压条件下,与原来相比相当于减小压强,减小压强平衡正向移动,反应物的转化率增大,所以平衡时n(CO)>0.6mol,故C正确;
D.平衡常数只与温度有关,Tb时,平衡时再充入1.1mol
CH4,平衡正向移动但温度不变平衡常数不变,故D错误;
故选:C。
13.【答案】D
【解答】解:A.闭合K1时为原电池,Zn发生失电子的氧化反应生成Zn(OH)42﹣,则Zn电极为负极,电极反应式为Zn+4OH﹣﹣2e﹣═Zn(OH)42﹣,故A正确;
B.闭合K1时为原电池,Zn电极为负极,Pd电极为正极,正极反应式为CO2+2e﹣+2H+═HCOOH,生成甲酸,溶液的酸性增强,NaCl溶液的pH减小,故B正确;
C.Zn﹣CO2电池中Zn电极为负极,Pd电极为正极,闭合K2时为电解池,Pd电极为阳极,与直流电源正极相连,故C正确;
D.闭合K2时为电解池,Pd电极为阳极,Zn电极为阴极,复合膜层间的H2O解离成的H+通过a膜移向Zn电极,OH﹣通过b膜向Pd电极方向移动,故D错误;
故选:D。
14.【答案】B
【解答】解:A.实验时先通入二氧化碳,可将装置内的氧气排出,避免干扰实验,故A正确;
B.由实验iii可知,滤液呈碱性,说明生成氢氧化钠,则白色物质含有碳酸钠和氧化钠,故B错误;
C.黑色固体为碳,加热条件下与浓硫酸反应生成二氧化碳、二氧化硫和水,方程式为C+2H2SO4(浓)CO2↑+2SO2↑+2H2O,故C正确;
D.K的活泼性比Na强,具有相似的化学性质,则CO2与金属K也可以发生反应并被还原,故D正确。
故选:B。
二、解答题(共5小题,满分58分)
15.【答案】(1)Fe﹣2e﹣═Fe2+;
(2)①6Fe(OH)2+O2═2Fe3O4+6H2O;
②12Cl﹣;6;12;12OH﹣;
(3)①>;
②作还原剂,将FeOCl还原为Fe3O4;
③取最后一次的洗涤液于试管中,加入HNO3酸化,再加入AgNO3溶液,无白色沉淀产生,证明FeOCl转化完全。
【解答】解:(1)反应中铁是负极,发生氧化反应,生成Fe2+,负极反应式是:Fe﹣2e﹣=Fe2+,
故答案为:Fe﹣2e﹣=Fe2+;
(2)①Fe(OH)2被空气中氧气氧化,生成四氧化三铁和水,反应的化学方程式:6Fe(OH)2+O2═2Fe3O4+6H2O,
故答案为:6Fe(OH)2+O2═2Fe3O4+6H2O;
②反应中O2中O元素的化合价降低4,Fe3O4中3个Fe的化合价共升高1,根据化合价升降守恒可知,Fe3O4的计量数为4,O2的计量数为1,反应的离子方程式:4Fe3O4+O2+12Cl﹣+6H2O═12FeOCl+12OH﹣,
故答案为:12Cl﹣;6;12;12OH﹣;
(3)①化学反应有从溶解度小的物质转化为溶解度更小的趋势,由于不溶物FeOCl→FeO(OH),所以FeOCl的溶解度大于FeO(OH),
故答案为:>;
②Na2SO3还原FeOCl生成Fe3O4,反应为:SO32﹣+6FeOCl+3H2O=SO42﹣+2Fe3O4+6H++6Cl﹣,
故答案为:作还原剂,将FeOCl还原为Fe3O4;
③检验FeOCl转化完全需检验Cl﹣,操作和现象是:取最后一次的洗涤液于试管中,加入HNO3酸化,再加入AgNO3溶液,无白色沉淀产生,证明FeOCl转化完全,
故答案为:取最后一次的洗涤液于试管中,加入HNO3酸化,再加入AgNO3溶液,无白色沉淀产生,证明FeOCl转化完全。
16.【答案】(1)①CH4+2H2O═4H2+CO2;
②降低温度,增大压强(或增大[Cu(NH3)2]Ac(aq)浓度,或增大NH3浓度);
(2)①N2(g)+3H2(g)?2NH3(g)
ΔH=﹣92.2kJ?mol﹣1;
②N2+6H++6e﹣═2NH3;
(3)①3NO2+H2O═2HNO3+NO;
②防止温度高造成HNO3分解(或温度高NO2溶解度降低);
③通入过量的O2,使生成的NO全部转化为硝酸。
【解答】解:(1)①甲烷与水蒸气反应有2种产物,其中一种是H2,且生成物的物质的量之比为1:4,则另一种产物是CO2,故化学方程式为CH4+2H2O═4H2+CO2,
故答案为:CH4+2H2O═4H2+CO2;
②利于CO被吸收就是要增大CO的转化率,降低温度、增大压强、增大[Cu(NH3)2]Ac(aq)浓度或增大NH3浓度均可使平衡向右移动,增大CO的转化率,所以降低温度,增大压强(或增大[Cu(NH3)2]Ac(aq)浓度,或增大NH3浓度)有利于CO被吸收,
故答案为:降低温度,增大压强(或增大[Cu(NH3)2]Ac(aq)浓度,或增大NH3浓度);
(2)①每生成1mol
NH3(g)放出46.1kJ热量,则每生成2mol
NH3(g)的热效应为ΔH=﹣46.1kJ?mol﹣1×2=﹣92.2kJ?mol﹣1,所以合成氨的热化学方程式为N2(g)+3H2(g)?2NH3(g)
ΔH=﹣92.2kJ?mol﹣1,
故答案为:N2(g)+3H2(g)?2NH3(g)
ΔH=﹣92.2kJ?mol﹣1;
②电极上反应物为N2和H+,产物为NH3,N的化合价降低须得电子,所以电极反应式为N2+6H++6e﹣═2NH3,
故答案为:N2+6H++6e﹣═2NH3;
(3)①步骤Ⅴ是NO2和H2O反应生成HNO3,产物除了HNO3外,还有NO,所以方程式为3NO2+H2O═2HNO3+NO,
故答案为:3NO2+H2O═2HNO3+NO;
②冷却NO2有利于提高HNO3产率,是因为HNO3受热易分解为NO2、O2等物质,另外,温度高也会降低NO2在水中溶解度,从而降低HNO3产率,因此冷却NO2有利于提高HNO3产率是因为防止温度高造成HNO3分解(或温度高NO2溶解度降低),
故答案为:防止温度高造成HNO3分解(或温度高NO2溶解度降低);
③NH3转化为HNO3的整个过程中,要想提高N原子的利用率,就要尽可能的使N原子全部转入HNO3中,并且最后一步NO2和H2O也生成了部分NO,所以可通入过量的O2,使生成的NO全部转化为硝酸,
故答案为:通入过量的O2,使生成的NO全部转化为硝酸。
17.【答案】(1)Sn和Pb均为第IVA元素,核电荷数Pb>Sn,电子层数Pb>Sn,原子半径Pb>Sn,失电子能力Pb>Sn,金属性Pb>Sn;
(2)SnO2+2NaOH═Na2SnO3+H2O;
(3)2;3;H2O;6;NaOH;
(4)①随着NaOH溶液浓度增大,c(Na+)增大,Na2SnO3溶解平衡:Na2SnO3(s)?2Na+(aq)+SnO32﹣(aq)逆向移动,使得Na2SnO3溶解度减小;
②蒸发结晶、趁热过滤;
(5)①K2Cr2O7酸性溶液可以氧化Cl﹣,产生实验误差;
②%。
【解答】解:(1)Sn在空气中不反应,Pb在空气中表面生成一层氧化膜,结合原子结构解释原因为Sn和Pb均为第IVA元素,核电荷数Pb>Sn,电子层数Pb>Sn,原子半径Pb>Sn,失电子能力Pb>Sn,金属性Pb>Sn,
故答案为:Sn和Pb均为第IVA元素,核电荷数Pb>Sn,电子层数Pb>Sn,原子半径Pb>Sn,失电子能力Pb>Sn,金属性Pb>Sn;
(2)SnO2与NaOH反应的化学方程式为SnO2+2NaOH═Na2SnO3+H2O,
故答案为:SnO2+2NaOH═Na2SnO3+H2O;
(3)滤液1中加入Na2S的目的是除铅,Pb元素的化合价降低,S元素的化合价升高,由电子及原子守恒可知反应为Na2PbO3+2Na2S+3H2O═PbS↓+S↓+6NaOH,
故答案为:2;3;H2O;6;NaOH;
(4)①相同温度下,Na2SnO3的溶解度随NaOH浓度增大而减小,结合平衡移动原理解释原因为随着NaOH溶液浓度增大,c(Na+)增大,Na2SnO3溶解平衡:Na2SnO3(s)?2Na+(aq)+SnO32﹣(aq)逆向移动,使得Na2SnO3溶解度减小,
故答案为:随着NaOH溶液浓度增大,c(Na+)增大,Na2SnO3溶解平衡:Na2SnO3(s)?2Na+(aq)+SnO32﹣(aq)逆向移动,使得Na2SnO3溶解度减小;
②由图可知,溶剂为水时随温度升高溶解度减小,则操作Ⅲ的具体方法为蒸发结晶、趁热过滤,
故答案为:蒸发结晶、趁热过滤;
(5)①溶解粗锡时不宜选用浓盐酸,理由是K2Cr2O7酸性溶液可以氧化Cl﹣,产生实验误差,
故答案为:K2Cr2O7酸性溶液可以氧化Cl﹣,产生实验误差;
②由Sn2++2Fe3+═Sn4++2Fe2+、Cr2O72﹣+6Fe2++14H+═2Cr3++6Fe3++7H2O可知存在3Sn2+~Cr2O72﹣,粗锡样品中Sn的纯度为×100%=%,
故答案为:%。
18.【答案】(1)①+41;
②反应ii为反应I的决速步,c(CO2)增大,反应ii速率加快,从而提高反应I速率;
(2)①800℃时,C2H4选择性比780℃略有降低,但CO2的转化率增大较多,有利于提高C2H4的产率;800℃时,C2H4选择性与820℃相比选择性略高;
②a.减小;
b.随增大,c(CO2)增大,c(C2H6)减小;c(CO2)增大促进反应I平衡正移,反应消耗的C2H6增多,也使c(C2H6)减小,反应II平衡逆移;上述因素导致产物中C2H4质量分数增大;
(3)①负;
②C2H6+O2﹣﹣2e﹣═C2H4+H2O。
【解答】解:(1)①ⅠC2H6(g)?C2H4(g)+H2(g)△H1=+136kJ?mol﹣1,
ⅡH2(g)+CO2(g)?H2O(g)+CO(g)△H2,
ⅢCO2(g)+C2H6(g)?C2H4(g)+H2O(g)+CO(g)△H=+177kJ?mol﹣1,
由盖斯定律可知,②=③﹣①,△H2=△H﹣△H1=+177kJ?mol﹣1﹣(+136kJ?mol﹣1)=+41kJ/mol,
②反应ⅱ.H2(g)+CO2(g)?H2O(g)+CO(g)△H2
反应速率较慢,对整个反应速率影响最大,反应ⅱ为反应Ⅰ的决速度,c(CO2)增大,反应ii速率加快,从而提高反应I速率,
故答案为:反应ⅱ为反应Ⅰ的决速度,c(CO2)增大,反应ii速率加快,从而提高反应I速率;
(2)①工业生产中反应Ⅰ选择800℃,原因是:800℃时,C2H4选择性比780℃略有降低,但CO2的转化率增大较多,有利于提高C2H4的产率;800℃时,C2H4选择性与820℃相比选择性略高,
故答案为:800℃时,C2H4选择性比780℃略有降低,但CO2的转化率增大较多,有利于提高C2H4的产率;800℃时,C2H4选择性与820℃相比选择性略高;
a.随增大,相当于在反应体系中增大二氧化碳的量,则平衡正向移动,但CO2转化率将减小,
故答案为:减小;
b.随增大,c(CO2)增大,c(C2H6)减小。c(CO2)增大促进反应Ⅰ平衡右移,反应消耗的C2H6增多,也使c(C2H6)减小,反应II平衡左移,上述因素导致产物中C2H4质量分数增大,
故答案为:随增大,c(CO2)增大,c(C2H6)减小。c(CO2)增大促进反应Ⅰ平衡右移,反应消耗的C2H6增多,也使c(C2H6)减小,反应II平衡左移,上述因素导致产物中C2H4质量分数增大;
(3)①N极CO2→CO,化合价降低,得电子,被还原,为负极,
故答案为:负;
②阳极C2H6→C2H4,失去2个电子且消耗氧离子,电极反应式为:C2H6+O2﹣﹣2e﹣═C2H4+H2O,
故答案为:C2H6+O2﹣﹣2e﹣═C2H4+H2O。
19.【答案】(1)溶液呈黄色;
(2)①Na2S2O3+H2SO4═Na2SO4+SO2↑+S↓+H2O;
②白色沉淀由SO32﹣与S2﹣在酸性条件下反应产生(或白色沉淀由生成的H2S与SO2反应产生);
(3)①剩余的Na2S也能与AgNO3溶液反应生成黑色的Ag2S沉淀;
②a.确认Ag2SO4和Ag2SO3都不易转化为黑色固体,排除SO42﹣、SO32﹣对S2O32﹣检验的干扰;
b.BaCl2溶液;AgNO3溶液;
(4)可以,稀盐酸将S2O32﹣、SO32﹣等除去,不会产生干扰;或:不可以,检验过程中H2S等低价含硫物质被O2氧化。
【解答】解:(1)如含有Na2Sx,则溶液成黄色,
故答案为:溶液呈黄色;
(2)①Na2S2O3与稀硫酸反应生成硫酸钠、二氧化硫和硫,反应的化学方程式为Na2S2O3+H2SO4═Na2SO4+SO2↑+S↓+H2O,
故答案为:Na2S2O3+H2SO4═Na2SO4+SO2↑+S↓+H2O;
②Na2S变质的产物中可能含有Na2SO3,二者在酸性条件下发生氧化还原反应生成硫,或白色沉淀由生成的H2S与SO2反应产生,
故答案为:白色沉淀由SO32﹣与S2﹣在酸性条件下反应产生(或白色沉淀由生成的H2S与SO2反应产生);
(3)①固体中含有硫化钠,硫化钠和硝酸银反应生成硫化银沉淀,为黑色固体,
故答案为:剩余的Na2S也能与AgNO3溶液反应生成黑色的Ag2S沉淀;
②a.实验一加入亚硫酸钠、硫酸钠,与硝酸银反应生成白色沉淀,可排除SO42﹣、SO32﹣对S2O32﹣检验的干扰,
故答案为:确认Ag2SO4和Ag2SO3都不易转化为黑色固体,排除SO42﹣、SO32﹣对S2O32﹣检验的干扰;
b.黄色溶液含有Na2Sx,如含有含有Na2S2O3,可加入氯化钡溶液,生成白色沉淀为BaS2O3,然后加入硝酸银溶液,可生成白色的Ag2S2O3,然后转化为Ag2S,
故答案为:BaCl2溶液;AgNO3溶液;
(4)可能有两种情况,加入稀盐酸,可将S2O32﹣、SO32﹣等除去,对实验无影响,但检验过程中H2S等低价含硫物质被O2氧化,则不可以,
故答案为:可以,稀盐酸将S2O32﹣、SO32﹣等除去,不会产生干扰;或:不可以,检验过程中H2S等低价含硫物质被O2氧化。
一、本部分共14题,每题3分,共42分。在每题列出的四个选项中,选出最符合题目要求的一项。
1.(3分)2020年7月23日我国首个火星探测器“天问一号”发射成功。火星车所涉及的下列材料中属于金属材料的是( )
A.探测仪镜头材料﹣﹣二氧化硅
B.车轮材料﹣﹣钛合金
C.温控涂层材料﹣﹣聚酰胺
D.太阳能电池复合材料﹣﹣石墨纤维和硅
2.(3分)下列有关化学用语表述正确的是( )
A.中子数为16的硫原子:S
B.纯碱的化学式:NaHCO3
C.CO2的电子式:
D.Al3+的结构示意图:
3.(3分)设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.常温下,将7.1g
Cl2通入水中,转移的电子数为0.1NA
B.1L
0.1mol?L﹣1乙酸溶液中含H+的数目为0.1NA
C.标准状况下,22.4L
CH4完全燃烧后恢复至原状态,所得产物中气体分子数为3NA
D.25℃时,1L
pH=11的Na2CO3溶液中由水电离出的OH﹣的数目为0.001NA
4.(3分)下列实验所涉及反应的离子方程式不正确的是( )
A.向氯化铁溶液中加入铁粉:2Fe3++Fe═3Fe2+
B.向硫酸铝溶液中加入过量氨水:Al3++4OH﹣═AlO2﹣+2H2O
C.向草酸溶液中滴加几滴高锰酸钾酸性溶液:2MnO4﹣+5H2C2O4+6H+═2Mn2++10CO2↑+8H2O
D.向海带灰浸出液中滴加几滴硫酸酸化的过氧化氢溶液:2I﹣+H2O2+2H+═I2+2H2O
5.(3分)用下列仪器或装置(夹持装置略)进行实验,不能达到实验目的的是( )
A.实验室制取氨气
B.分离乙酸乙酯和碳酸钠溶液
C.制备无水氯化镁
D.证明醋酸为弱酸
6.(3分)短周期元素G、M、W、X、Y、Z的原子半径及其最高正化合价随原子序数递增的变化如图所示,下列说法正确的是( )
A.碱性:GOH>XOH
B.还原性:HW>HZ>H2Y
C.酸性:HZO4<H2YO4
D.离子半径:M3﹣>W﹣>X+
7.(3分)海洋生物参与氮循环过程如图所示,下列说法不正确的是( )
A.反应②中有极性键断裂和非极性键生成
B.反应③中可能有氧气参与反应
C.反应①~⑤中包含3个氧化还原反应
D.等量NO2﹣参加反应,反应④转移电子数目比反应⑤多
8.(3分)生物质废物能源化的研究方向之一是热解耦合化学链制高纯H2,工艺流程示意图如图。下列说法不正确的是( )
A.燃料反应器中Fe2O3固体颗粒大小影响其与CO、H2反应的速率
B.蒸汽反应器中主要发生的反应为3Fe+4H2O(g)═Fe3O4+4H2
C.从蒸汽反应器所得H2和H2O的混合物中液化分离H2O,可获得高纯H2
D.当n(CO):n(H2)=1:1时,为使Fe2O3循环使用,理论上需要满足n(CO):n(O2)=2:1
9.(3分)热化学硫碘循环硫化氢分解联产氢气、硫磺是能源研究领域的重要课题。根据如图所给数据,下列说法正确的是( )
A.图1反应若使用催化剂,既可以改变反应路径,也可以改变其△H
B.图2中若H2O的状态为气态,则能量变化曲线可能为①
C.图3反应中反应物的总能量比生成物的总能量高
D.由图1、图2和图3可知,H2S(g)═H2(g)+S(s)△H=+20kJ?mol﹣1
10.(3分)实验小组同学制备KClO3并探究其性质,过程如图下列说法不正确的是( )
A.可用饱和NaCl溶液净化氯气
B.生成KClO3的离子方程式为3Cl2+6OH﹣ClO3﹣+5Cl﹣+3H2O
C.推测若取少量无色溶液a于试管中,滴加稀H2SO4后,溶液仍为无色
D.上述实验说明碱性条件下氧化性Cl2>KClO3,酸性条件下氧化性:Cl2<KClO3
11.(3分)25℃时,在20mL
0.1mol?L﹣1CH3COOH溶液中逐滴加入0.1mol?L﹣1NaOH溶液,pH变化曲线如图所示,下列说法不正确的是( )
A.若用10mL
H2O代替10mL
NaOH溶液,所得溶液pH小于a点
B.b点溶液中微粒浓度:c(Na+)>c(CH3COO﹣)>c(CH3COOH)
C.a点→c点的过程中n(CH3COO﹣)持续增大
D.若向a点对应的溶液中滴加1滴0.1mol?L﹣1NaOH溶液或1滴0.1mol?L﹣1醋酸溶液,pH变化均不大
12.(3分)向体积为10L的恒容密闭容器中通入1.1mol
CH4(g)和1.1mol
H2O(g)制备H2,反应原理为CH4(g)+H2O(g)?CO(g)+3H2(g)△H=+206.2kJ?mol﹣1。在不同温度(Ta、Tb)下测得容器中n(CO)随时间的变化曲线如图所示,下列说法正确的是( )
A.温度Ta<Tb
B.Ta时,0~4min内v(CH4)=0.25mol?L﹣1?min﹣1
C.Tb时,若改为恒温恒压容器,平衡时n(CO)>0.6mol
D.Tb时,平衡时再充入1.1mol
CH4,平衡常数增大
13.(3分)我国科学家研发了一种水系可逆Zn﹣CO2电池,电池工作时,复合膜(由a、b膜复合而成)层间的H2O解离成H+和OH﹣,在外加电场中可透过相应的离子膜定向移动。当闭合K1时,Zn﹣CO2电池工作原理如图所示,下列说法不正确的是( )
A.闭合K1时,Zn表面的电极反应式为Zn+4OH﹣﹣2e﹣═Zn(OH)42﹣
B.闭合K1时,反应一段时间后,NaCl溶液的pH减小
C.闭合K2时,Pd电极与直流电源正极相连
D.闭合K2时,H+通过a膜向Pd电极方向移动
14.(3分)实验小组研究Na与CO2的反应,装置、步骤和现象如图,
实验步骤和现象:
ⅰ.通入CO2至澄清石灰水浑浊后,点燃酒精灯。
ⅱ.一段时间后,硬质玻璃管中有白色物质产生,管壁上有黑色物质出现。检验CO的试剂未见明显变化。
ⅲ.将硬质玻璃管中的固体溶于水,未见气泡产生;过滤,向滤液中加入过量BaCl2溶液,产生白色沉淀;再次过滤,滤液呈碱性;取白色沉淀加入盐酸,产生气体。
ⅳ.将管壁上的黑色物质与浓硫酸混合加热,生成能使品红溶液褪色的气体。
下列说法不正确的是( )
A.步骤ⅰ的目的是排除O2的干扰
B.步骤ⅲ证明白色物质是Na2CO3
C.步骤ⅳ发生反应的化学方程式为C+2H2SO4(浓)CO2↑+2SO2↑+2H2O
D.根据以上实验推测:CO2与金属K也可以发生反应并被还原
二、解答题(共5小题,满分58分)
15.(10分)中国传统的农具、兵器曾大量使用铁,铁器的修复是文物保护的重要课题。
(1)潮湿环境中,铁器发生电化学腐蚀的负极反应式是
。
(2)铁器表面氧化层的成分有多种,性质如下:
成分
Fe3O4
FeO(OH)
FeOCl
性质
致密
疏松
疏松
①Fe(OH)2被空气氧化为Fe3O4的化学方程式是
。
②在有氧条件下,Fe3O4在含Cl﹣溶液中会转化为FeOCl,将相关反应的离子方程式补充完整:
4Fe3O4+O2+
+
H2O═
FeOCl+
。
(3)化学修复可以使FeOCl转化为Fe3O4致密保护层:用Na2SO3和NaOH混合溶液浸泡锈蚀的铁器,一段时间后取出,再用NaOH溶液反复洗涤。
①FeOCl在NaOH的作用下转变为FeO(OH),推测溶解度FeOCl
FeO(OH)(填“>”或“<”)。
②Na2SO3的作用是
。
③检验FeOCl转化完全的操作和现象是
。
16.(10分)硝酸是重要的化工原料,工业生产硝酸的流程如下图所示:
CH4H2NH3NONO2HNO3
已知:ⅰ.HNO3受热易分解为NO2、O2等物质;
ⅱ.原子利用率=。
(1)步骤Ⅰ:制高纯氢
①反应器中初始反应的生成物有两种,且物质的量之比为1:4,甲烷与水蒸气反应的化学方程式是
。
②所得H2中含有少量CO气体,影响后续反应催化剂活性,可利用如下反应吸收CO:[Cu(NH3)2]Ac(aq)+CO(g)+NH3(g)?[Cu(NH3)3]Ac?CO(aq)△H<0
(注:Ac﹣代表CH3COO﹣)
利于CO被吸收的反应条件有
(写出两点)。
(2)步骤Ⅱ:合成氨
①工业合成氨时,每生成1mol
NH3(g)放出46.1kJ热量,则合成氨的热化学方程式是
。
②用如图所示装置实现电化学合成氨。产生NH3的电极反应式是
。
(3)步骤Ⅲ和步骤Ⅳ均是放热反应,步骤Ⅴ在反应前需将NO2冷却。
①步骤Ⅴ的化学方程式是
。
②冷却NO2有利于提高HNO3产率,原因是
(写出一点即可)。
③提高由NH3转化为HNO3的整个过程中氮原子利用率的措施是
。
17.(12分)研究人员从处理废旧线路板后的固体残渣(含SnO2、PbO2等)中进一步回收金属锡(Sn),一种回收流程如图。
已知:ⅰ.50Sn、82Pb为ⅣA族元素。
ⅱ.SnO2、PbO2与强碱反应生成盐和水。
(1)Sn在空气中不反应,Pb在空气中表面生成一层氧化膜,结合原子结构解释原因
。
(2)SnO2与NaOH反应的化学方程式为
。
(3)滤液1中加入Na2S的目的是除铅,将相关方程式补充完整:
Na2PbO3+
Na2S+
═PbS↓+S↓+
(4)不同溶剂中Na2SnO3的溶解度随温度变化如图。
①相同温度下,Na2SnO3的溶解度随NaOH浓度增大而减小,结合平衡移动原理解释原因:
。
②操作Ⅲ的具体方法为
。
(5)测定粗锡中Sn的纯度:在强酸性环境中将ag粗锡样品溶解(此时Sn全部转化成Sn2+),迅速加入过量NH4Fe(SO4)2溶液,以二苯胺磺酸钠为指示剂,用cmol?L﹣1K2Cr2O7标准溶液滴定至终点。平行测定三次,消耗K2Cr2O7溶液的体积平均为vmL,计算Sn的纯度(Sn的摩尔质量为119g?mol﹣1)。
已知:Sn2++2Fe3+═Sn4++2Fe2+
Cr2O72﹣+6Fe2++14H+═2Cr3++6Fe3++7H2O
①溶解粗锡时不宜选用浓盐酸,理由是
。
②粗锡样品中Sn的纯度为
(用质量分数表示)。
18.(12分)将CO2转化成C2H4可以变废为宝、改善环境。以CO2、C2H6为原料合成C2H4涉及的主要反应如下:
Ⅰ.CO2(g)+C2H6(g)?C2H4(g)+H2O(g)+CO(g)△H=+177kJ?mol﹣1(主反应)
Ⅱ.C2H6(g)?CH4(g)+H2(g)+C(s)△H=+9kJ?mol﹣1(副反应)
(1)反应Ⅰ的反应历程可分为如下两步:
ⅰ.C2H6(g)?C2H4(g)+H2(g)△H1=+136kJ?mol﹣1(反应速率较快)
ⅱ.H2(g)+CO2(g)?H2O(g)+CO(g)△H2(反应速率较慢)
①△H2=
kJ?mol﹣1
②相比于提高c(C2H6),提高c(CO2)对反应Ⅰ速率影响更大,原因是
。
(2)0.1MPa时向密闭容器中充入CO2和C2H6,温度对催化剂K﹣Fe﹣Mn/Si﹣2性能的影响如图所示。
①工业生产中反应Ⅰ选择800℃,原因是
。
②800℃时,不同的CO2和C2H6体积比对反应影响的实验数据如下表:
v(CO2)/v(C2H6)
平衡时有机产物的质量分数
CH4
C2H4
15.0/15.0
7.7
92.3
20.0/10.0
6.4
93.6
24.0/6.0
4.5
95.5
a.随增大,CO2转化率将
(填“增大”或“减小”)。
b.解释对产物中C2H4的质量分数影响的原因:
。
(3)我国科学家使用电化学的方法(装置如图)用C2H6和CO2合成了C2H4。
①N是电源的
极。
②阳极电极反应式是
。
19.(14分)久置的Na2S固体会潮解、变质、颜色变黄,探究Na2S变质的产物。
资料:ⅰ.Na2S能与S反应生成Na2Sx(黄色),Na2Sx与酸反应生成S和H2S;
ⅱ.BaS、BaSx均易溶于水,H2S可溶于水,BaS2O3微溶于水;
ⅲ.白色的Ag2S2O3难溶于水,且易转化为黑色Ag2S。
将久置的Na2S固体溶于水,溶液呈黄色。取黄色溶液,滴加稀硫酸,产生白色沉淀(经检验该沉淀含S)。
(1)推测Na2S变质的产物含有Na2Sx,实验证据是
。
(2)研究白色沉淀产生的途径,实验小组同学进行如下假设:
途径一:白色沉淀由Na2Sx与稀硫酸反应产生。
途径二:Na2S变质的产物中可能含有Na2S2O3,白色沉淀由Na2S2O3与稀硫酸反应产生。
途径三:Na2S变质的产物中可能含有Na2SO3,白色沉淀由……。
①Na2S2O3与稀硫酸反应的化学方程式是
。
②请将途径三补充完全:
。
(3)为检验Na2S变质的产物中是否含有Na2S2O3,设计实验:
①取黄色溶液,向其中滴加AgNO3溶液,产生黑色沉淀。由此得出结论:Na2S变质的产物中含Na2S2O3。有同学认为得出该结论的理由不充分,原因是
。
②改进实验,方案和现象如下:
实验一:
实验二:
a.实验一的目的是
。
b.试剂1是
,试剂2是
。
(4)检验Na2S变质的产物中是否含有Na2SO4:取黄色溶液,加入过量稀盐酸,产生白色沉淀。离心沉降(分离固体)后向溶液中滴加BaCl2溶液,产生白色沉淀。你认为能否根据实验现象得出结论?说明理由:
。
2020-2021学年北京市朝阳区高三(上)期中化学试卷
试题解析
一、本部分共14题,每题3分,共42分。在每题列出的四个选项中,选出最符合题目要求的一项。
1.【答案】B
【解答】解:A.二氧化硅属于非金属氧化物,不是金属材料,故A错误;
B.钛合金是钛的合金,属于金属材料,故B正确;
C.聚酰胺属于有机高分子材料,不是金属材料,故C错误;
D.水泥属于无机硅酸盐材料,不是金属材料,故D错误;
故选:B。
2.【答案】A
【解答】解:A.中子数为16的硫离子的质量数是16+16=32,所以中子数为16的硫原子:S,故A正确;
B.纯碱是Na2CO3的俗名,故B错误;
C.二氧化碳为共价化合物,其分子中含有两个碳氧双键,二氧化碳的电子式为:,故C错误;
D.铝离子的核外有10个电子,铝离子的结构示意图为:,故D错误;
故选:A。
3.【答案】D
【解答】解:A.7.1g
Cl2的物质的量为:=0.1mol,由于反应后溶液中还存在Cl2,则转移电子的物质的量小于0.1mol,转移的电子数小于0.1NA,故A错误;
B.1L
0.1mol?L﹣1乙酸溶液中含有乙酸的物质的量为:0.1mol/L×1L=0.1mol,乙酸为弱酸,只能部分电离出氢离子,则溶液中含H+的数目小于0.1NA,故B错误;
C.标准状况下,22.4L
CH4为1mol,完全燃烧生成1mol二氧化碳和2mol水,由于标况下水为液态,则所得产物中气体分子数为NA,故C错误;
D.Na2CO3溶液中的OH﹣完全来自水的电离,该溶液中OH﹣的浓度为0.001mol/L,由水电离出的OH﹣的物质的量为:0.001mol/L×1L=0.001mol,数目为0.001NA,故D正确;
故选:D。
4.【答案】B
【解答】解:A.氯化铁溶液中加入铁粉会生成氯化亚铁,其反应的离子方程式为:2Fe3++Fe=3Fe2+,故A正确;
B.硫酸铝溶液中加入过量氨水的离子反应为Al3++3NH3?H2O=Al(OH)3↓+3NH4+,故B错误;
C.高锰酸钾酸性溶液与草酸溶液反应,离子方程式:2MnO4﹣+5H2C2O4+6H+═2Mn2++10CO2↑+8H2O,故C正确;
D.用过氧化氢从酸化的海带灰浸出液中提取碘,双氧水与过氧化氢发生氧化还原反应,反应的离子方程式为:2I﹣+H2O2+2H+═I2+2H2O,故D正确;
故选:B。
5.【答案】A
【解答】解:A.加热氯化铵分解,在试管口化合生成氯化铵,不能制备氨气,应选氯化铵与碱石灰加热制备,故A错误;
B.乙酸乙酯和碳酸钠溶液分层,可选分液漏斗分离,故B正确;
C.在HCl气体中可抑制镁离子水解,可制备无水氯化镁,故C正确;
D.醋酸钠水解显碱性,测定盐溶液的pH可证明醋酸为弱酸,故D正确;
故选:A。
6.【答案】D
【解答】解:A.金属性Na>Li,NaOH的碱性比LiOH强,故A错误;
B.非金属性F>Cl>S,元素的非金属性越强,对应的氢化物的还原性越弱,故B错误;
C.非金属性Cl>S,非金属性越强,对应的最高价氧化物的水化物的酸性越强,故C错误;
D.三种离子具有相同的核外电子排布,核电荷数越大离子半径越小,故D正确。
故选:D。
7.【答案】C
【解答】解:A.反应②中,NH2OH中存在极性键,反应时有极性键断裂,生成物N2H4中含有非极性键,则反应中有N﹣N非极性键生成,故A正确;
B.反应③N2H4中N元素的化合价升高,被氧化,氧气可以氧化N2H4,则可能有氧气参与反应,故B正确;
C.反应②③④⑤中,都存在N元素化合价的变化,均属于氧化还原反应,所以反应①~⑤中包含4个氧化还原反应,故C错误;
D.反应④中N元素的化合价从+3价降低到﹣3价,反应⑤中N元素的化合价从+3价降低到0价,则等量NO2﹣参加反应,反应④转移电子数目比反应⑤多,故D正确。
故选:C。
8.【答案】D
【解答】解:A.燃料反应器中Fe2O3固体颗粒越小,接触面积越大,反应速率越快,故A正确;
B.根据图示,蒸汽反应器中铁和水蒸气反应生成四氧化三铁和氢气,发生的反应为3Fe+4H2O(g)═Fe3O4+4H2,故B正确;
C.H2O的沸点比H2高得多,从蒸汽反应器所得H2和H2O的混合物中液化分离H2O,可获得高纯H2,故C正确;
D.根据氧元素守恒分析,反应体系有水蒸气通入,为使Fe2O3循环使用,理论上需要满足n(CO):n(O2)>2:1,故D错误;
故选:D。
9.【答案】D
【解答】解:A.图1反应若使用催化剂,可以改变反应路径,不改变其△H,焓变和反应路径无关,故A错误;
B.该反应反应物的总能量大于生成物的总能量,为吸热反应,而液态水转化为气态水还要吸收热量,所以能量变化曲线还要在生成物上方,故B错误;
C.该图象表示的反应物的总能量比生成物的总能量低,为吸热反应,故C错误;
D.已知①SO2(g)+I2(s)+2H2O(l)═2HI(aq)+H2S
O4(aq)△H1=﹣151kJ?mol﹣1,
②H2S
(g)+H2S
O4(aq)═S(s)+SO2(g)+2H2O(l)△H3=+61kJ?mol﹣1,
③2HI(aq)═H2(g)+I2(s)△H2=+110kJ?mol﹣1,
根据盖斯定律由①+②+③可得反应H2S
(g)=H2(g)+S(s),由此计算反应的△H,则△H=△H1+△H2﹣△H3=(61kJ?mol﹣1)+(﹣151kJ?mol﹣1)+(110kJ?mol﹣1)=20kJ?mol﹣1,此反应的热化学方程式为H2S
(g)=H2(g)+S(s)△H=+20kJ?mol﹣1,故D正确;
故选:D。
10.【答案】C
【解答】解:A.浓盐酸易挥发,可用饱和NaCl溶液净化氯气,故A正确;
B.生成KClO3时只有Cl元素的化合价变化,离子方程式为3Cl2+6OH﹣ClO3﹣+5Cl﹣+3H2O,故B正确;
C.若取少量无色溶液a于试管中,滴加稀H2SO4后,Cl﹣、IO3﹣发生氧化还原反应生成碘,溶液为黄色,故C错误;
D.由氯气与KOH的反应、氯酸钾与盐酸的反应,结合氧化剂的氧化性大于氧化产物的氧化性可知,上述实验说明碱性条件下氧化性Cl2>KClO3,酸性条件下氧化性:Cl2<KClO3,故D正确;
故选:C。
11.【答案】B
【解答】解:A.a点溶质CH3COOH和CH3COONa的混合液,pH=5,若用10mL
H2O代替10mL
NaOH溶液,开始pH=3,仅仅稀释0.5倍,pH<4,故A正确;
B.b点溶液pH=7,c(H+)=c(OH﹣),满足c(Na+)+c(H+)=c(OH﹣)+c(CH3COO﹣),b点时有c(CH3COO﹣)=c(Na+),故B错误;
C.a点是c(H+)=10﹣4mol/L,a
点溶液中
c(CH3COO﹣)约为
10﹣4mol?L﹣1,c点溶液为二者恰好反应点,c(CH3COO﹣)>c(Na+)≈0.05mol?L﹣1,a点→c点的过程中n(CH3COO﹣)持续增大,故C正确;
D.醋酸的电离是可逆反应:CH3COOH?CH3COO﹣+H+,向a点对应的溶液中滴加1滴0.1mol?L﹣1NaOH溶液或1滴0.1mol?L﹣1醋酸溶液,平衡正向移动,且量很小,氢离子浓度基本不变,所以pH变化均不大,故D正确;
故选:B。
12.【答案】C
【解答】解:A.根据“先拐先平数值大”知,其它条件相同时温度高的先达到平衡状态,根据图知Ta条件下先达到平衡状态,所以Ta>Tb,故A错误;
B.Ta时,0~4min内v(CO)==mol?L﹣1?min﹣1=0.0125mol?L﹣1?min﹣1,相同时间内v(CH4)=v(CO)=0.0125mol?L﹣1?min﹣1,故B错误;
C.图中Tb时为恒温恒容条件下发生的反应,随着反应进行气体物质的量增大导致容器内压强增大,如果改为恒温恒压条件下,与原来相比相当于减小压强,减小压强平衡正向移动,反应物的转化率增大,所以平衡时n(CO)>0.6mol,故C正确;
D.平衡常数只与温度有关,Tb时,平衡时再充入1.1mol
CH4,平衡正向移动但温度不变平衡常数不变,故D错误;
故选:C。
13.【答案】D
【解答】解:A.闭合K1时为原电池,Zn发生失电子的氧化反应生成Zn(OH)42﹣,则Zn电极为负极,电极反应式为Zn+4OH﹣﹣2e﹣═Zn(OH)42﹣,故A正确;
B.闭合K1时为原电池,Zn电极为负极,Pd电极为正极,正极反应式为CO2+2e﹣+2H+═HCOOH,生成甲酸,溶液的酸性增强,NaCl溶液的pH减小,故B正确;
C.Zn﹣CO2电池中Zn电极为负极,Pd电极为正极,闭合K2时为电解池,Pd电极为阳极,与直流电源正极相连,故C正确;
D.闭合K2时为电解池,Pd电极为阳极,Zn电极为阴极,复合膜层间的H2O解离成的H+通过a膜移向Zn电极,OH﹣通过b膜向Pd电极方向移动,故D错误;
故选:D。
14.【答案】B
【解答】解:A.实验时先通入二氧化碳,可将装置内的氧气排出,避免干扰实验,故A正确;
B.由实验iii可知,滤液呈碱性,说明生成氢氧化钠,则白色物质含有碳酸钠和氧化钠,故B错误;
C.黑色固体为碳,加热条件下与浓硫酸反应生成二氧化碳、二氧化硫和水,方程式为C+2H2SO4(浓)CO2↑+2SO2↑+2H2O,故C正确;
D.K的活泼性比Na强,具有相似的化学性质,则CO2与金属K也可以发生反应并被还原,故D正确。
故选:B。
二、解答题(共5小题,满分58分)
15.【答案】(1)Fe﹣2e﹣═Fe2+;
(2)①6Fe(OH)2+O2═2Fe3O4+6H2O;
②12Cl﹣;6;12;12OH﹣;
(3)①>;
②作还原剂,将FeOCl还原为Fe3O4;
③取最后一次的洗涤液于试管中,加入HNO3酸化,再加入AgNO3溶液,无白色沉淀产生,证明FeOCl转化完全。
【解答】解:(1)反应中铁是负极,发生氧化反应,生成Fe2+,负极反应式是:Fe﹣2e﹣=Fe2+,
故答案为:Fe﹣2e﹣=Fe2+;
(2)①Fe(OH)2被空气中氧气氧化,生成四氧化三铁和水,反应的化学方程式:6Fe(OH)2+O2═2Fe3O4+6H2O,
故答案为:6Fe(OH)2+O2═2Fe3O4+6H2O;
②反应中O2中O元素的化合价降低4,Fe3O4中3个Fe的化合价共升高1,根据化合价升降守恒可知,Fe3O4的计量数为4,O2的计量数为1,反应的离子方程式:4Fe3O4+O2+12Cl﹣+6H2O═12FeOCl+12OH﹣,
故答案为:12Cl﹣;6;12;12OH﹣;
(3)①化学反应有从溶解度小的物质转化为溶解度更小的趋势,由于不溶物FeOCl→FeO(OH),所以FeOCl的溶解度大于FeO(OH),
故答案为:>;
②Na2SO3还原FeOCl生成Fe3O4,反应为:SO32﹣+6FeOCl+3H2O=SO42﹣+2Fe3O4+6H++6Cl﹣,
故答案为:作还原剂,将FeOCl还原为Fe3O4;
③检验FeOCl转化完全需检验Cl﹣,操作和现象是:取最后一次的洗涤液于试管中,加入HNO3酸化,再加入AgNO3溶液,无白色沉淀产生,证明FeOCl转化完全,
故答案为:取最后一次的洗涤液于试管中,加入HNO3酸化,再加入AgNO3溶液,无白色沉淀产生,证明FeOCl转化完全。
16.【答案】(1)①CH4+2H2O═4H2+CO2;
②降低温度,增大压强(或增大[Cu(NH3)2]Ac(aq)浓度,或增大NH3浓度);
(2)①N2(g)+3H2(g)?2NH3(g)
ΔH=﹣92.2kJ?mol﹣1;
②N2+6H++6e﹣═2NH3;
(3)①3NO2+H2O═2HNO3+NO;
②防止温度高造成HNO3分解(或温度高NO2溶解度降低);
③通入过量的O2,使生成的NO全部转化为硝酸。
【解答】解:(1)①甲烷与水蒸气反应有2种产物,其中一种是H2,且生成物的物质的量之比为1:4,则另一种产物是CO2,故化学方程式为CH4+2H2O═4H2+CO2,
故答案为:CH4+2H2O═4H2+CO2;
②利于CO被吸收就是要增大CO的转化率,降低温度、增大压强、增大[Cu(NH3)2]Ac(aq)浓度或增大NH3浓度均可使平衡向右移动,增大CO的转化率,所以降低温度,增大压强(或增大[Cu(NH3)2]Ac(aq)浓度,或增大NH3浓度)有利于CO被吸收,
故答案为:降低温度,增大压强(或增大[Cu(NH3)2]Ac(aq)浓度,或增大NH3浓度);
(2)①每生成1mol
NH3(g)放出46.1kJ热量,则每生成2mol
NH3(g)的热效应为ΔH=﹣46.1kJ?mol﹣1×2=﹣92.2kJ?mol﹣1,所以合成氨的热化学方程式为N2(g)+3H2(g)?2NH3(g)
ΔH=﹣92.2kJ?mol﹣1,
故答案为:N2(g)+3H2(g)?2NH3(g)
ΔH=﹣92.2kJ?mol﹣1;
②电极上反应物为N2和H+,产物为NH3,N的化合价降低须得电子,所以电极反应式为N2+6H++6e﹣═2NH3,
故答案为:N2+6H++6e﹣═2NH3;
(3)①步骤Ⅴ是NO2和H2O反应生成HNO3,产物除了HNO3外,还有NO,所以方程式为3NO2+H2O═2HNO3+NO,
故答案为:3NO2+H2O═2HNO3+NO;
②冷却NO2有利于提高HNO3产率,是因为HNO3受热易分解为NO2、O2等物质,另外,温度高也会降低NO2在水中溶解度,从而降低HNO3产率,因此冷却NO2有利于提高HNO3产率是因为防止温度高造成HNO3分解(或温度高NO2溶解度降低),
故答案为:防止温度高造成HNO3分解(或温度高NO2溶解度降低);
③NH3转化为HNO3的整个过程中,要想提高N原子的利用率,就要尽可能的使N原子全部转入HNO3中,并且最后一步NO2和H2O也生成了部分NO,所以可通入过量的O2,使生成的NO全部转化为硝酸,
故答案为:通入过量的O2,使生成的NO全部转化为硝酸。
17.【答案】(1)Sn和Pb均为第IVA元素,核电荷数Pb>Sn,电子层数Pb>Sn,原子半径Pb>Sn,失电子能力Pb>Sn,金属性Pb>Sn;
(2)SnO2+2NaOH═Na2SnO3+H2O;
(3)2;3;H2O;6;NaOH;
(4)①随着NaOH溶液浓度增大,c(Na+)增大,Na2SnO3溶解平衡:Na2SnO3(s)?2Na+(aq)+SnO32﹣(aq)逆向移动,使得Na2SnO3溶解度减小;
②蒸发结晶、趁热过滤;
(5)①K2Cr2O7酸性溶液可以氧化Cl﹣,产生实验误差;
②%。
【解答】解:(1)Sn在空气中不反应,Pb在空气中表面生成一层氧化膜,结合原子结构解释原因为Sn和Pb均为第IVA元素,核电荷数Pb>Sn,电子层数Pb>Sn,原子半径Pb>Sn,失电子能力Pb>Sn,金属性Pb>Sn,
故答案为:Sn和Pb均为第IVA元素,核电荷数Pb>Sn,电子层数Pb>Sn,原子半径Pb>Sn,失电子能力Pb>Sn,金属性Pb>Sn;
(2)SnO2与NaOH反应的化学方程式为SnO2+2NaOH═Na2SnO3+H2O,
故答案为:SnO2+2NaOH═Na2SnO3+H2O;
(3)滤液1中加入Na2S的目的是除铅,Pb元素的化合价降低,S元素的化合价升高,由电子及原子守恒可知反应为Na2PbO3+2Na2S+3H2O═PbS↓+S↓+6NaOH,
故答案为:2;3;H2O;6;NaOH;
(4)①相同温度下,Na2SnO3的溶解度随NaOH浓度增大而减小,结合平衡移动原理解释原因为随着NaOH溶液浓度增大,c(Na+)增大,Na2SnO3溶解平衡:Na2SnO3(s)?2Na+(aq)+SnO32﹣(aq)逆向移动,使得Na2SnO3溶解度减小,
故答案为:随着NaOH溶液浓度增大,c(Na+)增大,Na2SnO3溶解平衡:Na2SnO3(s)?2Na+(aq)+SnO32﹣(aq)逆向移动,使得Na2SnO3溶解度减小;
②由图可知,溶剂为水时随温度升高溶解度减小,则操作Ⅲ的具体方法为蒸发结晶、趁热过滤,
故答案为:蒸发结晶、趁热过滤;
(5)①溶解粗锡时不宜选用浓盐酸,理由是K2Cr2O7酸性溶液可以氧化Cl﹣,产生实验误差,
故答案为:K2Cr2O7酸性溶液可以氧化Cl﹣,产生实验误差;
②由Sn2++2Fe3+═Sn4++2Fe2+、Cr2O72﹣+6Fe2++14H+═2Cr3++6Fe3++7H2O可知存在3Sn2+~Cr2O72﹣,粗锡样品中Sn的纯度为×100%=%,
故答案为:%。
18.【答案】(1)①+41;
②反应ii为反应I的决速步,c(CO2)增大,反应ii速率加快,从而提高反应I速率;
(2)①800℃时,C2H4选择性比780℃略有降低,但CO2的转化率增大较多,有利于提高C2H4的产率;800℃时,C2H4选择性与820℃相比选择性略高;
②a.减小;
b.随增大,c(CO2)增大,c(C2H6)减小;c(CO2)增大促进反应I平衡正移,反应消耗的C2H6增多,也使c(C2H6)减小,反应II平衡逆移;上述因素导致产物中C2H4质量分数增大;
(3)①负;
②C2H6+O2﹣﹣2e﹣═C2H4+H2O。
【解答】解:(1)①ⅠC2H6(g)?C2H4(g)+H2(g)△H1=+136kJ?mol﹣1,
ⅡH2(g)+CO2(g)?H2O(g)+CO(g)△H2,
ⅢCO2(g)+C2H6(g)?C2H4(g)+H2O(g)+CO(g)△H=+177kJ?mol﹣1,
由盖斯定律可知,②=③﹣①,△H2=△H﹣△H1=+177kJ?mol﹣1﹣(+136kJ?mol﹣1)=+41kJ/mol,
②反应ⅱ.H2(g)+CO2(g)?H2O(g)+CO(g)△H2
反应速率较慢,对整个反应速率影响最大,反应ⅱ为反应Ⅰ的决速度,c(CO2)增大,反应ii速率加快,从而提高反应I速率,
故答案为:反应ⅱ为反应Ⅰ的决速度,c(CO2)增大,反应ii速率加快,从而提高反应I速率;
(2)①工业生产中反应Ⅰ选择800℃,原因是:800℃时,C2H4选择性比780℃略有降低,但CO2的转化率增大较多,有利于提高C2H4的产率;800℃时,C2H4选择性与820℃相比选择性略高,
故答案为:800℃时,C2H4选择性比780℃略有降低,但CO2的转化率增大较多,有利于提高C2H4的产率;800℃时,C2H4选择性与820℃相比选择性略高;
a.随增大,相当于在反应体系中增大二氧化碳的量,则平衡正向移动,但CO2转化率将减小,
故答案为:减小;
b.随增大,c(CO2)增大,c(C2H6)减小。c(CO2)增大促进反应Ⅰ平衡右移,反应消耗的C2H6增多,也使c(C2H6)减小,反应II平衡左移,上述因素导致产物中C2H4质量分数增大,
故答案为:随增大,c(CO2)增大,c(C2H6)减小。c(CO2)增大促进反应Ⅰ平衡右移,反应消耗的C2H6增多,也使c(C2H6)减小,反应II平衡左移,上述因素导致产物中C2H4质量分数增大;
(3)①N极CO2→CO,化合价降低,得电子,被还原,为负极,
故答案为:负;
②阳极C2H6→C2H4,失去2个电子且消耗氧离子,电极反应式为:C2H6+O2﹣﹣2e﹣═C2H4+H2O,
故答案为:C2H6+O2﹣﹣2e﹣═C2H4+H2O。
19.【答案】(1)溶液呈黄色;
(2)①Na2S2O3+H2SO4═Na2SO4+SO2↑+S↓+H2O;
②白色沉淀由SO32﹣与S2﹣在酸性条件下反应产生(或白色沉淀由生成的H2S与SO2反应产生);
(3)①剩余的Na2S也能与AgNO3溶液反应生成黑色的Ag2S沉淀;
②a.确认Ag2SO4和Ag2SO3都不易转化为黑色固体,排除SO42﹣、SO32﹣对S2O32﹣检验的干扰;
b.BaCl2溶液;AgNO3溶液;
(4)可以,稀盐酸将S2O32﹣、SO32﹣等除去,不会产生干扰;或:不可以,检验过程中H2S等低价含硫物质被O2氧化。
【解答】解:(1)如含有Na2Sx,则溶液成黄色,
故答案为:溶液呈黄色;
(2)①Na2S2O3与稀硫酸反应生成硫酸钠、二氧化硫和硫,反应的化学方程式为Na2S2O3+H2SO4═Na2SO4+SO2↑+S↓+H2O,
故答案为:Na2S2O3+H2SO4═Na2SO4+SO2↑+S↓+H2O;
②Na2S变质的产物中可能含有Na2SO3,二者在酸性条件下发生氧化还原反应生成硫,或白色沉淀由生成的H2S与SO2反应产生,
故答案为:白色沉淀由SO32﹣与S2﹣在酸性条件下反应产生(或白色沉淀由生成的H2S与SO2反应产生);
(3)①固体中含有硫化钠,硫化钠和硝酸银反应生成硫化银沉淀,为黑色固体,
故答案为:剩余的Na2S也能与AgNO3溶液反应生成黑色的Ag2S沉淀;
②a.实验一加入亚硫酸钠、硫酸钠,与硝酸银反应生成白色沉淀,可排除SO42﹣、SO32﹣对S2O32﹣检验的干扰,
故答案为:确认Ag2SO4和Ag2SO3都不易转化为黑色固体,排除SO42﹣、SO32﹣对S2O32﹣检验的干扰;
b.黄色溶液含有Na2Sx,如含有含有Na2S2O3,可加入氯化钡溶液,生成白色沉淀为BaS2O3,然后加入硝酸银溶液,可生成白色的Ag2S2O3,然后转化为Ag2S,
故答案为:BaCl2溶液;AgNO3溶液;
(4)可能有两种情况,加入稀盐酸,可将S2O32﹣、SO32﹣等除去,对实验无影响,但检验过程中H2S等低价含硫物质被O2氧化,则不可以,
故答案为:可以,稀盐酸将S2O32﹣、SO32﹣等除去,不会产生干扰;或:不可以,检验过程中H2S等低价含硫物质被O2氧化。
同课章节目录
