2.4 化学反应的调控 课件(27张ppt)
文档属性
| 名称 | 2.4 化学反应的调控 课件(27张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-11-20 00:00:00 | ||
图片预览







文档简介
化学反应的调控
一、从合成氨说起
1.为什么要合成氨?
18世纪末,英国化学家克鲁克斯“先天下之忧而忧”,率先发出为了使子孙后代免于饥饿“向空气要氮肥”的号召。
化学创造了
第二个大自然!
从化学平衡的视角分析,合成氨应该可行!
想一想:从哪些角度选择固氮反应?
常温 K=3.8×10-31
常温 K=5.0×108
氧化法:
还原法:
N2(g) + 3H2(g) 2NH3(g)
N2(g) + O2(g) 2NO(g)
2. 合成氨很难吗?
18世纪末,有人试图在常温常压下合成氨,也有人在常温加压下进行实验。——都失败了
合成氨不容易,难在哪儿?
如果是你,你会怎样分析?
德国化学家哈伯向合成氨发起冲击。1908年7月,他在实验室用氮气和氢气在600 ℃、20 MPa下得到了氨,但是产率只有2%。
哈伯合成氨所用装置
冷却室
反应器
出水口
干燥室
液态NH3
出口
进水口
未反应气体通过循环泵返回
压缩
N2和H2进口
二、寻找工业合成氨的适宜条件
如果你是20世纪初的工程师,你如何为工厂设计合成氨的生产条件?可以从哪些角度分析?
化学平衡
化学反应速率
理论实践
想一想:
理论分析——合成氨反应有什么样的特点?如何通过选择反应条件提高平衡混合物中氨的含量?
{5940675A-B579-460E-94D1-54222C63F5DA}对合成氨反应的影响
影响因素
浓度
温度
压强
提高平衡混合物中氨的含量
N2(g) + 3H2(g) 2NH3(g) ?H =-92.4 kJ/mol
1. 从化学平衡分析
{5940675A-B579-460E-94D1-54222C63F5DA}对合成氨
反应的影响
影响因素
浓度
温度
压强
提高平衡
混合物中氨
的含量
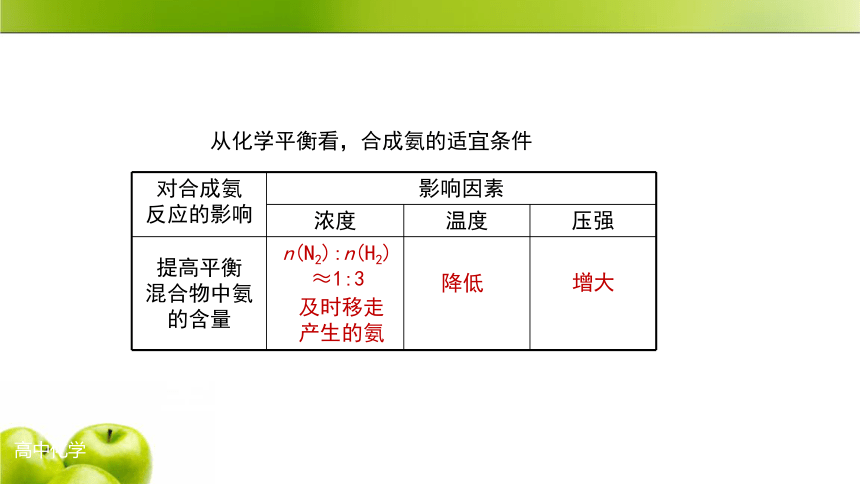
n(N2):n(H2)
≈1:3
及时移走产生的氨
降低
增大
从化学平衡看,合成氨的适宜条件
理论分析:
实验结果:
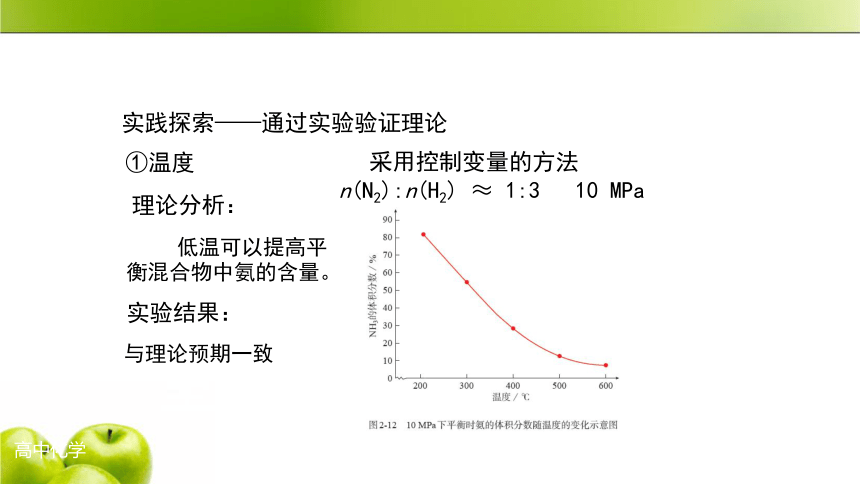
①温度
低温可以提高平衡混合物中氨的含量。
n(N2):n(H2) ≈ 1:3 10 MPa
与理论预期一致
实践探索——通过实验验证理论
采用控制变量的方法
n(N2):n(H2) ≈ 1:3 400 ℃
②压强
理论分析:
压强越大越有利于提高平衡混合物中氨的含量。
实验结果:
与理论预期一致
原料气 n(N2):n(H2)≈1:3
及时移走产生的氨
低温和高压
从化学平衡看,合成氨的适宜条件
想一想:
思考:为什么没有在常温合成氨?合成氨难在哪儿?还有什么因素制约氨的合成?
常温下合成氨化学反应速率很小!
合成氨反应为什么慢?
2. 从化学反应速率分析
——活化能高
如何增大合成氨的化学反应速率?
{5940675A-B579-460E-94D1-54222C63F5DA}对合成氨
反应的影响
影响因素
浓度
温度
压强
催化剂
增大合成氨
的反应速率
增大
升高
增大
使用
怎样降低反应的活化能?
——改变反应历程
{5940675A-B579-460E-94D1-54222C63F5DA}对合成氨
反应的影响
影响因素
浓度
温度
压强
催化剂
增大合成氨的反应速率
增大
升高
增大
使用
提高平衡混合物中氨的含量
n(N2):n(H2) ≈1:3
及时移走产生的氨
降低
增大
无影响
想一想:
3. 综合分析
实现工业生产:
综合考虑成本要低!
①压强
从化学反应速率与化学平衡考虑,都是压强越大越好。
综合成本与设备耐压:
10 MPa~30 MPa
3. 综合分析
②催化剂
增大化学反应速率,不改变平衡混合物的组成。
现在常用铁,其活性最好的温度为500 ℃左右。
3. 综合分析
③温度
综合考虑,特别是考虑催化剂的活性。
一般400~500 ℃
低温可以提高平衡混合物中氨的含量,但低温会减小化学反应速率。
在温度与压强的最佳条件下,平衡混合物中氨的含量仍不高,怎么办?
{5940675A-B579-460E-94D1-54222C63F5DA}温度/℃
氨的含量/%
0.1 MPa
10 MPa
20 MPa
30 MPa
60 MPa
100 MPa
200
15.3
81.5
86.4
89.9
95.4
98.8
300
2.20
52.0
64.2
71.0
84.2
92.6
400
0.40
25.1
38.2
47.0
65.2
79.8
500
0.10
10.6
19.1
26.4
42.2
57.5
600
0.05
4.50
9.10
13.8
23.1
31.4
想一想:
合成氨常用的生产条件:
使用催化剂
温度:400~500 ℃
压强: 10 MPa~30 MPa
将氨及时分离出来
原料气循环使用
二、寻找工业合成氨的适宜条件
三、化工生产中调控反应的一般思路
1.选取恰当的反应
思考并归纳出化工生产中调控反应的一般思路
试一试:
影响因素
调控反应
三、化工生产中调控反应的一般思路
反应
化学平衡
反应速率
最佳效果
2.分析调控方法
三、化工生产中调控反应的一般思路
3.探索最佳工艺
哈伯:
锇(剧毒)作催化剂
17.5 MPa~20.0 MPa、500~600 ℃
氨含量6%
三、化工生产中调控反应的一般思路
博施:
铁作催化剂
开发了适合高温、高压下的合成设备
设计了获得大量廉价原料气的方法
三、化工生产中调控反应的一般思路
埃特尔:
在合成氨反应初期,氮、氢分子被吸附在铁催化剂表面。进而确定吸附的氮原子和氢原子是反应活性物,整个反应就是氮原子逐步加氢最终生成氨分子的过程,并给出了每步反应的活化能。
原料用量n(N2):n(H2):
理论值为1:3
实际为1:2.8
哈伯
(1918年)
合成氨的基础开发工作
博施
(1931年)
实现了合成氨的工业化
埃特尔(2007年)
揭开了合成氨的“天机”
4.不断技术创新
合成氨与三次诺贝尔化学奖
“合成氨”里的中国人:2016年中科院大连化学物理研究所研究团队研制合成了一种新型催化剂,将合成氨的温度、压强分别降到了350 ℃、1 MPa 。
更加节能、降低成本
小结:化学反应的调控
明确目的
可行性
确定
反应
原理分析
实验摸索
找条件
化学平衡
反应速率
设备可行
成本核算
如何为一个化学反应选择适宜的生产条件?
一、从合成氨说起
1.为什么要合成氨?
18世纪末,英国化学家克鲁克斯“先天下之忧而忧”,率先发出为了使子孙后代免于饥饿“向空气要氮肥”的号召。
化学创造了
第二个大自然!
从化学平衡的视角分析,合成氨应该可行!
想一想:从哪些角度选择固氮反应?
常温 K=3.8×10-31
常温 K=5.0×108
氧化法:
还原法:
N2(g) + 3H2(g) 2NH3(g)
N2(g) + O2(g) 2NO(g)
2. 合成氨很难吗?
18世纪末,有人试图在常温常压下合成氨,也有人在常温加压下进行实验。——都失败了
合成氨不容易,难在哪儿?
如果是你,你会怎样分析?
德国化学家哈伯向合成氨发起冲击。1908年7月,他在实验室用氮气和氢气在600 ℃、20 MPa下得到了氨,但是产率只有2%。
哈伯合成氨所用装置
冷却室
反应器
出水口
干燥室
液态NH3
出口
进水口
未反应气体通过循环泵返回
压缩
N2和H2进口
二、寻找工业合成氨的适宜条件
如果你是20世纪初的工程师,你如何为工厂设计合成氨的生产条件?可以从哪些角度分析?
化学平衡
化学反应速率
理论实践
想一想:
理论分析——合成氨反应有什么样的特点?如何通过选择反应条件提高平衡混合物中氨的含量?
{5940675A-B579-460E-94D1-54222C63F5DA}对合成氨反应的影响
影响因素
浓度
温度
压强
提高平衡混合物中氨的含量
N2(g) + 3H2(g) 2NH3(g) ?H =-92.4 kJ/mol
1. 从化学平衡分析
{5940675A-B579-460E-94D1-54222C63F5DA}对合成氨
反应的影响
影响因素
浓度
温度
压强
提高平衡
混合物中氨
的含量
n(N2):n(H2)
≈1:3
及时移走产生的氨
降低
增大
从化学平衡看,合成氨的适宜条件
理论分析:
实验结果:
①温度
低温可以提高平衡混合物中氨的含量。
n(N2):n(H2) ≈ 1:3 10 MPa
与理论预期一致
实践探索——通过实验验证理论
采用控制变量的方法
n(N2):n(H2) ≈ 1:3 400 ℃
②压强
理论分析:
压强越大越有利于提高平衡混合物中氨的含量。
实验结果:
与理论预期一致
原料气 n(N2):n(H2)≈1:3
及时移走产生的氨
低温和高压
从化学平衡看,合成氨的适宜条件
想一想:
思考:为什么没有在常温合成氨?合成氨难在哪儿?还有什么因素制约氨的合成?
常温下合成氨化学反应速率很小!
合成氨反应为什么慢?
2. 从化学反应速率分析
——活化能高
如何增大合成氨的化学反应速率?
{5940675A-B579-460E-94D1-54222C63F5DA}对合成氨
反应的影响
影响因素
浓度
温度
压强
催化剂
增大合成氨
的反应速率
增大
升高
增大
使用
怎样降低反应的活化能?
——改变反应历程
{5940675A-B579-460E-94D1-54222C63F5DA}对合成氨
反应的影响
影响因素
浓度
温度
压强
催化剂
增大合成氨的反应速率
增大
升高
增大
使用
提高平衡混合物中氨的含量
n(N2):n(H2) ≈1:3
及时移走产生的氨
降低
增大
无影响
想一想:
3. 综合分析
实现工业生产:
综合考虑成本要低!
①压强
从化学反应速率与化学平衡考虑,都是压强越大越好。
综合成本与设备耐压:
10 MPa~30 MPa
3. 综合分析
②催化剂
增大化学反应速率,不改变平衡混合物的组成。
现在常用铁,其活性最好的温度为500 ℃左右。
3. 综合分析
③温度
综合考虑,特别是考虑催化剂的活性。
一般400~500 ℃
低温可以提高平衡混合物中氨的含量,但低温会减小化学反应速率。
在温度与压强的最佳条件下,平衡混合物中氨的含量仍不高,怎么办?
{5940675A-B579-460E-94D1-54222C63F5DA}温度/℃
氨的含量/%
0.1 MPa
10 MPa
20 MPa
30 MPa
60 MPa
100 MPa
200
15.3
81.5
86.4
89.9
95.4
98.8
300
2.20
52.0
64.2
71.0
84.2
92.6
400
0.40
25.1
38.2
47.0
65.2
79.8
500
0.10
10.6
19.1
26.4
42.2
57.5
600
0.05
4.50
9.10
13.8
23.1
31.4
想一想:
合成氨常用的生产条件:
使用催化剂
温度:400~500 ℃
压强: 10 MPa~30 MPa
将氨及时分离出来
原料气循环使用
二、寻找工业合成氨的适宜条件
三、化工生产中调控反应的一般思路
1.选取恰当的反应
思考并归纳出化工生产中调控反应的一般思路
试一试:
影响因素
调控反应
三、化工生产中调控反应的一般思路
反应
化学平衡
反应速率
最佳效果
2.分析调控方法
三、化工生产中调控反应的一般思路
3.探索最佳工艺
哈伯:
锇(剧毒)作催化剂
17.5 MPa~20.0 MPa、500~600 ℃
氨含量6%
三、化工生产中调控反应的一般思路
博施:
铁作催化剂
开发了适合高温、高压下的合成设备
设计了获得大量廉价原料气的方法
三、化工生产中调控反应的一般思路
埃特尔:
在合成氨反应初期,氮、氢分子被吸附在铁催化剂表面。进而确定吸附的氮原子和氢原子是反应活性物,整个反应就是氮原子逐步加氢最终生成氨分子的过程,并给出了每步反应的活化能。
原料用量n(N2):n(H2):
理论值为1:3
实际为1:2.8
哈伯
(1918年)
合成氨的基础开发工作
博施
(1931年)
实现了合成氨的工业化
埃特尔(2007年)
揭开了合成氨的“天机”
4.不断技术创新
合成氨与三次诺贝尔化学奖
“合成氨”里的中国人:2016年中科院大连化学物理研究所研究团队研制合成了一种新型催化剂,将合成氨的温度、压强分别降到了350 ℃、1 MPa 。
更加节能、降低成本
小结:化学反应的调控
明确目的
可行性
确定
反应
原理分析
实验摸索
找条件
化学平衡
反应速率
设备可行
成本核算
如何为一个化学反应选择适宜的生产条件?
