湖北省汉川市官备塘中学2020年九年级化学上册第6单元课题1 金刚石、石墨和C60—第2课时《单质碳的化学性质》(无答案)
文档属性
| 名称 | 湖北省汉川市官备塘中学2020年九年级化学上册第6单元课题1 金刚石、石墨和C60—第2课时《单质碳的化学性质》(无答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 216.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-11-22 00:00:00 | ||
图片预览


文档简介
课题1 第2课时《单质碳的化学性质》
1.某物质在空气中完全燃烧后,生成的气体能使澄清石灰水变浑浊,该物质一定是(
)
A.碳单质
B.含碳元素的化合物
C.含碳、氧元素的化合物
D.含碳元素的物质
2.下列性质中,不属于碳的化学性质的是( )
A.常温下的稳定性
B.氧化性
C.可燃性
D.还原性
3.“碳海绵”具备高弹性和疏松多孔的结构,主要成分是石墨烯和碳纳米管(两者都是碳单质)。下列关于“碳海绵”的说法不正确的是( )
A.常温下化学性质活泼
B.具有吸附性
C.在一定条件下可还原氧化铜
D.在氧气中完全燃烧的产物是二氧化碳
4.下列关于碳单质用途的叙述,错误的是(
)
A.金刚石用作钻探机的钻头
B.
用焦炭冶炼金属
C.用碳粉和铅可制成铅笔芯
D.用石墨做干电池的电极
5.有关碳的化学性质的叙述错误的是(
)
A.碳在常温下化学性质是比较稳定的
B.
碳和氧气反应时,产物可以是CO2也可以是CO
C.
碳和氧气的反应无论产物是什么,都是吸热反应
D.
碳和氧气的反应无论产物是什么,都是放热反应
6.“钻石恒久远,一颗永流传”这句广告词被美国“广告时代”评为20世纪经典广告之一。该广告词能体现钻石的(
)
A.硬度大
B.不能导电
C.化学性质稳定
D.熔点低
7.下列说法错误的是( )
A.木炭燃烧可放出大量的热,能用作燃料
B.碳和氧气反应时生成物一定是二氧化碳
C.碳的几种单质具有相似的化学性质
D.可利用焦炭的还原性冶炼金属
8.如图是碳还原氧化铜的实验,有关说法正确的是(
)
A.酒精灯加网罩的作用是防止火焰摆动
B.反应开始的标志是:导管口有气泡产生
C.反应结束的标志是:导管口不再产生气泡
D.实验结束时应先熄灭酒精灯,待试管冷却后再将导管从澄清石灰水中拿出
9.下列碳单质的各种用途中,利用了其化学性质的是( )
A.制作钻头
B.制作电极
C.冶炼金属
D.作冰箱除味剂
10.下列说法不正确的是( )
A.利用木炭的还原性由CuO冶炼铜
B.金刚石是最硬的非金属单质,可制成钻石
C.利用活性炭的稳定性来吸附冰箱中的异味
D.利用石墨的导电性制造石墨电极
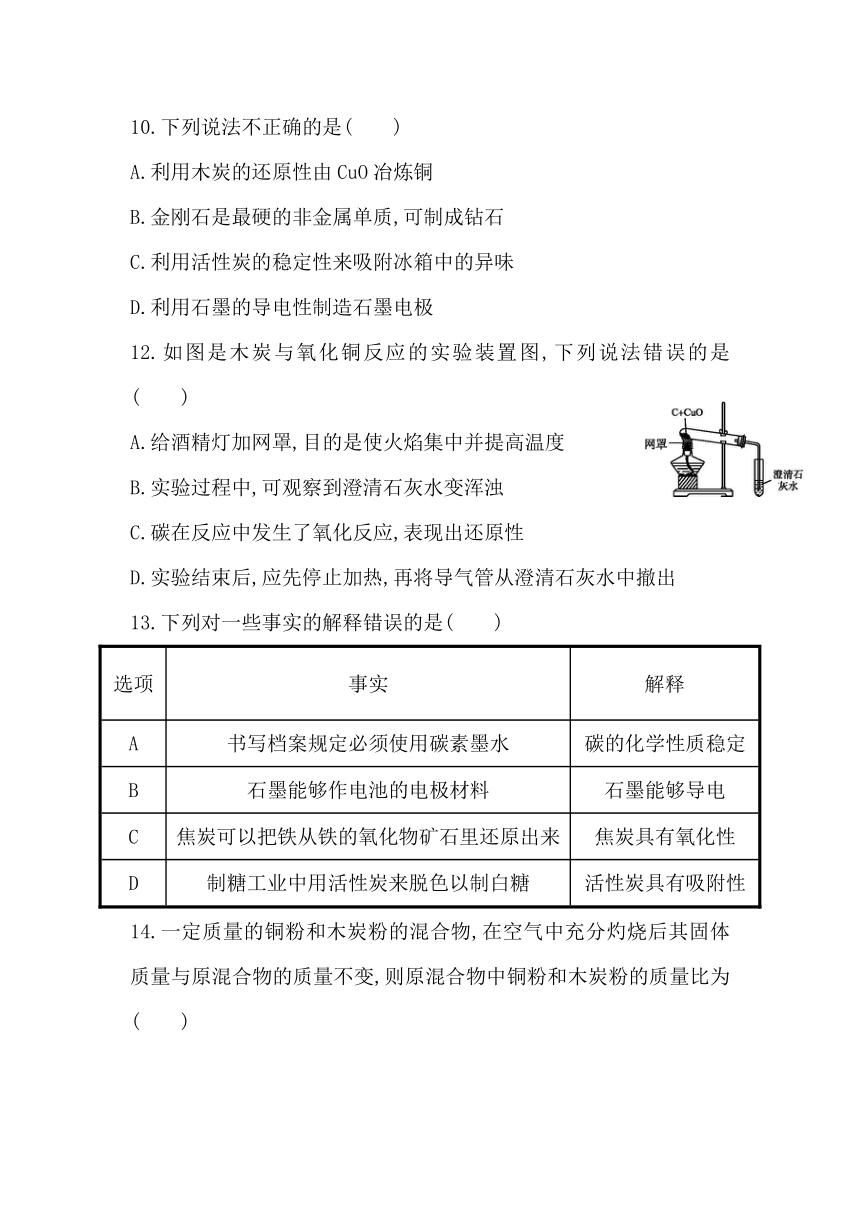
12.如图是木炭与氧化铜反应的实验装置图,下列说法错误的是( )
A.给酒精灯加网罩,目的是使火焰集中并提高温度
B.实验过程中,可观察到澄清石灰水变浑浊
C.碳在反应中发生了氧化反应,表现出还原性
D.实验结束后,应先停止加热,再将导气管从澄清石灰水中撤出
13.下列对一些事实的解释错误的是( )
选项
事实
解释
A
书写档案规定必须使用碳素墨水
碳的化学性质稳定
B
石墨能够作电池的电极材料
石墨能够导电
C
焦炭可以把铁从铁的氧化物矿石里还原出来
焦炭具有氧化性
D
制糖工业中用活性炭来脱色以制白糖
活性炭具有吸附性
14.一定质量的铜粉和木炭粉的混合物,在空气中充分灼烧后其固体质量与原混合物的质量不变,则原混合物中铜粉和木炭粉的质量比为( )
A.4∶1
B.2∶1
C.3∶2
D.1∶1
15.中国科学技术大学的科研人员在440
℃和高压下,利用金属钠与二氧化碳作用得到了金刚石(化学式:C)和碳酸钠,且金刚石的颗粒有望达到宝石级,它将给天然金刚石的开采业带来极大的挑战。下列说法中正确的是( )
A.金刚石是一种化合物
B.碳是金属元素
C.该反应中生成了新的原子
D.所得金刚石在氧气中充分燃烧生成二氧化碳
16.金刚石经琢磨后可成为璀璨夺目的装饰品——钻石,钻石素有“宝石之王”的美誉。近年来,市场上出现了合成碳化硅的钻石仿制品——莫桑钻,使不少消费者上当受骗。
(1)已知碳元素、硅元素的原子结构示意图分别为:
C
+6 Si
+14,碳、硅两种元素在原子结构上具有相同的 ,所以它们的化学性质相似。?
(2)碳化硅的化学式为 ,碳化硅属于 (填“单质”或“化合物”)。?
(3)目前,珠宝界通常利用一种名为二碘甲烷(CH2I2)的液体来鉴别莫桑钻和钻石。其鉴别方法是将莫桑钻和钻石分别放入二碘甲烷中,钻石下沉,莫桑钻上浮,这种鉴别方法所依据的原理是?
17.具体填写(1)—(3)物质性质不同的原因。并以此为例,另写两组。
(1)H2O2和H2O______________________________________。
(2)金刚石和石墨____________________________。
(3)钠原子和钠离子__________________________。
18.C60的发现使人类了解到一个全新的碳世界,回答下列问题。
(1)C60属于____________(填“单质”或“化合物”)。
(2)C60这种物质是由____________(填“分子”或“原子”)构成的。
(3)C60与金刚石、石墨具有相似的____________(填“化学”或“物理”)性质。
19.写出下列化学方程式。
(1)碳不完全燃烧:____________________________________。
(2)能将二氧化碳转化为一氧化碳的化合反应:________________。
20.某同学设计了如图所示的实验装置,进行碳还原性性质的验证,对实验进行分析并回答:
(1)检查装置气密性的方法:将导管浸入水中,_______________,说明装置气密性良好。
(2)证明碳具有还原性的实验现象是______________________,
___________________________________________________________。
(3)CuO发生________(填“氧化”或“还原”)反应。
(4)酒精灯加上网罩的作用是__________________________。
(5)实验结束后,应先__________________,再__________________。
21.我们的祖先很早就掌握了炼铜的工艺,通过学习,同学们知道木炭可以作还原剂把氧化铜中的铜还原出来,小明查阅了大量的资料后,建议用超细木炭粉与氧化铜粉末混合进行实验,他的理由是 。?
(1)同学们按如图装置进行实验,当看到澄清石灰水刚刚出现浑浊时, (填“可以”或“不能”)确定氧化铜和木炭粉已经开始反应。?
(2)为了使氧化铜中的铜完全被还原,对于下列三组氧化铜和木炭粉的质量比例,你建议选择 (填写字母),简要说明你的理由 。?
A.36∶3
B.40∶3
C.48∶3
22.碳及其氧化物性质的应用。
(1)在书写具有保存价值的档案时,规定应使用碳素墨水,原因是_________________________________________________。
(2)焦炭的主要成分是碳单质。工业上利用其还原性可__________。
(3)将一定质量的金刚石在足量的氧气中充分燃烧,固体全部消失,写出该反应的化学方程式:
___________________________________;将生成的产物用足量的氢氧化钠溶液来充分吸收并测定其质量,当金刚石的质量恰好等于___________________时,则可证明金刚石是由碳元素组成的单质。
23.若8
g氧化铜被木炭还原,试计算能生成铜的质量是多少。
1.某物质在空气中完全燃烧后,生成的气体能使澄清石灰水变浑浊,该物质一定是(
)
A.碳单质
B.含碳元素的化合物
C.含碳、氧元素的化合物
D.含碳元素的物质
2.下列性质中,不属于碳的化学性质的是( )
A.常温下的稳定性
B.氧化性
C.可燃性
D.还原性
3.“碳海绵”具备高弹性和疏松多孔的结构,主要成分是石墨烯和碳纳米管(两者都是碳单质)。下列关于“碳海绵”的说法不正确的是( )
A.常温下化学性质活泼
B.具有吸附性
C.在一定条件下可还原氧化铜
D.在氧气中完全燃烧的产物是二氧化碳
4.下列关于碳单质用途的叙述,错误的是(
)
A.金刚石用作钻探机的钻头
B.
用焦炭冶炼金属
C.用碳粉和铅可制成铅笔芯
D.用石墨做干电池的电极
5.有关碳的化学性质的叙述错误的是(
)
A.碳在常温下化学性质是比较稳定的
B.
碳和氧气反应时,产物可以是CO2也可以是CO
C.
碳和氧气的反应无论产物是什么,都是吸热反应
D.
碳和氧气的反应无论产物是什么,都是放热反应
6.“钻石恒久远,一颗永流传”这句广告词被美国“广告时代”评为20世纪经典广告之一。该广告词能体现钻石的(
)
A.硬度大
B.不能导电
C.化学性质稳定
D.熔点低
7.下列说法错误的是( )
A.木炭燃烧可放出大量的热,能用作燃料
B.碳和氧气反应时生成物一定是二氧化碳
C.碳的几种单质具有相似的化学性质
D.可利用焦炭的还原性冶炼金属
8.如图是碳还原氧化铜的实验,有关说法正确的是(
)
A.酒精灯加网罩的作用是防止火焰摆动
B.反应开始的标志是:导管口有气泡产生
C.反应结束的标志是:导管口不再产生气泡
D.实验结束时应先熄灭酒精灯,待试管冷却后再将导管从澄清石灰水中拿出
9.下列碳单质的各种用途中,利用了其化学性质的是( )
A.制作钻头
B.制作电极
C.冶炼金属
D.作冰箱除味剂
10.下列说法不正确的是( )
A.利用木炭的还原性由CuO冶炼铜
B.金刚石是最硬的非金属单质,可制成钻石
C.利用活性炭的稳定性来吸附冰箱中的异味
D.利用石墨的导电性制造石墨电极
12.如图是木炭与氧化铜反应的实验装置图,下列说法错误的是( )
A.给酒精灯加网罩,目的是使火焰集中并提高温度
B.实验过程中,可观察到澄清石灰水变浑浊
C.碳在反应中发生了氧化反应,表现出还原性
D.实验结束后,应先停止加热,再将导气管从澄清石灰水中撤出
13.下列对一些事实的解释错误的是( )
选项
事实
解释
A
书写档案规定必须使用碳素墨水
碳的化学性质稳定
B
石墨能够作电池的电极材料
石墨能够导电
C
焦炭可以把铁从铁的氧化物矿石里还原出来
焦炭具有氧化性
D
制糖工业中用活性炭来脱色以制白糖
活性炭具有吸附性
14.一定质量的铜粉和木炭粉的混合物,在空气中充分灼烧后其固体质量与原混合物的质量不变,则原混合物中铜粉和木炭粉的质量比为( )
A.4∶1
B.2∶1
C.3∶2
D.1∶1
15.中国科学技术大学的科研人员在440
℃和高压下,利用金属钠与二氧化碳作用得到了金刚石(化学式:C)和碳酸钠,且金刚石的颗粒有望达到宝石级,它将给天然金刚石的开采业带来极大的挑战。下列说法中正确的是( )
A.金刚石是一种化合物
B.碳是金属元素
C.该反应中生成了新的原子
D.所得金刚石在氧气中充分燃烧生成二氧化碳
16.金刚石经琢磨后可成为璀璨夺目的装饰品——钻石,钻石素有“宝石之王”的美誉。近年来,市场上出现了合成碳化硅的钻石仿制品——莫桑钻,使不少消费者上当受骗。
(1)已知碳元素、硅元素的原子结构示意图分别为:
C
+6 Si
+14,碳、硅两种元素在原子结构上具有相同的 ,所以它们的化学性质相似。?
(2)碳化硅的化学式为 ,碳化硅属于 (填“单质”或“化合物”)。?
(3)目前,珠宝界通常利用一种名为二碘甲烷(CH2I2)的液体来鉴别莫桑钻和钻石。其鉴别方法是将莫桑钻和钻石分别放入二碘甲烷中,钻石下沉,莫桑钻上浮,这种鉴别方法所依据的原理是?
17.具体填写(1)—(3)物质性质不同的原因。并以此为例,另写两组。
(1)H2O2和H2O______________________________________。
(2)金刚石和石墨____________________________。
(3)钠原子和钠离子__________________________。
18.C60的发现使人类了解到一个全新的碳世界,回答下列问题。
(1)C60属于____________(填“单质”或“化合物”)。
(2)C60这种物质是由____________(填“分子”或“原子”)构成的。
(3)C60与金刚石、石墨具有相似的____________(填“化学”或“物理”)性质。
19.写出下列化学方程式。
(1)碳不完全燃烧:____________________________________。
(2)能将二氧化碳转化为一氧化碳的化合反应:________________。
20.某同学设计了如图所示的实验装置,进行碳还原性性质的验证,对实验进行分析并回答:
(1)检查装置气密性的方法:将导管浸入水中,_______________,说明装置气密性良好。
(2)证明碳具有还原性的实验现象是______________________,
___________________________________________________________。
(3)CuO发生________(填“氧化”或“还原”)反应。
(4)酒精灯加上网罩的作用是__________________________。
(5)实验结束后,应先__________________,再__________________。
21.我们的祖先很早就掌握了炼铜的工艺,通过学习,同学们知道木炭可以作还原剂把氧化铜中的铜还原出来,小明查阅了大量的资料后,建议用超细木炭粉与氧化铜粉末混合进行实验,他的理由是 。?
(1)同学们按如图装置进行实验,当看到澄清石灰水刚刚出现浑浊时, (填“可以”或“不能”)确定氧化铜和木炭粉已经开始反应。?
(2)为了使氧化铜中的铜完全被还原,对于下列三组氧化铜和木炭粉的质量比例,你建议选择 (填写字母),简要说明你的理由 。?
A.36∶3
B.40∶3
C.48∶3
22.碳及其氧化物性质的应用。
(1)在书写具有保存价值的档案时,规定应使用碳素墨水,原因是_________________________________________________。
(2)焦炭的主要成分是碳单质。工业上利用其还原性可__________。
(3)将一定质量的金刚石在足量的氧气中充分燃烧,固体全部消失,写出该反应的化学方程式:
___________________________________;将生成的产物用足量的氢氧化钠溶液来充分吸收并测定其质量,当金刚石的质量恰好等于___________________时,则可证明金刚石是由碳元素组成的单质。
23.若8
g氧化铜被木炭还原,试计算能生成铜的质量是多少。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
