9.2 溶解度 第一课时(课件21页)
图片预览




文档简介
(共21张PPT)
课题2
溶解度
人教版
初中化学
第一课时
1.
知道什么是饱和溶液和不饱和溶液。
2.
能分析影响物质溶解能力的因素。
3.
掌握饱和溶液和不饱和溶液的相互转化。
学习目标
5g氯化钠
20ml水
再加5克氯化钠
5ml水
待溶解后
氯化钠溶液
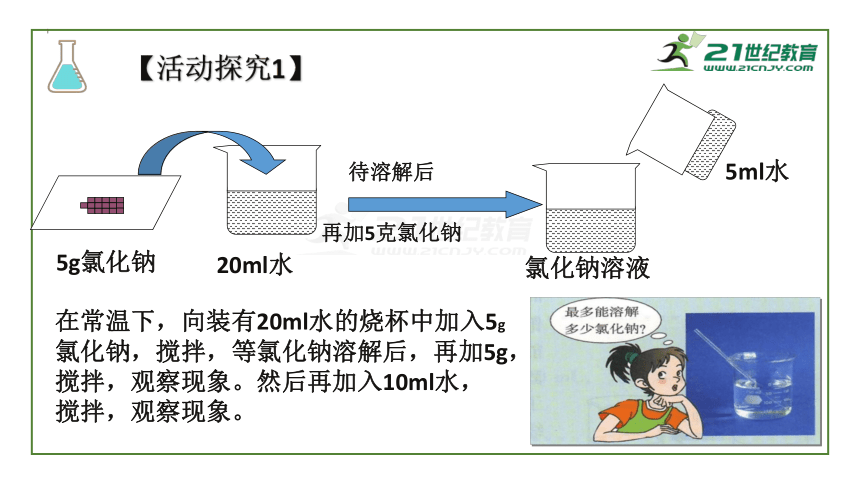
在常温下,向装有20ml水的烧杯中加入5g氯化钠,搅拌,等氯化钠溶解后,再加5g,搅拌,观察现象。然后再加入10ml水,搅拌,观察现象。
【活动探究1】
操作
加入5g
食盐搅拌
再加入5g
食盐搅拌
再加入
5mL水搅拌
现象
结论
食盐完
全溶解
食盐有少量剩余
剩余的食盐又溶解
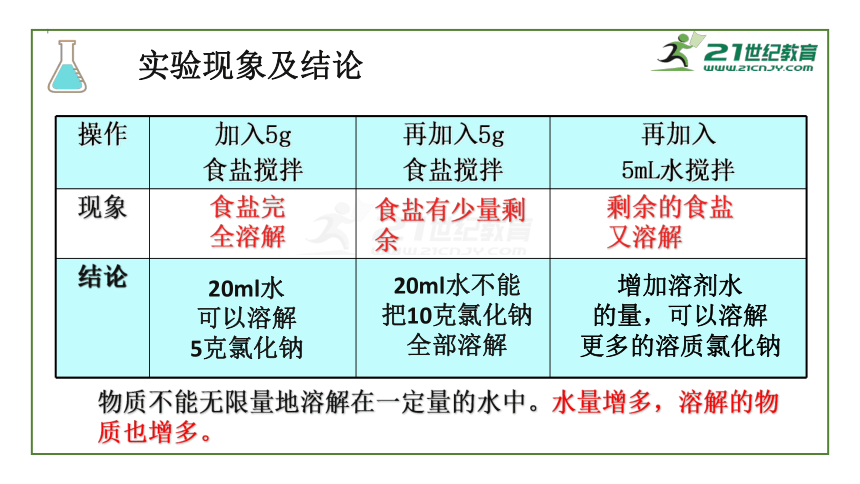
物质不能无限量地溶解在一定量的水中。水量增多,溶解的物质也增多。
实验现象及结论
20ml水
可以溶解
5克氯化钠
20ml水不能
把10克氯化钠
全部溶解
增加溶剂水
的量,可以溶解
更多的溶质氯化钠
在
,向
里加入某种溶质,当溶质不能继续溶解时所得到的溶液叫做饱和溶液
一定温度下
一定量溶剂
饱和溶液:
在
,向
里加入某种溶质,当溶质还能继续溶解时所得到的溶液叫做该物质的不饱和溶液
一定温度下
一定量溶剂
不饱和溶液:
饱和溶液二要素:
一定温度下
一定量溶剂
上面的实验现象,你能说出饱和溶液和不饱和溶液的概念吗?
方法:
在一定温度时,向溶液中加入少量同种溶质,如果不再溶解,则溶液是饱和溶液,如果继续溶解,则溶液是不饱和溶液。
一般地说,要确定某一溶液是否饱和,要看在一定温度下,该溶液中有没有不能继续溶解的剩余溶质存在,若存在未溶解的溶质且溶质的量不再减少,那么这种溶液就是该温度下该溶质的饱和溶液。
如何判断一种溶液是否饱和呢?
我们在说某溶液是饱和溶液,还是不饱和溶液时,为什么一定要强调“一定温度下,一定量的溶剂里”这两个条件呢?
提示:以上实验中已经不能溶解的氯化钠固体,加入15Ml的水后,又能溶解了。还有哪些因素影响物质溶解的多少呢?
思考:
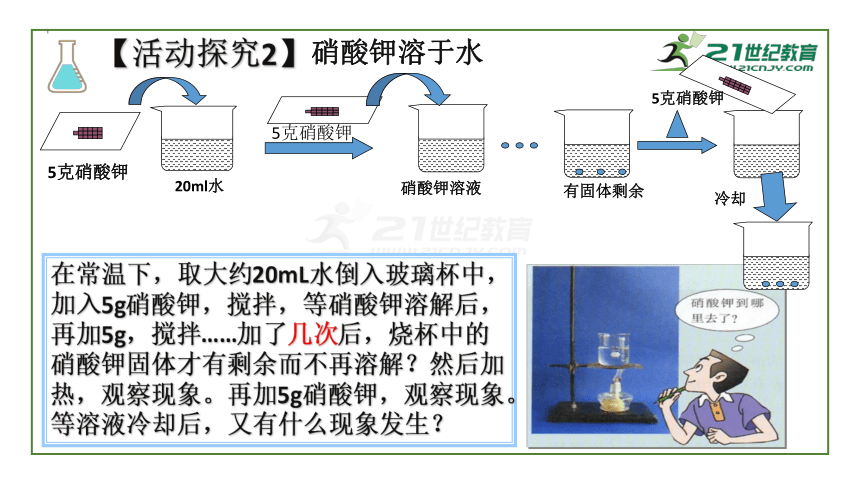
在常温下,取大约20mL水倒入玻璃杯中,加入5g硝酸钾,搅拌,等硝酸钾溶解后,再加5g,搅拌……加了几次后,烧杯中的硝酸钾固体才有剩余而不再溶解?然后加热,观察现象。再加5g硝酸钾,观察现象。等溶液冷却后,又有什么现象发生?
【活动探究2】
20ml水
5克硝酸钾
5克硝酸钾
硝酸钾溶液
有固体剩余
5克硝酸钾
冷却
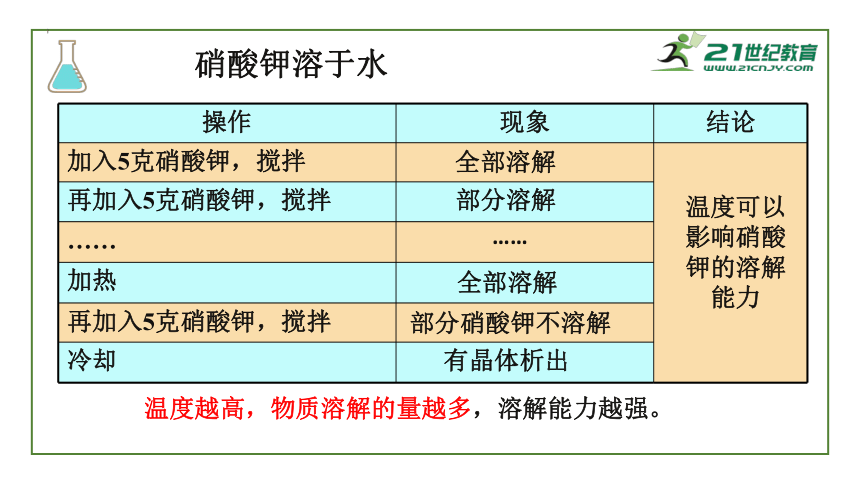
硝酸钾溶于水
操作
现象
结论
加入5克硝酸钾,搅拌
再加入5克硝酸钾,搅拌
……
加热
再加入5克硝酸钾,搅拌
冷却
全部溶解
部分溶解
部分硝酸钾不溶解
全部溶解
有晶体析出
……
温度可以影响硝酸钾的溶解能力
硝酸钾溶于水
温度越高,物质溶解的量越多,溶解能力越强。
2、温度越高,物质溶解的量越多;
1、增加溶剂的量,可以溶解更多的溶质;
可以通过哪些方法,溶解更多的溶质?
怎样实现饱和溶液与不饱和溶液的相互转化呢?
小结:
饱和溶液与不饱和溶液之间的转化
饱和溶液与不饱和溶液可以相互转化,对大多数溶质来说:
增加溶质、降低温度、蒸发溶剂
增加溶剂或升高温度
“升温”和“降温”两种方法适合大多数固态溶质的溶液,对极少数固体(如:氢氧化钙)来说恰好相反.
不饱和溶液
饱和溶液
不饱和溶液
饱和溶液
增加溶质、降低温度、恒温蒸发溶剂
增加溶剂、升高温度
“升温”和“降温”两种方法适合大多数固态溶质的溶液,对极少数固体(如:氢氧化钙)来说恰好相反.
注意:只有指明“在一定温度下”和“在一定量溶剂里”,溶液的“饱和”与“不饱和”才有确定的意义。
3.饱和溶液与不饱和溶液的转化(通常情况)
硝酸钾晶体
冷却热饱和溶液
结晶后所得到的溶液是饱和溶液。
(1)降温结晶/冷却热饱和溶液
结晶:溶解在溶液里的溶质以晶体的形式析出,叫做结晶。
(适用于溶解度受温度影响较大的物质:硝酸钾)
5、结晶(分离混合物的方法)
海水
贮水池
蒸发池
结晶池
食盐
母液
氯化钠
多种化工原料
从海水中提取食盐
蒸发溶剂
(2)蒸发结晶
NaCl的饱和溶液
恒温蒸发溶剂(适用于溶解度受温度影响比较小的物质:氯化钠)
课堂训练:
1.某物质的饱和溶液中,加入一些该溶质的固体,则下列说法正确的是(
)
A.
溶质质量减少;
B.
溶液质量增大;
C.
固体质量不变;
D.
溶质质量增加.
C
2.一定温度下,从500克的饱和溶液中倒出100克溶液,剩余的溶液里,下列数值比原溶液减少的是(
)
①溶质的质量;
②溶剂的质量;
③溶液的密度;
④溶液的质量;
⑤溶质的质量分数(即:浓度);
A.
①②③④
B.
②③④⑤
C.
①②④
D.
①②③④⑤
C
3.使不饱和溶液变为饱和溶液,最可靠的方法是(
)
A.升高温度
B.加入溶质
C.降低温度
D.倒出一部分溶液
B
4.
30℃时,往100
g硝酸钾溶液中加入10g硝酸钾晶体,充分搅拌后,尚有部分晶体未溶,稍加热后晶体全部溶解,试判断下列说法中正确的是(
)
A.
搅拌后及加热前一定是饱和溶液
B.
搅拌后及加热前一定是不饱和溶液
C.
加热后一定是饱和溶液
D.
加热后不一定是饱和溶液
AD
5.
20℃时,100克硝酸钾饱和溶液,当其他条件不变
温度升高到80℃时,该溶液为
(饱和溶液还是不饱和溶液),此时溶液的质量为
克。
不饱和溶液
100
6.
A、B、C、D四个烧杯里分别盛有质量相等的同种溶剂,向四个烧杯加入某溶质,且固体溶质质量依次减少(温度相同),充分溶解,(如下图所示)回答下列各问(填序号)
(1)______中盛的一定是饱和溶液;
(2)______中盛的可能是饱和溶液;
(3)______中盛的一定是不饱和溶液;
A
B
C
D
A
B
C
D
不饱和溶液
饱和溶液
增加溶质、降低温度、恒温蒸发溶剂
增加溶剂、升高温度
课堂小结:
结晶的方法
蒸发结晶
降温结晶(冷却热饱和溶液)
课题2
溶解度
人教版
初中化学
第一课时
1.
知道什么是饱和溶液和不饱和溶液。
2.
能分析影响物质溶解能力的因素。
3.
掌握饱和溶液和不饱和溶液的相互转化。
学习目标
5g氯化钠
20ml水
再加5克氯化钠
5ml水
待溶解后
氯化钠溶液
在常温下,向装有20ml水的烧杯中加入5g氯化钠,搅拌,等氯化钠溶解后,再加5g,搅拌,观察现象。然后再加入10ml水,搅拌,观察现象。
【活动探究1】
操作
加入5g
食盐搅拌
再加入5g
食盐搅拌
再加入
5mL水搅拌
现象
结论
食盐完
全溶解
食盐有少量剩余
剩余的食盐又溶解
物质不能无限量地溶解在一定量的水中。水量增多,溶解的物质也增多。
实验现象及结论
20ml水
可以溶解
5克氯化钠
20ml水不能
把10克氯化钠
全部溶解
增加溶剂水
的量,可以溶解
更多的溶质氯化钠
在
,向
里加入某种溶质,当溶质不能继续溶解时所得到的溶液叫做饱和溶液
一定温度下
一定量溶剂
饱和溶液:
在
,向
里加入某种溶质,当溶质还能继续溶解时所得到的溶液叫做该物质的不饱和溶液
一定温度下
一定量溶剂
不饱和溶液:
饱和溶液二要素:
一定温度下
一定量溶剂
上面的实验现象,你能说出饱和溶液和不饱和溶液的概念吗?
方法:
在一定温度时,向溶液中加入少量同种溶质,如果不再溶解,则溶液是饱和溶液,如果继续溶解,则溶液是不饱和溶液。
一般地说,要确定某一溶液是否饱和,要看在一定温度下,该溶液中有没有不能继续溶解的剩余溶质存在,若存在未溶解的溶质且溶质的量不再减少,那么这种溶液就是该温度下该溶质的饱和溶液。
如何判断一种溶液是否饱和呢?
我们在说某溶液是饱和溶液,还是不饱和溶液时,为什么一定要强调“一定温度下,一定量的溶剂里”这两个条件呢?
提示:以上实验中已经不能溶解的氯化钠固体,加入15Ml的水后,又能溶解了。还有哪些因素影响物质溶解的多少呢?
思考:
在常温下,取大约20mL水倒入玻璃杯中,加入5g硝酸钾,搅拌,等硝酸钾溶解后,再加5g,搅拌……加了几次后,烧杯中的硝酸钾固体才有剩余而不再溶解?然后加热,观察现象。再加5g硝酸钾,观察现象。等溶液冷却后,又有什么现象发生?
【活动探究2】
20ml水
5克硝酸钾
5克硝酸钾
硝酸钾溶液
有固体剩余
5克硝酸钾
冷却
硝酸钾溶于水
操作
现象
结论
加入5克硝酸钾,搅拌
再加入5克硝酸钾,搅拌
……
加热
再加入5克硝酸钾,搅拌
冷却
全部溶解
部分溶解
部分硝酸钾不溶解
全部溶解
有晶体析出
……
温度可以影响硝酸钾的溶解能力
硝酸钾溶于水
温度越高,物质溶解的量越多,溶解能力越强。
2、温度越高,物质溶解的量越多;
1、增加溶剂的量,可以溶解更多的溶质;
可以通过哪些方法,溶解更多的溶质?
怎样实现饱和溶液与不饱和溶液的相互转化呢?
小结:
饱和溶液与不饱和溶液之间的转化
饱和溶液与不饱和溶液可以相互转化,对大多数溶质来说:
增加溶质、降低温度、蒸发溶剂
增加溶剂或升高温度
“升温”和“降温”两种方法适合大多数固态溶质的溶液,对极少数固体(如:氢氧化钙)来说恰好相反.
不饱和溶液
饱和溶液
不饱和溶液
饱和溶液
增加溶质、降低温度、恒温蒸发溶剂
增加溶剂、升高温度
“升温”和“降温”两种方法适合大多数固态溶质的溶液,对极少数固体(如:氢氧化钙)来说恰好相反.
注意:只有指明“在一定温度下”和“在一定量溶剂里”,溶液的“饱和”与“不饱和”才有确定的意义。
3.饱和溶液与不饱和溶液的转化(通常情况)
硝酸钾晶体
冷却热饱和溶液
结晶后所得到的溶液是饱和溶液。
(1)降温结晶/冷却热饱和溶液
结晶:溶解在溶液里的溶质以晶体的形式析出,叫做结晶。
(适用于溶解度受温度影响较大的物质:硝酸钾)
5、结晶(分离混合物的方法)
海水
贮水池
蒸发池
结晶池
食盐
母液
氯化钠
多种化工原料
从海水中提取食盐
蒸发溶剂
(2)蒸发结晶
NaCl的饱和溶液
恒温蒸发溶剂(适用于溶解度受温度影响比较小的物质:氯化钠)
课堂训练:
1.某物质的饱和溶液中,加入一些该溶质的固体,则下列说法正确的是(
)
A.
溶质质量减少;
B.
溶液质量增大;
C.
固体质量不变;
D.
溶质质量增加.
C
2.一定温度下,从500克的饱和溶液中倒出100克溶液,剩余的溶液里,下列数值比原溶液减少的是(
)
①溶质的质量;
②溶剂的质量;
③溶液的密度;
④溶液的质量;
⑤溶质的质量分数(即:浓度);
A.
①②③④
B.
②③④⑤
C.
①②④
D.
①②③④⑤
C
3.使不饱和溶液变为饱和溶液,最可靠的方法是(
)
A.升高温度
B.加入溶质
C.降低温度
D.倒出一部分溶液
B
4.
30℃时,往100
g硝酸钾溶液中加入10g硝酸钾晶体,充分搅拌后,尚有部分晶体未溶,稍加热后晶体全部溶解,试判断下列说法中正确的是(
)
A.
搅拌后及加热前一定是饱和溶液
B.
搅拌后及加热前一定是不饱和溶液
C.
加热后一定是饱和溶液
D.
加热后不一定是饱和溶液
AD
5.
20℃时,100克硝酸钾饱和溶液,当其他条件不变
温度升高到80℃时,该溶液为
(饱和溶液还是不饱和溶液),此时溶液的质量为
克。
不饱和溶液
100
6.
A、B、C、D四个烧杯里分别盛有质量相等的同种溶剂,向四个烧杯加入某溶质,且固体溶质质量依次减少(温度相同),充分溶解,(如下图所示)回答下列各问(填序号)
(1)______中盛的一定是饱和溶液;
(2)______中盛的可能是饱和溶液;
(3)______中盛的一定是不饱和溶液;
A
B
C
D
A
B
C
D
不饱和溶液
饱和溶液
增加溶质、降低温度、恒温蒸发溶剂
增加溶剂、升高温度
课堂小结:
结晶的方法
蒸发结晶
降温结晶(冷却热饱和溶液)
同课章节目录
