初中化学粤教版前四章复习提纲
图片预览

文档简介
第一章复习要点
物理性质
物质的性质 (二者的区别)
化学性质
性质和变化的区别
物理变化
物质的变化 (二者的区别)
化学变化
化学实验基本操作:酒精灯、量筒、试管、胶头滴管等仪器的使用及药品的取用、加热等操作(参照实验报告册1-11页内容)
第二章复习要点
一、空气的成分:
氮气:78% (4/5)
氧气:21% (1/5)
1、 成分 稀有气体:0.94%
二氧化碳:0.03%
其他气体和杂质:0.03%
氮气
2、 用途
稀有气体
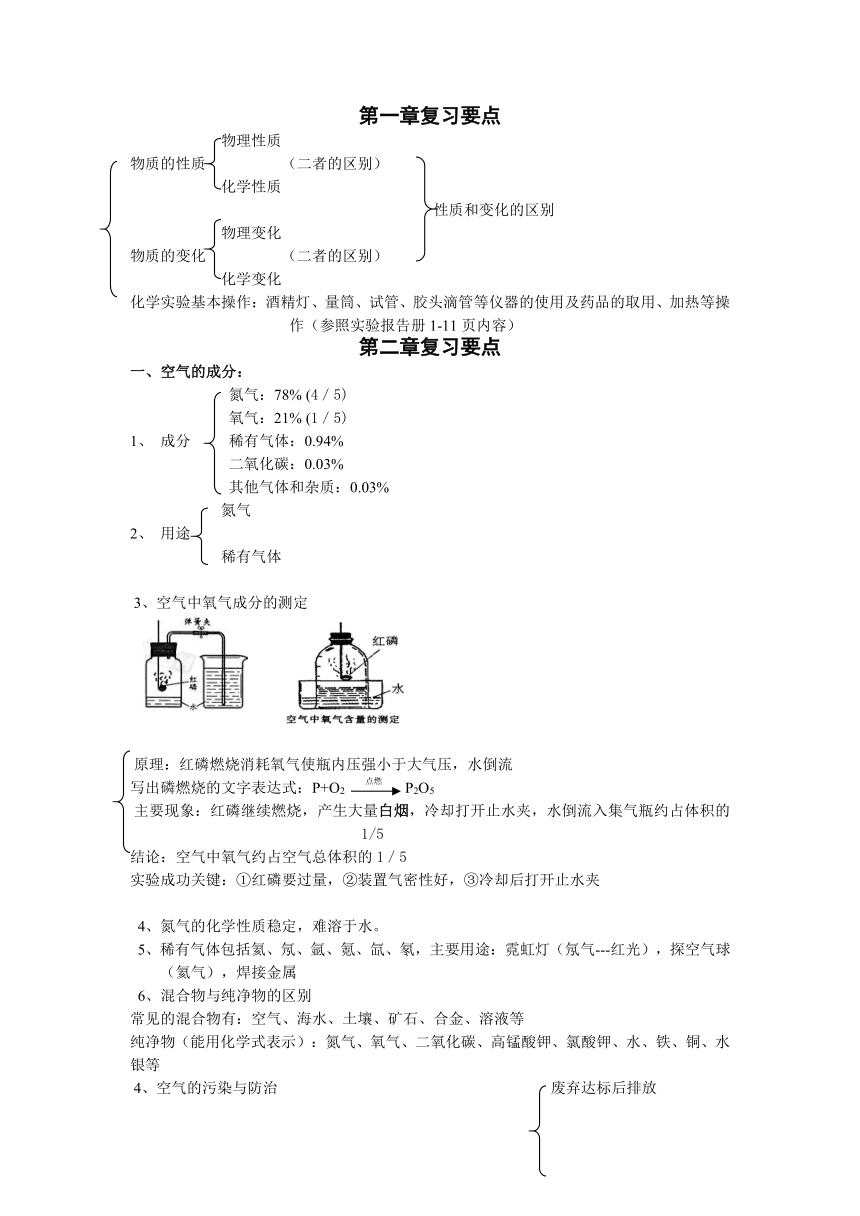
3、空气中氧气成分的测定
原理:红磷燃烧消耗氧气使瓶内压强小于大气压,水倒流
写出磷燃烧的文字表达式:P+O2 点燃 P2O5
主要现象:红磷继续燃烧,产生大量白烟,冷却打开止水夹,水倒流入集气瓶约占体积的1/5
结论:空气中氧气约占空气总体积的1/5
实验成功关键:①红磷要过量,②装置气密性好,③冷却后打开止水夹
4、氮气的化学性质稳定,难溶于水。
5、稀有气体包括氦、氖、氩、氪、氙、氡,主要用途:霓虹灯(氖气---红光),探空气球(氦气),焊接金属
6、混合物与纯净物的区别
常见的混合物有:空气、海水、土壤、矿石、合金、溶液等
纯净物(能用化学式表示):氮气、氧气、二氧化碳、高锰酸钾、氯酸钾、水、铁、铜、水银等
4、空气的污染与防治 废弃达标后排放
工业污染源 煤炭综合利用
污染源 交通污染源 防治 改变能源结构
生活污染源 使用无铅汽油
植树造林增大绿化面积
气体污染物(CO SO2 NO2)
污染物 颗粒污染物
首要污染物
质量日报 空气污染指数
空气质量级别
二、物质构成的奥秘:
概念:构成物质的一种微粒(保持物质化学性质的最小微粒)
体积、质量很小
分子 特性 不断运动
分子间有间隙
分子论提出者:阿伏伽德罗
概念:化学变化中的最小微粒
特性: 体积、质量很小
不断运动
1、微粒
原子 原子论提出者:道尔顿
该原子的质量
相对原子质量= (C-12的质量)x1/12 = 质子数 + 中子数
质子(1个质子带一个单位正电荷)
原子核(+)
内部结构: 原子 中子(不带电)
核外电子(一个电子带一个单位负电荷)
核电荷数=质子数=核外电子数
相对原子质量=质子数+中子数=一个原子的质量/1/12一个12C原子的质量。
离子 :带电的原子或原子团(Mg2+ SO42+)
2、原子结构示意图及离子结构示意图:
原子结构示意图:核内质子数==核外电子数
离子结构示意图:阳离子:核内质子数>核外电子数
阴离子:核内质子数<核外电子数
3、分子和原子的本质区别是什么?
第三章复习要点
一、氧气的物理性质与化学性质:
1、物理性质:无色、无味 、气体,密度比空气大,不易溶于水
2、化学性质:化学性质比较活泼的气体(助燃性,氧化性)
碳 + 氧气 点燃 二氧化碳 C+O2 点燃 CO2
磷 + 氧气 点燃 五氧化二磷 P+O2 点燃 P2O5 氧化
硫 + 氧气 点燃 二氧化硫 S+O2 点燃 SO2 化合 反应
镁 + 氧气 点燃 氧化镁 Mg+O2 点燃 MgO 反应
铁 + 氧气 点燃 四氧化三铁 Fe+O2 点燃 Fe 3O4
石蜡+氧气 点燃 二氧化碳+水
现象:①黑色的C和O2反应的现象是:在氧气中比在空气中更旺,发出白光,放热,生成能使澄清石灰水变浑浊的气体
②红色或白色的P和O2反应的现象是:产生大量白烟(用于发令枪、烟雾弹),放热。
氧气 ③S和O2反应的现象是发出蓝紫色的火焰,生成具有刺激性气味的气体。
④银白色的Mg和O2反应的现象是:发出耀眼的白光(用于照明弹等),放出大量热,生成白色固体。
⑤银白色的Fe铁丝和O2反应的现象是:剧烈燃烧,火星四射,生成黑色固体,注意点:预先放入少量水或者铺一层沙子,防止生成的高温熔物溅落炸裂集气瓶底部。
发生装置类型
3、制取 过氧化氢 二氧化锰 水 + 氧气 (固液不加热型)
原理 氯酸钾 二氧化锰 氯化钾 + 氧气 (固固加热型)
加热
高锰酸钾 加热 锰酸钾 + 二氧化锰 +氧气(同上
(1)实验室 装置:(查、装、定、点、收、离、熄 )
制法 收集方法: 向上排空气法
排水法
验满方法:带火星的木条放集气瓶口,观察木条是否复燃,若复燃证明已满
检验方法:带火星的木条伸入集气瓶中,观察木条是否复燃,若复燃是氧气
(2)工业制法:分离液态空气法、膜分离法
4、氧气的用途:供给呼吸、支持燃烧
装置的选择:
发生装置
装置类型 固固加热型 固液不加热型 固液不加热型
收集装置:
收集方法:向上排空气法 排水法
二、燃烧与灭火原理 燃烧条件
灭火原理
缓慢氧化 升温至 自燃 着火点 燃烧 有限空间 爆炸
着火点以上 以上 急速燃烧
四、元素:
1、一种元素与另一种元素的本质区别是质子数不同。
2、一般元素符号的意义有两点:宏观表示一种元素,微观表示一个原子。
由原子构成的物质元素符号还表示一种物质。
元素符号的前面加上数字只具有微观意义,如2H只表示2个氢原子。
4、根据所含元素不同把物质进行分类:(在短线上写出所举例子的化学式)
元素 混合物
(多种物质)
单原子 稀有气体
物质 根据组成 单质 构成 金属
物质的种类 (同种元素) 非金属(C S P Si)
纯净物 根据组成 其他
元素的种类 氧化物
化合物
(多种元素) 其他
第四章复习要点
一 水的存在、性质和组成
水资源 沉淀法(加明矾:使悬浮物沉降)
水的净化方法 过滤法 (活性炭:吸附杂质)
饮用水 水的纯化方法: 蒸馏法
硬水与软水 检验(肥皂水)
软化(工业:蒸馏法,生活:煮沸法)
水的性质 物理性质
化学性质:通电时分解
水的组成 水分解实验 仪器:直流电源
药品:水(内加氢氧化钠或硫酸,目的:增加溶液导电性) 现象:正极 带火星的木条复燃 (氧气)
负极 能燃烧,发出淡蓝色火焰 (氢气)
体积比:1:2(氧气:氢气)质量比:8:1(氧气:氢气)
结论:水 通电 氢气 + 氧气 H2O 通电 H2+O2
水是由氢元素和氧元素组成的,一个水分子是由两个氢原子和一个氧原子构成的,化学变化中,分子可分,原子不可分
二 化学用语
概念理解
规则
化合价 常见化合价(口诀)
求化合价
应用 判断化学式正误
书写化学式
定义 单原子单质
单质 多原子单质
化学式 书写
化合物 (排、标、叉、查)
表示意义:表示一种物质,表示物质的组成,表示一个分子,表示一个分子中所含原子的个数
计算:相对分子质量:
组成化合物各元素的质量比
化合物中某一元素的质量分数
化合物中某一元素的质量
提供依据 运用 (1)表示化学反应
质量守恒定律 化学方程式
遵循 依据 (2)有关计算
(1)反应物、生成物、反应条件 (2)各物质的质量关系
组成
物理性质
物质的性质 (二者的区别)
化学性质
性质和变化的区别
物理变化
物质的变化 (二者的区别)
化学变化
化学实验基本操作:酒精灯、量筒、试管、胶头滴管等仪器的使用及药品的取用、加热等操作(参照实验报告册1-11页内容)
第二章复习要点
一、空气的成分:
氮气:78% (4/5)
氧气:21% (1/5)
1、 成分 稀有气体:0.94%
二氧化碳:0.03%
其他气体和杂质:0.03%
氮气
2、 用途
稀有气体
3、空气中氧气成分的测定
原理:红磷燃烧消耗氧气使瓶内压强小于大气压,水倒流
写出磷燃烧的文字表达式:P+O2 点燃 P2O5
主要现象:红磷继续燃烧,产生大量白烟,冷却打开止水夹,水倒流入集气瓶约占体积的1/5
结论:空气中氧气约占空气总体积的1/5
实验成功关键:①红磷要过量,②装置气密性好,③冷却后打开止水夹
4、氮气的化学性质稳定,难溶于水。
5、稀有气体包括氦、氖、氩、氪、氙、氡,主要用途:霓虹灯(氖气---红光),探空气球(氦气),焊接金属
6、混合物与纯净物的区别
常见的混合物有:空气、海水、土壤、矿石、合金、溶液等
纯净物(能用化学式表示):氮气、氧气、二氧化碳、高锰酸钾、氯酸钾、水、铁、铜、水银等
4、空气的污染与防治 废弃达标后排放
工业污染源 煤炭综合利用
污染源 交通污染源 防治 改变能源结构
生活污染源 使用无铅汽油
植树造林增大绿化面积
气体污染物(CO SO2 NO2)
污染物 颗粒污染物
首要污染物
质量日报 空气污染指数
空气质量级别
二、物质构成的奥秘:
概念:构成物质的一种微粒(保持物质化学性质的最小微粒)
体积、质量很小
分子 特性 不断运动
分子间有间隙
分子论提出者:阿伏伽德罗
概念:化学变化中的最小微粒
特性: 体积、质量很小
不断运动
1、微粒
原子 原子论提出者:道尔顿
该原子的质量
相对原子质量= (C-12的质量)x1/12 = 质子数 + 中子数
质子(1个质子带一个单位正电荷)
原子核(+)
内部结构: 原子 中子(不带电)
核外电子(一个电子带一个单位负电荷)
核电荷数=质子数=核外电子数
相对原子质量=质子数+中子数=一个原子的质量/1/12一个12C原子的质量。
离子 :带电的原子或原子团(Mg2+ SO42+)
2、原子结构示意图及离子结构示意图:
原子结构示意图:核内质子数==核外电子数
离子结构示意图:阳离子:核内质子数>核外电子数
阴离子:核内质子数<核外电子数
3、分子和原子的本质区别是什么?
第三章复习要点
一、氧气的物理性质与化学性质:
1、物理性质:无色、无味 、气体,密度比空气大,不易溶于水
2、化学性质:化学性质比较活泼的气体(助燃性,氧化性)
碳 + 氧气 点燃 二氧化碳 C+O2 点燃 CO2
磷 + 氧气 点燃 五氧化二磷 P+O2 点燃 P2O5 氧化
硫 + 氧气 点燃 二氧化硫 S+O2 点燃 SO2 化合 反应
镁 + 氧气 点燃 氧化镁 Mg+O2 点燃 MgO 反应
铁 + 氧气 点燃 四氧化三铁 Fe+O2 点燃 Fe 3O4
石蜡+氧气 点燃 二氧化碳+水
现象:①黑色的C和O2反应的现象是:在氧气中比在空气中更旺,发出白光,放热,生成能使澄清石灰水变浑浊的气体
②红色或白色的P和O2反应的现象是:产生大量白烟(用于发令枪、烟雾弹),放热。
氧气 ③S和O2反应的现象是发出蓝紫色的火焰,生成具有刺激性气味的气体。
④银白色的Mg和O2反应的现象是:发出耀眼的白光(用于照明弹等),放出大量热,生成白色固体。
⑤银白色的Fe铁丝和O2反应的现象是:剧烈燃烧,火星四射,生成黑色固体,注意点:预先放入少量水或者铺一层沙子,防止生成的高温熔物溅落炸裂集气瓶底部。
发生装置类型
3、制取 过氧化氢 二氧化锰 水 + 氧气 (固液不加热型)
原理 氯酸钾 二氧化锰 氯化钾 + 氧气 (固固加热型)
加热
高锰酸钾 加热 锰酸钾 + 二氧化锰 +氧气(同上
(1)实验室 装置:(查、装、定、点、收、离、熄 )
制法 收集方法: 向上排空气法
排水法
验满方法:带火星的木条放集气瓶口,观察木条是否复燃,若复燃证明已满
检验方法:带火星的木条伸入集气瓶中,观察木条是否复燃,若复燃是氧气
(2)工业制法:分离液态空气法、膜分离法
4、氧气的用途:供给呼吸、支持燃烧
装置的选择:
发生装置
装置类型 固固加热型 固液不加热型 固液不加热型
收集装置:
收集方法:向上排空气法 排水法
二、燃烧与灭火原理 燃烧条件
灭火原理
缓慢氧化 升温至 自燃 着火点 燃烧 有限空间 爆炸
着火点以上 以上 急速燃烧
四、元素:
1、一种元素与另一种元素的本质区别是质子数不同。
2、一般元素符号的意义有两点:宏观表示一种元素,微观表示一个原子。
由原子构成的物质元素符号还表示一种物质。
元素符号的前面加上数字只具有微观意义,如2H只表示2个氢原子。
4、根据所含元素不同把物质进行分类:(在短线上写出所举例子的化学式)
元素 混合物
(多种物质)
单原子 稀有气体
物质 根据组成 单质 构成 金属
物质的种类 (同种元素) 非金属(C S P Si)
纯净物 根据组成 其他
元素的种类 氧化物
化合物
(多种元素) 其他
第四章复习要点
一 水的存在、性质和组成
水资源 沉淀法(加明矾:使悬浮物沉降)
水的净化方法 过滤法 (活性炭:吸附杂质)
饮用水 水的纯化方法: 蒸馏法
硬水与软水 检验(肥皂水)
软化(工业:蒸馏法,生活:煮沸法)
水的性质 物理性质
化学性质:通电时分解
水的组成 水分解实验 仪器:直流电源
药品:水(内加氢氧化钠或硫酸,目的:增加溶液导电性) 现象:正极 带火星的木条复燃 (氧气)
负极 能燃烧,发出淡蓝色火焰 (氢气)
体积比:1:2(氧气:氢气)质量比:8:1(氧气:氢气)
结论:水 通电 氢气 + 氧气 H2O 通电 H2+O2
水是由氢元素和氧元素组成的,一个水分子是由两个氢原子和一个氧原子构成的,化学变化中,分子可分,原子不可分
二 化学用语
概念理解
规则
化合价 常见化合价(口诀)
求化合价
应用 判断化学式正误
书写化学式
定义 单原子单质
单质 多原子单质
化学式 书写
化合物 (排、标、叉、查)
表示意义:表示一种物质,表示物质的组成,表示一个分子,表示一个分子中所含原子的个数
计算:相对分子质量:
组成化合物各元素的质量比
化合物中某一元素的质量分数
化合物中某一元素的质量
提供依据 运用 (1)表示化学反应
质量守恒定律 化学方程式
遵循 依据 (2)有关计算
(1)反应物、生成物、反应条件 (2)各物质的质量关系
组成
同课章节目录
