人教版选修5高中化学第三章第一节-醇酚-课件(27张PPT)
文档属性
| 名称 | 人教版选修5高中化学第三章第一节-醇酚-课件(27张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 687.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-11-30 00:00:00 | ||
图片预览





文档简介
(共28张PPT)
第一节
醇
酚
第三章
烃的含氧衍生物
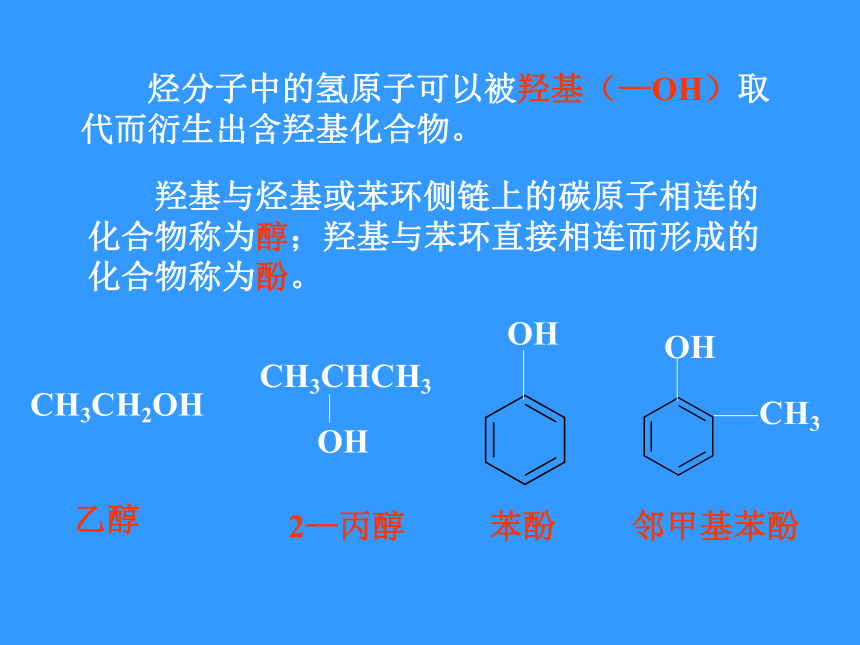
烃分子中的氢原子可以被羟基(—OH)取代而衍生出含羟基化合物。
羟基与烃基或苯环侧链上的碳原子相连的化合物称为醇;羟基与苯环直接相连而形成的化合物称为酚。
CH3CH2OH
CH3CHCH3
OH
乙醇
2—丙醇
OH
苯酚
OH
CH3
邻甲基苯酚
CH3—CH2—CH—CH3
OH
CH3—CH—C—OH
CH3
CH2—CH3
CH3
②
③
CH3—CH—CH2—OH
CH3
①
2—甲基—1—丙醇
2—丁醇
2,3—二甲基—3—戊醇
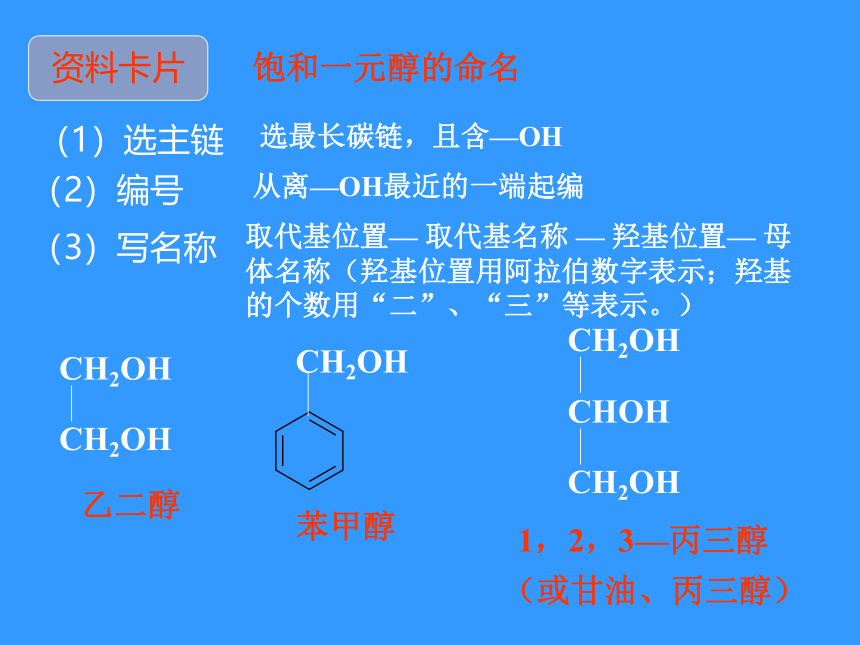
饱和一元醇的命名
(2)编号
(1)选主链
(3)写名称
选最长碳链,且含—OH
从离—OH最近的一端起编
取代基位置—
取代基名称
—
羟基位置—
母体名称(羟基位置用阿拉伯数字表示;羟基的个数用“二”、“三”等表示。)
资料卡片
CH2OH
苯甲醇
CH2OH
CH2OH
乙二醇
CH2OH
CH2OH
CHOH
1,2,3—丙三醇
(或甘油、丙三醇)
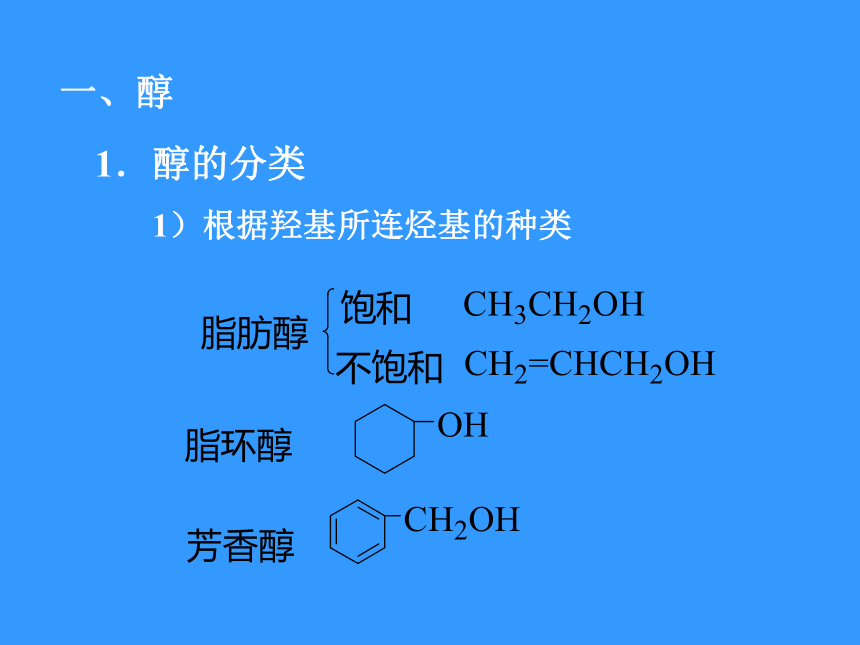
一、醇
1.醇的分类
1)根据羟基所连烃基的种类
2)
根据醇分子结构中羟基的数目,醇可分为一元醇、二元醇、三元醇……
乙二醇和丙三醇都是无色、黏稠、有甜味的液体,都易溶于水和乙醇,是重要的化工原料。
饱和一元醇通式:CnH2n+1OH或CnH2n+2O
乙二醇可用于汽车作防冻剂,丙三醇可用于配制化妆品。
思考与交流
结论:相对分子质量相近的醇和烷烃相比,醇的沸点远远高于烷烃。
原因:由于醇分子中羟基的氧原子与另一醇分子羟基的氢原子间存在着相互吸引作用,这种吸引作用叫氢键。
甲醇、乙醇、丙醇均可与水以任意比例混溶,这是因为甲醇、乙醇、丙醇与水形成了氢键。
学与问
乙二醇的沸点高于乙醇,1,2,3—丙三醇的沸点高于1,2—丙二醇,
1,2—丙二醇的沸点高于1—丙醇,其原因是:由于羟基数目增多,使得分子间形成的氢键增多增强。
思考与交流
处理反应釜中金属钠的最安全、合理的方法是第(3)种方案,向反应釜中慢慢加入乙醇,由于乙醇与金属钠的反应比水与钠的反应缓和,热效应小,因此是比较安全,可行的处理方法。
2.
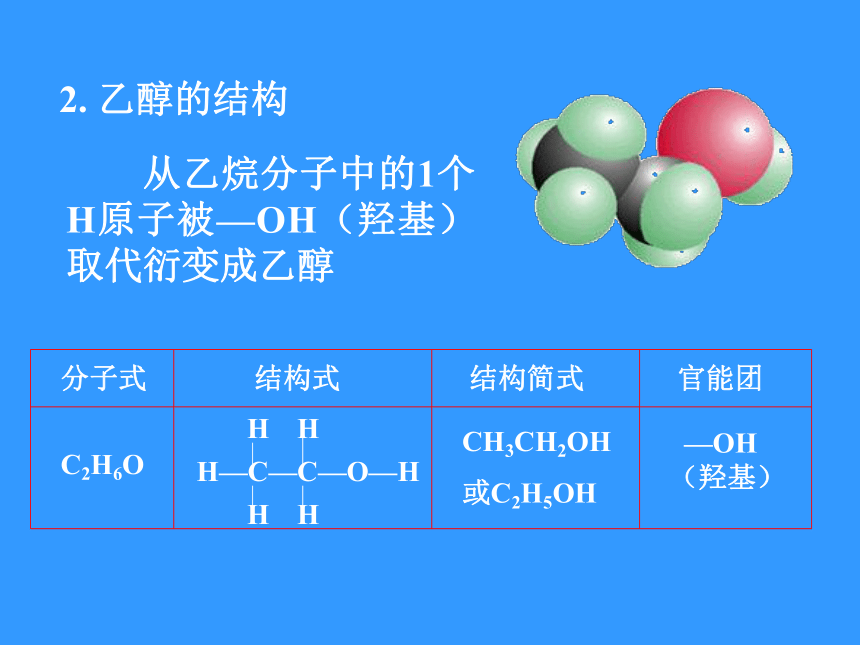
乙醇的结构
从乙烷分子中的1个H原子被—OH(羟基)取代衍变成乙醇
分子式
结构式
结构简式
官能团
C2H6O
H—C—C—O—H
H
H
H
H
CH3CH2OH
或C2H5OH
—OH(羟基)
3.
乙醇的物理性质
1)无色、透明、有特殊香味的液体;
2)沸点78℃,易挥发;
3)密度比水小;
4)能跟水以任意比互溶;
5)能溶解多种无机物和有机物。
4.
乙醇的化学性质
1)与金属钠反应(取代反应)
2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
2)消去反应
脱去—OH和与—OH相邻的碳原子上的1个H
断键位置:
浓硫酸的作用:催化剂和脱水剂
制乙烯实验装置
为何使液体温度迅速升到170℃?
酒精与浓硫酸体积比为何
要为1∶3?
放入几片碎瓷片作用是什么?
用排水集气法收集
浓硫酸的作用是什么?
温度计的位置?
混合液颜色如何变化?为什么?
有何杂质气体?如何除去?
1.
放入几片碎瓷片作用是什么?
防止暴沸
2.
浓硫酸的作用是什么?
催化剂和脱水剂
3.
酒精与浓硫酸体积比为何要为1∶3?
因为浓硫酸是催化剂和脱水剂,为了保证有足够的脱水性,硫酸要用98%的浓硫酸,酒精要用无水酒精,酒精与浓硫酸体积比以1∶3为宜。
4.
温度计的位置?
温度计感温泡要置于反应物的
中央位置因为需要测量的是反应物的温度。
5.
为何使液体温度迅速升到170℃?
因为无水酒精和浓硫酸混合物在170℃的温度下主要生成乙烯和水,而在140℃时乙醇将以另一种方式脱水,即分子间脱水,生成乙醚。
6.
混合液颜色如何变化?为什么?
烧瓶中的液体逐渐变黑。因为浓硫酸有多种特性。在加热的条件下,无水酒精和浓硫酸混合物的反应除可生成乙烯等物质以外,浓硫酸还能将无水酒精氧化生成碳的单质等多种物质,碳的单质使烧瓶内的液体带上了黑色。
7.
有何杂质气体?如何除去?
由于无水酒精和浓硫酸发生的氧化还原反应,反应制得的乙烯中往往混有H2O、CO2、SO2等气体。可将气体通过碱石灰。
8、为何可用排水集气法收集?
因为乙烯难溶于水,密度比空气密度略小。
学与问
CH3CH2OH
CH3CH2Br
反应条件
化学键的断裂
化学键的生成
反应产物
NaOH、乙醇溶液、加热
C—Br、C—H
C—O、C—H
C==C
C==C
CH2==CH2、HBr
CH2==CH2、H2O
浓硫酸、加热到170℃
3)取代反应
C2H5OH
+
HBr
C2H5Br
+
H2O
△
4)氧化反应
2CH3CH2OH+O2
2CH3CHO+2H2O
催化剂
有机物分子中加入氧原子或失去氢原子的反应叫做氧化反应。
CH3CH2OH
CH3CHO
CH3COOH
氧化
氧化
乙醇
乙醛
乙酸
②
①
⑤
③
④
H―C―C―O―H
H
H
H
H
反应
断键位置
分子间脱水
与HX反应
②④
②
①③
①②
与金属反应(酯化反应)
消去反应
催化氧化
①
燃烧
⑤
二、酚
1.
定义:羟基跟苯环直接相连的化合物。
2.
结构:
苯环和羟基会相互影响,将决定苯酚的化学性质
OH
3.
物理性质
无色晶体;具有特殊气味;常温下难溶于水,易溶于乙醇等有机溶剂。650C以上时,能与水混溶
;有毒,可用酒精洗涤。
医院常用的“来苏水”消毒剂便是苯酚钠盐的稀溶液。
放置时间长的苯酚往往是粉红色,因为空气中的氧气就能使苯酚慢慢地氧化成对-苯醌。
小资料
实验
现象
(1)向盛有少量苯酚晶体的试管中加入2mL蒸馏水,振荡试管
(2)向试管中逐滴加入5%的NaOH溶液,并振荡试管
(3)再向试管中加入稀盐酸
形成浑浊的液体
浑浊的液体变为澄清透明的液体
澄清透明的液体又变浑浊
实验3—3
4.
化学性质
1)弱酸性
苯酚能与碱反应,体现出它的弱酸性。因此,苯酚俗称石炭酸。
ONa
+CO2+H2O
OH
+NaHCO3
说明:苯酚酸性很弱,比碳酸还弱。
2)与溴反应
OH
+
3Br2
OH
Br
Br
Br
↓+3HBr
(可用于苯酚定性检验与定量测定)
①浓溴水与苯酚在苯环上发生取代反应。这说明
羟基对苯环产生了影响,使取代更易进行。
②溴取代苯环上羟基的邻、对位。(与甲苯相似)
③该反应很灵敏,可用于苯酚的定性检验
④不能用该反应来分离苯和苯酚
3)苯酚的显色反应
遇FeCl3溶液显紫色。这一反应可用于检验苯酚或Fe3+的存在。
苯酚
苯
反应物
反应条件
取代苯环上氢原子数
反应速率
结论
原因
溴
水与苯酚反应
液溴与纯苯
不用催化剂
FeBr3作催化剂
一次取代苯环上三个氢原子
一次取代苯环
上一个氢原子
瞬时完成
初始缓慢,后加快
苯酚与溴取代反应比苯容易
酚羟基对苯环影响,使苯环上氢原子变得活泼
苯酚与苯取代反应的比较
学与问
苯酚分子中苯环上连有一羟基,由于羟基对苯环的影响,使得苯酚分子中苯环上的氢原子比苯分子中的氢原子更活泼,因此苯酚比苯更易发生取代反应。
乙醇分子中—OH与乙基相连,—OH上H原子比水分子中H原子还难电离,因此乙醇不显酸性。而苯酚分子中的—OH与苯环相连,受苯环影响,—OH上H原子易电离,使苯酚显示一定酸性。
由此可见:不同的烃基与羟基相连,可以影响物质的化学性质。
5.
苯酚的用途
苯酚是一种重要的化工原料,可用来制造酚醛塑料(俗称电木)、合成纤维(如锦纶)、医药、染料、农药等。粗制的苯酚可用于环境消毒。纯净的苯酚可配成洗剂和软膏,有杀菌和止痛效用。药皂中也掺入少量的苯酚。?
酚醛树脂的合成
1.
怎样分离苯酚和苯的混合物
加入NaOH溶液→分液→在苯酚钠溶液中加酸或通入CO2
2.
如何鉴别苯酚
B
利用与浓溴水生成三溴苯酚白色沉淀
A利用与三价铁离子的显色反应
巩固练习
第一节
醇
酚
第三章
烃的含氧衍生物
烃分子中的氢原子可以被羟基(—OH)取代而衍生出含羟基化合物。
羟基与烃基或苯环侧链上的碳原子相连的化合物称为醇;羟基与苯环直接相连而形成的化合物称为酚。
CH3CH2OH
CH3CHCH3
OH
乙醇
2—丙醇
OH
苯酚
OH
CH3
邻甲基苯酚
CH3—CH2—CH—CH3
OH
CH3—CH—C—OH
CH3
CH2—CH3
CH3
②
③
CH3—CH—CH2—OH
CH3
①
2—甲基—1—丙醇
2—丁醇
2,3—二甲基—3—戊醇
饱和一元醇的命名
(2)编号
(1)选主链
(3)写名称
选最长碳链,且含—OH
从离—OH最近的一端起编
取代基位置—
取代基名称
—
羟基位置—
母体名称(羟基位置用阿拉伯数字表示;羟基的个数用“二”、“三”等表示。)
资料卡片
CH2OH
苯甲醇
CH2OH
CH2OH
乙二醇
CH2OH
CH2OH
CHOH
1,2,3—丙三醇
(或甘油、丙三醇)
一、醇
1.醇的分类
1)根据羟基所连烃基的种类
2)
根据醇分子结构中羟基的数目,醇可分为一元醇、二元醇、三元醇……
乙二醇和丙三醇都是无色、黏稠、有甜味的液体,都易溶于水和乙醇,是重要的化工原料。
饱和一元醇通式:CnH2n+1OH或CnH2n+2O
乙二醇可用于汽车作防冻剂,丙三醇可用于配制化妆品。
思考与交流
结论:相对分子质量相近的醇和烷烃相比,醇的沸点远远高于烷烃。
原因:由于醇分子中羟基的氧原子与另一醇分子羟基的氢原子间存在着相互吸引作用,这种吸引作用叫氢键。
甲醇、乙醇、丙醇均可与水以任意比例混溶,这是因为甲醇、乙醇、丙醇与水形成了氢键。
学与问
乙二醇的沸点高于乙醇,1,2,3—丙三醇的沸点高于1,2—丙二醇,
1,2—丙二醇的沸点高于1—丙醇,其原因是:由于羟基数目增多,使得分子间形成的氢键增多增强。
思考与交流
处理反应釜中金属钠的最安全、合理的方法是第(3)种方案,向反应釜中慢慢加入乙醇,由于乙醇与金属钠的反应比水与钠的反应缓和,热效应小,因此是比较安全,可行的处理方法。
2.
乙醇的结构
从乙烷分子中的1个H原子被—OH(羟基)取代衍变成乙醇
分子式
结构式
结构简式
官能团
C2H6O
H—C—C—O—H
H
H
H
H
CH3CH2OH
或C2H5OH
—OH(羟基)
3.
乙醇的物理性质
1)无色、透明、有特殊香味的液体;
2)沸点78℃,易挥发;
3)密度比水小;
4)能跟水以任意比互溶;
5)能溶解多种无机物和有机物。
4.
乙醇的化学性质
1)与金属钠反应(取代反应)
2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
2)消去反应
脱去—OH和与—OH相邻的碳原子上的1个H
断键位置:
浓硫酸的作用:催化剂和脱水剂
制乙烯实验装置
为何使液体温度迅速升到170℃?
酒精与浓硫酸体积比为何
要为1∶3?
放入几片碎瓷片作用是什么?
用排水集气法收集
浓硫酸的作用是什么?
温度计的位置?
混合液颜色如何变化?为什么?
有何杂质气体?如何除去?
1.
放入几片碎瓷片作用是什么?
防止暴沸
2.
浓硫酸的作用是什么?
催化剂和脱水剂
3.
酒精与浓硫酸体积比为何要为1∶3?
因为浓硫酸是催化剂和脱水剂,为了保证有足够的脱水性,硫酸要用98%的浓硫酸,酒精要用无水酒精,酒精与浓硫酸体积比以1∶3为宜。
4.
温度计的位置?
温度计感温泡要置于反应物的
中央位置因为需要测量的是反应物的温度。
5.
为何使液体温度迅速升到170℃?
因为无水酒精和浓硫酸混合物在170℃的温度下主要生成乙烯和水,而在140℃时乙醇将以另一种方式脱水,即分子间脱水,生成乙醚。
6.
混合液颜色如何变化?为什么?
烧瓶中的液体逐渐变黑。因为浓硫酸有多种特性。在加热的条件下,无水酒精和浓硫酸混合物的反应除可生成乙烯等物质以外,浓硫酸还能将无水酒精氧化生成碳的单质等多种物质,碳的单质使烧瓶内的液体带上了黑色。
7.
有何杂质气体?如何除去?
由于无水酒精和浓硫酸发生的氧化还原反应,反应制得的乙烯中往往混有H2O、CO2、SO2等气体。可将气体通过碱石灰。
8、为何可用排水集气法收集?
因为乙烯难溶于水,密度比空气密度略小。
学与问
CH3CH2OH
CH3CH2Br
反应条件
化学键的断裂
化学键的生成
反应产物
NaOH、乙醇溶液、加热
C—Br、C—H
C—O、C—H
C==C
C==C
CH2==CH2、HBr
CH2==CH2、H2O
浓硫酸、加热到170℃
3)取代反应
C2H5OH
+
HBr
C2H5Br
+
H2O
△
4)氧化反应
2CH3CH2OH+O2
2CH3CHO+2H2O
催化剂
有机物分子中加入氧原子或失去氢原子的反应叫做氧化反应。
CH3CH2OH
CH3CHO
CH3COOH
氧化
氧化
乙醇
乙醛
乙酸
②
①
⑤
③
④
H―C―C―O―H
H
H
H
H
反应
断键位置
分子间脱水
与HX反应
②④
②
①③
①②
与金属反应(酯化反应)
消去反应
催化氧化
①
燃烧
⑤
二、酚
1.
定义:羟基跟苯环直接相连的化合物。
2.
结构:
苯环和羟基会相互影响,将决定苯酚的化学性质
OH
3.
物理性质
无色晶体;具有特殊气味;常温下难溶于水,易溶于乙醇等有机溶剂。650C以上时,能与水混溶
;有毒,可用酒精洗涤。
医院常用的“来苏水”消毒剂便是苯酚钠盐的稀溶液。
放置时间长的苯酚往往是粉红色,因为空气中的氧气就能使苯酚慢慢地氧化成对-苯醌。
小资料
实验
现象
(1)向盛有少量苯酚晶体的试管中加入2mL蒸馏水,振荡试管
(2)向试管中逐滴加入5%的NaOH溶液,并振荡试管
(3)再向试管中加入稀盐酸
形成浑浊的液体
浑浊的液体变为澄清透明的液体
澄清透明的液体又变浑浊
实验3—3
4.
化学性质
1)弱酸性
苯酚能与碱反应,体现出它的弱酸性。因此,苯酚俗称石炭酸。
ONa
+CO2+H2O
OH
+NaHCO3
说明:苯酚酸性很弱,比碳酸还弱。
2)与溴反应
OH
+
3Br2
OH
Br
Br
Br
↓+3HBr
(可用于苯酚定性检验与定量测定)
①浓溴水与苯酚在苯环上发生取代反应。这说明
羟基对苯环产生了影响,使取代更易进行。
②溴取代苯环上羟基的邻、对位。(与甲苯相似)
③该反应很灵敏,可用于苯酚的定性检验
④不能用该反应来分离苯和苯酚
3)苯酚的显色反应
遇FeCl3溶液显紫色。这一反应可用于检验苯酚或Fe3+的存在。
苯酚
苯
反应物
反应条件
取代苯环上氢原子数
反应速率
结论
原因
溴
水与苯酚反应
液溴与纯苯
不用催化剂
FeBr3作催化剂
一次取代苯环上三个氢原子
一次取代苯环
上一个氢原子
瞬时完成
初始缓慢,后加快
苯酚与溴取代反应比苯容易
酚羟基对苯环影响,使苯环上氢原子变得活泼
苯酚与苯取代反应的比较
学与问
苯酚分子中苯环上连有一羟基,由于羟基对苯环的影响,使得苯酚分子中苯环上的氢原子比苯分子中的氢原子更活泼,因此苯酚比苯更易发生取代反应。
乙醇分子中—OH与乙基相连,—OH上H原子比水分子中H原子还难电离,因此乙醇不显酸性。而苯酚分子中的—OH与苯环相连,受苯环影响,—OH上H原子易电离,使苯酚显示一定酸性。
由此可见:不同的烃基与羟基相连,可以影响物质的化学性质。
5.
苯酚的用途
苯酚是一种重要的化工原料,可用来制造酚醛塑料(俗称电木)、合成纤维(如锦纶)、医药、染料、农药等。粗制的苯酚可用于环境消毒。纯净的苯酚可配成洗剂和软膏,有杀菌和止痛效用。药皂中也掺入少量的苯酚。?
酚醛树脂的合成
1.
怎样分离苯酚和苯的混合物
加入NaOH溶液→分液→在苯酚钠溶液中加酸或通入CO2
2.
如何鉴别苯酚
B
利用与浓溴水生成三溴苯酚白色沉淀
A利用与三价铁离子的显色反应
巩固练习
