鲁教版化学九年级上第六单元 燃烧与燃料测试题(含答案)
文档属性
| 名称 | 鲁教版化学九年级上第六单元 燃烧与燃料测试题(含答案) |  | |
| 格式 | docx | ||
| 文件大小 | 190.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-11-30 17:18:53 | ||
图片预览


文档简介
第六单元《燃烧与燃料》测试题
一、单选题
1.对比法是重要的研究方法.下列教科书里展示的探究活动未采用对比法的是(
)
A.认识燃烧需要具备的条件
B.CO2与NaOH溶液的反应
C.空气中氧气体积分数的测定
D.MnO2对H2O2分解速率的影响
2.下列反应属于分解反应的是
A.工业制氧气
B.用大理石和盐酸混合制二氧化碳
C.加热高锰酸钾制氧气
D.石蜡在空气中燃烧
3.下列关于不同物质比较的归纳,你认为不合理的是( )
A.冰和干冰:组成元素不同,状态相同,物质分类相同
B.五氧化二磷和氯化钠:组成元素不同,颜色相同,物质构成粒子相同
C.金刚石和石墨:组成元素相同,原子排列不同,物理性质不同
D.一氧化碳和二氧化碳:组成元素相同,分子结构不同,化学性质不同
4.下列关于化学变化的说法中,正确的是(
)
A.化学的发展导致了生态环境的恶化
B.物质有光和热现象产生就一定起化学变化
C.物质发生化学变化后就一定有新物质生成
D.化学变化中一定伴随放热、发光、放出气体、生成沉淀等现象
5.氨气(NH3)是一种无色、极易溶于水的气体。在实验室加热氯化铵和熟石灰两种固体的混合物可制取氨气,则该实验可选用的发生装置和收集方法正确的是( )
A.与加热分解KClO3制氧气的发生装置相同,用向下排空气法收集
B.与加热分解KClO3制氧气的发生装置相同,用向上排空气法收集
C.与实验室制取二氧化碳的发生装置相同,用排水法收集
D.与实验室制取二氧化碳的发生装置相同,用向下排空气法收集
6.对下列实验现象的描述正确的是
(
)
A.木炭在氧气中燃烧,发出白光,放出热量
B.硫在氧气中燃烧发出蓝紫色火焰,生成二氧化硫气体
C.红磷在空气中燃烧,产生大量的白色烟雾
D.铁丝在空气中剧烈燃烧,火星四射,放热,生成黑色固体
7.下列物质性质或现象描述错误的是(??
)
A.合金的硬度比组成它们的纯金属的硬度小
B.消防队员用水降低可燃物的温度来灭火
C.极易与血红蛋白结合的有毒气体是一氧化碳
D.硫在氧气中燃烧产生明亮的蓝紫色火焰
8.下列物质的用途仅与其物理性质有关的是
A.用金刚石切割玻璃
B.用氢气作高能燃料
C.用氮气作灯泡填充气
D.用二氧化碳灭火
9.属于分解反应的是( )
A.H2CO3→H2O+CO2↑
B.CH4+2O2CO2+2H2O
C.CaO+H2O→Ca(OH)2
D.2Mg+CO22MgO+C
10.往烧杯的水中加入一定量氢氧化钠固体能引起试管中的白磷燃烧。下列说法正确的是
A.未加氢氧化钠固体,白磷与氧气不会发生缓慢氧化
B.氢氧化钠固体溶于水会吸收热量
C.白磷燃烧产生棕黄色的雾
D.溶液温度升高,达到了白磷的着火点
11.下列说法中,错误的是
A.溶液一定是均一、稳定的混合物
B.氦气充入食品袋中可防腐
C.用过滤的方法不能使硬水变软
D.燃烧离不开氧气,它是一种重要的燃料
12.下列关于CO2的说法中,不正确的是( )
A.将CO2通入CaCl2溶液中,有白色沉淀生成
B.空气中的CO2使正常雨水的pH<7
C.久置的氢氧化钠溶液会吸收空气中的CO2变质
D.将CO2通入紫色石蕊溶液中,可看到溶液变红
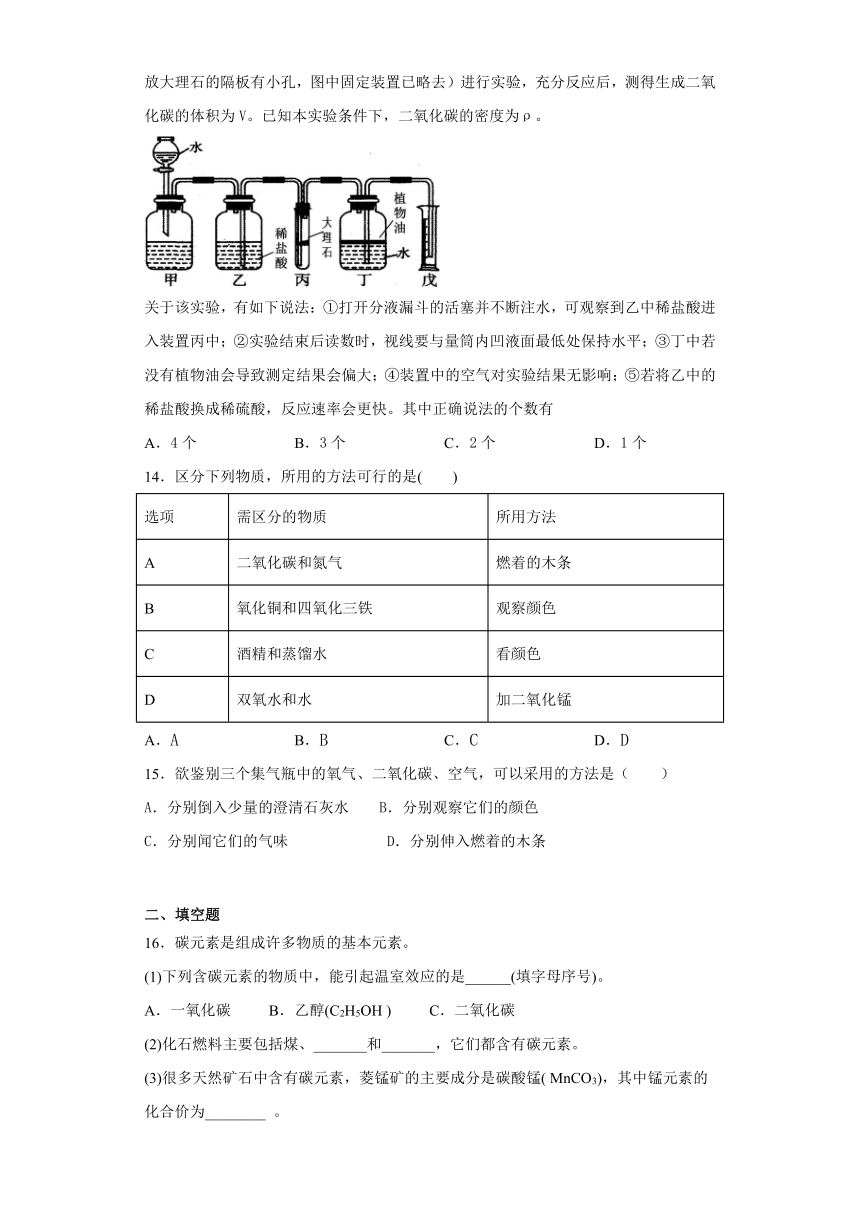
13.某化学兴趣小组的同学欲在常温、常压下,用一定质量的大理石与足量的稀盐酸反应,测定大理石中碳酸钙的质量分数(杂质不参与反应)。利用如下图所示的装置(盛放大理石的隔板有小孔,图中固定装置已略去)进行实验,充分反应后,测得生成二氧化碳的体积为V。已知本实验条件下,二氧化碳的密度为ρ。
关于该实验,有如下说法:①打开分液漏斗的活塞并不断注水,可观察到乙中稀盐酸进入装置丙中;②实验结束后读数时,视线要与量筒内凹液面最低处保持水平;③丁中若没有植物油会导致测定结果会偏大;④装置中的空气对实验结果无影响;⑤若将乙中的稀盐酸换成稀硫酸,反应速率会更快。其中正确说法的个数有
A.4个
B.3个
C.2个
D.1个
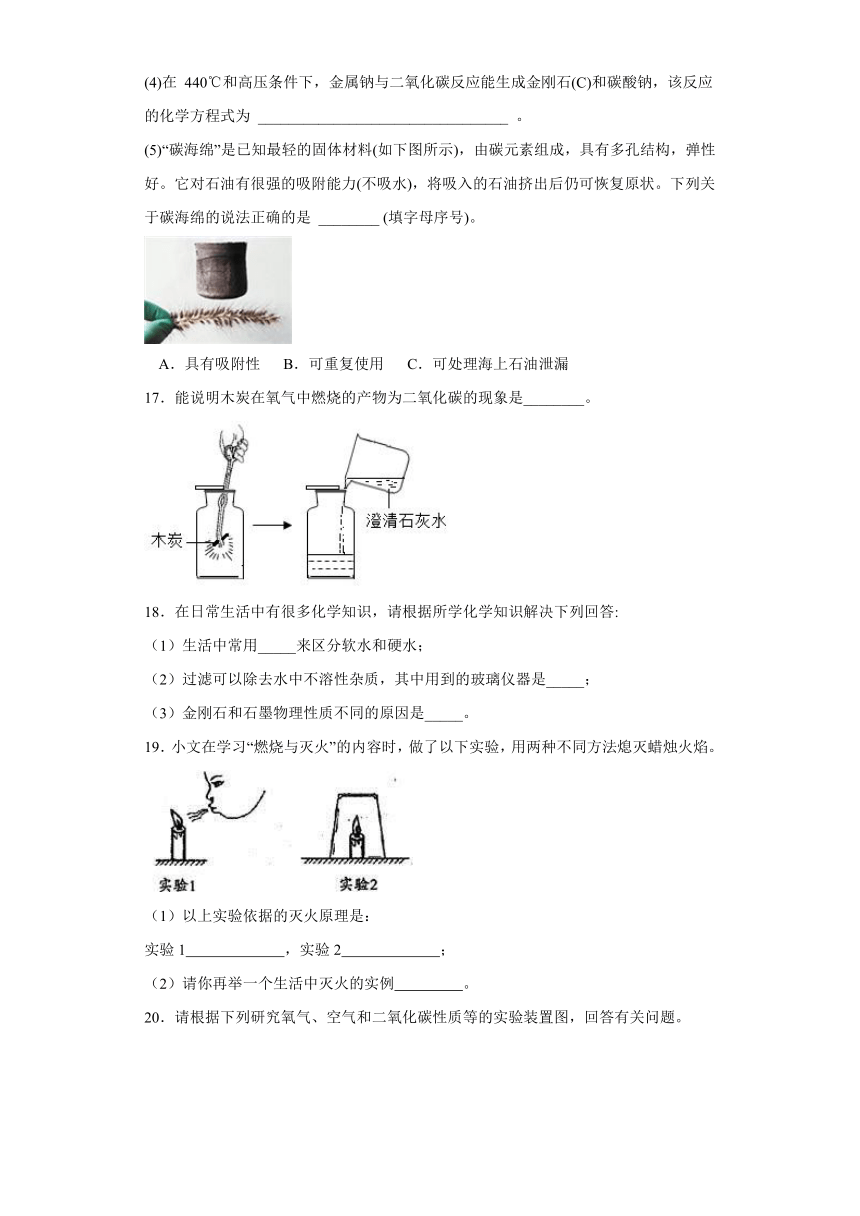
14.区分下列物质,所用的方法可行的是(
)
选项
需区分的物质
所用方法
A
二氧化碳和氮气
燃着的木条
B
氧化铜和四氧化三铁
观察颜色
C
酒精和蒸馏水
看颜色
D
双氧水和水
加二氧化锰
A.A
B.B
C.C
D.D
15.欲鉴别三个集气瓶中的氧气、二氧化碳、空气,可以采用的方法是( )
A.分别倒入少量的澄清石灰水
B.分别观察它们的颜色
C.分别闻它们的气味
D.分别伸入燃着的木条
二、填空题
16.碳元素是组成许多物质的基本元素。
(1)下列含碳元素的物质中,能引起温室效应的是______(填字母序号)。
A.一氧化碳
B.乙醇(C2H5OH
)
C.二氧化碳
(2)化石燃料主要包括煤、_______和_______,它们都含有碳元素。
(3)很多天然矿石中含有碳元素,菱锰矿的主要成分是碳酸锰(
MnCO3),其中锰元素的化合价为________
。
(4)在
440℃和高压条件下,金属钠与二氧化碳反应能生成金刚石(C)和碳酸钠,该反应的化学方程式为
_________________________________
。
(5)“碳海绵”是已知最轻的固体材料(如下图所示),由碳元素组成,具有多孔结构,弹性好。它对石油有很强的吸附能力(不吸水),将吸入的石油挤出后仍可恢复原状。下列关于碳海绵的说法正确的是
________
(填字母序号)。
A.具有吸附性
B.可重复使用
C.可处理海上石油泄漏
17.能说明木炭在氧气中燃烧的产物为二氧化碳的现象是________。
18.在日常生活中有很多化学知识,请根据所学化学知识解决下列回答:
(1)生活中常用_____来区分软水和硬水;
(2)过滤可以除去水中不溶性杂质,其中用到的玻璃仪器是_____;
(3)金刚石和石墨物理性质不同的原因是_____。
19.小文在学习“燃烧与灭火”的内容时,做了以下实验,用两种不同方法熄灭蜡烛火焰。
(1)以上实验依据的灭火原理是:
实验1
,实验2
;
(2)请你再举一个生活中灭火的实例
。
20.请根据下列研究氧气、空气和二氧化碳性质等的实验装置图,回答有关问题。
(1)从物质分类的角度看,空气属于_____(填“混合物”或“纯净物”)
(2)从构成物质的微粒看,铁丝在氧气中燃烧是铁原子与氧分子发生化学反应,请用化学符号表示:3个铁原子:_____,2个氧分子:_____。
(3)从宏观现象的角度看,实验C的现象为___,由可知二氧化碳的性质有__,___,____。
(4)从变化过程的角度看,某同学对B装置改进后如图D所示,实验时,从分液漏斗向瓶内迅速注入80℃的水至闷没白磷,然后倾斜装置至白磷露出水面时,白磷立即燃烧,这说明物质燃烧需要的条件是____;若集气瓶的容积为320mL,注射器内活塞头部在实验前所处的刻度为80mL,加入的热水为120mL,在实验过程中需要不断地推拉注射器的活塞,其目的是____;当反应完全并冷却至室温后,注射器内活塞头部所处的刻度约为____mL。
三、推断题
21.现有A一F六种常见物质,其中B是食品包装中常用的干燥剂,A、B、C三种白色固体都含有同种金属元素,E是固体单质,D、E、F都含有同种非金属元素。它们的转化关系如下图所示。请回答:
(1)写出下列物质的化学式:B._________、D.__________;
(2)写出下列反应的化学方程式:
C→B:_________________;
F→D:_____________________。
22.A、B、C、D是初中化学常见的物质,这四种物质中均含有同一种元素。其中A是无色气体单质。B、C均为组成元素相同的气体,D是大理石的主要成分。它们之间的转化关系如图所示(图中反应条件及部分反应物、生成物已省略):
(1)写出物质A的化学式_____。
(2)写出C转化为D化学方程式_____。
(3)写出B转化为C化学方程式_____(合理即可)。
四、实验题
23.实验室里现有氯酸钾、二氧化锰、稀硫酸、石灰石和稀盐酸,以及下列伩器:
(1)实验室利用上述仪器和药品可以制取二氧化碳,你选择的仪器是______(填序号),反应的化学方程式为______________________.
(2)实验室若用上述给定的药品来制取氧气,需要补充的一种仪器是_______,反应的化学方程式为_______________________.
(3)实验室若用上述药品中的稀硫酸来制取氢气,需要补充一种合适的药品是________.
24.小强在回家的途中经过一鱼塘边时,发现养鱼师傅向鱼塘中撒一种微黄色的固体,鱼塘中顿时产生大量气泡,经咨询得知,这种固体的主要成分是过氧化钙(CaO2),请你与小强共同探究。
(1)为研究鱼塘中大量气泡是何种气体所致,小强使用如图所示的装置进行实验。实验过程如下:打开分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃,说明生成的气体是_______。由此可知养鱼师傅向鱼塘中撒过氧化钙的目的是__________________,试解释仪器a中导气管口产生气泡可能的原理_______________。
(2)根据质量守恒定律,小强认为过氧化钙与过量水反应还应产生某种含有钙元素的产物。开始小强假设该产物为CaO,但通过思考他很快否定了原先的假设,并重新假设生成的含钙产物为Ca(OH)2。请解释小强否定原假设建立新假设的理由:______________________________。
(3)请写出过氧化钙与水反应的化学方程式:___________________________________。
五、计算题
25.某化学兴趣小组取12.5克的大理石样品(杂质不与盐酸反应),向其中加入稀盐酸,产生CO2的质量与稀盐酸的质量关系如图所示。请计算:
(1)生成CO2的质量是___g。
(2)该大理石样品中碳酸钙的质量分数。
(3)该盐酸的溶质质量分数
(计算结果保留0.1%)。
26.学校研究性学习小组为了测定当地矿山石灰石中碳酸钙的含量,取来了一些矿石样品,并取稀盐酸200
g,平均分成4份,进行实验。
实验
1
2
3
4
加入样品的质量/g
5
10
15
20
生成CO2的质量/g
1.76
3.52
4.4
M
(1)哪几次反应矿石有剩余?___________。
(2)上表中M的数值是_________。
(3)试计算这种石灰石中碳酸钙的质量分数。
参考答案
1.C
2.C
3.B
4.C
5.A
6.A
7.A
8.A
9.A
10.D
11.D
12.A
13.B
14.D
15.D
16.C
石油
天然气
+2
4Na+3CO2C+2Na2CO3
A、B、C
17.右边集气瓶中的澄清石灰水变浑浊
18.肥皂水
烧杯、漏斗、玻璃棒
碳原子的排列方式不同
19.(1)使可燃物得温度降低到着火点以下
使可燃物与空气(或氧气)隔绝
(2)油锅着火用锅盖盖灭(其它合理答案均可)
20.混合物
3Fe
2O2
低处的蜡烛先熄灭,高处的蜡烛后熄灭
密度比空气大
不燃烧
不支持燃烧
燃烧需要氧气
使氧气充分参与反应
24
21.CaO
CO2
22.O2
(或者一氧化碳还原氧化铜、氧化铁等,合理即可)
23.①②⑦⑧
CaCO3+2HCl=CaCl2+H2O+CO2↑
试管
2KClO3
2KCl+3O2↑
锌
24.氧气
向鱼塘中增加氧气
过氧化钙与水反应放出热量,使集气瓶内气体受热膨胀,从导管口逸出
反应前有氢元素,反应后也必须有氢元素
2CaO2+2H2O=2Ca(OH)2+O2↑
25.(1)4.4g
(2)80%
(3)7.3%
26.(1)第3次;(2)4.4;(3)80%
一、单选题
1.对比法是重要的研究方法.下列教科书里展示的探究活动未采用对比法的是(
)
A.认识燃烧需要具备的条件
B.CO2与NaOH溶液的反应
C.空气中氧气体积分数的测定
D.MnO2对H2O2分解速率的影响
2.下列反应属于分解反应的是
A.工业制氧气
B.用大理石和盐酸混合制二氧化碳
C.加热高锰酸钾制氧气
D.石蜡在空气中燃烧
3.下列关于不同物质比较的归纳,你认为不合理的是( )
A.冰和干冰:组成元素不同,状态相同,物质分类相同
B.五氧化二磷和氯化钠:组成元素不同,颜色相同,物质构成粒子相同
C.金刚石和石墨:组成元素相同,原子排列不同,物理性质不同
D.一氧化碳和二氧化碳:组成元素相同,分子结构不同,化学性质不同
4.下列关于化学变化的说法中,正确的是(
)
A.化学的发展导致了生态环境的恶化
B.物质有光和热现象产生就一定起化学变化
C.物质发生化学变化后就一定有新物质生成
D.化学变化中一定伴随放热、发光、放出气体、生成沉淀等现象
5.氨气(NH3)是一种无色、极易溶于水的气体。在实验室加热氯化铵和熟石灰两种固体的混合物可制取氨气,则该实验可选用的发生装置和收集方法正确的是( )
A.与加热分解KClO3制氧气的发生装置相同,用向下排空气法收集
B.与加热分解KClO3制氧气的发生装置相同,用向上排空气法收集
C.与实验室制取二氧化碳的发生装置相同,用排水法收集
D.与实验室制取二氧化碳的发生装置相同,用向下排空气法收集
6.对下列实验现象的描述正确的是
(
)
A.木炭在氧气中燃烧,发出白光,放出热量
B.硫在氧气中燃烧发出蓝紫色火焰,生成二氧化硫气体
C.红磷在空气中燃烧,产生大量的白色烟雾
D.铁丝在空气中剧烈燃烧,火星四射,放热,生成黑色固体
7.下列物质性质或现象描述错误的是(??
)
A.合金的硬度比组成它们的纯金属的硬度小
B.消防队员用水降低可燃物的温度来灭火
C.极易与血红蛋白结合的有毒气体是一氧化碳
D.硫在氧气中燃烧产生明亮的蓝紫色火焰
8.下列物质的用途仅与其物理性质有关的是
A.用金刚石切割玻璃
B.用氢气作高能燃料
C.用氮气作灯泡填充气
D.用二氧化碳灭火
9.属于分解反应的是( )
A.H2CO3→H2O+CO2↑
B.CH4+2O2CO2+2H2O
C.CaO+H2O→Ca(OH)2
D.2Mg+CO22MgO+C
10.往烧杯的水中加入一定量氢氧化钠固体能引起试管中的白磷燃烧。下列说法正确的是
A.未加氢氧化钠固体,白磷与氧气不会发生缓慢氧化
B.氢氧化钠固体溶于水会吸收热量
C.白磷燃烧产生棕黄色的雾
D.溶液温度升高,达到了白磷的着火点
11.下列说法中,错误的是
A.溶液一定是均一、稳定的混合物
B.氦气充入食品袋中可防腐
C.用过滤的方法不能使硬水变软
D.燃烧离不开氧气,它是一种重要的燃料
12.下列关于CO2的说法中,不正确的是( )
A.将CO2通入CaCl2溶液中,有白色沉淀生成
B.空气中的CO2使正常雨水的pH<7
C.久置的氢氧化钠溶液会吸收空气中的CO2变质
D.将CO2通入紫色石蕊溶液中,可看到溶液变红
13.某化学兴趣小组的同学欲在常温、常压下,用一定质量的大理石与足量的稀盐酸反应,测定大理石中碳酸钙的质量分数(杂质不参与反应)。利用如下图所示的装置(盛放大理石的隔板有小孔,图中固定装置已略去)进行实验,充分反应后,测得生成二氧化碳的体积为V。已知本实验条件下,二氧化碳的密度为ρ。
关于该实验,有如下说法:①打开分液漏斗的活塞并不断注水,可观察到乙中稀盐酸进入装置丙中;②实验结束后读数时,视线要与量筒内凹液面最低处保持水平;③丁中若没有植物油会导致测定结果会偏大;④装置中的空气对实验结果无影响;⑤若将乙中的稀盐酸换成稀硫酸,反应速率会更快。其中正确说法的个数有
A.4个
B.3个
C.2个
D.1个
14.区分下列物质,所用的方法可行的是(
)
选项
需区分的物质
所用方法
A
二氧化碳和氮气
燃着的木条
B
氧化铜和四氧化三铁
观察颜色
C
酒精和蒸馏水
看颜色
D
双氧水和水
加二氧化锰
A.A
B.B
C.C
D.D
15.欲鉴别三个集气瓶中的氧气、二氧化碳、空气,可以采用的方法是( )
A.分别倒入少量的澄清石灰水
B.分别观察它们的颜色
C.分别闻它们的气味
D.分别伸入燃着的木条
二、填空题
16.碳元素是组成许多物质的基本元素。
(1)下列含碳元素的物质中,能引起温室效应的是______(填字母序号)。
A.一氧化碳
B.乙醇(C2H5OH
)
C.二氧化碳
(2)化石燃料主要包括煤、_______和_______,它们都含有碳元素。
(3)很多天然矿石中含有碳元素,菱锰矿的主要成分是碳酸锰(
MnCO3),其中锰元素的化合价为________
。
(4)在
440℃和高压条件下,金属钠与二氧化碳反应能生成金刚石(C)和碳酸钠,该反应的化学方程式为
_________________________________
。
(5)“碳海绵”是已知最轻的固体材料(如下图所示),由碳元素组成,具有多孔结构,弹性好。它对石油有很强的吸附能力(不吸水),将吸入的石油挤出后仍可恢复原状。下列关于碳海绵的说法正确的是
________
(填字母序号)。
A.具有吸附性
B.可重复使用
C.可处理海上石油泄漏
17.能说明木炭在氧气中燃烧的产物为二氧化碳的现象是________。
18.在日常生活中有很多化学知识,请根据所学化学知识解决下列回答:
(1)生活中常用_____来区分软水和硬水;
(2)过滤可以除去水中不溶性杂质,其中用到的玻璃仪器是_____;
(3)金刚石和石墨物理性质不同的原因是_____。
19.小文在学习“燃烧与灭火”的内容时,做了以下实验,用两种不同方法熄灭蜡烛火焰。
(1)以上实验依据的灭火原理是:
实验1
,实验2
;
(2)请你再举一个生活中灭火的实例
。
20.请根据下列研究氧气、空气和二氧化碳性质等的实验装置图,回答有关问题。
(1)从物质分类的角度看,空气属于_____(填“混合物”或“纯净物”)
(2)从构成物质的微粒看,铁丝在氧气中燃烧是铁原子与氧分子发生化学反应,请用化学符号表示:3个铁原子:_____,2个氧分子:_____。
(3)从宏观现象的角度看,实验C的现象为___,由可知二氧化碳的性质有__,___,____。
(4)从变化过程的角度看,某同学对B装置改进后如图D所示,实验时,从分液漏斗向瓶内迅速注入80℃的水至闷没白磷,然后倾斜装置至白磷露出水面时,白磷立即燃烧,这说明物质燃烧需要的条件是____;若集气瓶的容积为320mL,注射器内活塞头部在实验前所处的刻度为80mL,加入的热水为120mL,在实验过程中需要不断地推拉注射器的活塞,其目的是____;当反应完全并冷却至室温后,注射器内活塞头部所处的刻度约为____mL。
三、推断题
21.现有A一F六种常见物质,其中B是食品包装中常用的干燥剂,A、B、C三种白色固体都含有同种金属元素,E是固体单质,D、E、F都含有同种非金属元素。它们的转化关系如下图所示。请回答:
(1)写出下列物质的化学式:B._________、D.__________;
(2)写出下列反应的化学方程式:
C→B:_________________;
F→D:_____________________。
22.A、B、C、D是初中化学常见的物质,这四种物质中均含有同一种元素。其中A是无色气体单质。B、C均为组成元素相同的气体,D是大理石的主要成分。它们之间的转化关系如图所示(图中反应条件及部分反应物、生成物已省略):
(1)写出物质A的化学式_____。
(2)写出C转化为D化学方程式_____。
(3)写出B转化为C化学方程式_____(合理即可)。
四、实验题
23.实验室里现有氯酸钾、二氧化锰、稀硫酸、石灰石和稀盐酸,以及下列伩器:
(1)实验室利用上述仪器和药品可以制取二氧化碳,你选择的仪器是______(填序号),反应的化学方程式为______________________.
(2)实验室若用上述给定的药品来制取氧气,需要补充的一种仪器是_______,反应的化学方程式为_______________________.
(3)实验室若用上述药品中的稀硫酸来制取氢气,需要补充一种合适的药品是________.
24.小强在回家的途中经过一鱼塘边时,发现养鱼师傅向鱼塘中撒一种微黄色的固体,鱼塘中顿时产生大量气泡,经咨询得知,这种固体的主要成分是过氧化钙(CaO2),请你与小强共同探究。
(1)为研究鱼塘中大量气泡是何种气体所致,小强使用如图所示的装置进行实验。实验过程如下:打开分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃,说明生成的气体是_______。由此可知养鱼师傅向鱼塘中撒过氧化钙的目的是__________________,试解释仪器a中导气管口产生气泡可能的原理_______________。
(2)根据质量守恒定律,小强认为过氧化钙与过量水反应还应产生某种含有钙元素的产物。开始小强假设该产物为CaO,但通过思考他很快否定了原先的假设,并重新假设生成的含钙产物为Ca(OH)2。请解释小强否定原假设建立新假设的理由:______________________________。
(3)请写出过氧化钙与水反应的化学方程式:___________________________________。
五、计算题
25.某化学兴趣小组取12.5克的大理石样品(杂质不与盐酸反应),向其中加入稀盐酸,产生CO2的质量与稀盐酸的质量关系如图所示。请计算:
(1)生成CO2的质量是___g。
(2)该大理石样品中碳酸钙的质量分数。
(3)该盐酸的溶质质量分数
(计算结果保留0.1%)。
26.学校研究性学习小组为了测定当地矿山石灰石中碳酸钙的含量,取来了一些矿石样品,并取稀盐酸200
g,平均分成4份,进行实验。
实验
1
2
3
4
加入样品的质量/g
5
10
15
20
生成CO2的质量/g
1.76
3.52
4.4
M
(1)哪几次反应矿石有剩余?___________。
(2)上表中M的数值是_________。
(3)试计算这种石灰石中碳酸钙的质量分数。
参考答案
1.C
2.C
3.B
4.C
5.A
6.A
7.A
8.A
9.A
10.D
11.D
12.A
13.B
14.D
15.D
16.C
石油
天然气
+2
4Na+3CO2C+2Na2CO3
A、B、C
17.右边集气瓶中的澄清石灰水变浑浊
18.肥皂水
烧杯、漏斗、玻璃棒
碳原子的排列方式不同
19.(1)使可燃物得温度降低到着火点以下
使可燃物与空气(或氧气)隔绝
(2)油锅着火用锅盖盖灭(其它合理答案均可)
20.混合物
3Fe
2O2
低处的蜡烛先熄灭,高处的蜡烛后熄灭
密度比空气大
不燃烧
不支持燃烧
燃烧需要氧气
使氧气充分参与反应
24
21.CaO
CO2
22.O2
(或者一氧化碳还原氧化铜、氧化铁等,合理即可)
23.①②⑦⑧
CaCO3+2HCl=CaCl2+H2O+CO2↑
试管
2KClO3
2KCl+3O2↑
锌
24.氧气
向鱼塘中增加氧气
过氧化钙与水反应放出热量,使集气瓶内气体受热膨胀,从导管口逸出
反应前有氢元素,反应后也必须有氢元素
2CaO2+2H2O=2Ca(OH)2+O2↑
25.(1)4.4g
(2)80%
(3)7.3%
26.(1)第3次;(2)4.4;(3)80%
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
