人教版选修四高中化学4.4金属的电化学腐蚀与防护(49张PPT)
文档属性
| 名称 | 人教版选修四高中化学4.4金属的电化学腐蚀与防护(49张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-11-30 00:00:00 | ||
图片预览










文档简介
(共49张PPT)
第四章
电化学基础
第4节
金属的电化学腐蚀与防护
请比较下列Fe腐蚀的快慢?
铁与酸反应,铁被腐蚀。
铁与碳形成原电池铁作负极被腐蚀。
腐蚀速率较慢。
腐蚀速率较快。
金属的腐蚀现象非常普遍:
1、钢铁生锈:
铁锈的主要成分:
金属腐蚀的不利后果有哪些?
Fe2O3·XH2O
Cu2(OH)2CO3
2、铜器表面生成铜绿:
铜绿的主要成分:
金属的腐蚀现象非常普遍:
金属腐蚀的不利后果有哪些?
Fe2O3·XH2O
Cu2(OH)2CO3
2、铜器表面生成铜绿:
铜绿的主要成分:
1、钢铁生锈:
铁锈的主要成分:
2007年8月1日,美国明尼苏达州一座跨越密西西比河的大桥发生坍塌。事故造成6人死亡。
金属制品的腐蚀
金属腐蚀给生产生活带来很多不便,造成了巨大的经济损失。
全世界每年因为金属腐蚀造成的直接经济损失约达7000亿美元,是地震、水灾、台风等自然灾害造成损失总和的6倍。
我国因金属腐蚀造成的损失占国民生产总值(GNP)的4%,钢铁因腐蚀而报废的数量约占钢铁当年产量的25%-30%。
金属腐蚀还可能造成环境污染。
资
料
在
线
一、金属腐蚀的本质:
是金属或合金与周围接触到的气体或液体发生氧化还原反应而引起损耗的过程。
M
-
ne-
=
Mn+
二、金属腐蚀的类型:
(1)化学腐蚀
金属跟接触到的物质直接发生化学反应而引起的腐蚀叫做化学腐蚀。
(2)电化学腐蚀
不纯的金属跟电解质溶液接触时,会发生原电池反应,比较活泼的金属失电子而被氧化的腐蚀叫做电化学腐蚀。
化学腐蚀和电化学腐蚀的比较
相互关系
反应
现象
条件
电化学腐蚀
化学腐蚀
化学腐蚀和电化学腐蚀同时发生,
但电化学腐蚀更普遍
较活泼的金属被氧化
金属被氧化
有微弱的电流产生
不产生电流
不纯金属或合金跟电解质溶液接触
金属跟接触的物质反应
钢铁在干燥的空气里长时间不易被腐蚀,但在潮湿的空气里却很快被腐蚀,这是什么原因呢?
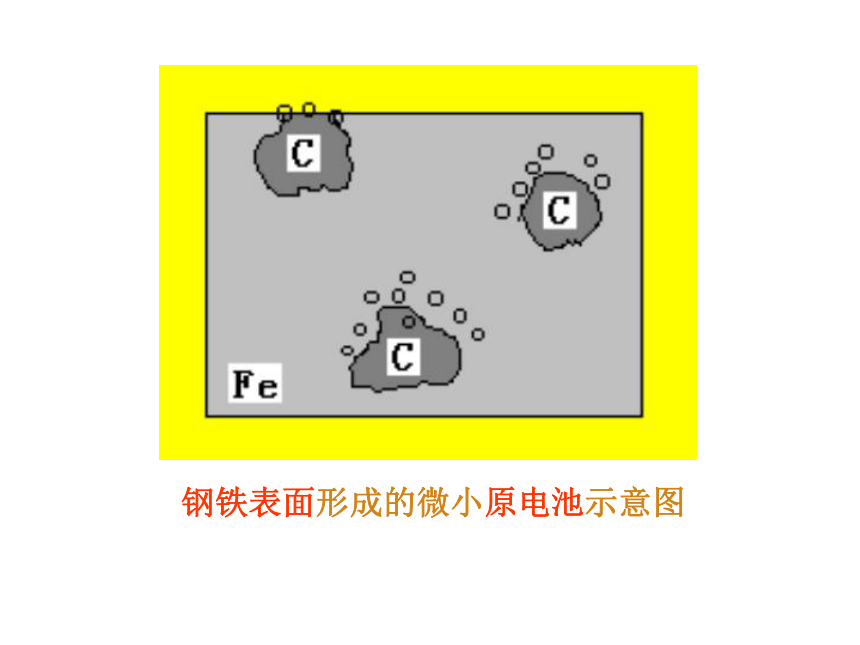
在潮湿的空气里,钢铁表面吸附了一层薄薄的水膜。水中溶有O2、CO2、SO2等气体,这样在钢铁表面形成了一层电解质溶液的薄膜,它跟钢铁里的铁和少量的碳构成无数微小的原电池。
钢铁表面形成的微小原电池示意图
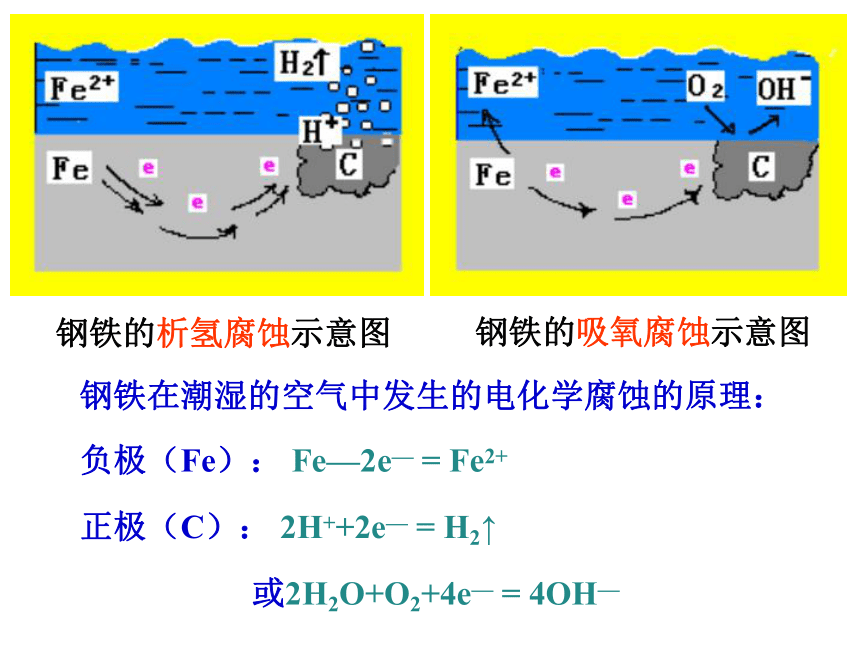
钢铁的析氢腐蚀示意图
钢铁的吸氧腐蚀示意图
钢铁在潮湿的空气中发生的电化学腐蚀的原理:
负极(Fe):
Fe—2e—
=
Fe2+
正极(C):
2H++2e—
=
H2↑
或2H2O+O2+4e—
=
4OH—
4.钢铁的析氢腐蚀和吸氧腐蚀比较
Fe2O3
·
nH2O
(铁锈)
通常两种腐蚀同时存在,但以后者更普遍。
析氢腐蚀
吸氧腐蚀
条件
水膜呈酸性。
水膜呈中性或酸性很弱。
电极反应
负极Fe(-
)
Fe-2e=Fe2+
2Fe-4e=2Fe2+
正极C(+)
2H
+
+
2e-
=
H2↑
O2+2H2O+4e=4OH-
总反应:
Fe
+
2H
+
==
=Fe2+
+
H2↑
2Fe+2H2O+O2=
2
Fe(OH)2
4Fe(OH)2+2H2O+O2=4Fe(OH)3
联系
金属腐蚀的快慢:
电解原理引起的腐蚀>原电池原理引起的腐蚀>化学腐蚀>有防护措施的腐蚀
同一金属在不同物质中腐蚀的快慢:
强电解质>弱电解质>非电解质
5.金属腐蚀快慢的判断:
(1)与构成微电池两极的材料有关。两极材料的活动性差别越大,氧化还原反应的速率越
,活泼金属被腐蚀的速度越
。
(2)
电解原理引起的腐蚀
原电池原理引起的腐蚀
化学腐蚀
有防腐措施的腐蚀。
(3)同一种金属的腐蚀:在强电解质中
弱电解质中
非电解质中
(4)一般说来:原电池原理引起的腐蚀
化学腐蚀
有防腐措施的腐蚀。
注意:在钢铁的腐蚀过程中,其电化学腐蚀更严重,在电化学腐蚀中,吸氧腐蚀更普遍。
>
>
>
>
>
快
快
>
>
[反馈练习]
1.下列情况下,海水中铁腐蚀最快的是(
)
B
2.如图所示,甲、乙两试管中各放一枚铁钉,甲试管中为NaCl溶液,乙试管为NH4Cl溶液(溶液呈弱酸性).数天后观察到的现象是
,
甲中正极反应为_______________.
乙中正极反应为
.
试管中残留气体平均相对分子质量的变化为甲
,乙
.
O2+2H2O+4e-=4OH-
2H++2e—
=
H2↑
减少
减少
Fe被腐蚀,U型管中甲端的液面高于乙端的液面
思考与交流
请根据生活常识以及下图总结金属防护常用的方法,并解释这些方法为什么可以达到防止金属腐蚀的目的。
健身器材刷油漆以防锈
衣架和电线的外面包上一层塑料层
某些工具的“机械转动部位”选用油脂来防锈,为什么不能用油漆
自行车的钢圈和车铃是在钢上镀上一层既耐腐蚀又耐磨的Cr
三、金属的防护
(1)
改善金属的内部组织结构(内因)
——制成合金(不锈钢)
(2)在金属表面覆盖保护层——电镀、油漆、钝化等
(3)电化学保护法——牺牲阳极的阴极保护法、外加直流电源的阴极保护法
牺牲阳极的阴极保护法
形成原电池反应时,让被保护金属做正极,不反应,起到保护作用;而活泼金属反应受到腐蚀。
你还知道哪些防止金属腐蚀的方法?请举例说明。
用牺牲镁块的方法来防止地下钢铁管道的腐蚀,镁块必须定期更换
制成不锈钢,在金属表面镀一层比要保护的金属耐腐蚀的金属。
用牺牲锌块的方法来保护船身,锌块必须定期更换
锌块
外加电流的阴极保护法
将被保护金属与另一附加电极作为电解池的两个极,使被保护的金属作为阴极,在外加直流电的作用下使阴极得到保护。此法主要用于防止土壤、海水及水中金属设备的腐蚀。
烤蓝
涂机油
烤漆
涂凡士林
镀锌
镀铬
[交流研讨]
你知道自行车的金属部件采用了什么样的防护措施吗?
方法
防腐效果
价格
镀塑
差
便宜
涂油漆
一般
便宜
镀锡
好
中等
镀铬
好
昂贵
镀锌
很好
中等
使用不锈钢
很好
昂贵
铁器烤蓝
好
中等
金属常用防腐蚀方法的比较
1.解释下列现象:
(1)马口铁(镀Sn铁皮)做的罐头,打开后为什么极易生锈?
(2)
轮船船壳的水线以下部分,为什么要装上一定数量Zn块?
(3)烧过菜的铁锅未及时洗净(残液NaCl),第二天便出现红褐色锈斑。
C
c
2.下列制氢气的反应速率最快的是(
)
A.
纯锌和1mol/L
硫酸
B.
纯锌和18
mol/L
硫酸
C.
粗锌和1mol/L
硫酸
D.
粗锌和18mol/L
硫酸
3.下列叙述中可说明金属甲比乙活泼性强的是(
)
A.
甲和乙用导线连接插入稀盐酸溶液中,乙溶解,甲上有H2气放出;
B.
在氧化–还原反应中,甲比乙失去的电子多
C.
将甲乙作电极组成原电池时甲是负极
D.
同价态的阳离子,甲比乙的氧化性强
4、下列各情况,在其中Fe片腐蚀由快到慢的顺序__________________
(5)>(2)>(1)>(3)>(4)
5、下列装置中四块相同的Zn片,放置一段时间后腐蚀速率由慢到快的顺序是________________________
(4)>(2)>(1)>(3)
6、分析右图,按要求写出有关反应方程式:
(1)铁棒上的电极反应式为:
_________________________
(2)碳棒上的电极反应式为:
_________________________
(3)溶液中发生反应的化学方程式:
_________________________
_________________________
2Fe+2H2O+O2=
2
Fe(OH)2
4Fe(OH)2+2H2O+O2=4Fe(OH)3
O2+2H2O+4e-=4OH-
2Fe–4e-=2Fe2+
7、盐酸与锌片反应时,若加入可溶性醋酸铜晶体[(CH3COO)2Cu],将产生两种影响生成速率的因素.
其一是:
_______
___
______
_______,
其二是:
_______
___
_______________________________。
H+与CH3COO-结合生成醋酸,使H+浓度减小,从而减慢了反应速率
Zn置换出Cu形成了原电池,从而加快了反应速率
?[课堂练习]:
一.选择题(每小题有1~2个正答案确)
1.下列叙述正确的是
(
)
A、构成原电池正极和负极的材料必须是两种金属
B、由Cu、Zn作电极与CuSO4溶液组成的原电池中Cu是负极。
C、马口铁(镀锡铁)破损时与电解质溶液接触,锡先被腐蚀。
D、铜锌原电池工作时,若有13g锌被溶解,电路中就有0.4mol电子通过
D
2.钢铁锈蚀过程中可能发生的变化是(
)
①
Fe由单质转化为+2价;
②
Fe由+2价转化为+3价;
③
产生氢气;④产生氧气;
⑤
杂质C被氧化除去;
⑥
Fe(OH)3失水变成Fe2O3·3H2O.
?
A.
①
②
③
⑥??
B.
①
③
④??
C.
只有①
③??
D.
全部
A
3.为保护地下钢管不被腐蚀,可采用的方法是(
)
A、与直流电源负极相连接
B、与直流电源的正极相连接
C、与铜板相连接
D、与锌板相连接
4.下列说法正确的是
(
)
A.钢铁因含杂质而容易发生电化腐蚀,所以合金都不耐腐蚀
B.原电池反应是导致金属腐蚀的主要原因,故不能用来减缓金属的腐蚀
C.钢铁电化腐蚀的两种类型主要区别在于水膜的pH不同,引起的正极反应不同D.无论哪种类型的腐蚀,其实质都是金属被氧化
AD
CD
5.
铜制品上的铝质铆钉,在潮湿空气中易腐蚀的原因可描述为
(
)
A.
形成原电池铝作负极
B.
形成原电池时铜作负极
C.
形成原电池时,电流由铝经导线流向铜
D.
铝质铆钉发生了化学腐蚀
6.
以下现象与电化腐蚀无关的是
(
)
A.
黄铜(铜锌合金)制作的铜锣不易产生铜锈
B.
生铁比软铁芯(几乎是纯铁)容易生锈
C.
铁质器件附有铜质配件,在接触处易生锈
D.
银质奖牌久置后表面变暗
A
D
7.钢铁表面镀有下列金属时,当镀层部分被破坏时,铁不易被腐蚀的是
(
)
A.Sn?????
B.Zn??????
C.Cu?????
D.Ag
8.
如图各烧杯中盛有海水,铁在其中被腐蚀由快到慢的顺序为
(
)
A.②①③④
B.④③①②
C.④②①③
D.③②④①
B
C
9.下列事实不能用电化学理论解释的是(
)
A.
轮船水线以下的船壳上镶嵌有一定量的
锌块
B.镀锌的铁制品比镀锡的铁制品耐用
C.
铝片不用特殊方法保存
D.常温下铝跟稀硫酸快速反应,跟浓硫酸几
乎不反应
10、下列叙述中不正确的是
(
)
A、金属的电化腐蚀比化学腐蚀普遍
B、钢铁在干燥空气里不易腐蚀
C、用铝质铆钉铆接铁板,铁板易被腐蚀
D、原电池中电子由正极流入负极
CD
CD
11、下列叙述正确的是
(
)
A、原电池中阳离子向负极移动
B、原电池的负极发生氧化反应
C、马口铁(镀锡)的表面一旦破损,铁腐
蚀加快
D、白铁(镀锌)的表面一旦破损,铁腐蚀
加快
12.自来水管与下列材料做成的水龙头连接,锈蚀最快的铁水管连接的是
(
)
A、铜水龙头
B、铁水龙头
C、塑料水龙头
D、陶瓷水龙头
BC
A
二、填空题
1、在经常受酸雨危害的地区,金属制品易受腐蚀。其中铁制品主要发生____
腐蚀,负极反应式为_____________________;铜制品发生______腐蚀,正极反应式是_____________________。
析氢
Fe
-
2e-
=
Fe2+
吸氧
O2+4H++4e-=
2H2O
2、烧过菜的铁锅未及时洗去含有NaCl的残液,过一段时间便出现红棕色的铁锈斑点,已知该锈斑为Fe(OH)3失水的产物。表示Fe(OH)3生成的电极反应式、离子方程式和化学方程式分别为;
(1)负极
,
正极
;
(2)
;
(3)
。
2Fe
-
4e-
=
2Fe2+
O2+2H2O+4e-=4OH-
2Fe+2H2O+O2=
2
Fe(OH)2
4Fe(OH)2+2H2O+O2=4Fe(OH)3
3、在含有H2S气体的空气中,银器表面易变黑(生成了Ag2S),原因是银发生了______(填“析氢”或“吸氧”)腐蚀,其电极反应式为:正极
,
负极
,
最终在银器表面生成Ag2S的离子方程式是:
。
吸氧
O2+2H2O+4e-
=
4OH-
Ag-e-
=
Ag+
2Ag++H2S=Ag2S+2H+
为了除去银器表面的Ag2S,可采用如下方法:在一个铝制的容器中放入食盐溶液,将银器浸入食盐溶液,使银器与铝接触良好。过一段时间,银器表面变为银白色,并闻到臭鸡蛋的气味,观察到有少量白色絮状沉淀生成。请用电极反应式和离子方程式表示上述过程。
除去银器表面的Ag2S时:
(-)2Al-6e=2Al3+
(+)3Ag2S+6e=6Ag+3S2-溶液中发生如下反应:
2Al3++3S2-+6H2O=2Al(OH)3↓+3H2S↑
(Al3+和S2-的水解反应进行到底。)
4、市场上出售的“热敷袋”其中的成分主要是铁粉、碳粉、木屑和少量氯化钠、水等,热敷袋用塑料袋密封,使用时从袋中取出轻轻揉搓就会放出热量,用完后袋内有大量铁锈生成,回答下列各问:
(1)
热敷袋放出的热是来自
.
(2)
碳粉和氯化钠的作用分别是:
(3)
写出有关的电极反应式和化学方程式:
Fe被氧化
C
与Fe、NaCl溶液构成原电池,加速Fe的氧化;NaCl溶于水,形成电解质溶液
2Fe
-
4e-
=
2Fe2+
O2+2H2O+4e-=4OH-
Fe2++2OH-=
Fe(OH)2
4Fe(OH)2+2H2O+O2=4Fe(OH)3
[课堂练习]
1.把a、b、c、d 4块金属片浸入稀硫酸中,用导线两两相连可以组成几个原电池。若a、b相连时a为负极;c、d相连时电流由d到c;a、c相连时c极上产生大量气泡;b、d相连时b上有大量气泡产生;则四种金属的活动性顺序由强到弱为:
(a>c>d>b)
2.有M、N两种金属,分别与盐酸反应,产生H2速率相近,试设计一个实验比较M、N两种金属的活泼性。
3.有人设计以Pt和Zn为电极材料,埋入人体内作为某种心脏病人的心脏起搏器的能源。它依靠人体内血液种含有一定浓度的溶解氧、H+和Zn2+进行工作。它的两极电极反应式分别为:
。
正极:Zn-2e=Zn2+
负极:2H2O+O2+4e=4OH-
再
见
第四章
电化学基础
第4节
金属的电化学腐蚀与防护
请比较下列Fe腐蚀的快慢?
铁与酸反应,铁被腐蚀。
铁与碳形成原电池铁作负极被腐蚀。
腐蚀速率较慢。
腐蚀速率较快。
金属的腐蚀现象非常普遍:
1、钢铁生锈:
铁锈的主要成分:
金属腐蚀的不利后果有哪些?
Fe2O3·XH2O
Cu2(OH)2CO3
2、铜器表面生成铜绿:
铜绿的主要成分:
金属的腐蚀现象非常普遍:
金属腐蚀的不利后果有哪些?
Fe2O3·XH2O
Cu2(OH)2CO3
2、铜器表面生成铜绿:
铜绿的主要成分:
1、钢铁生锈:
铁锈的主要成分:
2007年8月1日,美国明尼苏达州一座跨越密西西比河的大桥发生坍塌。事故造成6人死亡。
金属制品的腐蚀
金属腐蚀给生产生活带来很多不便,造成了巨大的经济损失。
全世界每年因为金属腐蚀造成的直接经济损失约达7000亿美元,是地震、水灾、台风等自然灾害造成损失总和的6倍。
我国因金属腐蚀造成的损失占国民生产总值(GNP)的4%,钢铁因腐蚀而报废的数量约占钢铁当年产量的25%-30%。
金属腐蚀还可能造成环境污染。
资
料
在
线
一、金属腐蚀的本质:
是金属或合金与周围接触到的气体或液体发生氧化还原反应而引起损耗的过程。
M
-
ne-
=
Mn+
二、金属腐蚀的类型:
(1)化学腐蚀
金属跟接触到的物质直接发生化学反应而引起的腐蚀叫做化学腐蚀。
(2)电化学腐蚀
不纯的金属跟电解质溶液接触时,会发生原电池反应,比较活泼的金属失电子而被氧化的腐蚀叫做电化学腐蚀。
化学腐蚀和电化学腐蚀的比较
相互关系
反应
现象
条件
电化学腐蚀
化学腐蚀
化学腐蚀和电化学腐蚀同时发生,
但电化学腐蚀更普遍
较活泼的金属被氧化
金属被氧化
有微弱的电流产生
不产生电流
不纯金属或合金跟电解质溶液接触
金属跟接触的物质反应
钢铁在干燥的空气里长时间不易被腐蚀,但在潮湿的空气里却很快被腐蚀,这是什么原因呢?
在潮湿的空气里,钢铁表面吸附了一层薄薄的水膜。水中溶有O2、CO2、SO2等气体,这样在钢铁表面形成了一层电解质溶液的薄膜,它跟钢铁里的铁和少量的碳构成无数微小的原电池。
钢铁表面形成的微小原电池示意图
钢铁的析氢腐蚀示意图
钢铁的吸氧腐蚀示意图
钢铁在潮湿的空气中发生的电化学腐蚀的原理:
负极(Fe):
Fe—2e—
=
Fe2+
正极(C):
2H++2e—
=
H2↑
或2H2O+O2+4e—
=
4OH—
4.钢铁的析氢腐蚀和吸氧腐蚀比较
Fe2O3
·
nH2O
(铁锈)
通常两种腐蚀同时存在,但以后者更普遍。
析氢腐蚀
吸氧腐蚀
条件
水膜呈酸性。
水膜呈中性或酸性很弱。
电极反应
负极Fe(-
)
Fe-2e=Fe2+
2Fe-4e=2Fe2+
正极C(+)
2H
+
+
2e-
=
H2↑
O2+2H2O+4e=4OH-
总反应:
Fe
+
2H
+
==
=Fe2+
+
H2↑
2Fe+2H2O+O2=
2
Fe(OH)2
4Fe(OH)2+2H2O+O2=4Fe(OH)3
联系
金属腐蚀的快慢:
电解原理引起的腐蚀>原电池原理引起的腐蚀>化学腐蚀>有防护措施的腐蚀
同一金属在不同物质中腐蚀的快慢:
强电解质>弱电解质>非电解质
5.金属腐蚀快慢的判断:
(1)与构成微电池两极的材料有关。两极材料的活动性差别越大,氧化还原反应的速率越
,活泼金属被腐蚀的速度越
。
(2)
电解原理引起的腐蚀
原电池原理引起的腐蚀
化学腐蚀
有防腐措施的腐蚀。
(3)同一种金属的腐蚀:在强电解质中
弱电解质中
非电解质中
(4)一般说来:原电池原理引起的腐蚀
化学腐蚀
有防腐措施的腐蚀。
注意:在钢铁的腐蚀过程中,其电化学腐蚀更严重,在电化学腐蚀中,吸氧腐蚀更普遍。
>
>
>
>
>
快
快
>
>
[反馈练习]
1.下列情况下,海水中铁腐蚀最快的是(
)
B
2.如图所示,甲、乙两试管中各放一枚铁钉,甲试管中为NaCl溶液,乙试管为NH4Cl溶液(溶液呈弱酸性).数天后观察到的现象是
,
甲中正极反应为_______________.
乙中正极反应为
.
试管中残留气体平均相对分子质量的变化为甲
,乙
.
O2+2H2O+4e-=4OH-
2H++2e—
=
H2↑
减少
减少
Fe被腐蚀,U型管中甲端的液面高于乙端的液面
思考与交流
请根据生活常识以及下图总结金属防护常用的方法,并解释这些方法为什么可以达到防止金属腐蚀的目的。
健身器材刷油漆以防锈
衣架和电线的外面包上一层塑料层
某些工具的“机械转动部位”选用油脂来防锈,为什么不能用油漆
自行车的钢圈和车铃是在钢上镀上一层既耐腐蚀又耐磨的Cr
三、金属的防护
(1)
改善金属的内部组织结构(内因)
——制成合金(不锈钢)
(2)在金属表面覆盖保护层——电镀、油漆、钝化等
(3)电化学保护法——牺牲阳极的阴极保护法、外加直流电源的阴极保护法
牺牲阳极的阴极保护法
形成原电池反应时,让被保护金属做正极,不反应,起到保护作用;而活泼金属反应受到腐蚀。
你还知道哪些防止金属腐蚀的方法?请举例说明。
用牺牲镁块的方法来防止地下钢铁管道的腐蚀,镁块必须定期更换
制成不锈钢,在金属表面镀一层比要保护的金属耐腐蚀的金属。
用牺牲锌块的方法来保护船身,锌块必须定期更换
锌块
外加电流的阴极保护法
将被保护金属与另一附加电极作为电解池的两个极,使被保护的金属作为阴极,在外加直流电的作用下使阴极得到保护。此法主要用于防止土壤、海水及水中金属设备的腐蚀。
烤蓝
涂机油
烤漆
涂凡士林
镀锌
镀铬
[交流研讨]
你知道自行车的金属部件采用了什么样的防护措施吗?
方法
防腐效果
价格
镀塑
差
便宜
涂油漆
一般
便宜
镀锡
好
中等
镀铬
好
昂贵
镀锌
很好
中等
使用不锈钢
很好
昂贵
铁器烤蓝
好
中等
金属常用防腐蚀方法的比较
1.解释下列现象:
(1)马口铁(镀Sn铁皮)做的罐头,打开后为什么极易生锈?
(2)
轮船船壳的水线以下部分,为什么要装上一定数量Zn块?
(3)烧过菜的铁锅未及时洗净(残液NaCl),第二天便出现红褐色锈斑。
C
c
2.下列制氢气的反应速率最快的是(
)
A.
纯锌和1mol/L
硫酸
B.
纯锌和18
mol/L
硫酸
C.
粗锌和1mol/L
硫酸
D.
粗锌和18mol/L
硫酸
3.下列叙述中可说明金属甲比乙活泼性强的是(
)
A.
甲和乙用导线连接插入稀盐酸溶液中,乙溶解,甲上有H2气放出;
B.
在氧化–还原反应中,甲比乙失去的电子多
C.
将甲乙作电极组成原电池时甲是负极
D.
同价态的阳离子,甲比乙的氧化性强
4、下列各情况,在其中Fe片腐蚀由快到慢的顺序__________________
(5)>(2)>(1)>(3)>(4)
5、下列装置中四块相同的Zn片,放置一段时间后腐蚀速率由慢到快的顺序是________________________
(4)>(2)>(1)>(3)
6、分析右图,按要求写出有关反应方程式:
(1)铁棒上的电极反应式为:
_________________________
(2)碳棒上的电极反应式为:
_________________________
(3)溶液中发生反应的化学方程式:
_________________________
_________________________
2Fe+2H2O+O2=
2
Fe(OH)2
4Fe(OH)2+2H2O+O2=4Fe(OH)3
O2+2H2O+4e-=4OH-
2Fe–4e-=2Fe2+
7、盐酸与锌片反应时,若加入可溶性醋酸铜晶体[(CH3COO)2Cu],将产生两种影响生成速率的因素.
其一是:
_______
___
______
_______,
其二是:
_______
___
_______________________________。
H+与CH3COO-结合生成醋酸,使H+浓度减小,从而减慢了反应速率
Zn置换出Cu形成了原电池,从而加快了反应速率
?[课堂练习]:
一.选择题(每小题有1~2个正答案确)
1.下列叙述正确的是
(
)
A、构成原电池正极和负极的材料必须是两种金属
B、由Cu、Zn作电极与CuSO4溶液组成的原电池中Cu是负极。
C、马口铁(镀锡铁)破损时与电解质溶液接触,锡先被腐蚀。
D、铜锌原电池工作时,若有13g锌被溶解,电路中就有0.4mol电子通过
D
2.钢铁锈蚀过程中可能发生的变化是(
)
①
Fe由单质转化为+2价;
②
Fe由+2价转化为+3价;
③
产生氢气;④产生氧气;
⑤
杂质C被氧化除去;
⑥
Fe(OH)3失水变成Fe2O3·3H2O.
?
A.
①
②
③
⑥??
B.
①
③
④??
C.
只有①
③??
D.
全部
A
3.为保护地下钢管不被腐蚀,可采用的方法是(
)
A、与直流电源负极相连接
B、与直流电源的正极相连接
C、与铜板相连接
D、与锌板相连接
4.下列说法正确的是
(
)
A.钢铁因含杂质而容易发生电化腐蚀,所以合金都不耐腐蚀
B.原电池反应是导致金属腐蚀的主要原因,故不能用来减缓金属的腐蚀
C.钢铁电化腐蚀的两种类型主要区别在于水膜的pH不同,引起的正极反应不同D.无论哪种类型的腐蚀,其实质都是金属被氧化
AD
CD
5.
铜制品上的铝质铆钉,在潮湿空气中易腐蚀的原因可描述为
(
)
A.
形成原电池铝作负极
B.
形成原电池时铜作负极
C.
形成原电池时,电流由铝经导线流向铜
D.
铝质铆钉发生了化学腐蚀
6.
以下现象与电化腐蚀无关的是
(
)
A.
黄铜(铜锌合金)制作的铜锣不易产生铜锈
B.
生铁比软铁芯(几乎是纯铁)容易生锈
C.
铁质器件附有铜质配件,在接触处易生锈
D.
银质奖牌久置后表面变暗
A
D
7.钢铁表面镀有下列金属时,当镀层部分被破坏时,铁不易被腐蚀的是
(
)
A.Sn?????
B.Zn??????
C.Cu?????
D.Ag
8.
如图各烧杯中盛有海水,铁在其中被腐蚀由快到慢的顺序为
(
)
A.②①③④
B.④③①②
C.④②①③
D.③②④①
B
C
9.下列事实不能用电化学理论解释的是(
)
A.
轮船水线以下的船壳上镶嵌有一定量的
锌块
B.镀锌的铁制品比镀锡的铁制品耐用
C.
铝片不用特殊方法保存
D.常温下铝跟稀硫酸快速反应,跟浓硫酸几
乎不反应
10、下列叙述中不正确的是
(
)
A、金属的电化腐蚀比化学腐蚀普遍
B、钢铁在干燥空气里不易腐蚀
C、用铝质铆钉铆接铁板,铁板易被腐蚀
D、原电池中电子由正极流入负极
CD
CD
11、下列叙述正确的是
(
)
A、原电池中阳离子向负极移动
B、原电池的负极发生氧化反应
C、马口铁(镀锡)的表面一旦破损,铁腐
蚀加快
D、白铁(镀锌)的表面一旦破损,铁腐蚀
加快
12.自来水管与下列材料做成的水龙头连接,锈蚀最快的铁水管连接的是
(
)
A、铜水龙头
B、铁水龙头
C、塑料水龙头
D、陶瓷水龙头
BC
A
二、填空题
1、在经常受酸雨危害的地区,金属制品易受腐蚀。其中铁制品主要发生____
腐蚀,负极反应式为_____________________;铜制品发生______腐蚀,正极反应式是_____________________。
析氢
Fe
-
2e-
=
Fe2+
吸氧
O2+4H++4e-=
2H2O
2、烧过菜的铁锅未及时洗去含有NaCl的残液,过一段时间便出现红棕色的铁锈斑点,已知该锈斑为Fe(OH)3失水的产物。表示Fe(OH)3生成的电极反应式、离子方程式和化学方程式分别为;
(1)负极
,
正极
;
(2)
;
(3)
。
2Fe
-
4e-
=
2Fe2+
O2+2H2O+4e-=4OH-
2Fe+2H2O+O2=
2
Fe(OH)2
4Fe(OH)2+2H2O+O2=4Fe(OH)3
3、在含有H2S气体的空气中,银器表面易变黑(生成了Ag2S),原因是银发生了______(填“析氢”或“吸氧”)腐蚀,其电极反应式为:正极
,
负极
,
最终在银器表面生成Ag2S的离子方程式是:
。
吸氧
O2+2H2O+4e-
=
4OH-
Ag-e-
=
Ag+
2Ag++H2S=Ag2S+2H+
为了除去银器表面的Ag2S,可采用如下方法:在一个铝制的容器中放入食盐溶液,将银器浸入食盐溶液,使银器与铝接触良好。过一段时间,银器表面变为银白色,并闻到臭鸡蛋的气味,观察到有少量白色絮状沉淀生成。请用电极反应式和离子方程式表示上述过程。
除去银器表面的Ag2S时:
(-)2Al-6e=2Al3+
(+)3Ag2S+6e=6Ag+3S2-溶液中发生如下反应:
2Al3++3S2-+6H2O=2Al(OH)3↓+3H2S↑
(Al3+和S2-的水解反应进行到底。)
4、市场上出售的“热敷袋”其中的成分主要是铁粉、碳粉、木屑和少量氯化钠、水等,热敷袋用塑料袋密封,使用时从袋中取出轻轻揉搓就会放出热量,用完后袋内有大量铁锈生成,回答下列各问:
(1)
热敷袋放出的热是来自
.
(2)
碳粉和氯化钠的作用分别是:
(3)
写出有关的电极反应式和化学方程式:
Fe被氧化
C
与Fe、NaCl溶液构成原电池,加速Fe的氧化;NaCl溶于水,形成电解质溶液
2Fe
-
4e-
=
2Fe2+
O2+2H2O+4e-=4OH-
Fe2++2OH-=
Fe(OH)2
4Fe(OH)2+2H2O+O2=4Fe(OH)3
[课堂练习]
1.把a、b、c、d 4块金属片浸入稀硫酸中,用导线两两相连可以组成几个原电池。若a、b相连时a为负极;c、d相连时电流由d到c;a、c相连时c极上产生大量气泡;b、d相连时b上有大量气泡产生;则四种金属的活动性顺序由强到弱为:
(a>c>d>b)
2.有M、N两种金属,分别与盐酸反应,产生H2速率相近,试设计一个实验比较M、N两种金属的活泼性。
3.有人设计以Pt和Zn为电极材料,埋入人体内作为某种心脏病人的心脏起搏器的能源。它依靠人体内血液种含有一定浓度的溶解氧、H+和Zn2+进行工作。它的两极电极反应式分别为:
。
正极:Zn-2e=Zn2+
负极:2H2O+O2+4e=4OH-
再
见
