重庆市万州第二高级中学2020-2021学年度九年级期中考试化学试卷(Word版含答案)
文档属性
| 名称 | 重庆市万州第二高级中学2020-2021学年度九年级期中考试化学试卷(Word版含答案) | 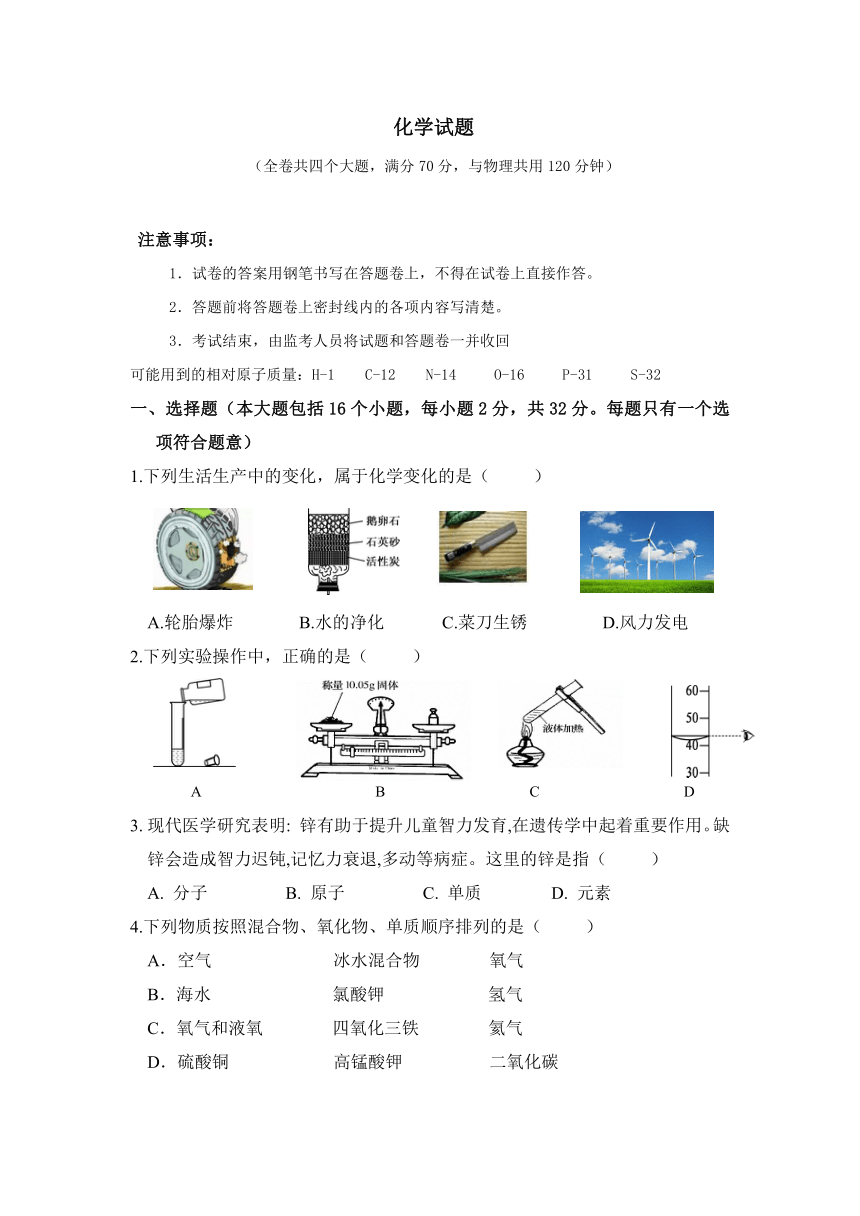 | |
| 格式 | zip | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-12-01 09:34:47 | ||
图片预览



文档简介
化学试题
(全卷共四个大题,满分70分,与物理共用120分钟)
注意事项:
1.试卷的答案用钢笔书写在答题卷上,不得在试卷上直接作答。
2.答题前将答题卷上密封线内的各项内容写清楚。
3.考试结束,由监考人员将试题和答题卷一并收回
可能用到的相对原子质量:H-1
C-12
N-14
O-16
P-31
S-32
一、选择题(本大题包括16个小题,每小题2分,共32分。每题只有一个选项符合题意)
1.下列生活生产中的变化,属于化学变化的是(
)
A.轮胎爆炸
B.水的净化
C.菜刀生锈
D.风力发电
2.下列实验操作中,正确的是(
)
A
B
C
D
3.?现代医学研究表明:
锌有助于提升儿童智力发育,在遗传学中起着重要作用。缺锌会造成智力迟钝,记忆力衰退,多动等病症。这里的锌是指(
)
A.
分子
B.
原子
C.
单质
D.
元素
4.下列物质按照混合物、氧化物、单质顺序排列的是(
)
A.空气
冰水混合物
氧气
B.海水
氯酸钾
氢气
C.氧气和液氧
四氧化三铁
氦气
D.硫酸铜
高锰酸钾
二氧化碳
5.下列有关实验现象的描述,正确的是(
)
A.
木炭在空气中燃烧发出红色火焰,生成二氧化碳气体
B.
细铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体
C.
硫在空气中燃烧,发出蓝紫色火焰
D.
红磷在空气中燃烧产生大量烟雾
6.下列对于宏观现象的微观解释中错误的(
)
A.“酒香不怕巷子深”,说明分子在不断运动
B.空气中的氧气和海水中的氧气都能供给呼吸,说明同种分子性质相同
C.20mL水与
20mL酒精混合后体积小于40mL,是因为分子数目减少
D.1滴水中大约有1.67×1021个水分子,说明水分子的质量和体积都很小
7.2019年诺贝尔化学奖授予了在开发锂离子电池方面作出贡献的三位科学家。新型锂离子电池的主要成分是磷酸铁锂(LiFePO4),已知锂(Li)的化合价为+1价,Fe的化合价为+2,则LiFePO4中P的化合价是(
)
A.+2
B.+3
C.+5
D.+6
8.下列有关实验操作的“先”“后”的说法中,正确的是(
)
A.用托盘天平称量10g固体样品时,先放药品,后放砝码
B.点燃氢气等可燃性气体前一定要检验其纯度,验纯后才能点燃
C.用胶头滴管取细口瓶内的液体时,先将其伸入液体内,后挤压胶头取液
D.加热高锰酸钾并用排水法收集O2的实验结束时,先熄灭酒精灯,后从水槽中移出导管
9.下列微粒符号中,对“2”含义的理解正确的是(
)
A.Fe2+中的“2”表示一个铁离子带有二个单位的正电荷
B.
2Zn中的“2”表示2个锌元素
C.H2O中的“2”表示一个水分子中含有两个氢原子
D
.
中化学式上方的“-2”表示硫元素为-2价
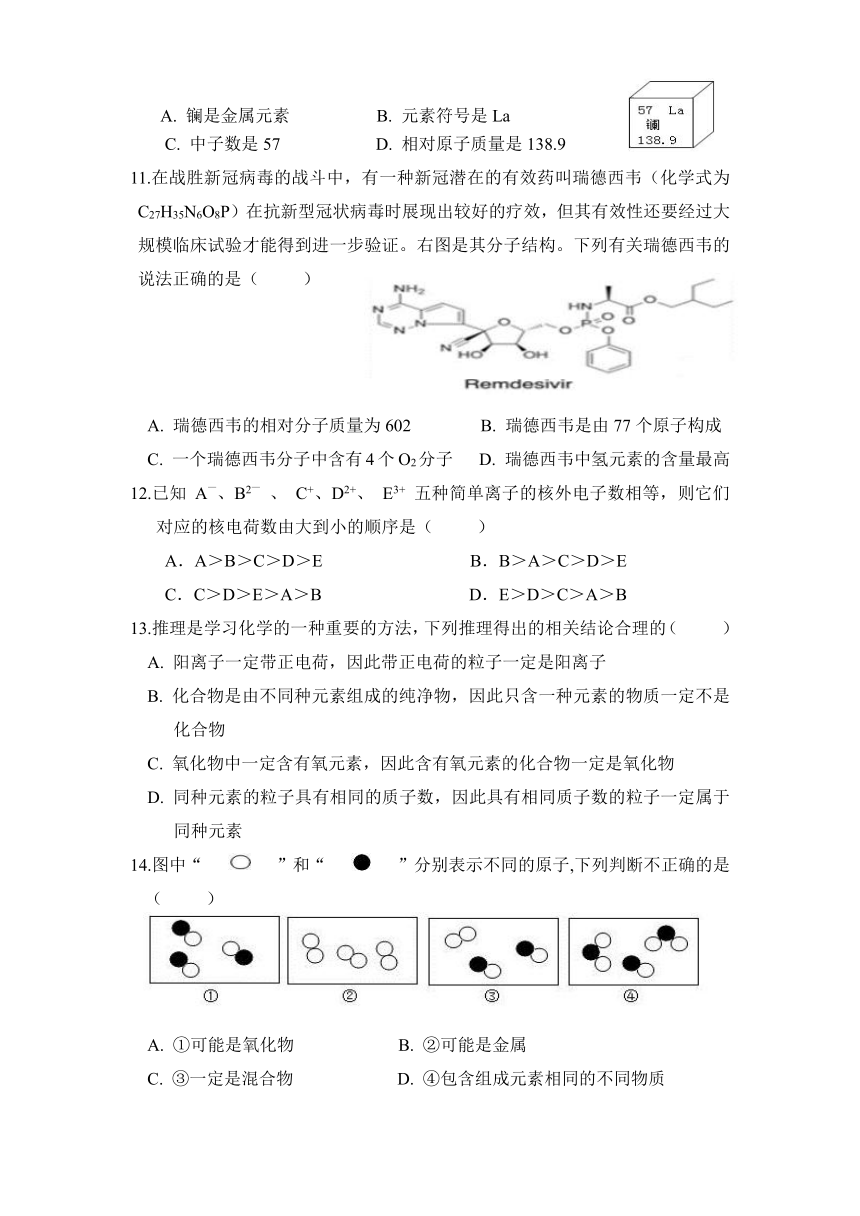
10.著名化学家徐光宪曾获得我国的最高科学技术奖,他的研究成果使稀土元素的分离变得更加简单。稀土元素包括镧(La)等17种元素,被称为当代的“工业味精”。元素周期表中镧元素的某些信息如下图所示,下列说法不正确的是(
)
A.
镧是金属元素
B.
元素符号是La
C.
中子数是57
D.
相对原子质量是138.9
11.在战胜新冠病毒的战斗中,有一种新冠潜在的有效药叫瑞德西韦(化学式为C27H35N6O8P)在抗新型冠状病毒时展现出较好的疗效,但其有效性还要经过大规模临床试验才能得到进一步验证。右图是其分子结构。下列有关瑞德西韦的说法正确的是(
)
A.
瑞德西韦的相对分子质量为602
B.
瑞德西韦是由77个原子构成
C.
一个瑞德西韦分子中含有4个O2分子
D.
瑞德西韦中氢元素的含量最高
12.已知
A—、B2—
、
C+、D2+、
E3+
五种简单离子的核外电子数相等,则它们对应的核电荷数由大到小的顺序是(
)
A.A>B>C>D>E
B.B>A>C>D>E
C.C>D>E>A>B
D.E>D>C>A>B
13.推理是学习化学的一种重要的方法,下列推理得出的相关结论合理的(
)
A.
阳离子一定带正电荷,因此带正电荷的粒子一定是阳离子
B.
化合物是由不同种元素组成的纯净物,因此只含一种元素的物质一定不是化合物
C.
氧化物中一定含有氧元素,因此含有氧元素的化合物一定是氧化物
D.
同种元素的粒子具有相同的质子数,因此具有相同质子数的粒子一定属于同种元素
14.图中“
”和“
”分别表示不同的原子,下列判断不正确的是
(
)
A.
①可能是氧化物
B.
②可能是金属
C.
③一定是混合物
D.
④包含组成元素相同的不同物质
15.下列关于四种微粒结构示意图的说法正确的是(
)
A.表示离子的是①②
B.化学性质相似的原子是①③
C.③④表示的元素能形成XY2化合物
D.④表示元素在化合物中只能显-1价
16.某化学兴趣小组用如图所示的装置来制取干燥的氧气,并测定氧气体积。装置气密性良好,图Ⅰ中的锥形瓶内盛有过氧化氢溶液,燃烧匙内装有二氧化锰,燃烧匙可上下移动,干燥管内装有干燥剂。下列说法正确的是(
)
①实验过程中,先检查装置的气密性,再装入药品;
②将装置Ⅰ分别与装置Ⅱ、Ⅲ、Ⅳ连接,均能达到实验目的;
③实验中,只须将装有二氧化锰的燃烧匙上提,离开过氧化氢溶液的液面,反应即可停止;
④若用装置Ⅲ收集氧气,可将带火星的木条伸入瓶中验满;
⑤若用装置Ⅳ测量生成氧气的体积,集气瓶上方原有空气对测量结果无影响。
A.①③⑤
B.②③⑤
C.①⑤
D.①②④
二、填空题(本大题包括4小题,共19分)
17.(4分)用适当的化学用语填空。
(1)3个铝离子___________。
(2)氢氧根离子___________。
(3)氦气___________。
(4)标出高锰酸钾中锰元素的化合价______。
18.
(4分)
化学与工农业生产、人类生活密切相关。回答下列问题:
(1)在生活中缓慢氧化的例子很多,以下不属于缓慢氧化的有______(填序号)。
①硫粉燃烧
②钢铁生锈
③火药爆炸
④食物的腐烂
⑤冰慢慢融化
⑥动植物的呼吸
(2)人类生活离不开空气.防止空气污染采取措施,政府提倡并要求各企事业单位必须使用低硫优质煤,这种做法能有效减少有害的气体是___________(填化学式)。
(3)为了检验从净水器里接的水是硬水还是软水,可向其中加入________。
(4)某些易碎、易潮的松脆食品,通常在其密封塑料包装袋中充入一种气体,从食品卫生、食品安全和经济角度综合考虑,下列最适宜用来作充入的气体是__________________(填序号)。
A.空气
B.氮气
C氧气
D.二氧化碳
E.稀有气体
19.(5分)联合国宣布2019年是“国际化学元素周期表年”。元素周期表示学习化学的重要工具,下图是根据元素周期表画出的1-18号元素的原子结构示意图,请回答下列问题:
(1)俄国科学家_________对元素周期表的发现和完善做出了重大贡献。
(2)元素周期表中不同元素间最本质的区别是___________(填字母)。
A.质子数不同
B.中子数不同
C.相对原子质量不同 D.电子数不同
(3)画出硫元素的原子结构示意图____________。
(4)在元素周期表中,同一族(纵行)的元素具有相似的化学性质,则下列各组元素具有相似化学性质的是_________
(填字母)。
A.C和Ne B.Be和Mg
C.Al和Si
D.F和Cl
(5)钙元素的原子结构示意图为
:
据此推测钙元素在元素周期表中的位置应该是_______周期。
20.(6分)A、B均为纯净物,C、D、E均为混合物;⑤五条途径(见下图)都会产生气体M,实验室可利用途径①、②、③反应来制取M,工业上可通过途径④来生产M,自然界可通过途径⑤来提供M;途径①、②、③反应类型相同,途径①反应生成的一种物质N可作为途径②、③反应的催化剂。图中部分物质未写出,请回答下列问题:
(1)N的名称是__________。
(2)常温下,A、B为固体,C为液体,写出途径②反应的化学符号表达式:___________________________,属于___________反应(填基本反应类型)。
(3)工业上需要大量的M时,一般采用叫做______________的方法,这个过程属于____________(填“物理”或“化学”)变化。
(4)自然界可通过途径⑤由二氧化碳和水在光照和叶绿素的作用下产生葡萄糖
(C6H12O6)和M。请写出反应符号表达式__________________________。
三、实验题(本大题包括3小题,共15分)
21.(5分)水是生命之源,“珍惜水,节约水,保护水”
是每个公民的责任和义务。右图是电解水的实验装置
图实。回答下列问题:
(1)玻璃管a是连接的电源的____________
(填“正”或“负”)极。
(2)写出该反应的化学符号表达式为______________________。
(3)实验刚开始时,a和b气体的体积比>2:1,则可能
原因是:________
(一条即可)。
(4)
电解水时,需要在水中预先加少量氢氧化钠或硫酸钠,目的是:_________。
(5)以下关于电解水的有关说法正确的是:__________(填序号)。
A.
负极产生的气体可以用带火星的木条检验
B.
水的电解实验说明水是由氢氧两种元素组成的
C.
电解水的实验证明化学变化中分子可以再分而原子不能再分
D.
电解水的实验中是将化学能转化为电能
22.(5分)周末小明去万州郊区的苎溪河游玩时,用瓶装了一些河水带回实验室,准备按下列流程进行实验,制取蒸馏水。请回答下列问题:
(1)小明将取回的水加入明矾的目的是___________。
(2)小明将加入了明矾的河水过滤后发现滤液仍浑浊,其原因可能是:_________
(一条即可)。
(3)市场上出售的净水器,有些就是利用________来吸附、过滤水中的杂质的
(4)生活中降低水的硬度的方法是:____________。
(5)下列关于水的说法中,不正确的有:__________(填序号)。
A.
地球上的水储量是丰富的,可供利用的淡水资源是无限的
B.
城市生活污水、工业废水应遵循“先净化,后排放”的原则
C.
农业生活中改变灌溉方式,由喷灌改为漫灌
D.
生活中改变不良的用水习惯,尽可能充分利用每一滴水
E.
爱护水资源主要从节约用水和防治水体污染两方面采取相应措施
23.(5分)某化学兴趣小组做镁在空气中燃烧的实验时,发现生成物中有少许黑色固体,针对这一现象,他们开展了以下探究,请仔细阅读并完成探究报告:
【探究目的】探究黑色固体是镁与空气中什么物质反应产生的?
【分析猜想】分析空气中各种成分,寻找猜想依据:
空气成分一:氧气;
空气成分二:水蒸气;
空气成分三:氮气;
空气成分四:二氧化碳;
空气成分五:稀有气体
小组同学认为不可能是稀有气体,因为__________________。
【实验一】镁带与氧气的反应
(1)请写出镁带与氧气反应的符号表达式:__________________________。
(2)将打磨光亮的镁带点燃后伸入盛满氧气的集气瓶中,镁带剧烈燃烧,发出耀眼的白光,生成白色固体。
实验结论:镁与氧气反应生成白色的氧化镁。
【实验二】镁带与水蒸气的反应
实验装置如图1所示:
(1)实验开始时,应先点燃A处酒精灯,等观察到水沸腾一会后,再点燃B处酒精灯,这样做的目的是:___________________________________。
(2)将生成的气体通入肥皂液中,用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中,说明生成的气体是_________。
实验结论:镁粉能和水蒸气反应,但装置B中并没有产生黑色固体。
【实验三】镁带与氮气的反应:将打磨光亮的镁带在氮气中充分燃烧,实验结束后,集气瓶内壁附着一层淡黄色的固体。
实验结论:镁与氮气在点燃的条件下发生化合反应生成淡黄色的氮化镁,
【探究结论】根据以上信息,可以推理得出镁在空气中燃烧产生的黑色固体是镁与空气中的二氧化碳反应产生的,该黑色固体应该是:________(写出化学式)。
四、计算题(本大题包括1小题,共4分)
24.(4分)我国科学家屠呦呦因为“发现青蒿素(化学式为C15H22O5)—一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命”而获得2015年诺贝尔生理学或医学奖。磺胺(化学式为C6H8N2O2S)是青蒿素之前最热门的抗疟药物之一。回答下列问题:
(1)一个青蒿素分子有
___________个原子。
(2)青蒿素中的碳元素与氧元素的质量比是:__________(最简整数比)。
(3)14.1克青蒿素中含有碳元素的质量与多少克磺胺中含有碳元素的质量
相等?(列式计算)
答案
选择题(32分)
CCDAB
CCBCC
ADBBCC
17.
(4分)3Al3+
OH-
He
18(4分)①③⑤
SO2
肥皂水,
B
19(5分)门捷列夫,A,
BD
四,
20
(6分)
二氧化锰,
KClO3
KCl+O2
分解,分离液态空气,物理
”
21(5分)负
H2O
H2
+O2
,02比H2易溶于水(合理即可)
增强水的导电性,
BC
22(5分)吸附沉淀,滤纸破损,活性炭,煮沸,AC,
23(5分)稀有气体化学性质很不活泼,Mg+O2
MgO
排除装置内的空气,避免影响实验结果,
氢气(H2)
C
24(4分)42,
9:4
(全卷共四个大题,满分70分,与物理共用120分钟)
注意事项:
1.试卷的答案用钢笔书写在答题卷上,不得在试卷上直接作答。
2.答题前将答题卷上密封线内的各项内容写清楚。
3.考试结束,由监考人员将试题和答题卷一并收回
可能用到的相对原子质量:H-1
C-12
N-14
O-16
P-31
S-32
一、选择题(本大题包括16个小题,每小题2分,共32分。每题只有一个选项符合题意)
1.下列生活生产中的变化,属于化学变化的是(
)
A.轮胎爆炸
B.水的净化
C.菜刀生锈
D.风力发电
2.下列实验操作中,正确的是(
)
A
B
C
D
3.?现代医学研究表明:
锌有助于提升儿童智力发育,在遗传学中起着重要作用。缺锌会造成智力迟钝,记忆力衰退,多动等病症。这里的锌是指(
)
A.
分子
B.
原子
C.
单质
D.
元素
4.下列物质按照混合物、氧化物、单质顺序排列的是(
)
A.空气
冰水混合物
氧气
B.海水
氯酸钾
氢气
C.氧气和液氧
四氧化三铁
氦气
D.硫酸铜
高锰酸钾
二氧化碳
5.下列有关实验现象的描述,正确的是(
)
A.
木炭在空气中燃烧发出红色火焰,生成二氧化碳气体
B.
细铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体
C.
硫在空气中燃烧,发出蓝紫色火焰
D.
红磷在空气中燃烧产生大量烟雾
6.下列对于宏观现象的微观解释中错误的(
)
A.“酒香不怕巷子深”,说明分子在不断运动
B.空气中的氧气和海水中的氧气都能供给呼吸,说明同种分子性质相同
C.20mL水与
20mL酒精混合后体积小于40mL,是因为分子数目减少
D.1滴水中大约有1.67×1021个水分子,说明水分子的质量和体积都很小
7.2019年诺贝尔化学奖授予了在开发锂离子电池方面作出贡献的三位科学家。新型锂离子电池的主要成分是磷酸铁锂(LiFePO4),已知锂(Li)的化合价为+1价,Fe的化合价为+2,则LiFePO4中P的化合价是(
)
A.+2
B.+3
C.+5
D.+6
8.下列有关实验操作的“先”“后”的说法中,正确的是(
)
A.用托盘天平称量10g固体样品时,先放药品,后放砝码
B.点燃氢气等可燃性气体前一定要检验其纯度,验纯后才能点燃
C.用胶头滴管取细口瓶内的液体时,先将其伸入液体内,后挤压胶头取液
D.加热高锰酸钾并用排水法收集O2的实验结束时,先熄灭酒精灯,后从水槽中移出导管
9.下列微粒符号中,对“2”含义的理解正确的是(
)
A.Fe2+中的“2”表示一个铁离子带有二个单位的正电荷
B.
2Zn中的“2”表示2个锌元素
C.H2O中的“2”表示一个水分子中含有两个氢原子
D
.
中化学式上方的“-2”表示硫元素为-2价
10.著名化学家徐光宪曾获得我国的最高科学技术奖,他的研究成果使稀土元素的分离变得更加简单。稀土元素包括镧(La)等17种元素,被称为当代的“工业味精”。元素周期表中镧元素的某些信息如下图所示,下列说法不正确的是(
)
A.
镧是金属元素
B.
元素符号是La
C.
中子数是57
D.
相对原子质量是138.9
11.在战胜新冠病毒的战斗中,有一种新冠潜在的有效药叫瑞德西韦(化学式为C27H35N6O8P)在抗新型冠状病毒时展现出较好的疗效,但其有效性还要经过大规模临床试验才能得到进一步验证。右图是其分子结构。下列有关瑞德西韦的说法正确的是(
)
A.
瑞德西韦的相对分子质量为602
B.
瑞德西韦是由77个原子构成
C.
一个瑞德西韦分子中含有4个O2分子
D.
瑞德西韦中氢元素的含量最高
12.已知
A—、B2—
、
C+、D2+、
E3+
五种简单离子的核外电子数相等,则它们对应的核电荷数由大到小的顺序是(
)
A.A>B>C>D>E
B.B>A>C>D>E
C.C>D>E>A>B
D.E>D>C>A>B
13.推理是学习化学的一种重要的方法,下列推理得出的相关结论合理的(
)
A.
阳离子一定带正电荷,因此带正电荷的粒子一定是阳离子
B.
化合物是由不同种元素组成的纯净物,因此只含一种元素的物质一定不是化合物
C.
氧化物中一定含有氧元素,因此含有氧元素的化合物一定是氧化物
D.
同种元素的粒子具有相同的质子数,因此具有相同质子数的粒子一定属于同种元素
14.图中“
”和“
”分别表示不同的原子,下列判断不正确的是
(
)
A.
①可能是氧化物
B.
②可能是金属
C.
③一定是混合物
D.
④包含组成元素相同的不同物质
15.下列关于四种微粒结构示意图的说法正确的是(
)
A.表示离子的是①②
B.化学性质相似的原子是①③
C.③④表示的元素能形成XY2化合物
D.④表示元素在化合物中只能显-1价
16.某化学兴趣小组用如图所示的装置来制取干燥的氧气,并测定氧气体积。装置气密性良好,图Ⅰ中的锥形瓶内盛有过氧化氢溶液,燃烧匙内装有二氧化锰,燃烧匙可上下移动,干燥管内装有干燥剂。下列说法正确的是(
)
①实验过程中,先检查装置的气密性,再装入药品;
②将装置Ⅰ分别与装置Ⅱ、Ⅲ、Ⅳ连接,均能达到实验目的;
③实验中,只须将装有二氧化锰的燃烧匙上提,离开过氧化氢溶液的液面,反应即可停止;
④若用装置Ⅲ收集氧气,可将带火星的木条伸入瓶中验满;
⑤若用装置Ⅳ测量生成氧气的体积,集气瓶上方原有空气对测量结果无影响。
A.①③⑤
B.②③⑤
C.①⑤
D.①②④
二、填空题(本大题包括4小题,共19分)
17.(4分)用适当的化学用语填空。
(1)3个铝离子___________。
(2)氢氧根离子___________。
(3)氦气___________。
(4)标出高锰酸钾中锰元素的化合价______。
18.
(4分)
化学与工农业生产、人类生活密切相关。回答下列问题:
(1)在生活中缓慢氧化的例子很多,以下不属于缓慢氧化的有______(填序号)。
①硫粉燃烧
②钢铁生锈
③火药爆炸
④食物的腐烂
⑤冰慢慢融化
⑥动植物的呼吸
(2)人类生活离不开空气.防止空气污染采取措施,政府提倡并要求各企事业单位必须使用低硫优质煤,这种做法能有效减少有害的气体是___________(填化学式)。
(3)为了检验从净水器里接的水是硬水还是软水,可向其中加入________。
(4)某些易碎、易潮的松脆食品,通常在其密封塑料包装袋中充入一种气体,从食品卫生、食品安全和经济角度综合考虑,下列最适宜用来作充入的气体是__________________(填序号)。
A.空气
B.氮气
C氧气
D.二氧化碳
E.稀有气体
19.(5分)联合国宣布2019年是“国际化学元素周期表年”。元素周期表示学习化学的重要工具,下图是根据元素周期表画出的1-18号元素的原子结构示意图,请回答下列问题:
(1)俄国科学家_________对元素周期表的发现和完善做出了重大贡献。
(2)元素周期表中不同元素间最本质的区别是___________(填字母)。
A.质子数不同
B.中子数不同
C.相对原子质量不同 D.电子数不同
(3)画出硫元素的原子结构示意图____________。
(4)在元素周期表中,同一族(纵行)的元素具有相似的化学性质,则下列各组元素具有相似化学性质的是_________
(填字母)。
A.C和Ne B.Be和Mg
C.Al和Si
D.F和Cl
(5)钙元素的原子结构示意图为
:
据此推测钙元素在元素周期表中的位置应该是_______周期。
20.(6分)A、B均为纯净物,C、D、E均为混合物;⑤五条途径(见下图)都会产生气体M,实验室可利用途径①、②、③反应来制取M,工业上可通过途径④来生产M,自然界可通过途径⑤来提供M;途径①、②、③反应类型相同,途径①反应生成的一种物质N可作为途径②、③反应的催化剂。图中部分物质未写出,请回答下列问题:
(1)N的名称是__________。
(2)常温下,A、B为固体,C为液体,写出途径②反应的化学符号表达式:___________________________,属于___________反应(填基本反应类型)。
(3)工业上需要大量的M时,一般采用叫做______________的方法,这个过程属于____________(填“物理”或“化学”)变化。
(4)自然界可通过途径⑤由二氧化碳和水在光照和叶绿素的作用下产生葡萄糖
(C6H12O6)和M。请写出反应符号表达式__________________________。
三、实验题(本大题包括3小题,共15分)
21.(5分)水是生命之源,“珍惜水,节约水,保护水”
是每个公民的责任和义务。右图是电解水的实验装置
图实。回答下列问题:
(1)玻璃管a是连接的电源的____________
(填“正”或“负”)极。
(2)写出该反应的化学符号表达式为______________________。
(3)实验刚开始时,a和b气体的体积比>2:1,则可能
原因是:________
(一条即可)。
(4)
电解水时,需要在水中预先加少量氢氧化钠或硫酸钠,目的是:_________。
(5)以下关于电解水的有关说法正确的是:__________(填序号)。
A.
负极产生的气体可以用带火星的木条检验
B.
水的电解实验说明水是由氢氧两种元素组成的
C.
电解水的实验证明化学变化中分子可以再分而原子不能再分
D.
电解水的实验中是将化学能转化为电能
22.(5分)周末小明去万州郊区的苎溪河游玩时,用瓶装了一些河水带回实验室,准备按下列流程进行实验,制取蒸馏水。请回答下列问题:
(1)小明将取回的水加入明矾的目的是___________。
(2)小明将加入了明矾的河水过滤后发现滤液仍浑浊,其原因可能是:_________
(一条即可)。
(3)市场上出售的净水器,有些就是利用________来吸附、过滤水中的杂质的
(4)生活中降低水的硬度的方法是:____________。
(5)下列关于水的说法中,不正确的有:__________(填序号)。
A.
地球上的水储量是丰富的,可供利用的淡水资源是无限的
B.
城市生活污水、工业废水应遵循“先净化,后排放”的原则
C.
农业生活中改变灌溉方式,由喷灌改为漫灌
D.
生活中改变不良的用水习惯,尽可能充分利用每一滴水
E.
爱护水资源主要从节约用水和防治水体污染两方面采取相应措施
23.(5分)某化学兴趣小组做镁在空气中燃烧的实验时,发现生成物中有少许黑色固体,针对这一现象,他们开展了以下探究,请仔细阅读并完成探究报告:
【探究目的】探究黑色固体是镁与空气中什么物质反应产生的?
【分析猜想】分析空气中各种成分,寻找猜想依据:
空气成分一:氧气;
空气成分二:水蒸气;
空气成分三:氮气;
空气成分四:二氧化碳;
空气成分五:稀有气体
小组同学认为不可能是稀有气体,因为__________________。
【实验一】镁带与氧气的反应
(1)请写出镁带与氧气反应的符号表达式:__________________________。
(2)将打磨光亮的镁带点燃后伸入盛满氧气的集气瓶中,镁带剧烈燃烧,发出耀眼的白光,生成白色固体。
实验结论:镁与氧气反应生成白色的氧化镁。
【实验二】镁带与水蒸气的反应
实验装置如图1所示:
(1)实验开始时,应先点燃A处酒精灯,等观察到水沸腾一会后,再点燃B处酒精灯,这样做的目的是:___________________________________。
(2)将生成的气体通入肥皂液中,用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中,说明生成的气体是_________。
实验结论:镁粉能和水蒸气反应,但装置B中并没有产生黑色固体。
【实验三】镁带与氮气的反应:将打磨光亮的镁带在氮气中充分燃烧,实验结束后,集气瓶内壁附着一层淡黄色的固体。
实验结论:镁与氮气在点燃的条件下发生化合反应生成淡黄色的氮化镁,
【探究结论】根据以上信息,可以推理得出镁在空气中燃烧产生的黑色固体是镁与空气中的二氧化碳反应产生的,该黑色固体应该是:________(写出化学式)。
四、计算题(本大题包括1小题,共4分)
24.(4分)我国科学家屠呦呦因为“发现青蒿素(化学式为C15H22O5)—一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命”而获得2015年诺贝尔生理学或医学奖。磺胺(化学式为C6H8N2O2S)是青蒿素之前最热门的抗疟药物之一。回答下列问题:
(1)一个青蒿素分子有
___________个原子。
(2)青蒿素中的碳元素与氧元素的质量比是:__________(最简整数比)。
(3)14.1克青蒿素中含有碳元素的质量与多少克磺胺中含有碳元素的质量
相等?(列式计算)
答案
选择题(32分)
CCDAB
CCBCC
ADBBCC
17.
(4分)3Al3+
OH-
He
18(4分)①③⑤
SO2
肥皂水,
B
19(5分)门捷列夫,A,
BD
四,
20
(6分)
二氧化锰,
KClO3
KCl+O2
分解,分离液态空气,物理
”
21(5分)负
H2O
H2
+O2
,02比H2易溶于水(合理即可)
增强水的导电性,
BC
22(5分)吸附沉淀,滤纸破损,活性炭,煮沸,AC,
23(5分)稀有气体化学性质很不活泼,Mg+O2
MgO
排除装置内的空气,避免影响实验结果,
氢气(H2)
C
24(4分)42,
9:4
同课章节目录
