人教版初中化学九年级下册10.2 酸和碱的中和反应 第一课时课件 (28张PPT)
文档属性
| 名称 | 人教版初中化学九年级下册10.2 酸和碱的中和反应 第一课时课件 (28张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 4.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-12-01 00:00:00 | ||
图片预览






文档简介
第十单元 酸和碱
课题2 酸和碱的中和反应
学习目标
(1)知道酸和碱发生了中和反应,
(2)能够写酸和碱发生的中和反应的化学方程式,
(3)掌握酸和碱发生的中和反应的实质,
(2)了解中和反应在实际中的应用。
【 H + + 酸根离子】
2.酸能使紫色石蕊试液变 色,使无色酚酞溶液
红
不变色。
1.常见的酸有
盐酸(HCl)、硫酸(H2SO4)等
3.常见的碱有 , 其中最便宜的是 ,可以用 与水反应直接制得。
氢氧化钠(NaOH)、氢氧化钙(Ca(OH)2)等
氢氧化钙
生石灰
4. 碱溶液能使紫色石蕊试液变 色,使无色酚酞溶 液变 色。
蓝
红
【 OH— + 金属离子(铵根离子)】
温故知新:
酸 碱
实验1、氢氧化铜与稀硫酸反应
实验2、氢氧化钠溶液和稀盐酸反应
实验探究一
观察实验有没有明显的现象,
它们是否发生了反应呢?
稀硫酸与氢氧化铜反应
现象:
蓝色沉淀逐渐消失,溶液变成蓝色
化学
方程式:
H2SO4 + Cu(OH)2 CuSO4+2H2O
反思:
稀盐酸滴入氢氧化钠溶液中,无明显现象,它们是否发生了反应呢?
实验探究一
观点一:氢氧化钠和稀盐酸没有反应
观点二:氢氧化钠和稀盐酸反应了但是没有明显现象
你倾向于哪一种观点呢?请你试一试,
设计一种有明显现象的实验来证明…
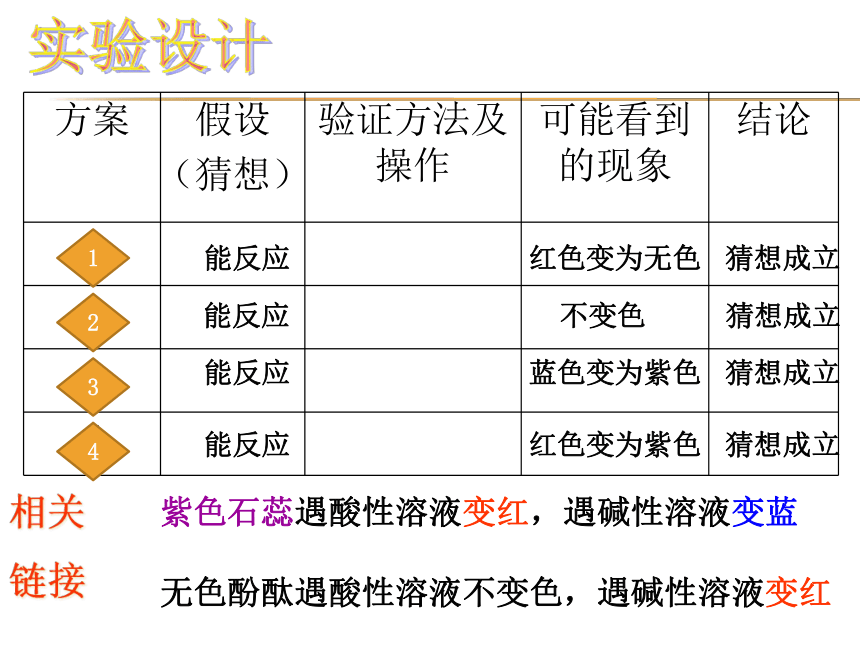
方案
假设
(猜想)
验证方法及操作
可能看到的现象
结论
1
2
3
4
紫色石蕊遇酸性溶液变红,遇碱性溶液变蓝
无色酚酞遇酸性溶液不变色,遇碱性溶液变红
相关
链接
能反应 红色变为无色 猜想成立
能反应 不变色 猜想成立
能反应 蓝色变为紫色 猜想成立
能反应 红色变为紫色 猜想成立
2
1
3
4
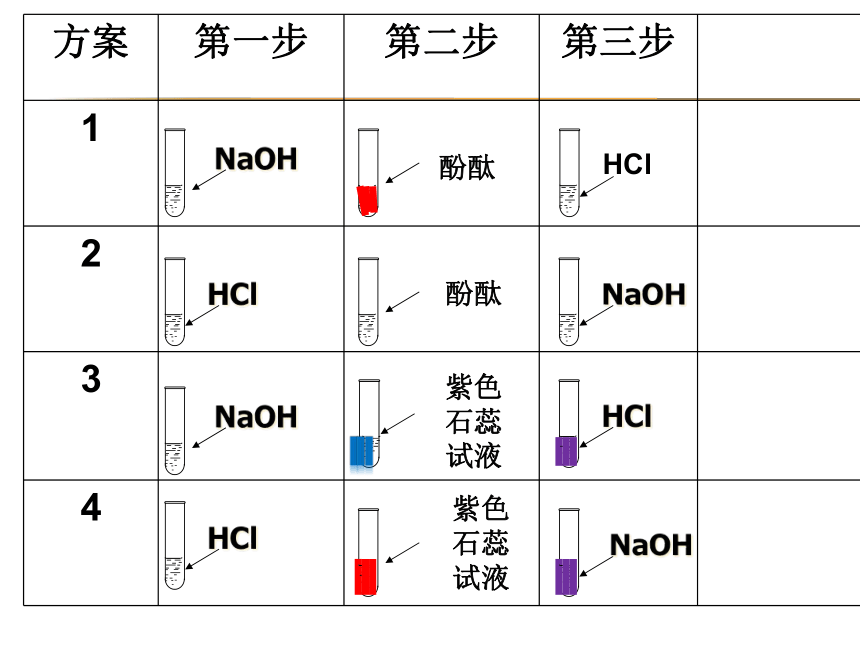
方案
第一步
第二步
第三步
1
2
3
4
NaOH
酚酞
NaOH
HCl
紫色石蕊试液
HCl
NaOH
HCl
紫色石蕊试液
酚酞
HCl
NaOH
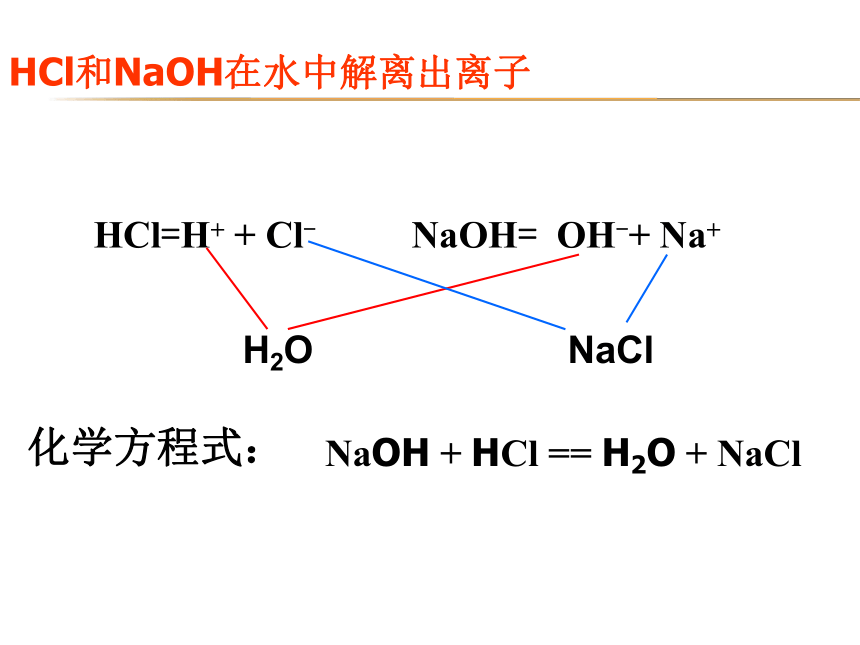
HCl=H+ + Cl-
NaOH= OH-+ Na+
HCl和NaOH在水中解离出离子
H2O
NaCl
NaOH + HCl == H2O + NaCl
化学方程式:
Cl-
OH-
H2O
Cl-
Cl-
Cl-
H2O
H+
H+
Na+
Na+
Na+
Na+
OH-
实质:H++OH-=H2O
NaOH + HCl == H2O + NaCl
观察动画,用H+ 、 Cl- 、 Na+ 、OH- 、 H2O 回答下列问题。
1、反应前稀盐酸中有 离子,
氢氧化钠溶液中有 离子。
2、两种溶液混合后溶液中有 微粒,溶液中减少的微粒是 。
3、可以发现反应前后没有变化的微粒是 ,整个反应过程中只有 和 结合成了H2O
4、发生中和反应的实质可表示为 。
H+ 、 Cl-
Na+ 、OH-
Cl-、Na+、H2O
H+ 、 OH-
H+ 、 OH-
Na+ 、Cl-
H++OH-=H2O
小试一把
NaOH + HCl === NaCl + H2O
碱
酸
水
?
盐
金属
离子
铵根
离子
酸根
离子
试试身手吧!
HCl + NaOH === NaCl + H2O
酸
+
碱
===
盐
+
水
H2SO4 + NaOH ----
HCl + Ca(OH)2 ----
H2SO4 + Ca(OH)2 ----
2 ---- Na2SO4 + 2H2O
2 ---- CaCl2 + 2H2O
---- CaSO4 + 2H2O
HCl + NaOH === NaCl + H2O
2 CaCl2 + 2H2O
H2SO4 + NaOH ===
HCl + Ca(OH)2 ===
H2SO4 + Ca(OH)2 ===
2 Na2SO4 + 2H2O
CaSO4 + 2H2O
这些反应有什么共同点吗?
中和反应的实质:
H++OH- H2O
酸与碱作用生成盐和水的反应
酸 + 碱 → 盐 + 水
中和反应:
生成盐和水的反应是中和反应吗?
CO2 +2NaOH=Na2CO3+H2O
Fe2O3+6HCl=2FeCl3+3H2O
下列反应,属于中和反应的是( )
A Zn +2HCl == ZnCl2 + H2
B CuO + 2HCl == CuCl2 + H2O
C Cu(OH)2 + H2SO4 == CuSO4 + 2H2O
D AgNO3 + HCl == AgCl + HNO3
C
中和反应在实际中的应用
用于医药
处理工业废水
改良土壤的酸碱性
1.改良土壤的酸碱性
加入酸 性物质
中性土壤
中性土壤
酸性土壤
熟石灰
Ca(OH)2
盐碱地
碱性土壤
2. 处理工厂的废水
⑴ 如何处理硫酸厂生产中形成的含硫酸的污水?
⑵ 请写出有关反应的化学方程式:
⑶用CaO来中和污水行不行?
H2SO4+?Ca(OH)2?=?CaSO4?+?2 H2O
H2SO4+?Ca(OH)2?=?CaSO4?+?2 H2O
CaO?+?H2O?=Ca(OH)2
处理突发事件:
2011年11月11日一辆盛有浓盐酸的罐车在环湾大道瑞昌路上桥口处泄露,两辆消防车迅速赶到现场先用熟石灰Ca(OH)2进行处理,又耗水20吨稀释处理。这次事故因处理得当、及时,所以没有对路面和花草造成太大影响。也不会造成环境污染。
2HCl + Ca(OH)2 = CaCl2 + 2H2O
熟石灰Ca(OH)
3、用于医药卫生
胃酸的主要成分是
盐酸
氢氧化铝【Al(OH)3】
Al(OH)3 + 3HCl === AlCl3 + 3H2O
氢氧化铝能中和胃酸
你能写出化学方程式吗?
斯达舒胶囊的主要成分
Al(OH)3
NaOH
CaCO3
Mg(OH)2
CaO
√
√
√
治疗蚊虫叮咬
蚊虫能在人的皮肤内分泌蚁酸,可用 物质如 来处理蚊虫叮咬
碱性
牙膏/肥皂水
本节课收获
1、中和反应: 酸和碱作用生成盐和水。
酸 + 碱 → 盐 + 水
HCl + NaOH === NaCl + H2O
2. 中和反应在实际中的应用。
天道酬勤 !
课题2 酸和碱的中和反应
学习目标
(1)知道酸和碱发生了中和反应,
(2)能够写酸和碱发生的中和反应的化学方程式,
(3)掌握酸和碱发生的中和反应的实质,
(2)了解中和反应在实际中的应用。
【 H + + 酸根离子】
2.酸能使紫色石蕊试液变 色,使无色酚酞溶液
红
不变色。
1.常见的酸有
盐酸(HCl)、硫酸(H2SO4)等
3.常见的碱有 , 其中最便宜的是 ,可以用 与水反应直接制得。
氢氧化钠(NaOH)、氢氧化钙(Ca(OH)2)等
氢氧化钙
生石灰
4. 碱溶液能使紫色石蕊试液变 色,使无色酚酞溶 液变 色。
蓝
红
【 OH— + 金属离子(铵根离子)】
温故知新:
酸 碱
实验1、氢氧化铜与稀硫酸反应
实验2、氢氧化钠溶液和稀盐酸反应
实验探究一
观察实验有没有明显的现象,
它们是否发生了反应呢?
稀硫酸与氢氧化铜反应
现象:
蓝色沉淀逐渐消失,溶液变成蓝色
化学
方程式:
H2SO4 + Cu(OH)2 CuSO4+2H2O
反思:
稀盐酸滴入氢氧化钠溶液中,无明显现象,它们是否发生了反应呢?
实验探究一
观点一:氢氧化钠和稀盐酸没有反应
观点二:氢氧化钠和稀盐酸反应了但是没有明显现象
你倾向于哪一种观点呢?请你试一试,
设计一种有明显现象的实验来证明…
方案
假设
(猜想)
验证方法及操作
可能看到的现象
结论
1
2
3
4
紫色石蕊遇酸性溶液变红,遇碱性溶液变蓝
无色酚酞遇酸性溶液不变色,遇碱性溶液变红
相关
链接
能反应 红色变为无色 猜想成立
能反应 不变色 猜想成立
能反应 蓝色变为紫色 猜想成立
能反应 红色变为紫色 猜想成立
2
1
3
4
方案
第一步
第二步
第三步
1
2
3
4
NaOH
酚酞
NaOH
HCl
紫色石蕊试液
HCl
NaOH
HCl
紫色石蕊试液
酚酞
HCl
NaOH
HCl=H+ + Cl-
NaOH= OH-+ Na+
HCl和NaOH在水中解离出离子
H2O
NaCl
NaOH + HCl == H2O + NaCl
化学方程式:
Cl-
OH-
H2O
Cl-
Cl-
Cl-
H2O
H+
H+
Na+
Na+
Na+
Na+
OH-
实质:H++OH-=H2O
NaOH + HCl == H2O + NaCl
观察动画,用H+ 、 Cl- 、 Na+ 、OH- 、 H2O 回答下列问题。
1、反应前稀盐酸中有 离子,
氢氧化钠溶液中有 离子。
2、两种溶液混合后溶液中有 微粒,溶液中减少的微粒是 。
3、可以发现反应前后没有变化的微粒是 ,整个反应过程中只有 和 结合成了H2O
4、发生中和反应的实质可表示为 。
H+ 、 Cl-
Na+ 、OH-
Cl-、Na+、H2O
H+ 、 OH-
H+ 、 OH-
Na+ 、Cl-
H++OH-=H2O
小试一把
NaOH + HCl === NaCl + H2O
碱
酸
水
?
盐
金属
离子
铵根
离子
酸根
离子
试试身手吧!
HCl + NaOH === NaCl + H2O
酸
+
碱
===
盐
+
水
H2SO4 + NaOH ----
HCl + Ca(OH)2 ----
H2SO4 + Ca(OH)2 ----
2 ---- Na2SO4 + 2H2O
2 ---- CaCl2 + 2H2O
---- CaSO4 + 2H2O
HCl + NaOH === NaCl + H2O
2 CaCl2 + 2H2O
H2SO4 + NaOH ===
HCl + Ca(OH)2 ===
H2SO4 + Ca(OH)2 ===
2 Na2SO4 + 2H2O
CaSO4 + 2H2O
这些反应有什么共同点吗?
中和反应的实质:
H++OH- H2O
酸与碱作用生成盐和水的反应
酸 + 碱 → 盐 + 水
中和反应:
生成盐和水的反应是中和反应吗?
CO2 +2NaOH=Na2CO3+H2O
Fe2O3+6HCl=2FeCl3+3H2O
下列反应,属于中和反应的是( )
A Zn +2HCl == ZnCl2 + H2
B CuO + 2HCl == CuCl2 + H2O
C Cu(OH)2 + H2SO4 == CuSO4 + 2H2O
D AgNO3 + HCl == AgCl + HNO3
C
中和反应在实际中的应用
用于医药
处理工业废水
改良土壤的酸碱性
1.改良土壤的酸碱性
加入酸 性物质
中性土壤
中性土壤
酸性土壤
熟石灰
Ca(OH)2
盐碱地
碱性土壤
2. 处理工厂的废水
⑴ 如何处理硫酸厂生产中形成的含硫酸的污水?
⑵ 请写出有关反应的化学方程式:
⑶用CaO来中和污水行不行?
H2SO4+?Ca(OH)2?=?CaSO4?+?2 H2O
H2SO4+?Ca(OH)2?=?CaSO4?+?2 H2O
CaO?+?H2O?=Ca(OH)2
处理突发事件:
2011年11月11日一辆盛有浓盐酸的罐车在环湾大道瑞昌路上桥口处泄露,两辆消防车迅速赶到现场先用熟石灰Ca(OH)2进行处理,又耗水20吨稀释处理。这次事故因处理得当、及时,所以没有对路面和花草造成太大影响。也不会造成环境污染。
2HCl + Ca(OH)2 = CaCl2 + 2H2O
熟石灰Ca(OH)
3、用于医药卫生
胃酸的主要成分是
盐酸
氢氧化铝【Al(OH)3】
Al(OH)3 + 3HCl === AlCl3 + 3H2O
氢氧化铝能中和胃酸
你能写出化学方程式吗?
斯达舒胶囊的主要成分
Al(OH)3
NaOH
CaCO3
Mg(OH)2
CaO
√
√
√
治疗蚊虫叮咬
蚊虫能在人的皮肤内分泌蚁酸,可用 物质如 来处理蚊虫叮咬
碱性
牙膏/肥皂水
本节课收获
1、中和反应: 酸和碱作用生成盐和水。
酸 + 碱 → 盐 + 水
HCl + NaOH === NaCl + H2O
2. 中和反应在实际中的应用。
天道酬勤 !
同课章节目录
