2011年10月海南省中学化学课堂教学评比:临高二中陈小花选修四《原电池》教案
文档属性
| 名称 | 2011年10月海南省中学化学课堂教学评比:临高二中陈小花选修四《原电池》教案 |

|
|
| 格式 | zip | ||
| 文件大小 | 85.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2011-11-04 00:00:00 | ||
图片预览

文档简介
选修4《化学反应原理》
1 原电池
临高二中 陈小花
一、教学目标
1、知识与技能:
(1)在必修2的基础上,进一步学习原电池的工作原理,探究简单原电池的不足和改进。
(2)学习实验研究的方法,能设计并完成化学能与电能转化的化学实验。
(3)理解原电池的工作原理,掌握电极反应式及电池反应方程式的书写。
2、过程与方法
经历对化学能与电能转化的化学实验探究的过程,进一步理解探究的意义,学习科学探究的基本方法,提高科学探究的能力。
3、情感态度与价值观
发展学习化学的兴趣,乐于探究化学能转化成电能的奥秘,体验科学探究的艰辛和喜悦,感受化学世界的奇妙与和谐。
二、教学重点
进一步了解原电池的工作原理,能够写电极反应式及电池反应。
三、教学难点
原电池的工作原理
四、教学方法与手段
启发式提问,实验探究法,多媒体等辅助教学手段。
五、教学过程
(一)引入新课
展示各种电池应用的图片,引入课题一原电池,而后由学生回忆必修2的内容,回答原电池的定义、形成条件、正负电极的判断以及电流的方向和电子的流向。
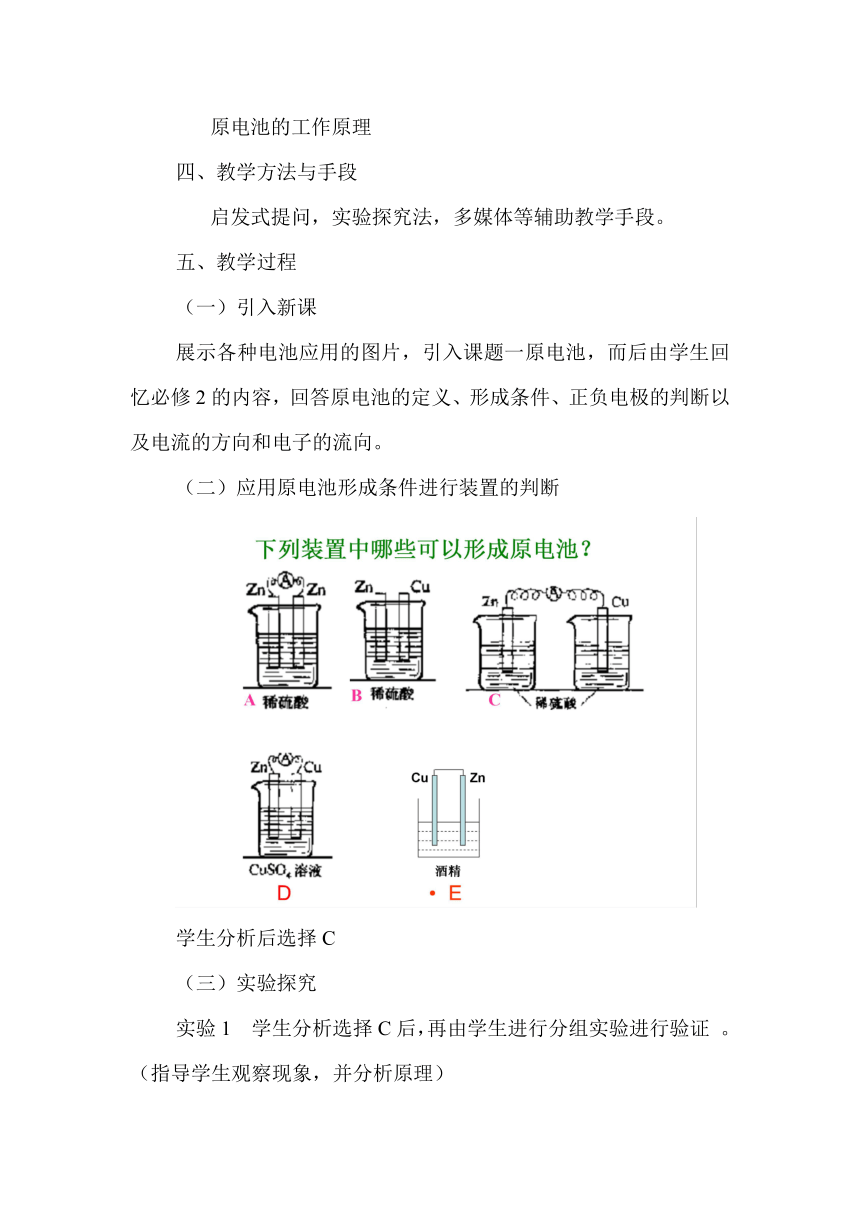
(二)应用原电池形成条件进行装置的判断
学生分析后选择C
(三)实验探究
实验1 学生分析选择C后,再由学生进行分组实验进行验证 。(指导学生观察现象,并分析原理)
并要求学生完成电极反应式及原电池的反应方程式。
电极反应式:
负极: Zn - 2e - = Zn 2+ (氧化反应)
正极: Cu 2+ + 2e - = Cu (还原反应)
总电池反应方程式为:Zn + Cu 2+ = Zn 2+ + Cu
思考:如何形成持续、稳定的原电池?
实验2 P71实验4-1
(学生自主实验探究,指导学生观察现象,并分析原理,点出半电池、盐桥、内电路、外电路等概念)
(四)、小结
通过以上二个实验的比较,得出如何才能设计出持续、稳定电流的原电池。从本节课的学习我们学到了科学探究的基本方法。
(五)、练习
1、依据氧化还原反应:2Ag+ (aq) + Cu(s) == Cu 2+ (aq) + 2Ag(s)设计的原电池如图所示。
请回答下列问题:
(1)电极X的材料是_________;电解质溶液Y是____;
(2)银电极为电池的_______极,发生的电极反应为_____________;X电极上发生的电极反应为_;
(3)外电路中的电子是从_____电极流向______电极。
2、作业
实 验 设 计
请利用:Cu+2AgNO3 = Cu(NO3)2+2Ag 的反应原理,设计一个能产生持续电流的原电池装置,画此出装置简图。
(1)、注明原电池的正极和负极
(2)、注明外电路中电子的流向?
(3)、写出电极反应式
需要实验设备要求:电流毫安表6个,盐桥6个,锌片及铜片、导线若干
.精品资料。欢迎使用。 ( http: / / www.21cnjy.com / " \o "欢迎登陆21世纪教育网 )
1 原电池
临高二中 陈小花
一、教学目标
1、知识与技能:
(1)在必修2的基础上,进一步学习原电池的工作原理,探究简单原电池的不足和改进。
(2)学习实验研究的方法,能设计并完成化学能与电能转化的化学实验。
(3)理解原电池的工作原理,掌握电极反应式及电池反应方程式的书写。
2、过程与方法
经历对化学能与电能转化的化学实验探究的过程,进一步理解探究的意义,学习科学探究的基本方法,提高科学探究的能力。
3、情感态度与价值观
发展学习化学的兴趣,乐于探究化学能转化成电能的奥秘,体验科学探究的艰辛和喜悦,感受化学世界的奇妙与和谐。
二、教学重点
进一步了解原电池的工作原理,能够写电极反应式及电池反应。
三、教学难点
原电池的工作原理
四、教学方法与手段
启发式提问,实验探究法,多媒体等辅助教学手段。
五、教学过程
(一)引入新课
展示各种电池应用的图片,引入课题一原电池,而后由学生回忆必修2的内容,回答原电池的定义、形成条件、正负电极的判断以及电流的方向和电子的流向。
(二)应用原电池形成条件进行装置的判断
学生分析后选择C
(三)实验探究
实验1 学生分析选择C后,再由学生进行分组实验进行验证 。(指导学生观察现象,并分析原理)
并要求学生完成电极反应式及原电池的反应方程式。
电极反应式:
负极: Zn - 2e - = Zn 2+ (氧化反应)
正极: Cu 2+ + 2e - = Cu (还原反应)
总电池反应方程式为:Zn + Cu 2+ = Zn 2+ + Cu
思考:如何形成持续、稳定的原电池?
实验2 P71实验4-1
(学生自主实验探究,指导学生观察现象,并分析原理,点出半电池、盐桥、内电路、外电路等概念)
(四)、小结
通过以上二个实验的比较,得出如何才能设计出持续、稳定电流的原电池。从本节课的学习我们学到了科学探究的基本方法。
(五)、练习
1、依据氧化还原反应:2Ag+ (aq) + Cu(s) == Cu 2+ (aq) + 2Ag(s)设计的原电池如图所示。
请回答下列问题:
(1)电极X的材料是_________;电解质溶液Y是____;
(2)银电极为电池的_______极,发生的电极反应为_____________;X电极上发生的电极反应为_;
(3)外电路中的电子是从_____电极流向______电极。
2、作业
实 验 设 计
请利用:Cu+2AgNO3 = Cu(NO3)2+2Ag 的反应原理,设计一个能产生持续电流的原电池装置,画此出装置简图。
(1)、注明原电池的正极和负极
(2)、注明外电路中电子的流向?
(3)、写出电极反应式
需要实验设备要求:电流毫安表6个,盐桥6个,锌片及铜片、导线若干
.精品资料。欢迎使用。 ( http: / / www.21cnjy.com / " \o "欢迎登陆21世纪教育网 )
