2011版初中化学新课标金榜学案配套课件:单元评价检测四(鲁教版九年级全一册)(五四制)
文档属性
| 名称 | 2011版初中化学新课标金榜学案配套课件:单元评价检测四(鲁教版九年级全一册)(五四制) |

|
|
| 格式 | rar | ||
| 文件大小 | 601.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2011-11-04 00:00:00 | ||
图片预览











文档简介
(共42张PPT)
第四单元 化学与健康
(45分钟 100分)
可能用到的相对原子质量:H-1 C-12 N-14
O-16 S-32
一、选择题(本题包括10个小题,每小题3分,共30分)
1.医生建议患甲状腺肿大的病人多食海带等海产品,这是因为海带中含有较丰富的( )
A.氟元素 B.碘元素 C.锌元素 D.钙元素
【解析】选B。缺乏碘元素易患甲状腺肿大,海带中含有丰富的碘元素。
2.将下列物质加入蛋白质试液中,不会使蛋白质失去原有生理功能的是( )
A.甲醛 B.硫酸钠溶液
C.乙酸铅溶液 D.浓硝酸
【解析】选B。能使蛋白质失去生理活性的物质包含:重金属盐、甲醛、浓硝酸等物质,在加热的条件下也能使蛋白质失去生理活性,硫酸钠不属于重金属盐,不能使蛋白质失去生理活性,故选B。
3.某品牌妙脆角的主要配料如下:
大米粉、食用植物油、白砂糖、食
用盐、抗氧化剂、牛奶和大豆。
判断这种食品中不含哪种营养
素( )
A.糖类 B.油脂
C.蛋白质 D.维生素
【解析】选D。从某品牌妙脆角的配料成分可知:大米粉中富含淀粉,淀粉属于糖类物质;食用植物油中富含油脂;牛奶和大豆中富含蛋白质;不含有维生素。故选D。
4.微量元素在人体内的质量总和不到人体质量的千分之一,但这些元素对人体的正常发育和健康起着重要的作用。下列各元素全部属于人体中微量元素的是( )
A.Na Cl O B.H O N
C.N Ca C D.I Fe Zn
【解析】选D。根据元素含量的分类:其含量小于0.01%的元素为微量元素,其含量大于0.01%的称为常量元素,其中氧元素为65%,碳元素为18%,氮元素为3%,都不是微量元素,故A、B、C错误。
5.人体成长所需的蛋白质,有些必须在食物中才能获取。那么人体通过食物获取蛋白质的主要作用是( )
A.与水发生一系列反应,最终变成葡萄糖
B.在肠胃里与水发生反应,生成氨基酸
C.调节新陈代谢、预防疾病
D.维持恒定体温、提供能量
【解析】选B。食物中的蛋白质进入人体后,在蛋白酶和水的作用下,逐步分解成可被人体吸收的氨基酸,其中一部分重新组合成人体所需的各种蛋白质,另一部分排出体外。
6.下列几种物品都是日常生活中常见的食物,其中富含糖类的食品是( )
A.①③ B.①④ C.②④ D.①②
【解析】选D。本题主要考查人体中所需的营养素在哪些食品中含量较多,其中玉米和大米中富含淀粉,淀粉属于糖类物质,豆油中富含油脂;鱼中富含蛋白质,故选D。
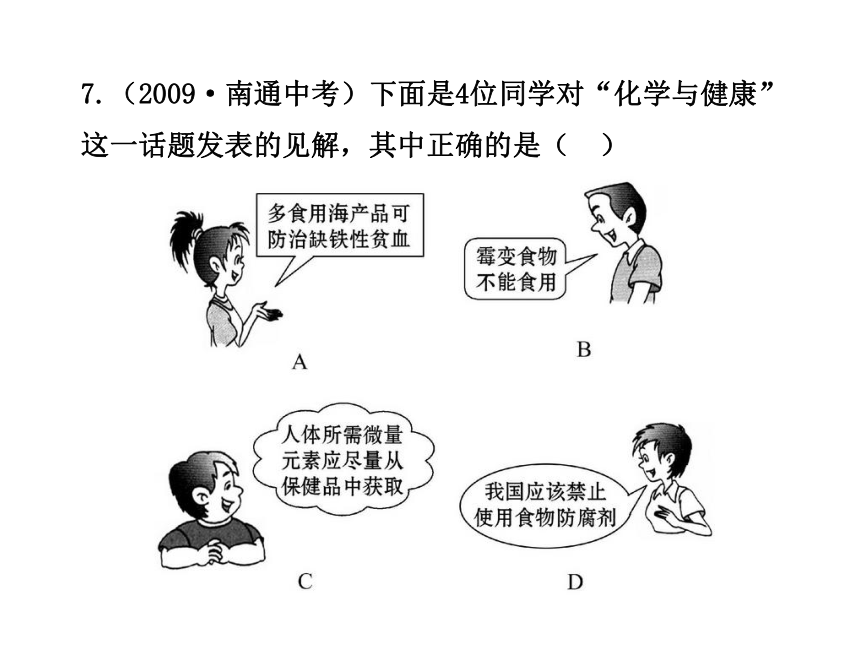
7.(2009·南通中考)下面是4位同学对“化学与健康”这一话题发表的见解,其中正确的是( )
【解析】选B。霉变食物中含有致癌作用的黄曲霉素,对健康非常有害,故不能食用。
8.日常生活中有很多错误的做法在威胁着我们的身体健康。请考虑下列做法不会危及我们健康的是( )
A.把霉变大米淘净后继续食用
B.用甲醛水溶液浸泡水产品
C.根据医嘱适量服用补钙剂
D.变质的剩饭加热后再吃
【解析】选C。霉变的食物,受到菌类的污染,对身体造成多种危害,不能继续食用,故A、D的做法不正确;甲醛属于有毒物质,能使蛋白质失去生理活性,故B的做法不正确;微量元素对人体的成长十分的重要,如果食品中不能提供足量的微量元素,就可通过药品或保健品来适量补充。故选C。
9.(2009·鄂州中考)小明同学出现了腹泻的症状,医生建议他暂时不要吃富含蛋白质和油脂的食物。小明同学应该选择的早餐是( )
A.馒头和稀饭 B.鸡蛋和牛奶
C.油条和豆浆 D.肯德基和酸奶
【解析】选A。鸡蛋、牛奶、豆浆、酸奶中富含蛋白质,油条和肯德基中富含油脂。馒头和稀饭中富含淀粉等糖类物质,可以作为早餐。
10.某2.3 g有机化合物跟4.8 g氧气恰好完全燃烧,生成4.4 g二氧化碳和2.7 g水,则该有机物的化学式
为( )
A.CH4 B.C2H2 C.C2H6O D.C2H4O2
【解析】选C。根据质量守恒可知:反应前后同一种元
素的质量不变。可求出4.4 g二氧化碳中含有碳元素
1.2 g,2.7 g水中含氢元素0.3 g,由此可知有机物中
含氧元素的质量为:2.3 g-1.2 g-0.3 g=0.8 g。则有
机物中碳、氢、氧三种元素原子个数比为:
=2∶6∶1。即化学式为C2H6O。
二、理解与应用(本题包括4个小题,共30分)
11.(8分)下面的方框内是某食品包装上的部分说明,请从其中标出的配料中选出一种符合条件的物质填在下列相应的空格中:
(1)____________________中富含蛋白质;
(2)___________________中富含油脂;
(3)___________________属于维生素;
(4)____________________属于无机盐。
【解析】本题将课本知识与生活实际有机地结合起来,利于学生正确的识别各食品中所含的营养素。由食品的配料可知:小麦粉、麦芽糖中富含糖类;食用植物油中富含油脂;食用盐、碳酸钙、焦亚硫酸钠中主要成分为无机盐;鸡全蛋粉、全脂奶粉中富含蛋白质;维生素D属于维生素。
答案:(1)鸡全蛋粉、全脂奶粉 (2)食用植物油
(3)维生素D (4)食用盐、碳酸钙、焦亚硫酸钠
12.(6分)下表是豆腐中一些成分的平均质量分数:
除水和无机盐外,豆腐中含有的营养素还有_______,含人体所需的微量元素是________。若成年人每天食用80 g豆腐,则摄入铁的质量为_______g。
【解析】由豆腐的成分可知:豆腐中含有人体所需的六种营养素(水、无机盐、糖类、蛋白质、油脂、维生素)。元素在人体中含量在0.01%以下的为微量元素,如铁、锌、碘、硒等。成年人每天摄入铁的质量为:
80 g×1.4%=1.12 g。
答案:糖类、蛋白质、油脂、维生素 铁 1.12
13.(8分)古人云:“民以食为天”,人们一日三餐的主食多为淀粉类食品,如米饭、面包等。食物中的淀粉[(C5H10O5)n]在人体内不能直接被吸收利用,而是在淀粉酶和水的作用下转化为葡萄糖(C6H12O6),并溶解在血液中,提供营养和能量。试根据题意回答下列问题:
(1)淀粉属于_____(填“无机物”或“有机物”)。
(2)葡萄糖分子中碳、氢、氧的原子个数之比为____
(最简整数比)。葡萄糖在人体内发生如下化学反应:C6H12O6+6O2====6CO2+6H2O,该反应的类型属于__反应。
(3)欲检验某食物中是否含有淀粉,下列试剂中,最宜选用的是_____(填序号)。
A.石蕊试液 B.碳酸钠溶液 C.稀盐酸
D.碘水 E.氢氧化钠溶液
【解析】淀粉属于有机物中的糖类物质;葡萄糖的化学式为:C6H12O6,则可知其原子个数比为:1∶2∶1;物质与氧气发生的反应属于氧化反应;检验某种物质中是否含有淀粉,我们常用碘水。
答案:(1)有机物 (2)1∶2∶1 氧化 (3)D
14.(8分)(2009·乌鲁木齐中考)在人的胃液中,盐酸(HCl)的质量分数大约是0.45%~0.6%。它具有以下生理功能:①促进胃蛋白酶的催化作用,使蛋白质水解而被人体吸收;②使糖类物质进一步水解;③杀菌。
请结合上述内容回答下列问题:
(1)如果用Al(OH)3的混合剂治疗胃酸过多,则发生反应的化学方程式为________。
(2)人类食用适量的NaCl有利于________。
A.促进盐酸产生
B.帮助消化和增进食欲
C.治疗胃酸过多
D.治疗缺碘性甲状腺肿大
(3)糖类、____、油脂、维生素、无机盐和水是人体的六大营养物质。在这六大营养物质中,不经过消化,就可以在消化道内直接被人体吸收的有____。
【解析】(1)注意方程式的配平;(2)依据题中所给资料可知:NaCl被摄入人体后,其中的Cl在酶的作用下利于HCl的形成,NaCl作为调味品能增加人们的食欲。(3)属于识记内容。
答案:(1)Al(OH)3+3HCl====AlCl3+3H2O
(2)A、B
(3)蛋白质 维生素、无机盐和水
三、实验与探究(本题包括2个小题,共24分)
15.(12分)化学可以帮助人类认识改造周围的世界,促进社会发展。糖类、油脂、蛋白质和维生素都是人类的基本营养物质。下表为某品牌燕麦片标签中的一部分。
(1)燕麦片的营养成分中能与水反应生成氨基酸的营养物质是______;每克营养物质氧化时放出能量最多的是________;人体必需的微量元素是______。
(2)维生素C易溶于水,向其水溶液中滴入紫色石蕊试液,石蕊变红色,加热该溶液至沸腾,红色消失。因此,烹调富含维生素C的食物时,应该注意________;在碱性条件下,维生素C易被空气氧化,烧煮时最好加一点_____________。
【解析】蛋白质摄入人体后在水与酶的作用下生成人体必需的氨基酸,油脂氧化放出的能量为糖类的2倍还要多,人体中必需的微量元素为铁、锌、碘、硒等,维生素C的水溶液能使石蕊试液变红色说明其水溶液显酸性,加热时红色消失说明加热过程中,维生素C因分解而消失;碱性条件下,维生素C易被氧化,为了防止其氧化,可在烧煮时加一点食醋。
答案:(1)蛋白质 油脂 锌
(2)不要高温加热 食醋
16.(12分)下图是某橙汁饮料标签上的部分内容:
(1)除配料中涉及的营养物质外,人体必需的营养物质还有________、______。
(2)该饮料的pH_____7(选填“大于”、“小于”或“等于”)。
(3)如何检验一种无色溶液是否具有酸性?请设计两种实验方案:
方案一:实验步骤_______________________;
实验现象_______________________________;
结论___________________________________。
方案二:实验步骤_______________________;
实验现象_______________________________;
结论___________________________________。
【解析】在人体所需的六种营养素中,该饮料中含有水、无机盐、糖类、维生素;缺少蛋白质和油脂。该饮料中含有柠檬酸,所以显酸性,pH小于7。要验证溶液显酸性,需在溶液中加入某种物质,使其产生明显的现象,以证明溶液具有酸性。
答案:(1)蛋白质 油脂(2)小于
(3)方案一:取少量该溶液置于试管中,向其中滴加几滴紫色石蕊试液 石蕊试液变红色 证明该溶液具有酸性 方案二:取少量该溶液置于试管中,向其中滴加碳酸钠溶液 有气泡产生 证明该溶液具有酸性(答案合理即可)
四、分析与计算(本题包括2个小题,共16分)
17.(4分)自从三鹿奶制品被查之后,我国许多的食品
行业被查出三聚氰胺超标。三聚氰胺对人体有害。牛奶
和奶粉等添加三聚氰胺(C3N6H6)以提高氮的含量的做法
是违法的。三聚氰胺中氮元素的质量分数为__(精确到
0.1%)。它可由以下反应制取:6CO(NH2)2 一定条件C3N6H6+6X+3CO2则X的化学式为___________________。
人体除必需的蛋白质、无机盐和水外,还必需的营养素
有______________________。
=======
【解析】三聚氰胺中氮元素的质量分数为: ×100%
=66.7%,根据化学反应前后元素种类和原子数目不变,
可以确定X的化学式为NH3,人体的营养素有:蛋白质、
糖类、油脂、维生素、无机盐和水六种,除蛋白质、无
机盐和水外,还应有糖类、油脂、维生素。
答案:66.7% NH3 糖类、油脂、维生素
18.(12分)为了测定某牛奶中蛋白质的含量,现采用“盖尔达法”分解其中的蛋白质。其原理是把蛋白质中的氮元素完全转化为氨气(NH3),再用稀硫酸吸收氨气,反应的化学方程式为:2NH3+H2SO4====(NH4)2SO4
现取该牛奶样品30 mL,用“盖尔达法”分解其中的蛋白质,产生的氨气用9.5 g溶质质量分数为4.9%的稀硫酸恰好完全吸收。计算并回答下列问题:
(1)产生氨气的质量是多少克?(计算结果精确到0.01,下同)
(2)30 mL牛奶中含氮元素的质量是多少克?
(3)如图所示为该牛奶包装标签上的部分内容。已知牛奶中的蛋白质含氮元素的质量分数为16%,请你通过计算确定,该牛奶中蛋白质的含量是否达到了包装标签所示的蛋白质的标准。
【解析】(1)在化学方程式:2NH3+H2SO4====(NH4)2SO4中已知硫酸的质量可以求出氨气的质量。
(2)先求出氨气中氮元素的质量分数,因为一个氨气分子中只有一个氮原子,所以30 mL牛奶中含氮元素的质量就可以由氨气的质量乘以氮元素的质量分数求得。
(3)用牛奶中含氮元素的质量求出含蛋白质的质量,再求出100 mL牛奶中蛋白质的含量。与标签比较,有没有达到质量标准。
答案:(1)解:设产生氨气的质量为x
2NH3+H2SO4====(NH4)2SO4
34 98
x 9.5 g×4.9%
x=0.16 g
答:产生氨气的质量为0.16 g。
(2)30 mL牛奶中含氮元素的质量:
×0.16 g=0.13 g
(3)30 mL牛奶中含蛋白质的质量:
=0.81 g
100 mL牛奶中含蛋白质的质量:
0.81 g× =2.70 g
因为2.70 g<2.90 g,故蛋白质的质量没有达到质量标准。
第四单元 化学与健康
(45分钟 100分)
可能用到的相对原子质量:H-1 C-12 N-14
O-16 S-32
一、选择题(本题包括10个小题,每小题3分,共30分)
1.医生建议患甲状腺肿大的病人多食海带等海产品,这是因为海带中含有较丰富的( )
A.氟元素 B.碘元素 C.锌元素 D.钙元素
【解析】选B。缺乏碘元素易患甲状腺肿大,海带中含有丰富的碘元素。
2.将下列物质加入蛋白质试液中,不会使蛋白质失去原有生理功能的是( )
A.甲醛 B.硫酸钠溶液
C.乙酸铅溶液 D.浓硝酸
【解析】选B。能使蛋白质失去生理活性的物质包含:重金属盐、甲醛、浓硝酸等物质,在加热的条件下也能使蛋白质失去生理活性,硫酸钠不属于重金属盐,不能使蛋白质失去生理活性,故选B。
3.某品牌妙脆角的主要配料如下:
大米粉、食用植物油、白砂糖、食
用盐、抗氧化剂、牛奶和大豆。
判断这种食品中不含哪种营养
素( )
A.糖类 B.油脂
C.蛋白质 D.维生素
【解析】选D。从某品牌妙脆角的配料成分可知:大米粉中富含淀粉,淀粉属于糖类物质;食用植物油中富含油脂;牛奶和大豆中富含蛋白质;不含有维生素。故选D。
4.微量元素在人体内的质量总和不到人体质量的千分之一,但这些元素对人体的正常发育和健康起着重要的作用。下列各元素全部属于人体中微量元素的是( )
A.Na Cl O B.H O N
C.N Ca C D.I Fe Zn
【解析】选D。根据元素含量的分类:其含量小于0.01%的元素为微量元素,其含量大于0.01%的称为常量元素,其中氧元素为65%,碳元素为18%,氮元素为3%,都不是微量元素,故A、B、C错误。
5.人体成长所需的蛋白质,有些必须在食物中才能获取。那么人体通过食物获取蛋白质的主要作用是( )
A.与水发生一系列反应,最终变成葡萄糖
B.在肠胃里与水发生反应,生成氨基酸
C.调节新陈代谢、预防疾病
D.维持恒定体温、提供能量
【解析】选B。食物中的蛋白质进入人体后,在蛋白酶和水的作用下,逐步分解成可被人体吸收的氨基酸,其中一部分重新组合成人体所需的各种蛋白质,另一部分排出体外。
6.下列几种物品都是日常生活中常见的食物,其中富含糖类的食品是( )
A.①③ B.①④ C.②④ D.①②
【解析】选D。本题主要考查人体中所需的营养素在哪些食品中含量较多,其中玉米和大米中富含淀粉,淀粉属于糖类物质,豆油中富含油脂;鱼中富含蛋白质,故选D。
7.(2009·南通中考)下面是4位同学对“化学与健康”这一话题发表的见解,其中正确的是( )
【解析】选B。霉变食物中含有致癌作用的黄曲霉素,对健康非常有害,故不能食用。
8.日常生活中有很多错误的做法在威胁着我们的身体健康。请考虑下列做法不会危及我们健康的是( )
A.把霉变大米淘净后继续食用
B.用甲醛水溶液浸泡水产品
C.根据医嘱适量服用补钙剂
D.变质的剩饭加热后再吃
【解析】选C。霉变的食物,受到菌类的污染,对身体造成多种危害,不能继续食用,故A、D的做法不正确;甲醛属于有毒物质,能使蛋白质失去生理活性,故B的做法不正确;微量元素对人体的成长十分的重要,如果食品中不能提供足量的微量元素,就可通过药品或保健品来适量补充。故选C。
9.(2009·鄂州中考)小明同学出现了腹泻的症状,医生建议他暂时不要吃富含蛋白质和油脂的食物。小明同学应该选择的早餐是( )
A.馒头和稀饭 B.鸡蛋和牛奶
C.油条和豆浆 D.肯德基和酸奶
【解析】选A。鸡蛋、牛奶、豆浆、酸奶中富含蛋白质,油条和肯德基中富含油脂。馒头和稀饭中富含淀粉等糖类物质,可以作为早餐。
10.某2.3 g有机化合物跟4.8 g氧气恰好完全燃烧,生成4.4 g二氧化碳和2.7 g水,则该有机物的化学式
为( )
A.CH4 B.C2H2 C.C2H6O D.C2H4O2
【解析】选C。根据质量守恒可知:反应前后同一种元
素的质量不变。可求出4.4 g二氧化碳中含有碳元素
1.2 g,2.7 g水中含氢元素0.3 g,由此可知有机物中
含氧元素的质量为:2.3 g-1.2 g-0.3 g=0.8 g。则有
机物中碳、氢、氧三种元素原子个数比为:
=2∶6∶1。即化学式为C2H6O。
二、理解与应用(本题包括4个小题,共30分)
11.(8分)下面的方框内是某食品包装上的部分说明,请从其中标出的配料中选出一种符合条件的物质填在下列相应的空格中:
(1)____________________中富含蛋白质;
(2)___________________中富含油脂;
(3)___________________属于维生素;
(4)____________________属于无机盐。
【解析】本题将课本知识与生活实际有机地结合起来,利于学生正确的识别各食品中所含的营养素。由食品的配料可知:小麦粉、麦芽糖中富含糖类;食用植物油中富含油脂;食用盐、碳酸钙、焦亚硫酸钠中主要成分为无机盐;鸡全蛋粉、全脂奶粉中富含蛋白质;维生素D属于维生素。
答案:(1)鸡全蛋粉、全脂奶粉 (2)食用植物油
(3)维生素D (4)食用盐、碳酸钙、焦亚硫酸钠
12.(6分)下表是豆腐中一些成分的平均质量分数:
除水和无机盐外,豆腐中含有的营养素还有_______,含人体所需的微量元素是________。若成年人每天食用80 g豆腐,则摄入铁的质量为_______g。
【解析】由豆腐的成分可知:豆腐中含有人体所需的六种营养素(水、无机盐、糖类、蛋白质、油脂、维生素)。元素在人体中含量在0.01%以下的为微量元素,如铁、锌、碘、硒等。成年人每天摄入铁的质量为:
80 g×1.4%=1.12 g。
答案:糖类、蛋白质、油脂、维生素 铁 1.12
13.(8分)古人云:“民以食为天”,人们一日三餐的主食多为淀粉类食品,如米饭、面包等。食物中的淀粉[(C5H10O5)n]在人体内不能直接被吸收利用,而是在淀粉酶和水的作用下转化为葡萄糖(C6H12O6),并溶解在血液中,提供营养和能量。试根据题意回答下列问题:
(1)淀粉属于_____(填“无机物”或“有机物”)。
(2)葡萄糖分子中碳、氢、氧的原子个数之比为____
(最简整数比)。葡萄糖在人体内发生如下化学反应:C6H12O6+6O2====6CO2+6H2O,该反应的类型属于__反应。
(3)欲检验某食物中是否含有淀粉,下列试剂中,最宜选用的是_____(填序号)。
A.石蕊试液 B.碳酸钠溶液 C.稀盐酸
D.碘水 E.氢氧化钠溶液
【解析】淀粉属于有机物中的糖类物质;葡萄糖的化学式为:C6H12O6,则可知其原子个数比为:1∶2∶1;物质与氧气发生的反应属于氧化反应;检验某种物质中是否含有淀粉,我们常用碘水。
答案:(1)有机物 (2)1∶2∶1 氧化 (3)D
14.(8分)(2009·乌鲁木齐中考)在人的胃液中,盐酸(HCl)的质量分数大约是0.45%~0.6%。它具有以下生理功能:①促进胃蛋白酶的催化作用,使蛋白质水解而被人体吸收;②使糖类物质进一步水解;③杀菌。
请结合上述内容回答下列问题:
(1)如果用Al(OH)3的混合剂治疗胃酸过多,则发生反应的化学方程式为________。
(2)人类食用适量的NaCl有利于________。
A.促进盐酸产生
B.帮助消化和增进食欲
C.治疗胃酸过多
D.治疗缺碘性甲状腺肿大
(3)糖类、____、油脂、维生素、无机盐和水是人体的六大营养物质。在这六大营养物质中,不经过消化,就可以在消化道内直接被人体吸收的有____。
【解析】(1)注意方程式的配平;(2)依据题中所给资料可知:NaCl被摄入人体后,其中的Cl在酶的作用下利于HCl的形成,NaCl作为调味品能增加人们的食欲。(3)属于识记内容。
答案:(1)Al(OH)3+3HCl====AlCl3+3H2O
(2)A、B
(3)蛋白质 维生素、无机盐和水
三、实验与探究(本题包括2个小题,共24分)
15.(12分)化学可以帮助人类认识改造周围的世界,促进社会发展。糖类、油脂、蛋白质和维生素都是人类的基本营养物质。下表为某品牌燕麦片标签中的一部分。
(1)燕麦片的营养成分中能与水反应生成氨基酸的营养物质是______;每克营养物质氧化时放出能量最多的是________;人体必需的微量元素是______。
(2)维生素C易溶于水,向其水溶液中滴入紫色石蕊试液,石蕊变红色,加热该溶液至沸腾,红色消失。因此,烹调富含维生素C的食物时,应该注意________;在碱性条件下,维生素C易被空气氧化,烧煮时最好加一点_____________。
【解析】蛋白质摄入人体后在水与酶的作用下生成人体必需的氨基酸,油脂氧化放出的能量为糖类的2倍还要多,人体中必需的微量元素为铁、锌、碘、硒等,维生素C的水溶液能使石蕊试液变红色说明其水溶液显酸性,加热时红色消失说明加热过程中,维生素C因分解而消失;碱性条件下,维生素C易被氧化,为了防止其氧化,可在烧煮时加一点食醋。
答案:(1)蛋白质 油脂 锌
(2)不要高温加热 食醋
16.(12分)下图是某橙汁饮料标签上的部分内容:
(1)除配料中涉及的营养物质外,人体必需的营养物质还有________、______。
(2)该饮料的pH_____7(选填“大于”、“小于”或“等于”)。
(3)如何检验一种无色溶液是否具有酸性?请设计两种实验方案:
方案一:实验步骤_______________________;
实验现象_______________________________;
结论___________________________________。
方案二:实验步骤_______________________;
实验现象_______________________________;
结论___________________________________。
【解析】在人体所需的六种营养素中,该饮料中含有水、无机盐、糖类、维生素;缺少蛋白质和油脂。该饮料中含有柠檬酸,所以显酸性,pH小于7。要验证溶液显酸性,需在溶液中加入某种物质,使其产生明显的现象,以证明溶液具有酸性。
答案:(1)蛋白质 油脂(2)小于
(3)方案一:取少量该溶液置于试管中,向其中滴加几滴紫色石蕊试液 石蕊试液变红色 证明该溶液具有酸性 方案二:取少量该溶液置于试管中,向其中滴加碳酸钠溶液 有气泡产生 证明该溶液具有酸性(答案合理即可)
四、分析与计算(本题包括2个小题,共16分)
17.(4分)自从三鹿奶制品被查之后,我国许多的食品
行业被查出三聚氰胺超标。三聚氰胺对人体有害。牛奶
和奶粉等添加三聚氰胺(C3N6H6)以提高氮的含量的做法
是违法的。三聚氰胺中氮元素的质量分数为__(精确到
0.1%)。它可由以下反应制取:6CO(NH2)2 一定条件C3N6H6+6X+3CO2则X的化学式为___________________。
人体除必需的蛋白质、无机盐和水外,还必需的营养素
有______________________。
=======
【解析】三聚氰胺中氮元素的质量分数为: ×100%
=66.7%,根据化学反应前后元素种类和原子数目不变,
可以确定X的化学式为NH3,人体的营养素有:蛋白质、
糖类、油脂、维生素、无机盐和水六种,除蛋白质、无
机盐和水外,还应有糖类、油脂、维生素。
答案:66.7% NH3 糖类、油脂、维生素
18.(12分)为了测定某牛奶中蛋白质的含量,现采用“盖尔达法”分解其中的蛋白质。其原理是把蛋白质中的氮元素完全转化为氨气(NH3),再用稀硫酸吸收氨气,反应的化学方程式为:2NH3+H2SO4====(NH4)2SO4
现取该牛奶样品30 mL,用“盖尔达法”分解其中的蛋白质,产生的氨气用9.5 g溶质质量分数为4.9%的稀硫酸恰好完全吸收。计算并回答下列问题:
(1)产生氨气的质量是多少克?(计算结果精确到0.01,下同)
(2)30 mL牛奶中含氮元素的质量是多少克?
(3)如图所示为该牛奶包装标签上的部分内容。已知牛奶中的蛋白质含氮元素的质量分数为16%,请你通过计算确定,该牛奶中蛋白质的含量是否达到了包装标签所示的蛋白质的标准。
【解析】(1)在化学方程式:2NH3+H2SO4====(NH4)2SO4中已知硫酸的质量可以求出氨气的质量。
(2)先求出氨气中氮元素的质量分数,因为一个氨气分子中只有一个氮原子,所以30 mL牛奶中含氮元素的质量就可以由氨气的质量乘以氮元素的质量分数求得。
(3)用牛奶中含氮元素的质量求出含蛋白质的质量,再求出100 mL牛奶中蛋白质的含量。与标签比较,有没有达到质量标准。
答案:(1)解:设产生氨气的质量为x
2NH3+H2SO4====(NH4)2SO4
34 98
x 9.5 g×4.9%
x=0.16 g
答:产生氨气的质量为0.16 g。
(2)30 mL牛奶中含氮元素的质量:
×0.16 g=0.13 g
(3)30 mL牛奶中含蛋白质的质量:
=0.81 g
100 mL牛奶中含蛋白质的质量:
0.81 g× =2.70 g
因为2.70 g<2.90 g,故蛋白质的质量没有达到质量标准。
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
