浙教版科学九年级上册章节检测 2.5 物质的转化 第2课时 金属的冶炼【含答案】
文档属性
| 名称 | 浙教版科学九年级上册章节检测 2.5 物质的转化 第2课时 金属的冶炼【含答案】 |

|
|
| 格式 | doc | ||
| 文件大小 | 217.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2020-12-04 00:00:00 | ||
图片预览


文档简介
2.5 物质的转化 第2课时 金属的冶炼
满分85分
一、单选(本部分共有7道题,共21分)
1.?(3分)炼铁高炉中发生了下列反应:①高温下一氧化碳将铁矿石还原为铁;②高温煅烧石灰石;③灼热的焦炭和二氧化碳反应;④焦炭充分燃烧。其中属于化合反应的是(??? )
? A.?①和④ B.?②和③ C.?③和④ D.?只有④
2.?(3分)在反应CuO+H2=ΔCu+H2O中,属于还原剂的是(??? )
A.?CuO B.?H2 C.?Cu D.?H2O
3.?(3分)下列有关工业炼铁的叙述中,不正确的是(??? )
? A.?炼铁用的设备是高炉
? B.?炼铁的原料是焦炭、石灰石、铁矿石
? C.?炼铁得到的生铁仍为混合物
D.?炼铁是用空气中的氧气将铁矿石中的杂质氧化除去
4.?(3分)实验室用氢气还原氧化铜的实验步骤如下:①向试管里通氢气? ②检验氢气纯度? ③给盛有氧化铜的试管加热? ④停止加热? ⑤继续通氢气直到试管冷却。其正确的操作顺序是(??? )
? A.?①②③④⑤ B.?②①③④⑤ C.?②①③⑤④ D.?②③①④⑤
5.?(3分)通过对反应2CuO+C=高温2Cu+CO2↑;CuO+CO=ΔCu+CO2↑的比较分析,小丁同学得出了如下结论。你认为其中说法有错误的是(??? )
? A.?C和CO都具有还原性
? B.?反应中CuO都提供了氧,具有氧化性
C.?两个反应的基本类型相同
? D.?两个反应所需的能量不同
6.?(3分)用“W”形玻璃管进行微型实验,如图所示;下列说法不正确的是(??? )
? A.?a处红棕色粉末变为黑色
B.?a处的反应为CO+Fe2O3=2Fe+CO2
? C.?b处澄清石灰水变浑浊证明有CO2生成
? D.?可利用点燃的方法进行尾气处理
7.?(3分)如图是实验室炼铁的过程中,通人CO质量与红色粉末质量的关系。根据图示,下列说法不正确的是(??? )
? A.?b点表示通入CO一段时间后加热,反应开始发生
? B.?c点表示红色粉末已充分参加反应
C.?可根据通入CO的质量计算出红色粉末的质量
? D.?d点表示反应结束后仍需继续通入CO
二、填空(本部分共有2道题,共12分)
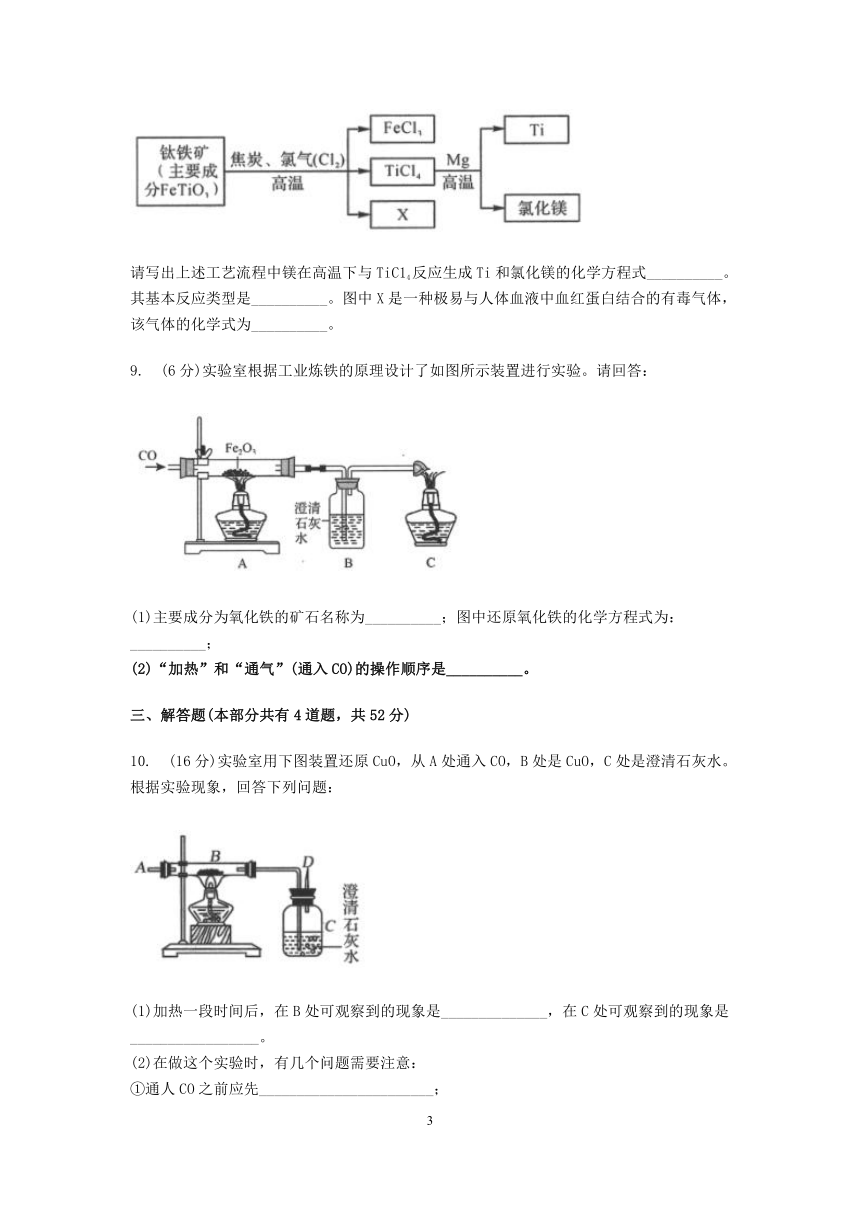
8.?(6分)钛因其密度小,熔点高,常温下耐酸碱、耐腐蚀等优良性能,被誉为“未来金属”。工业上以钛铁矿(主要成分为FeTiO3)为原料生产钛,其主要工艺流程如图所示:
请写出上述工艺流程中镁在高温下与TiC14反应生成Ti和氯化镁的化学方程式__________。其基本反应类型是__________。图中X是一种极易与人体血液中血红蛋白结合的有毒气体,该气体的化学式为__________。
9.?(6分)实验室根据工业炼铁的原理设计了如图所示装置进行实验。请回答:
(1)主要成分为氧化铁的矿石名称为__________;图中还原氧化铁的化学方程式为:__________;
(2)“加热”和“通气”(通入CO)的操作顺序是__________。
三、解答题(本部分共有4道题,共52分)
10.?(16分)实验室用下图装置还原CuO,从A处通入CO,B处是CuO,C处是澄清石灰水。根据实验现象,回答下列问题:
(1)加热一段时间后,在B处可观察到的现象是______________,在C处可观察到的现象是_________________。
(2)在做这个实验时,有几个问题需要注意:
①通人CO之前应先_______________________;
②应先_____________,再给试管_____________,以免_____________;
③D处排出的气体不能直接排放到空气中,应_____________,以免_____________。
11.?(8分)高炉冶铁工艺流程如图所示。
回答下列问题:
(1)该工艺流程中,甲烷的作用是_________,冶炼出的铁水属于_________(填“纯净物”或“混合物”)。
(2)用化学方程式表示还原反应室内炼铁的原理_____________________。(写一个)
(3)该工艺流程中,可循环利用的物质是______________。
12.?(14分)已知碱式碳酸铜[Cu2(OH)2CO3]受热易分解,能与酸反应。孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物。某校化学研究小组以孔雀石为原料制备CuSO4·5H2O的流程如下图:
请回答下列问题:
(1)流程中,X的化学式是______________;由溶液B获得CuSO4·5H2O,需要经过加热蒸发、______________、过滤等操作。
(2)若通过置换反应由溶液B制备金属铜,反应的化学方程式是____________________。若选用下列物质与氧化铜反应制备铜,写出反应的化学方程式:
①选用非金属单质________________;②选用氧化物________________。
(3)工业上用焦炭在高温电炉中还原SiO2可得到含有少量杂质的Si和CO,反应的化学方程式是________________,反应类型为________________。
13.?(14分)某实验小组同学用加热草酸晶体制得CO,并利用CO来完成炼铁实验,请你参与实验并回答下列问题。
【查阅资料】
(1)实验室常用氢氧化钠溶液除去二氧化碳,用澄清石灰水检验二氧化碳。
(2)草酸晶体(H2C204·3H20)在浓硫酸作用下受热分解,化学方程式为H2C2O4·3H20
【问题讨论】
(1)实验室提供下列仪器供选择使用:①试管②烧杯③集气瓶④蒸发皿⑤酒精灯⑥带导管的橡皮塞⑦铁架台(含铁夹)。其中你认为在加热分解草酸晶体的装置中,需要用到的仪器有_________。(填序号)
(2)进入D装置的气体是纯净、干燥的CO,则A、C装置中的试剂依次是______________________。
(3)写出A装置中发生反应的化学方程式__________________。
(4)B装置的作用是__________________________。
(5)证明草酸晶体分解产物中存在CO的现象是__________________。
【实验评价】
请指出上述实验装置的一个明显缺陷__________________。
参考答案
满分85分
一、单选(本部分共有7道题,共21分)
1.?(3分)B
2.?(3分)A
3.?(3分)D
4.?(3分)B
5.?(3分)C
6.?(3分)B
7.?(3分)C
二、填空(本部分共有2道题,共12分)
8.?(6分)2Mg+TiCl2=点燃2MgCl2+Ti;置换反应;CO
9.?(6分)(1)赤铁矿;3CO+Fe2O3=高温2Fe+3CO2 (2)先通气后加热
三、解答题(本部分共有4道题,共52分)
10.?(16分)(1)黑色粉末变红;澄清石灰水变浑浊(2)①检验CO的纯度;②通入CO;加热;加热不纯的CO气体引起爆炸;③点燃处理;污染空气
11.?(8分)(1)燃烧产生热量、做生产合成气的原料;混合物(2)3CO+Fe2O3=高温2Fe+3CO2或3H2+Fe2O3=高温2Fe+3H2O(3)CO2和H2O
12.?(14分)(1)H2SO4;冷却结晶或结晶(2)CuSO4+Fe==FeSO4+Cu①2CuO+C=高温2Cu+CO2↑或CuO+H2=Cu+H2O②CuO+CO=Cu+CO2(3)SiO2+2C=Si+2CO↑;置换反应
13.?(14分)(1)①⑤⑥⑦(2)氢氧化钠溶液;浓硫酸(3)2NaOH+CO2==Na2CO3+H2O(4)检验一氧化碳中是否含有二氧化碳(5)D装置中的红色粉末慢慢变成黑色[实验评价]没有尾气处理装置
满分85分
一、单选(本部分共有7道题,共21分)
1.?(3分)炼铁高炉中发生了下列反应:①高温下一氧化碳将铁矿石还原为铁;②高温煅烧石灰石;③灼热的焦炭和二氧化碳反应;④焦炭充分燃烧。其中属于化合反应的是(??? )
? A.?①和④ B.?②和③ C.?③和④ D.?只有④
2.?(3分)在反应CuO+H2=ΔCu+H2O中,属于还原剂的是(??? )
A.?CuO B.?H2 C.?Cu D.?H2O
3.?(3分)下列有关工业炼铁的叙述中,不正确的是(??? )
? A.?炼铁用的设备是高炉
? B.?炼铁的原料是焦炭、石灰石、铁矿石
? C.?炼铁得到的生铁仍为混合物
D.?炼铁是用空气中的氧气将铁矿石中的杂质氧化除去
4.?(3分)实验室用氢气还原氧化铜的实验步骤如下:①向试管里通氢气? ②检验氢气纯度? ③给盛有氧化铜的试管加热? ④停止加热? ⑤继续通氢气直到试管冷却。其正确的操作顺序是(??? )
? A.?①②③④⑤ B.?②①③④⑤ C.?②①③⑤④ D.?②③①④⑤
5.?(3分)通过对反应2CuO+C=高温2Cu+CO2↑;CuO+CO=ΔCu+CO2↑的比较分析,小丁同学得出了如下结论。你认为其中说法有错误的是(??? )
? A.?C和CO都具有还原性
? B.?反应中CuO都提供了氧,具有氧化性
C.?两个反应的基本类型相同
? D.?两个反应所需的能量不同
6.?(3分)用“W”形玻璃管进行微型实验,如图所示;下列说法不正确的是(??? )
? A.?a处红棕色粉末变为黑色
B.?a处的反应为CO+Fe2O3=2Fe+CO2
? C.?b处澄清石灰水变浑浊证明有CO2生成
? D.?可利用点燃的方法进行尾气处理
7.?(3分)如图是实验室炼铁的过程中,通人CO质量与红色粉末质量的关系。根据图示,下列说法不正确的是(??? )
? A.?b点表示通入CO一段时间后加热,反应开始发生
? B.?c点表示红色粉末已充分参加反应
C.?可根据通入CO的质量计算出红色粉末的质量
? D.?d点表示反应结束后仍需继续通入CO
二、填空(本部分共有2道题,共12分)
8.?(6分)钛因其密度小,熔点高,常温下耐酸碱、耐腐蚀等优良性能,被誉为“未来金属”。工业上以钛铁矿(主要成分为FeTiO3)为原料生产钛,其主要工艺流程如图所示:
请写出上述工艺流程中镁在高温下与TiC14反应生成Ti和氯化镁的化学方程式__________。其基本反应类型是__________。图中X是一种极易与人体血液中血红蛋白结合的有毒气体,该气体的化学式为__________。
9.?(6分)实验室根据工业炼铁的原理设计了如图所示装置进行实验。请回答:
(1)主要成分为氧化铁的矿石名称为__________;图中还原氧化铁的化学方程式为:__________;
(2)“加热”和“通气”(通入CO)的操作顺序是__________。
三、解答题(本部分共有4道题,共52分)
10.?(16分)实验室用下图装置还原CuO,从A处通入CO,B处是CuO,C处是澄清石灰水。根据实验现象,回答下列问题:
(1)加热一段时间后,在B处可观察到的现象是______________,在C处可观察到的现象是_________________。
(2)在做这个实验时,有几个问题需要注意:
①通人CO之前应先_______________________;
②应先_____________,再给试管_____________,以免_____________;
③D处排出的气体不能直接排放到空气中,应_____________,以免_____________。
11.?(8分)高炉冶铁工艺流程如图所示。
回答下列问题:
(1)该工艺流程中,甲烷的作用是_________,冶炼出的铁水属于_________(填“纯净物”或“混合物”)。
(2)用化学方程式表示还原反应室内炼铁的原理_____________________。(写一个)
(3)该工艺流程中,可循环利用的物质是______________。
12.?(14分)已知碱式碳酸铜[Cu2(OH)2CO3]受热易分解,能与酸反应。孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物。某校化学研究小组以孔雀石为原料制备CuSO4·5H2O的流程如下图:
请回答下列问题:
(1)流程中,X的化学式是______________;由溶液B获得CuSO4·5H2O,需要经过加热蒸发、______________、过滤等操作。
(2)若通过置换反应由溶液B制备金属铜,反应的化学方程式是____________________。若选用下列物质与氧化铜反应制备铜,写出反应的化学方程式:
①选用非金属单质________________;②选用氧化物________________。
(3)工业上用焦炭在高温电炉中还原SiO2可得到含有少量杂质的Si和CO,反应的化学方程式是________________,反应类型为________________。
13.?(14分)某实验小组同学用加热草酸晶体制得CO,并利用CO来完成炼铁实验,请你参与实验并回答下列问题。
【查阅资料】
(1)实验室常用氢氧化钠溶液除去二氧化碳,用澄清石灰水检验二氧化碳。
(2)草酸晶体(H2C204·3H20)在浓硫酸作用下受热分解,化学方程式为H2C2O4·3H20
【问题讨论】
(1)实验室提供下列仪器供选择使用:①试管②烧杯③集气瓶④蒸发皿⑤酒精灯⑥带导管的橡皮塞⑦铁架台(含铁夹)。其中你认为在加热分解草酸晶体的装置中,需要用到的仪器有_________。(填序号)
(2)进入D装置的气体是纯净、干燥的CO,则A、C装置中的试剂依次是______________________。
(3)写出A装置中发生反应的化学方程式__________________。
(4)B装置的作用是__________________________。
(5)证明草酸晶体分解产物中存在CO的现象是__________________。
【实验评价】
请指出上述实验装置的一个明显缺陷__________________。
参考答案
满分85分
一、单选(本部分共有7道题,共21分)
1.?(3分)B
2.?(3分)A
3.?(3分)D
4.?(3分)B
5.?(3分)C
6.?(3分)B
7.?(3分)C
二、填空(本部分共有2道题,共12分)
8.?(6分)2Mg+TiCl2=点燃2MgCl2+Ti;置换反应;CO
9.?(6分)(1)赤铁矿;3CO+Fe2O3=高温2Fe+3CO2 (2)先通气后加热
三、解答题(本部分共有4道题,共52分)
10.?(16分)(1)黑色粉末变红;澄清石灰水变浑浊(2)①检验CO的纯度;②通入CO;加热;加热不纯的CO气体引起爆炸;③点燃处理;污染空气
11.?(8分)(1)燃烧产生热量、做生产合成气的原料;混合物(2)3CO+Fe2O3=高温2Fe+3CO2或3H2+Fe2O3=高温2Fe+3H2O(3)CO2和H2O
12.?(14分)(1)H2SO4;冷却结晶或结晶(2)CuSO4+Fe==FeSO4+Cu①2CuO+C=高温2Cu+CO2↑或CuO+H2=Cu+H2O②CuO+CO=Cu+CO2(3)SiO2+2C=Si+2CO↑;置换反应
13.?(14分)(1)①⑤⑥⑦(2)氢氧化钠溶液;浓硫酸(3)2NaOH+CO2==Na2CO3+H2O(4)检验一氧化碳中是否含有二氧化碳(5)D装置中的红色粉末慢慢变成黑色[实验评价]没有尾气处理装置
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
