黑龙江省哈尔滨市第三十二中学2020-2021学年高二上学期期中考试化学试题 含答案
文档属性
| 名称 | 黑龙江省哈尔滨市第三十二中学2020-2021学年高二上学期期中考试化学试题 含答案 |

|
|
| 格式 | doc | ||
| 文件大小 | 225.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-12-05 00:00:00 | ||
图片预览

文档简介
哈32中2020~2021学年高二上学期期中考试
化学试卷
(考试范围:必修一、必修二 适用班级:高二学年)
可能用到的相对原子质量: H-1 C-12 N-14 O-16 Na-23 C1-35.5 S-32 Cu-64
一、选择题(每小题只有1个选项符合题意,每小题2分,共60分)
1.下列资源的开发利用过程中,只发生物理变化的是
A.石油分馏 B.石油裂化 C.高炉炼铁 D.从海水中提取镁
2.根据物质的组成与性质进行分类,HClO 属于
A.氧化物 B.酸 C.碱 D.盐
3.铝的核素中的“27”表示的是
A.质量数 B.质子数 C.中子数 D.电子数
4.当光束通过下列分散系时,可能产生丁达尔效应的是
A.泥浆 B.稀盐酸 C. NaCl 溶液 D.氢氧化铝胶体
5.实验室制取下列气体时,不能用排空气法收集的是
A. H2 B. CH4 C. NO D. NO2
6.、下列变化必须加入还原剂才能发生的是
A. CO2→CO B. NH3→NO
C. SO2→H2SO3 D. CuO→CuCl2
7.下列物质中,能作为制备木材防火剂原料的是
A.硅酸钠 B.氢氟酸 C.碳酸钠 D.漂白粉
8.下列仪器名称错误的是
A.酒精灯 B.圆底烧瓶
C.量筒 D.烧杯
9.在含有大量Na+、HCO3—、Cl—的溶液中,还可能大量存在的离子是
A. Ag+ B. OH— C. NO3— D. H+
10.工业上常用电解法冶炼活泼金属。下列金属使用电解法冶炼的是
A.钠 B.铁 C.铜 D.金
11.分别灼烧下列各组溶液,火焰呈黄色是
A. NaCl溶液 B.稀盐酸 C. K2CO3 溶液 D. CuCl2 溶液
12.下列物质互为同分异构体的一组是
A.和 B.白磷和红磷
C. CH3CH2OH 和CH3OCH3 D. CH4和C2H6
13.下列化学用语表示正确的是
A.乙醇的结构式:C2H6O B.氯化氢的电子式:
C. Mg2+的结构示意图: D. CaCl2的电离方程式:CaCl2=Ca2++ Cl22-
14. 下列物质中,属于共价化合物的是
A. MgCl2 B. CO2 C.H2 D. NaOH
15.下列因素能减慢H2O2溶液分解反应速率的是
A.加入MnO2 B.降低温度 C.升高温度 D.增大H2O2的浓度
16.用NA表示阿伏加德罗常数的值,下列说法正确的是
A. CO的摩尔质量是28 g
B.常温常压下,1 mol N2的体积是22.4 L
C.18 g H2O中含有的氢原子总数为2NA
D.0.1 mol/L Na2SO4溶液中,Na+的物质的量浓度为0.1 mol/L
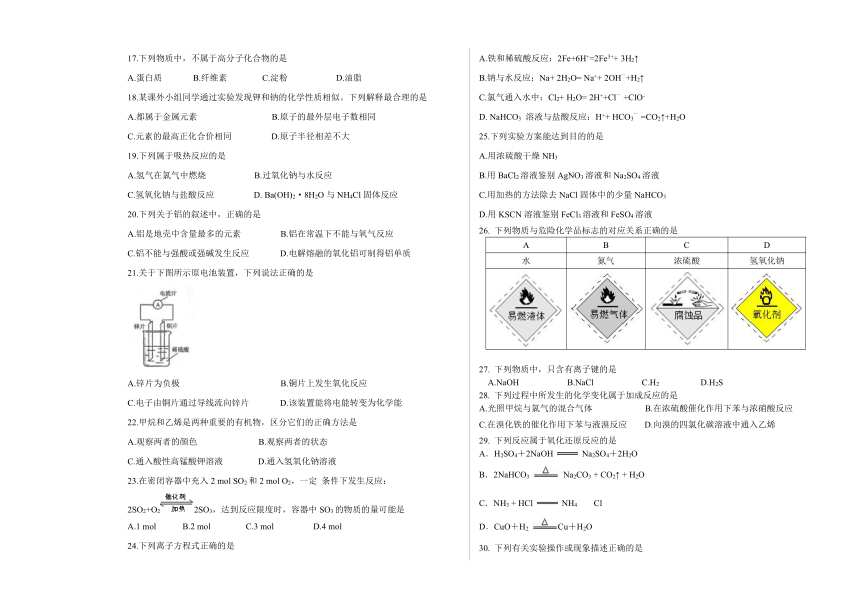
17.下列物质中,不属于高分子化合物的是
A.蛋白质 B.纤维素 C.淀粉 D.油脂
18.某课外小组同学通过实验发现钾和钠的化学性质相似。下列解释最合理的是
A.都属于金属元素 B.原子的最外层电子数相同
C.元素的最高正化合价相同 D.原子半径相差不大
19.下列属于吸热反应的是
A.氢气在氯气中燃烧 B.过氧化钠与水反应
C.氢氧化钠与盐酸反应 D. Ba(OH)2·8H2O与NH4Cl固体反应
20.下列关于铝的叙述中,正确的是
A.铝是地壳中含量最多的元素 B.铝在常温下不能与氧气反应
C.铝不能与强酸或强碱发生反应 D.电解熔融的氧化铝可制得铝单质
21.关于下图所示原电池装置,下列说法正确的是
A.锌片为负极 B.铜片上发生氧化反应
C.电子由铜片通过导线流向锌片 D.该装置能将电能转变为化学能
22.甲烷和乙烯是两种重要的有机物,区分它们的正确方法是
A.观察两者的颜色 B.观察两者的状态
C.通入酸性高锰酸钾溶液 D.通入氢氧化钠溶液
23.在密闭容器中充入2 mol SO2和2 mol O2,一定 条件下发生反应:2SO2+O22SO3,达到反应限度时,容器中SO3的物质的量可能是
A.1 mol B.2 mol C.3 mol D.4 mol
24.下列离子方程式正确的是
A.铁和稀硫酸反应:2Fe+6H+=2Fe3++ 3H2↑
B.钠与水反应:Na+ 2H2O= Na++ 2OH—+H2↑
C.氯气通入水中:Cl2+ H2O= 2H++Cl— +ClO-
D. NaHCO3 溶液与盐酸反应:H++ HCO3— =CO2↑+H2O
25.下列实验方案能达到目的的是
A.用浓硫酸干燥NH3
B.用BaCl2溶液鉴别AgNO3溶液和Na2SO4溶液
C.用加热的方法除去NaCl固体中的少量NaHCO3
D.用KSCN溶液鉴别FeCl3溶液和FeSO4溶液
26. 下列物质与危险化学品标志的对应关系正确的是
A B C D
水 氮气 浓硫酸 氢氧化钠
27. 下列物质中,只含有离子键的是
A.NaOH???? B.NaCl???????? C.H2??????? D.H2S
28. 下列过程中所发生的化学变化属于加成反应的是
A.光照甲烷与氯气的混合气体 B.在浓硫酸催化作用下苯与浓硝酸反应
C.在溴化铁的催化作用下苯与液溴反应 D.向溴的四氯化碳溶液中通入乙烯
29. 下列反应属于氧化还原反应的是
A.H2SO4+2NaOH Na2SO4+2H2O
B.2NaHCO3 Na2CO3 + CO2↑ + H2O
C.NH3 + HCl NH4Cl
D.CuO+H2 Cu+H2O
30. 下列有关实验操作或现象描述正确的是
A.实验室用图1装置制备Cl2
B.加热后图2中溶液颜色恢复红色
C.用图3装置除去Cl2中含有的少量HCl
D.实验室用图4装置制取少量蒸馏水
二、填空题(本大题包括6小题,共40分)
31. (4分)2019年是门捷列夫发现元素周期律150周年。下表为元素周期表的一部分。
碳 W Y
X
硫 Z
回答下列问题:
(1)X元素的名称是________。?
(2)Y元素的氢化物H2Y的稳定性________(填“>”或“<”)H2S。?
(3)表中元素的最高价氧化物对应的水化物酸性最强的是___________________
(填化学式)。
(4)W元素最高价氧化物对应水化物与氢氧化钠溶液反应的化学方程式
。?
32. (4分)已知A、B、C是中学化学中常见的有机物,它们与乙烯之间有如图的转化关系(图中部分产物已略去)。
请回答下列问题:
(1)A的结构简式为____________。?
(2)反应②的反应类型为____________。?
(3)反应③的化学方程式为______________。
33.(6分)实验小组需要配制100 mL0.5 mol/L的Na2CO3溶液,同学们分工合作进行实验。
(1)甲同学需要称取Na2CO3固体的质量是_____________g。
(2)乙同学溶解Na2CO3固体时,需要用到的仪器有:量筒、烧杯和___________。
(3)丙同学的下列操作中,正确的是_____________。
A.转移液体时,不慎将溶液洒落在容量瓶外
B.液面离容量瓶颈刻度线下1~2 cm时,改用胶头滴管滴加蒸馏水
C.溶液配制完成后,长期将溶液储存在容量瓶中
(4)若在定容时俯视刻度线,则此操作导致所配Na2CO3溶液的物质的量浓度________(填“偏高”或“偏低”)。
34.(6分)研究性学习小组的同学们按下图装置进行SO2的制备及性质探究实验。
(查阅资料得到SO2气体的制备原理:Na2SO3(固)+H2SO4(浓)=Na2SO4+SO2↑+H2O),回答问题:
(1)图中a的仪器名称是_______, 亚硫酸钠应放在_________(填“a”或“b”)中。
(2)实验过程中,可以观察到装置B中品红溶液_______(填实验现象),该现象说明SO2具有_____性(填“氧化”、“还原”或“漂白”)。
(3)酸性条件下,SO2 与KMnO4在发生如下反应:5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2H2SO4,使溶液褪色。反应中SO2是________(填“氧化”、“还原”剂)。
(4)尾气可采用________溶液吸收。
35. (10分)改善生态环境、建设美丽家园是全人类共同的呼声。
(1)酸雨是指pH_______5.6 (填“>”或“<”)的降水;_______ (填“SO2”或 “N2")是形成酸雨的主要气体之一。
(2)水是生命之源,净化水中的细小悬浮颗粒时,常加入_______ (填“食盐”或 “明矾”)使其聚集成较大颗粒沉淀而与水分离。
(3)汽车尾气中的CO和NO在催化剂作用下发生反应生成CO2和N2,该反应的化学方程式为________________。
(4)“垃圾分类”成为时代新风尚,下列属于可回收标志的是________(填字母序号)。
a. b. C.
36. (10分) (1)树立健康观念,促进身心健康全面发展现有下列四种物质:
A.淀粉 B.油脂 C.氨基酸 D.阿司匹林
请回答下列问题(填字母代号):
①具有解热镇痛作用,为人们熟知的治感冒药是________;
②能在体内水解,且最终转化为葡萄糖的天然高分子化合物是________;
(2)材料是人类赖以生存和发展的重要物质。请回答下列问题:
①生铁和钢是含碳量不同的两种铁碳合金。其中含碳量较低的是________;
A.生铁 B.钢
②钢铁容易发生腐蚀,在生产和生活中比较普遍的腐蚀是________;
A.化学腐蚀 B.电化学腐蚀
③我们常说三大合成材料是____________、合成纤维和合成橡胶。
哈32中2020~2021学年高二上学期期中考试
化学试卷答案
(考试范围:必修一、必修二 适用班级:高二学年)
一、选择题(每小题只有1个选项符合题意,每小题2分,共60分)
1 2 3 4 5 6 7 8 9 10
A B A D C A A B C A
11 12 13 14 15 16 17 18 19 20
A C C B B C D B D D
21 22 23 24 25 26 27 28 29 30
A C A D D C B D D B
二.综合题(40分)
31.(4分) (1)硅 (2)> (3)HClO4 (4)HNO3+NaOH=NaNO3+H2O
32.(4分)(1)CH2BrCH2Br (2)加成反应 (3)2CH3CH2OH+O2→2CH3CHO+2H2O
33. (6分)(1)5.3 (2)玻璃棒 (3)B (4)偏高
34. (6分)(1)分液漏斗 b (2)褪色 漂白 (3)还原 (4)NaOH
35. (10分)(1)< SO2 (2)明矾 (3)2CO+2NO=2CO2+N2 (4)b
36. (10分)(1)①D ②A (2)①B ②B ③塑料
化学试卷
(考试范围:必修一、必修二 适用班级:高二学年)
可能用到的相对原子质量: H-1 C-12 N-14 O-16 Na-23 C1-35.5 S-32 Cu-64
一、选择题(每小题只有1个选项符合题意,每小题2分,共60分)
1.下列资源的开发利用过程中,只发生物理变化的是
A.石油分馏 B.石油裂化 C.高炉炼铁 D.从海水中提取镁
2.根据物质的组成与性质进行分类,HClO 属于
A.氧化物 B.酸 C.碱 D.盐
3.铝的核素中的“27”表示的是
A.质量数 B.质子数 C.中子数 D.电子数
4.当光束通过下列分散系时,可能产生丁达尔效应的是
A.泥浆 B.稀盐酸 C. NaCl 溶液 D.氢氧化铝胶体
5.实验室制取下列气体时,不能用排空气法收集的是
A. H2 B. CH4 C. NO D. NO2
6.、下列变化必须加入还原剂才能发生的是
A. CO2→CO B. NH3→NO
C. SO2→H2SO3 D. CuO→CuCl2
7.下列物质中,能作为制备木材防火剂原料的是
A.硅酸钠 B.氢氟酸 C.碳酸钠 D.漂白粉
8.下列仪器名称错误的是
A.酒精灯 B.圆底烧瓶
C.量筒 D.烧杯
9.在含有大量Na+、HCO3—、Cl—的溶液中,还可能大量存在的离子是
A. Ag+ B. OH— C. NO3— D. H+
10.工业上常用电解法冶炼活泼金属。下列金属使用电解法冶炼的是
A.钠 B.铁 C.铜 D.金
11.分别灼烧下列各组溶液,火焰呈黄色是
A. NaCl溶液 B.稀盐酸 C. K2CO3 溶液 D. CuCl2 溶液
12.下列物质互为同分异构体的一组是
A.和 B.白磷和红磷
C. CH3CH2OH 和CH3OCH3 D. CH4和C2H6
13.下列化学用语表示正确的是
A.乙醇的结构式:C2H6O B.氯化氢的电子式:
C. Mg2+的结构示意图: D. CaCl2的电离方程式:CaCl2=Ca2++ Cl22-
14. 下列物质中,属于共价化合物的是
A. MgCl2 B. CO2 C.H2 D. NaOH
15.下列因素能减慢H2O2溶液分解反应速率的是
A.加入MnO2 B.降低温度 C.升高温度 D.增大H2O2的浓度
16.用NA表示阿伏加德罗常数的值,下列说法正确的是
A. CO的摩尔质量是28 g
B.常温常压下,1 mol N2的体积是22.4 L
C.18 g H2O中含有的氢原子总数为2NA
D.0.1 mol/L Na2SO4溶液中,Na+的物质的量浓度为0.1 mol/L
17.下列物质中,不属于高分子化合物的是
A.蛋白质 B.纤维素 C.淀粉 D.油脂
18.某课外小组同学通过实验发现钾和钠的化学性质相似。下列解释最合理的是
A.都属于金属元素 B.原子的最外层电子数相同
C.元素的最高正化合价相同 D.原子半径相差不大
19.下列属于吸热反应的是
A.氢气在氯气中燃烧 B.过氧化钠与水反应
C.氢氧化钠与盐酸反应 D. Ba(OH)2·8H2O与NH4Cl固体反应
20.下列关于铝的叙述中,正确的是
A.铝是地壳中含量最多的元素 B.铝在常温下不能与氧气反应
C.铝不能与强酸或强碱发生反应 D.电解熔融的氧化铝可制得铝单质
21.关于下图所示原电池装置,下列说法正确的是
A.锌片为负极 B.铜片上发生氧化反应
C.电子由铜片通过导线流向锌片 D.该装置能将电能转变为化学能
22.甲烷和乙烯是两种重要的有机物,区分它们的正确方法是
A.观察两者的颜色 B.观察两者的状态
C.通入酸性高锰酸钾溶液 D.通入氢氧化钠溶液
23.在密闭容器中充入2 mol SO2和2 mol O2,一定 条件下发生反应:2SO2+O22SO3,达到反应限度时,容器中SO3的物质的量可能是
A.1 mol B.2 mol C.3 mol D.4 mol
24.下列离子方程式正确的是
A.铁和稀硫酸反应:2Fe+6H+=2Fe3++ 3H2↑
B.钠与水反应:Na+ 2H2O= Na++ 2OH—+H2↑
C.氯气通入水中:Cl2+ H2O= 2H++Cl— +ClO-
D. NaHCO3 溶液与盐酸反应:H++ HCO3— =CO2↑+H2O
25.下列实验方案能达到目的的是
A.用浓硫酸干燥NH3
B.用BaCl2溶液鉴别AgNO3溶液和Na2SO4溶液
C.用加热的方法除去NaCl固体中的少量NaHCO3
D.用KSCN溶液鉴别FeCl3溶液和FeSO4溶液
26. 下列物质与危险化学品标志的对应关系正确的是
A B C D
水 氮气 浓硫酸 氢氧化钠
27. 下列物质中,只含有离子键的是
A.NaOH???? B.NaCl???????? C.H2??????? D.H2S
28. 下列过程中所发生的化学变化属于加成反应的是
A.光照甲烷与氯气的混合气体 B.在浓硫酸催化作用下苯与浓硝酸反应
C.在溴化铁的催化作用下苯与液溴反应 D.向溴的四氯化碳溶液中通入乙烯
29. 下列反应属于氧化还原反应的是
A.H2SO4+2NaOH Na2SO4+2H2O
B.2NaHCO3 Na2CO3 + CO2↑ + H2O
C.NH3 + HCl NH4Cl
D.CuO+H2 Cu+H2O
30. 下列有关实验操作或现象描述正确的是
A.实验室用图1装置制备Cl2
B.加热后图2中溶液颜色恢复红色
C.用图3装置除去Cl2中含有的少量HCl
D.实验室用图4装置制取少量蒸馏水
二、填空题(本大题包括6小题,共40分)
31. (4分)2019年是门捷列夫发现元素周期律150周年。下表为元素周期表的一部分。
碳 W Y
X
硫 Z
回答下列问题:
(1)X元素的名称是________。?
(2)Y元素的氢化物H2Y的稳定性________(填“>”或“<”)H2S。?
(3)表中元素的最高价氧化物对应的水化物酸性最强的是___________________
(填化学式)。
(4)W元素最高价氧化物对应水化物与氢氧化钠溶液反应的化学方程式
。?
32. (4分)已知A、B、C是中学化学中常见的有机物,它们与乙烯之间有如图的转化关系(图中部分产物已略去)。
请回答下列问题:
(1)A的结构简式为____________。?
(2)反应②的反应类型为____________。?
(3)反应③的化学方程式为______________。
33.(6分)实验小组需要配制100 mL0.5 mol/L的Na2CO3溶液,同学们分工合作进行实验。
(1)甲同学需要称取Na2CO3固体的质量是_____________g。
(2)乙同学溶解Na2CO3固体时,需要用到的仪器有:量筒、烧杯和___________。
(3)丙同学的下列操作中,正确的是_____________。
A.转移液体时,不慎将溶液洒落在容量瓶外
B.液面离容量瓶颈刻度线下1~2 cm时,改用胶头滴管滴加蒸馏水
C.溶液配制完成后,长期将溶液储存在容量瓶中
(4)若在定容时俯视刻度线,则此操作导致所配Na2CO3溶液的物质的量浓度________(填“偏高”或“偏低”)。
34.(6分)研究性学习小组的同学们按下图装置进行SO2的制备及性质探究实验。
(查阅资料得到SO2气体的制备原理:Na2SO3(固)+H2SO4(浓)=Na2SO4+SO2↑+H2O),回答问题:
(1)图中a的仪器名称是_______, 亚硫酸钠应放在_________(填“a”或“b”)中。
(2)实验过程中,可以观察到装置B中品红溶液_______(填实验现象),该现象说明SO2具有_____性(填“氧化”、“还原”或“漂白”)。
(3)酸性条件下,SO2 与KMnO4在发生如下反应:5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2H2SO4,使溶液褪色。反应中SO2是________(填“氧化”、“还原”剂)。
(4)尾气可采用________溶液吸收。
35. (10分)改善生态环境、建设美丽家园是全人类共同的呼声。
(1)酸雨是指pH_______5.6 (填“>”或“<”)的降水;_______ (填“SO2”或 “N2")是形成酸雨的主要气体之一。
(2)水是生命之源,净化水中的细小悬浮颗粒时,常加入_______ (填“食盐”或 “明矾”)使其聚集成较大颗粒沉淀而与水分离。
(3)汽车尾气中的CO和NO在催化剂作用下发生反应生成CO2和N2,该反应的化学方程式为________________。
(4)“垃圾分类”成为时代新风尚,下列属于可回收标志的是________(填字母序号)。
a. b. C.
36. (10分) (1)树立健康观念,促进身心健康全面发展现有下列四种物质:
A.淀粉 B.油脂 C.氨基酸 D.阿司匹林
请回答下列问题(填字母代号):
①具有解热镇痛作用,为人们熟知的治感冒药是________;
②能在体内水解,且最终转化为葡萄糖的天然高分子化合物是________;
(2)材料是人类赖以生存和发展的重要物质。请回答下列问题:
①生铁和钢是含碳量不同的两种铁碳合金。其中含碳量较低的是________;
A.生铁 B.钢
②钢铁容易发生腐蚀,在生产和生活中比较普遍的腐蚀是________;
A.化学腐蚀 B.电化学腐蚀
③我们常说三大合成材料是____________、合成纤维和合成橡胶。
哈32中2020~2021学年高二上学期期中考试
化学试卷答案
(考试范围:必修一、必修二 适用班级:高二学年)
一、选择题(每小题只有1个选项符合题意,每小题2分,共60分)
1 2 3 4 5 6 7 8 9 10
A B A D C A A B C A
11 12 13 14 15 16 17 18 19 20
A C C B B C D B D D
21 22 23 24 25 26 27 28 29 30
A C A D D C B D D B
二.综合题(40分)
31.(4分) (1)硅 (2)> (3)HClO4 (4)HNO3+NaOH=NaNO3+H2O
32.(4分)(1)CH2BrCH2Br (2)加成反应 (3)2CH3CH2OH+O2→2CH3CHO+2H2O
33. (6分)(1)5.3 (2)玻璃棒 (3)B (4)偏高
34. (6分)(1)分液漏斗 b (2)褪色 漂白 (3)还原 (4)NaOH
35. (10分)(1)< SO2 (2)明矾 (3)2CO+2NO=2CO2+N2 (4)b
36. (10分)(1)①D ②A (2)①B ②B ③塑料
同课章节目录
